作者:北京安贞医院 刘巍 高雅楠

导语:
行冠状动脉造影的患者中约5%的患者有冠状动脉瘤样扩张。无论是否存在冠状动脉粥样硬化性疾病,冠状动脉瘤或冠状动脉扩张往往与远期不良预后相关。其治疗手段包括药物治疗、外科切除、冠状动脉旁路移植术(CABG)、经皮冠状动脉介入治疗(PCI)。目前关于该疾病尚缺乏随机试验或指南推荐,因此临床医师在面对此类患者时往往较难抉择。本文旨在分享冠状动脉瘤样疾病的病理学机制、分类、临床表现、评估手段和管理策略。
定义及分类
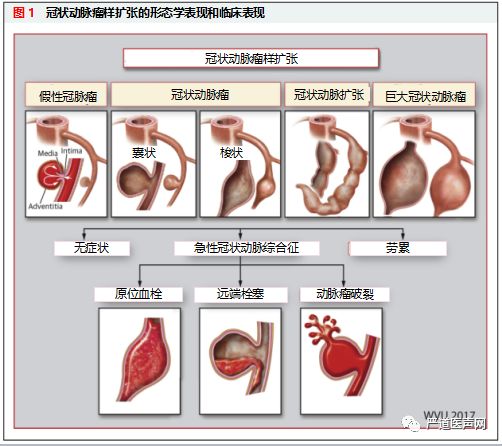
冠状动脉瘤(coronary artery aneurysm,CAA)的定义为冠状动脉局部扩张超过邻近正常节段的1.5倍。当横径大于纵径时称为囊状动脉瘤;反之则称为梭状动脉瘤。
冠状动脉扩张( coronary artery ectasia,CAE)则一般是指更为弥漫的病变。
此外,还可根据形态学或血管内成像对CAA和CAE进行再分类。

流行病学
冠状动脉瘤的发病率为0.3-5%,男性多于女性,冠脉近端多于远端。研究显示CAA合并CAE的发生率高于CAA,CAA的发生率<1%。冠状动脉瘤好发于右冠状动脉(40%),其次为左前降支(32%),左主干处较少见(3.5%),但囊状冠脉瘤好发于左前降支。冠状动脉粥样硬化性和血管性CAA常有超过1根血管受累,先天性和医源性CAA则常局限于一根血管。
病理学机制
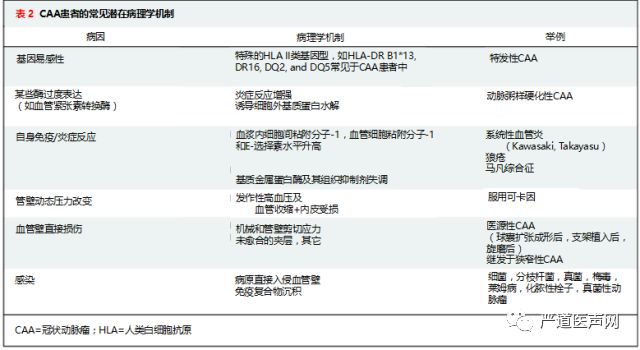
CAA的病理学机制尚未完全明确。有证据表明某些危险因素与CAA之间存在关联,相关危险因素见表2。
此外,有一种少见但不容忽视的动脉瘤——主动脉大隐静脉桥动脉瘤(SVGAs)。与其他冠状动脉瘤相比,这种类型的动脉瘤特点鲜明:1)常见于旁路移植术术后极晚期 ;2)尺寸明显大于CAAs;3)随时间发生进展 ;4)有时可出现机械并发症(如压迫邻近心脏组织或静脉,破裂)。
临床表现
大多数CAA无症状,仅在行冠脉造影或CT时偶然发现。当存在以下情况时,患者往往有临床症状:1)合并阻塞性动脉粥样硬化性疾病时可有劳力性心绞痛或急性冠脉综合征表现;2)巨大动脉瘤阻塞管腔时导致远端栓塞和心肌梗死;3)某些CAA和SVGA扩张可压迫邻近组织;4)动脉瘤破裂较少见,一旦破裂可引起急性心脏压塞;5)即使无显著的冠状动脉狭窄,也可发生因微血管功能障碍导致的应激性心肌缺血。
评估手段
冠脉造影是目前最常用的评价冠状动脉扩张或动脉瘤的成像手段。但是,前向造影剂充盈延迟、节段性返流、造影剂瘀滞于扩张节段往往使得冠脉造影无法获得最佳图像。强力长时间注射造影剂可以有效避免动脉瘤处造影剂瘀滞导致血栓形成,在巨大动脉瘤中效果尤为显著。
此外,血管内超声(IVUS)也是一种非常有用的成像手段,可以对管壁进行成像,区分真性动脉瘤、假性动脉瘤和因斑块破裂或邻近节段狭窄所致的动脉瘤样外观。此外,IVUS可以准确测量CAA和/或邻近狭窄管腔的尺寸,在需要行PCI时协助选择支架尺寸。支架植入后行IVUS时需格外小心,避免造成支架移位。
红外光谱较窄,因而光学相干断层成像(OCT)在评价CAA时略显不足。
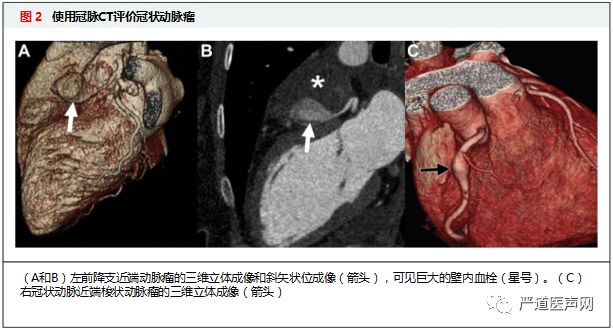
与侵入性冠脉造影相比,冠脉CT对于动脉瘤尺寸、血栓及钙化程度的评价更为准确,越来越多的患者选择冠脉CT作为成像评价手段。对于巨大动脉瘤和SVGA的患者来说,使用CT可以避免冠脉造影的不足,同时可以准确评价动脉瘤相关机械并发症,因而更具优势。
管理策略
鉴于以下原因,目前CAA患者的治疗颇具挑战性:冠状动脉瘤的自然病程尚不清楚,因此偶然发现的CAA或无冠脉狭窄或闭塞的冠脉扩张尚无最佳治疗策略;有心绞痛或急性心梗表现的患者无论是接受介入治疗还是外科血运重建在技术上都具有挑战性;此外,无论是有症状还是无症状的CAA患者,目前均缺乏相关随机试验或大规模试验的数据。目前大多数推荐都是基于小型病例研究或经验。 基于此,我们应该根据CAA的位置和形态、患者特征及临床表现进行个体化治疗。
● 药物治疗
动脉粥样硬化在CAA的病因中占据很大比例,尤其是老年患者中。因此修正相关危险因素的重要性不言而喻。
双联抗血小板或抗凝治疗在CAA患者尤其是偶然发现CAA的患者当中的应用目前仍有争议。不幸的是,目前尚无高质量证据支持或反对抗血小板或抗栓治疗在这类患者当中的应用。既往研究的结果各异。近期一项研究显示CAE 合并急性冠脉综合征的患者接受口服抗凝药治疗并达到治疗时间窗>60%后,MACE事件发生率由33%降至0%,提示CAE合并急性冠脉综合征的患者接受抗凝治疗可有获益。
关于Kawasaki病患者接受抗凝治疗后减少血栓事件的证据同样十分有限。因此目前的指南仅推荐有大CAA或CAA快速进展的Kawasaki病患者接受抗凝治疗。
一些学者发现血管紧张素转换酶可以预防或延缓CAA进展,但这一结论尚未在长期研究中得到证实。值得注意的是,血管舒张剂如硝酸盐类可以加速有孤立大CAA或CAE患者的心肌缺血进展,因此应避免使用。Kawasaki病患者经静脉使用免疫球蛋白可以降低MACE事件发生率。
● 介入治疗
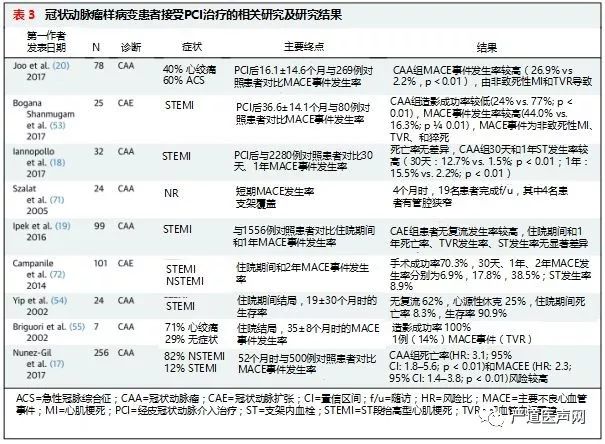
由CAA所致的急性冠脉综合征患者其治疗重点在于恢复血流。鉴于这类患者往往血栓负荷较重,因此在扩张动脉或动脉瘤处行PCI时常选择血栓切除(抽吸或机械切除)联合血小板糖蛋白IIb/IIIa抑制剂(图3)。尽管如此,无复流和远端栓塞的发生率仍较高。无急性冠脉综合征的CAA患者其干预治疗更为复杂。尽管如此,当患者有高危临床或解剖特征时往往考虑干预治疗。其治疗手段因动脉瘤形状和范围有所不同,具体见图6
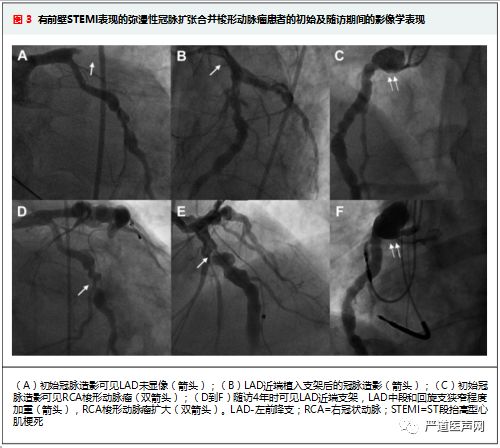
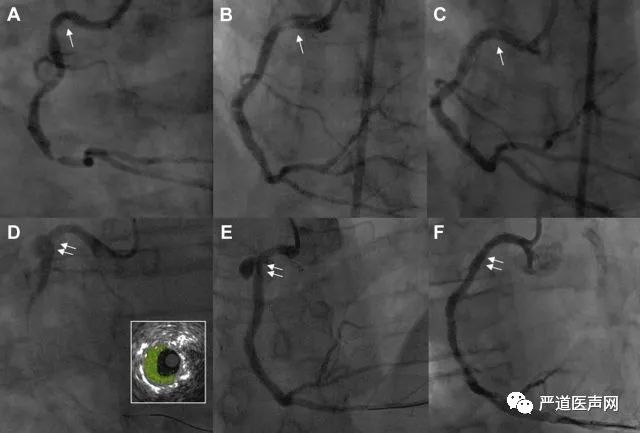
图 4
(A)RCA远端重度狭窄,RCA近端可见Amplatz指引导管(箭头);
(B)支架植入RCA远端后近端发生夹层(箭头);
(C)使用药物洗脱支架治疗夹层(箭头);
(D)8年后复查造影可见RCA中段闭塞(前壁STEMI的罪犯病变),RCA近端假性动脉瘤可疑(IVUS图像为双箭头处);
(E)使用药物洗脱支架治疗RCA STEMI;
(F)使用GRAFTMASTER覆膜支架治疗假性动脉瘤

CAA的介入治疗也面临着一些挑战:
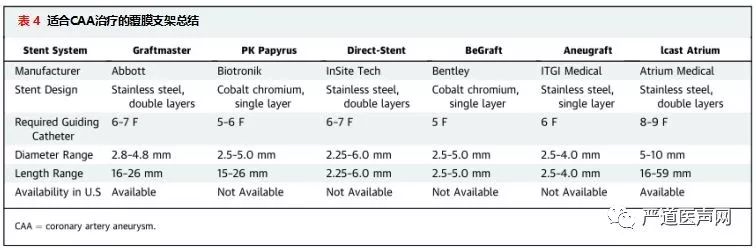
1.专用器械:目前尚无专为治疗CAA而设计的覆膜支架,适合用于CAA治疗的覆膜支架见表4。
2. 血栓负荷: 当患者有急性冠脉综合征表现时,于罪犯动脉瘤处行PCI往往不良事件发生率和失败率较高,这主要是由血栓负荷较重所致。2项随机试验证实AngioJet 装置 (Boston Scientific , Marlborough , Massachusetts)可以有效降低有巨大血栓需在静脉桥或原位冠脉处行PCI患者的栓塞率。一些病例报告同样证实了该装置在CAA患者中的有效性。
3. 尺寸和着陆区域的评估:准确测量CAA的尺寸是降低支架内血栓和支架移位的关键因素。但CAA处血栓形成往往导致低估动脉瘤的真实大小。此外,CAA完全扩张时的边界往往难以描绘,因此准确判断支架着陆区同样有较高的难度。在动脉瘤较长的节段内,往往需要重叠植入几枚支架以保证动脉瘤完全被覆盖。
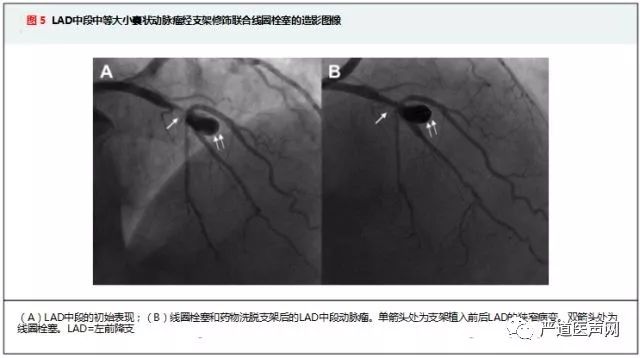
4.覆膜支架的输送:覆膜支架往往较硬,需要通过较大的指引导管输送,增加了手术相关并发症的发生率,尤其是在较为扭曲的血管中。此外,覆膜支架输送入边支较困难,可能导致动脉瘤覆盖不完全。某些情况下覆膜支架无法输送,可考虑使用支架联合线圈栓塞,其机制见图7.
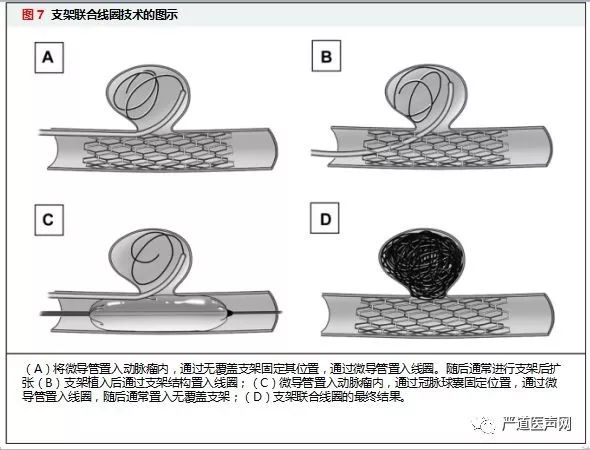
川崎病患者发生动脉瘤后行PCI的经验局限于儿童和青年患者。这些数据确实有一些有趣的发现:1)川崎病患者狭窄的动脉瘤管壁处往往有大量血栓,因此常常使用IVUS测量血管的真实直径;2)川崎病患者接受PCI治疗后往往需要重复治疗;3)CABG的长期结果优于PCI。当今美国心脏协会指南推荐限制PCI在合并单支血管或局限性多支血管病变的川崎病患者中的应用。
● 外科干预
目前尚无理想的外科干预手段。CAA的手术治疗手段包括动脉瘤结扎、切除和插入移植物后袋形缝合。最常用的外科干预手段为切除CAA,缝合其近端及远端血管,必要时行旁路移植术
待解决问题和前景
目前关于CAA和CAE的最佳治疗策略仍颇具争议,此外该领域仍存在一些尚未解决的疑问,具体见下图。
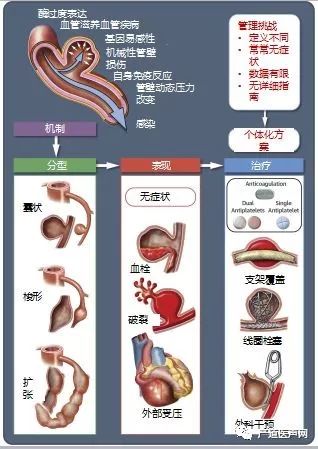
未来相关研究应对以下重要问题给出解答:
1) CAA和CAE的潜在病因是什么?CAA和CAE到底是两种不同的疾病还是一种疾病的两种类型?
2) 这种异常是否会导致无症状患者不良事件的发生率增加?
3) 双联抗血小板或抗凝治疗能否作为血栓性并发症的一级或二级预防策略?
4) 偶然发现的CAA是否需要进行干预?
5) CAA的理想治疗措施是什么?(裸金属支架 vs DES,覆膜支架移植物,支架联合线圈,外科切除等)
6) 进行干预治疗术中和术后的最佳药物治疗是什么?
结论
冠状动脉瘤样扩张并不少见,其管理目前仍颇具挑战性。理解其自然进程、评估手段及干预手段对于达到最佳结果至关重要。