

01
流体动力再通术(HDR)操作步骤
步骤1:双体位造影:在多个投照角度进行。评估血管解剖是否适合HDR。
步骤2:定位CTO近端纤维帽:明确CTO近端纤维帽位置。
步骤3:穿刺近端纤维帽:当CTO的近端纤维帽被识别后,将微导管沿工作导丝送至近端纤维帽附近,使用具有中等或高穿透力的导丝(依据术者偏好),穿刺近端纤维帽。首选Gaia或Gaia Next 2导丝,必要时升级至Confianza Pro 12或Hornet 14导丝。可使用可旋转微导管(Turnpike LP、Corsair Pro)。
步骤4:导丝浅进:仅将导丝推进入CTO体部2-4mm,避免进入斑块外间隙。
步骤5:推进微导管:沿导丝推进微导管。确保微导管头端明显越过近端纤维帽。
步骤6:排空气体:用生理盐水或造影剂填充微导管尾端。在撤出导丝时,防止空气进入微导管。
步骤7:确认无空气:连接3ml鲁尔锁注射器,抽取纯造影剂。回抽以确保管腔内无空气。
步骤8:微量注射造影剂:透视下缓慢注射≤0.5ml造影剂,直至微导管头端以远的CTO体部出现造影剂染色。
步骤9:对侧造影:根据造影剂染色点距CTO远端纤维帽的距离,评估真实的CTO长度。
步骤10:判断斑块内造影剂染色类型:
类型1:斑片状/局灶性
类型2a:线性显影,可见远端真腔
类型2b:线性显影,可见远端边支
类型3:斑片状起源,伴有通向远端真腔的线性轨迹
步骤11:插入聚合物涂层导丝:移除造影剂注射器,沿造影剂标记的轨迹插入导丝。优选导丝:Fielder系列(头端弯曲<2mm)或Gladius Mongo导丝。
步骤12:必要时重复斑块内注射:如果导丝无法前进,将微导管推进数毫米。再次进行斑块内注射。重复直到闭塞段被通过或操作停止。
步骤13:导丝失败处理:如果导丝未能进入远端管腔、进入斑块外间隙或形成袢:
(a)在不同位置重新穿刺近端纤维帽,重复HDR。
(b)转换为替代策略(导丝升级或正向夹层再入技术ADR)。
02
流体动力再通术(HDR):一种新的CTO-PCI开通技术
03
摘要
背景:在慢性完全闭塞病变(CTO)的经皮冠状动脉介入治疗(PCI)中,已使用斑块内注射造影剂来显示解剖结构和辅助导丝通过。但将其作为CTO首次通过的初始核心手段,尚未见报道与验证。
目的:本文介绍一种全新技术——流体动力再通术(HydroDynamic Recanalization,HDR),该技术结合斑块内注射造影剂的诊断与治疗作用,实现CTO首次通过。
方法:HDR是一种CTO正向开通技术,核心是造影剂微量注射与聚合物涂层导丝协同使用。本研究为回顾性、首次人体病例系列研究,纳入解剖条件适宜的CTO患者(近端纤维帽可见、远端靶目标可识别),采用HDR行CTO-PCI。主要终点为手术成功率,次要终点为手术相关并发症。
结果:共有43名患者(45处CTO)接受了使用HDR的CTO-PCI。患者平均年龄为64.3±11岁。平均J-CTO评分和PROGRESS CTO评分分别为2.3±0.7和1.8±0.7。CTO复杂性高,其中34处(76%)为模糊或钝头近端纤维帽;27处(60%)病变长度≥20mm;36处(80%)为中/重度钙化。使用HDR的手术成功率为100%。无并发症发生。
结论:本研究显示了HDR在CTO-PCI中的效用。HDR似乎是一种安全且有前景的新型基于造影剂注射的初始开通技术,适用于筛选后的患者。该策略有待更大规模前瞻性研究进一步评估。

致谢:感谢牛铁生教授、CTOCC俱乐部分享原文。
04
引言
正向导丝技术是目前CTO-PCI最常用的通过策略。相较于正向夹层再入(ADR)与逆向技术,正向导丝操作简便、术者熟悉、安全性更高。专用微导管、复合核心导丝的研发,以及标准化通过流程的普及,进一步提升了CTO-PCI成功率。
经微导管行斑块内造影剂注射(Carlino技术),是杂交术者常用的辅助操作,可在正向与逆向路径中辅助通过困难闭塞病变,成功率高、并发症率低。
尽管多项研究证实Carlino技术的安全性,但该方法仍多作为复杂CTO解剖结构的补救手段,原因包括:Carlino技术作用机制不明确、斑块内注射安全性顾虑、操作缺乏标准化、担心血管损伤影响进一步的开通策略,以及对造影剂染色形态认知不足。即便如此,斑块内造影剂注射仍是CTO术者重要(尽管未充分利用)的工具,用于处理复杂、解剖模糊的CTO病变。
本文(发表于2024年)介绍一种全新CTO开通技术——流体动力再通术(HDR),核心是造影剂微量注射联合聚合物涂层导丝协同应用。HDR是CTO-PCI造影剂斑块改型技术的进一步升级,基于以下观察:斑块内注射微量(≤0.5mL)造影剂,可冲开斑块内富含脂质的松软区域,辅助聚合物涂层导丝通过。本病例系列展示了HDR可适用的多种CTO解剖类型。
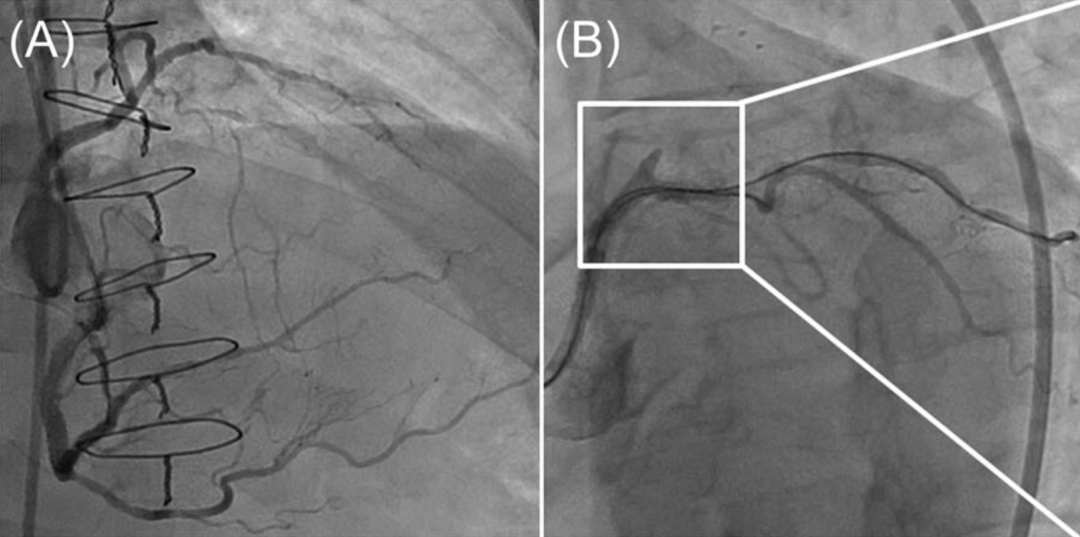
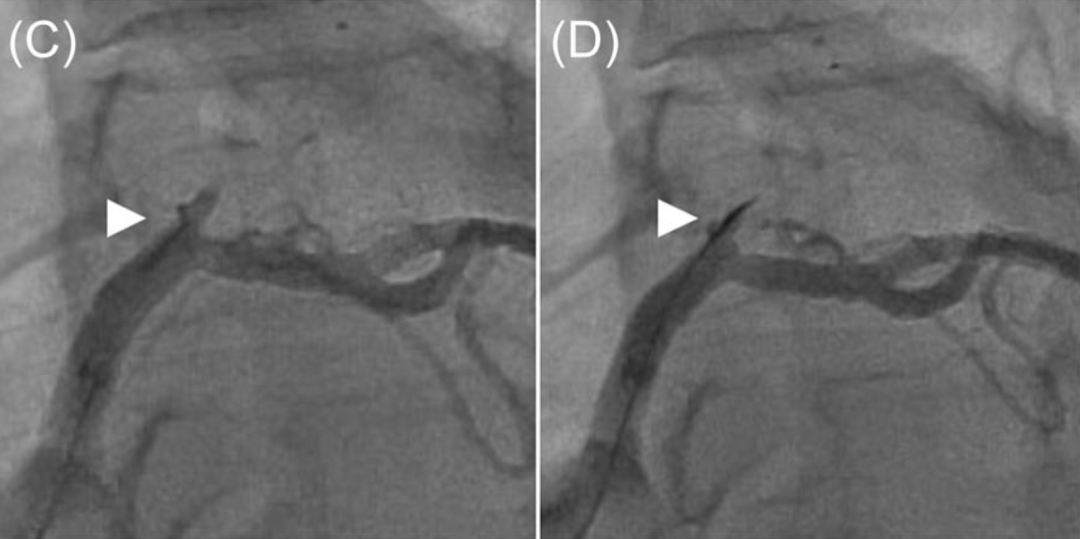
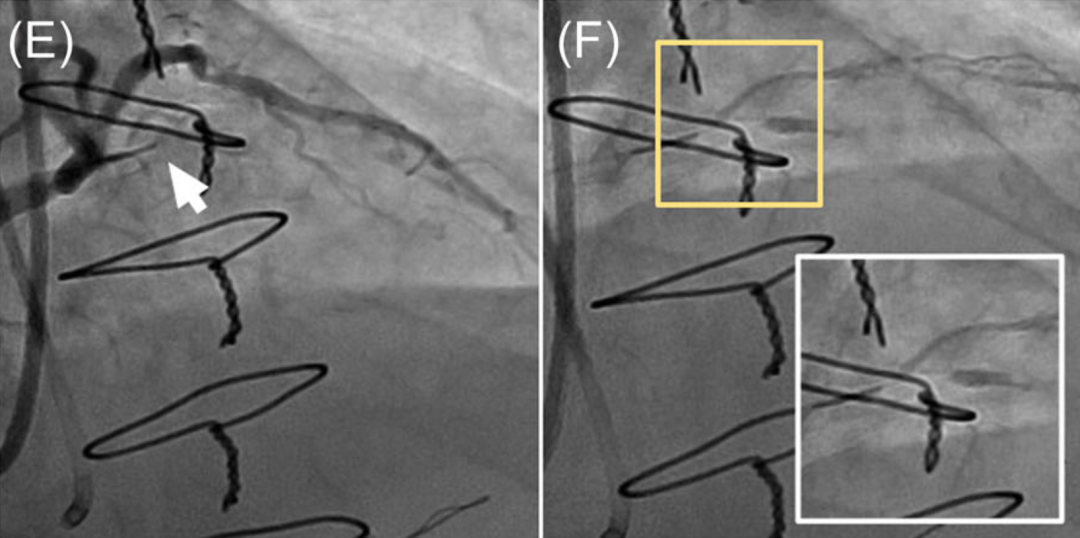
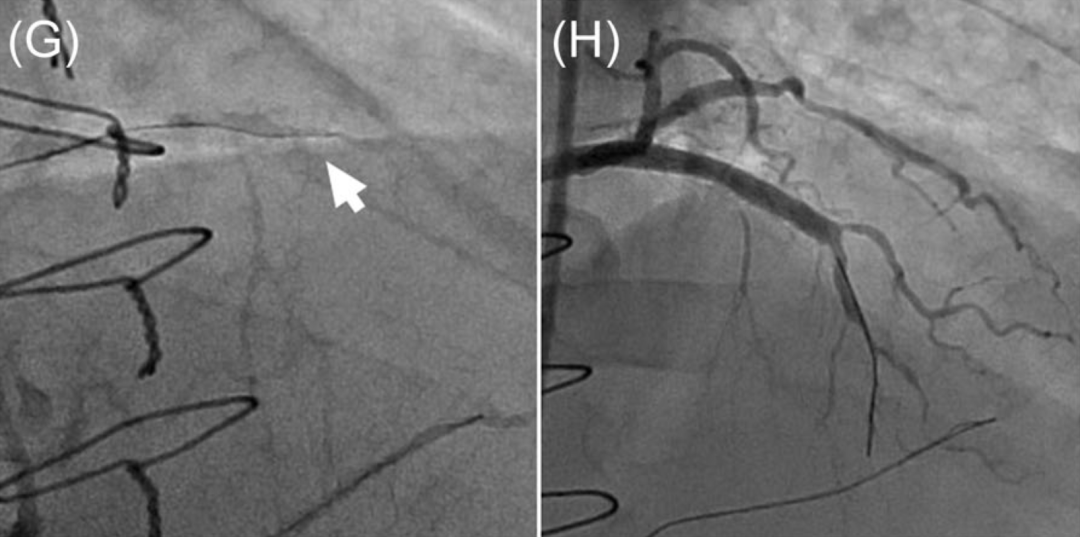
图1 HDR操作步骤
A、B:采用双侧造影明确CTO长度并定位近端纤维帽。C:将微导管送至CTO近端纤维帽处(箭头)。D:使用中等头端负荷导丝(如Gaia 2)穿刺近端纤维帽(箭头),并将微导管向前推送2–3mm进入闭塞段(箭头,E)。F:在透视下缓慢向闭塞段内注射小剂量造影剂(0.5mL),观察造影剂染色(插图)。G:在透视引导下,将聚合物涂层导丝(如图中Fielder XTR)沿造影剂标记路径送入远端真腔(箭头)。H:前降支近中段PCI成功后的最终造影图像。
05
方法
研究设计:这是一项回顾性分析,纳入了2022年10月至2024年4月期间在以下三个中心接受使用HDR进行CTO-PCI的患者:(a)意大利米兰San Raffaele科学研究所IRCCS;(b)美国德克萨斯州休斯顿Texas大学;(c)巴基斯坦Tabba心脏研究所。
入选标准:患者至少有一处冠状动脉CTO;优化药物治疗后仍有症状,或心脏PET提示缺血区域>15%。
HDR适用指征:①近端存在通畅节段;②闭塞动脉远端靶目标可识别。
收集所有人口统计学、临床和技术数据以完成分析。
研究终点
主要终点:技术成功,定义为术后靶病变残余狭窄<30%,所有≥2.5mm远端分支正向血流达TIMI 2级及以上。
次要终点:手术相关并发症(冠状动脉穿孔、心肌梗死、死亡)。
同时记录CTO通过时间(导丝置入至确认远端真腔后撤出微导管的时间)、CTO通过及手术全程所用导丝数量。
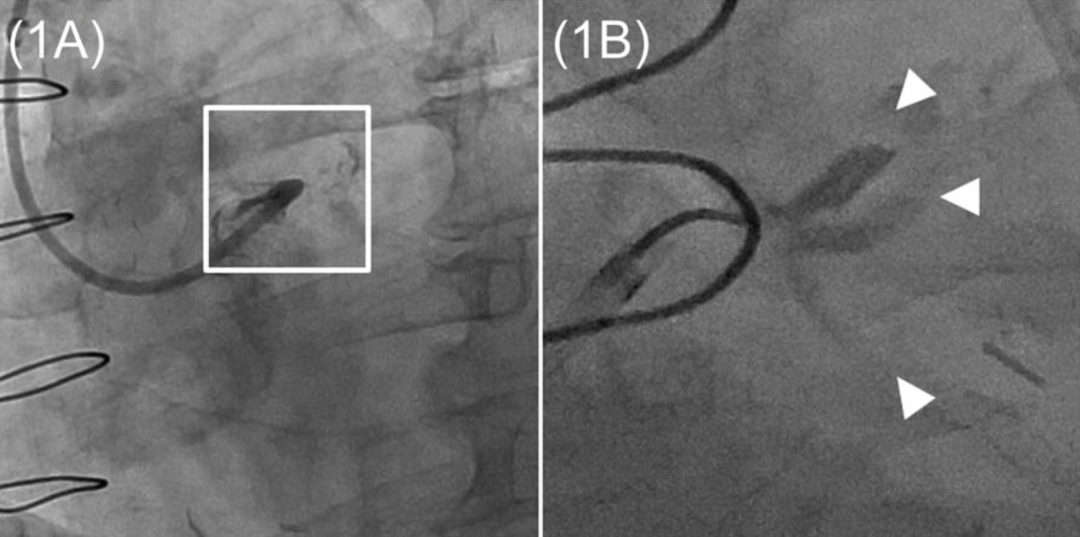
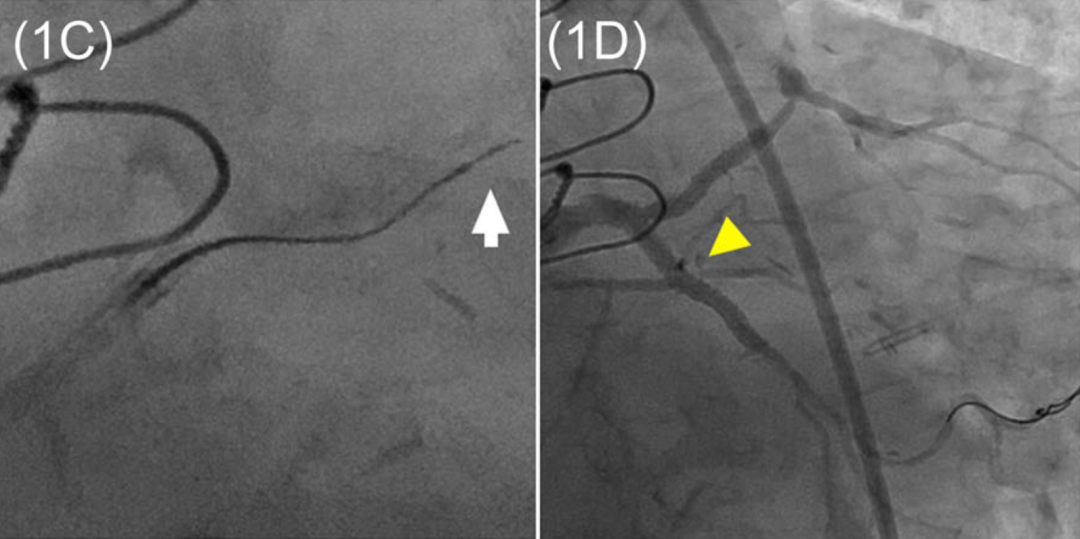
病例1:使用HDR成功处理闭塞的左主干(A)。斑块内注射造影剂形成三叉状染色(箭头,B),兼具1型与2型特征。Fielder XT导丝(箭头,C)顺利进入中间支。最终造影显示左主干、回旋支血运重建成功,侧支保留完好(箭头,D)。
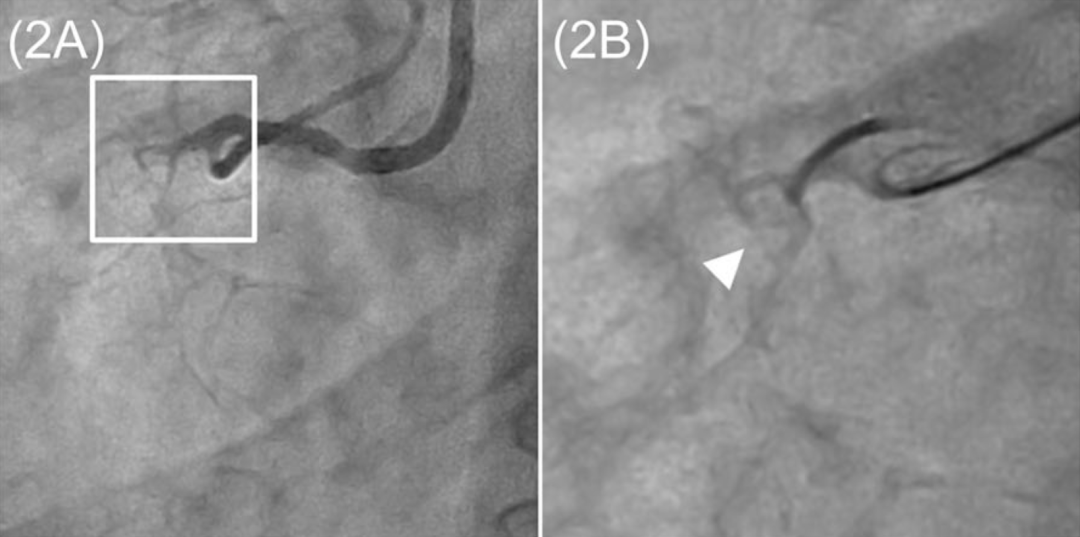
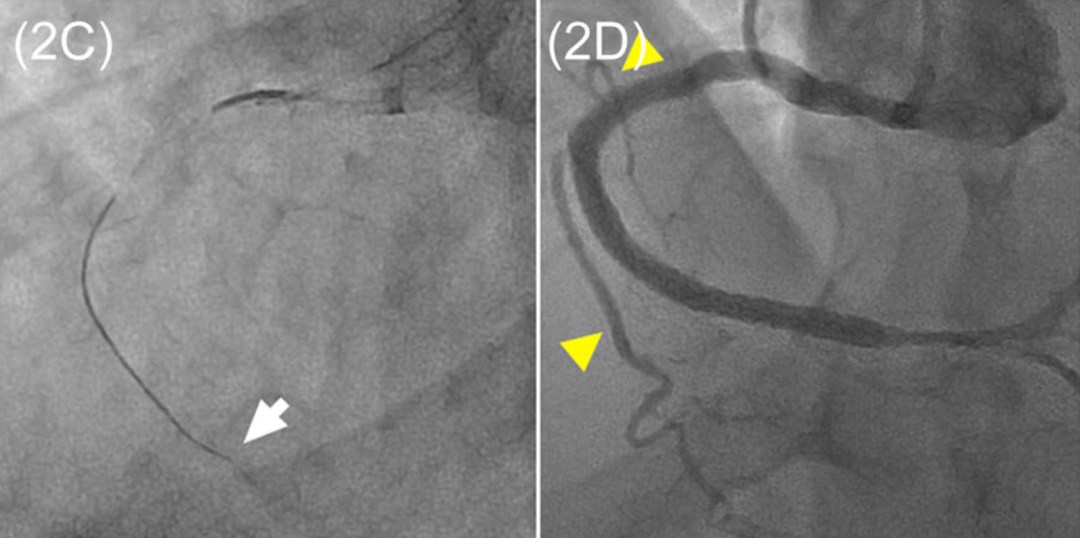
病例2:使用HDR成功处理闭塞的RCA(A)。斑块内注射造影剂形成线性染色(箭头,B)。Fielder XT导丝(箭头,C)顺利通过长节段RCA闭塞病变。最终造影显示RCA血运重建成功,侧支保留完好(箭头,D)。
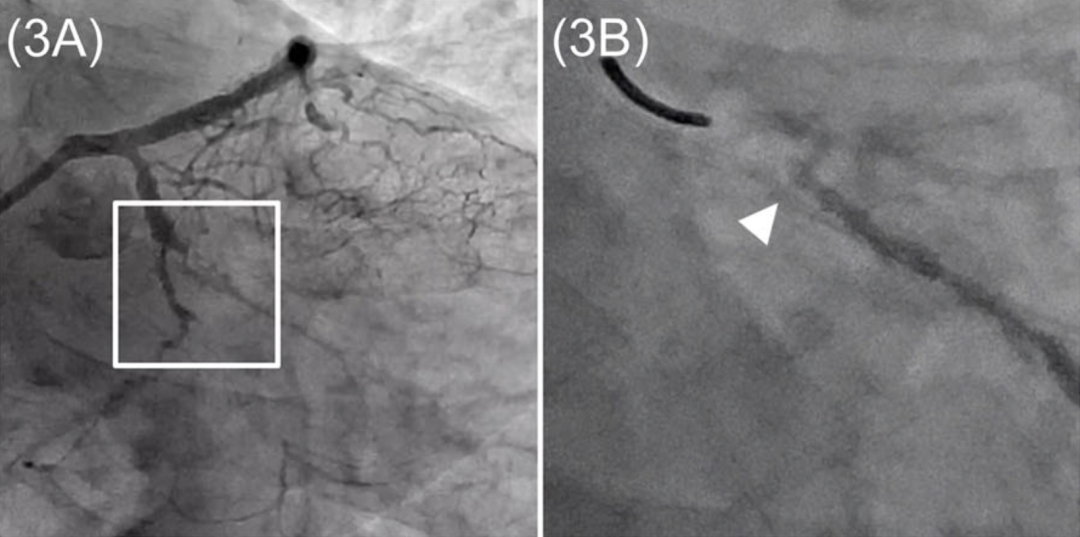

病例3:使用HDR成功处理两支闭塞的钝缘支(A)。向第一钝缘支近端纤维帽内微量注射造影剂,呈现2A型染色(箭头,B)。向第二钝缘支近端纤维帽内第二次微量注射造影剂,呈现2B型染色(箭头,C)。回旋支系统重建后的最终造影显示侧支保留完好(箭头,D)。
图2 HDR典型病例
06
结果
在研究期间,共有43名患者的45处CTO接受了采用主要HDR策略的CTO-PCI。患者特征见表1,血管造影和手术特征见表2,技术数据见表3。代表性病例见图1和图2。
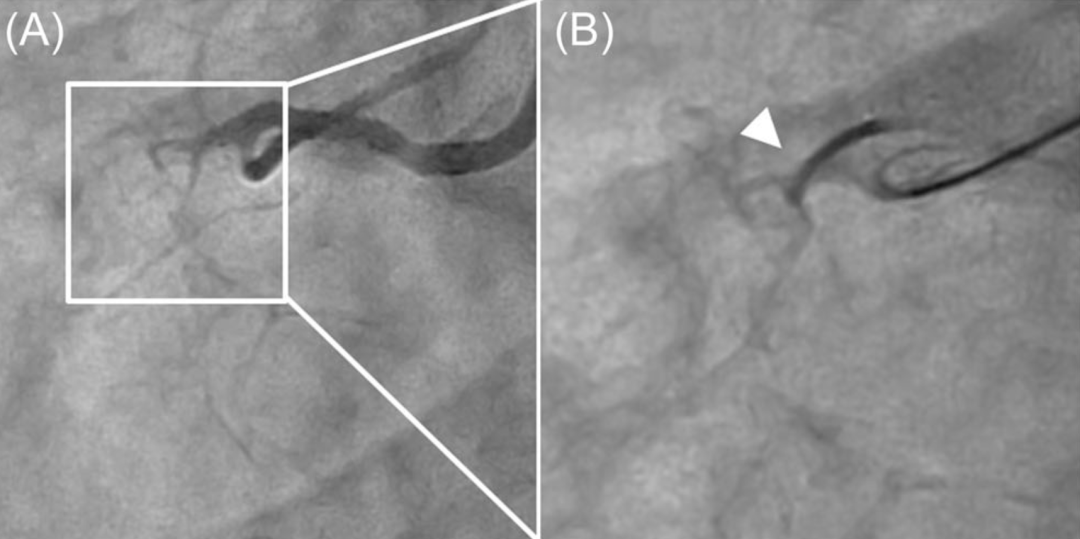
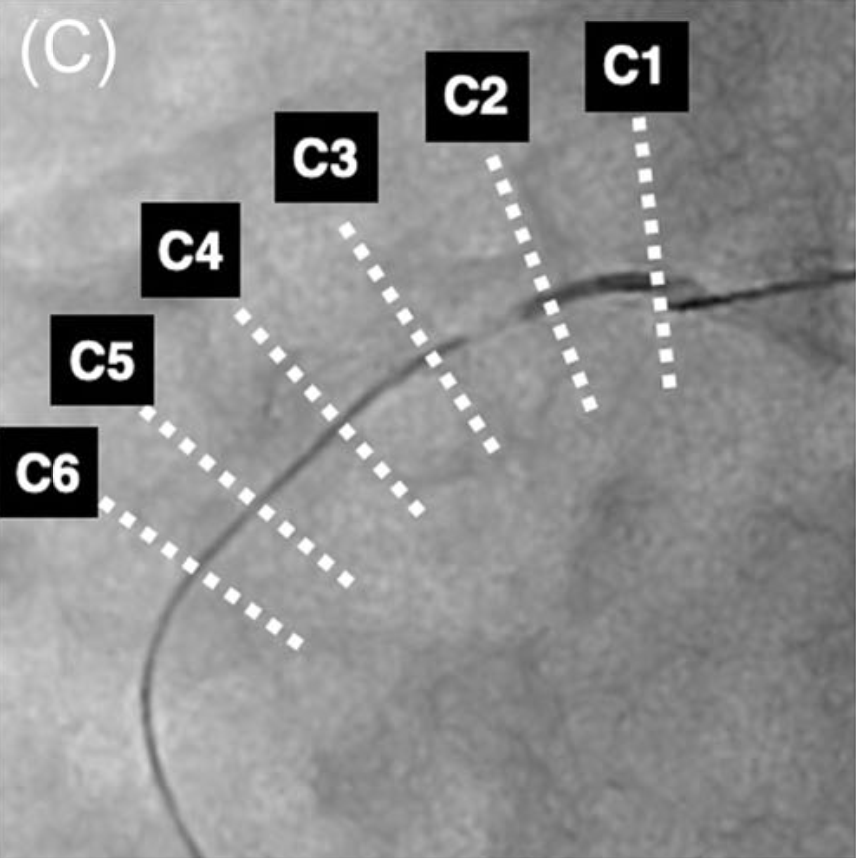
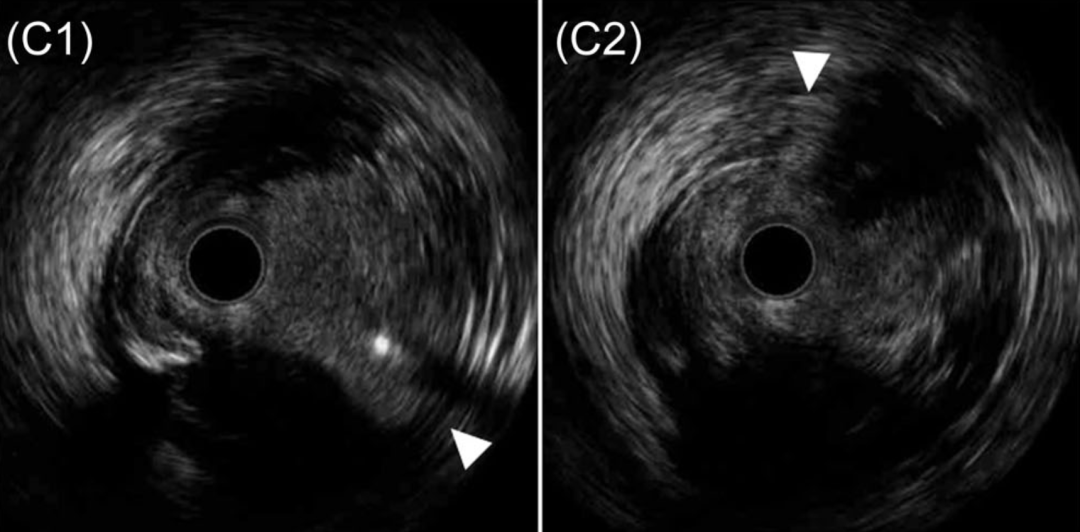
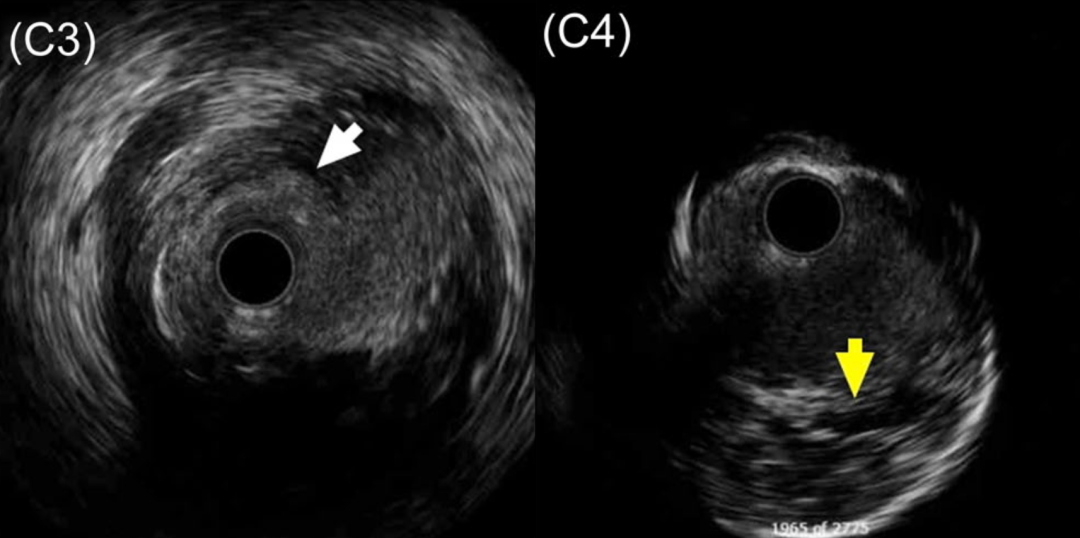

图 3 HDR术后IVUS表现(来自图2病例2)
A、B、C:闭塞RCA的HDR操作。导丝通过后,使用2mm球囊行血管成形术,便于IVUS导管通过。C1–C6:IVUS回撤图像共6个部位:RCA近端伴分支(箭头,C1、C2)、近端纤维帽入口点(箭头,C3)、造影剂充盈的斑块内通道(箭头,C4、C5)、远端纤维帽穿出至真腔(C6)。各部位IVUS导管均位于管腔内。
基线患者特征
患者平均年龄为64.3±11岁,男性占79%(34例),糖尿病占39%(17例)。
左心室射血分数平均51±9%,估算肾小球滤过率平均72±23mL/min/1.73m²。
所有患者均有心绞痛,加拿大心血管学会(CCS)分级平均2.1±0.9级,70%(30例)患者服用≥2种抗心绞痛药物。
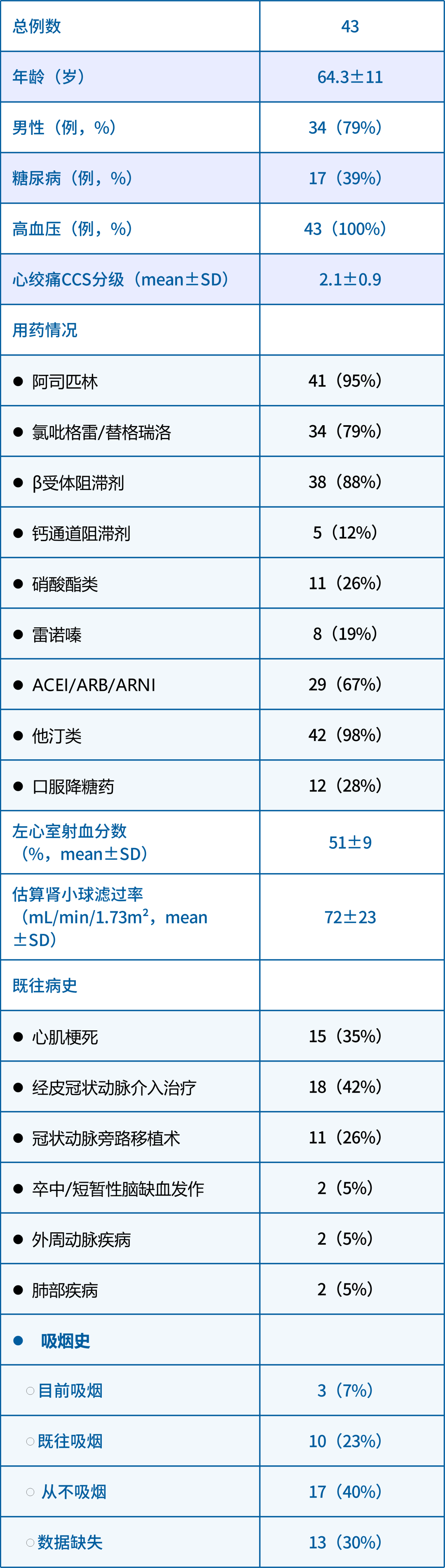
表1患者基线资料与用药情况

基线病变特征
共45处CTO病变,J-CTO评分2.28±0.7分,PROGRESS CTO评分1.8±0.7分。复杂特征占比高:
76%(34例)为模糊/钝头近端纤维帽。
60%(27例)病变长度>20mm。
80%(36例)伴中或重度钙化。
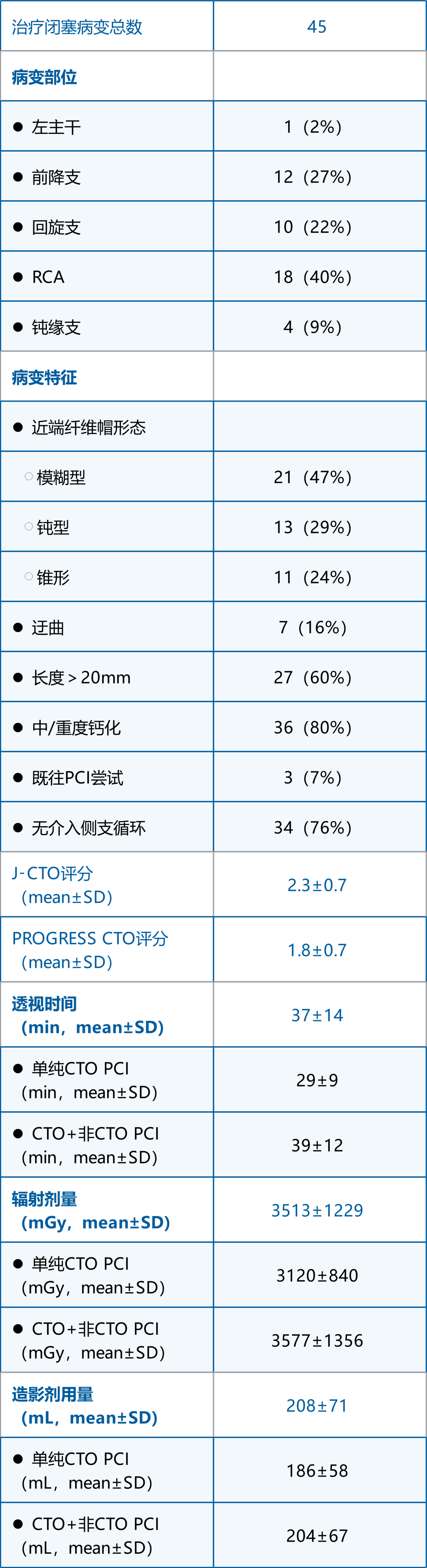
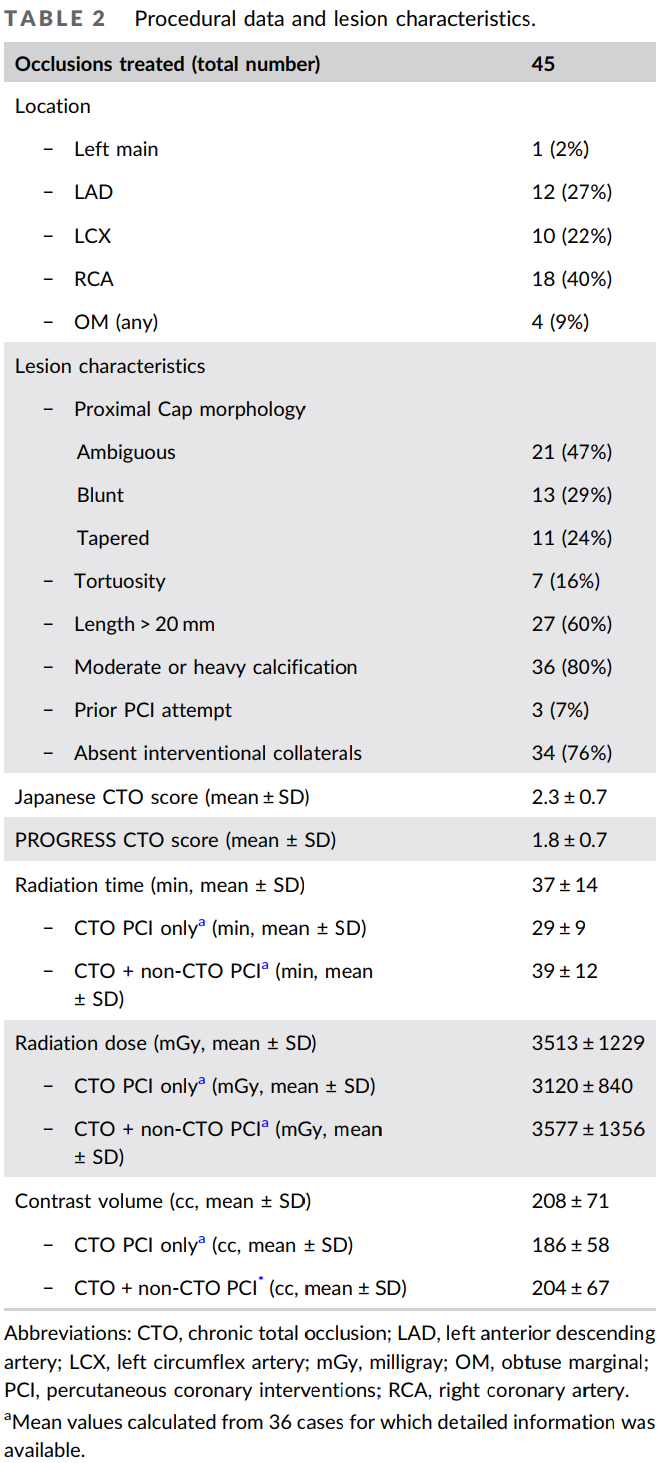
表2手术资料与病变特征
手术细节
CTO病变分布:左主干1处(2%)、前降支12处(27%)、回旋支10处(22%)、右冠17处(39%)、钝缘支4处(9%)。
2例同期处理回旋支+相邻钝缘支闭塞分叉病变,1例单纯钝缘支CTO,1例分期处理前降支+右冠CTO。
3例既往曾行CTO-PCI,58%(25例)在同一手术中进行了非CTO-PCI,33%(14例)术中使用血管内超声(IVUS)指导。
平均透视时间37±14min(范围14–75min),辐射剂量3513±1229mGy(范围1070–5840mGy),造影剂用量208±71mL(范围80–390mL)。
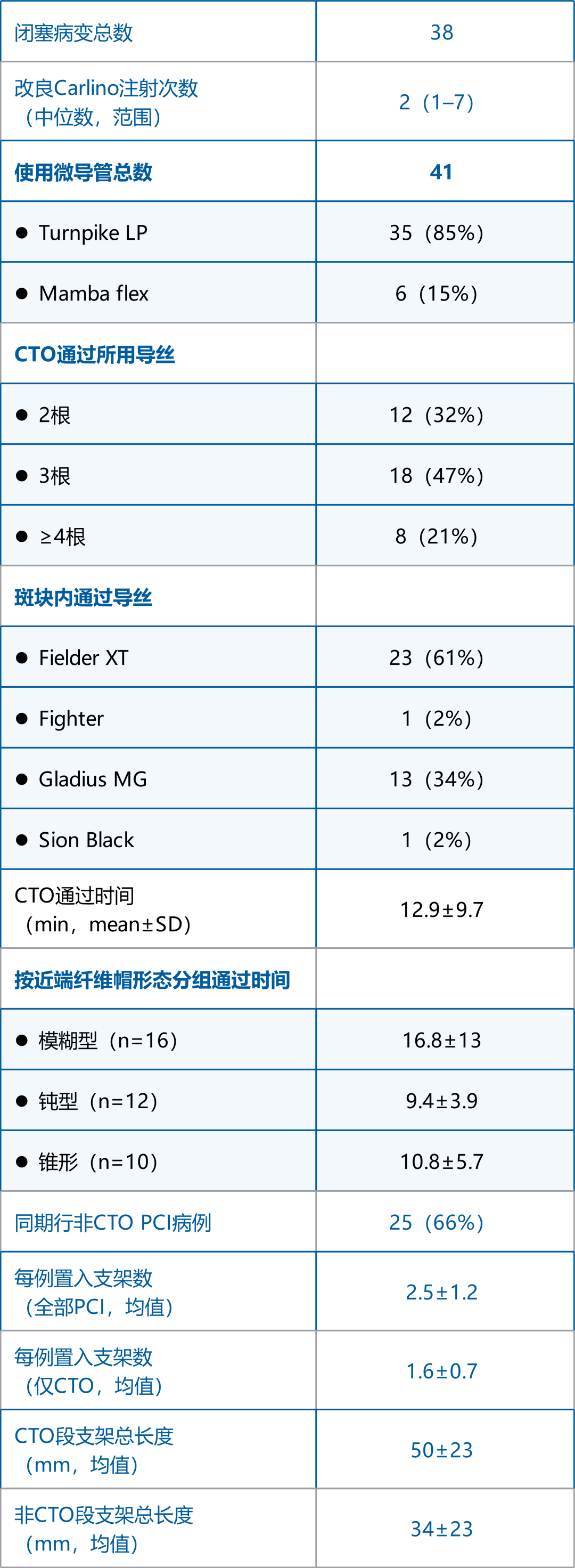
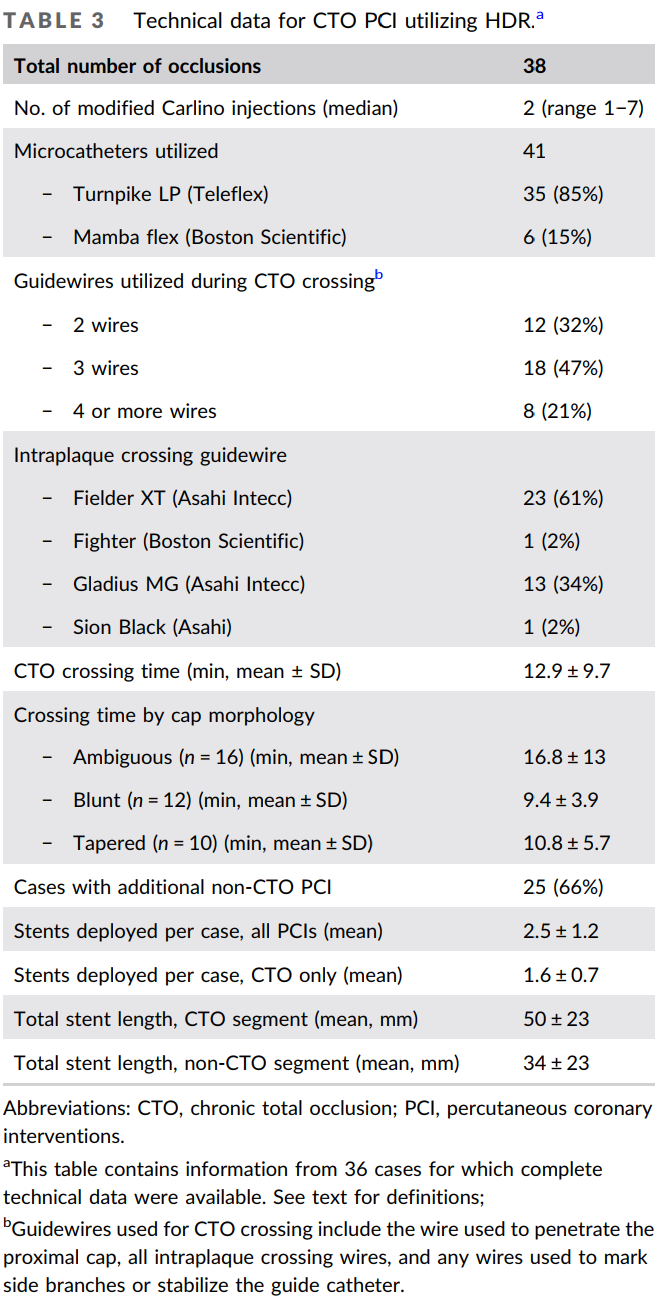
表3基于HDR的CTO PCI技术数据
研究终点
HDR用于治疗43名患者的45处CTO,技术成功率为100%。
无冠状动脉穿孔、心肌梗死、死亡等并发症。
36例有完整导丝通过时间数据:平均通过时间12.9±9.7min,中位数12min。
CTO-PCI所需的中位导丝数为3根(范围2–5根),全程导丝数4根(范围3–7根)。
模糊/钝头近端纤维帽较锥形近端纤维帽,通过时间(10±1 vs. 16.7±3.4min,p=0.04)与手术时间(38.6±2.6 vs. 28.9±2.4min,p=0.02)更长。
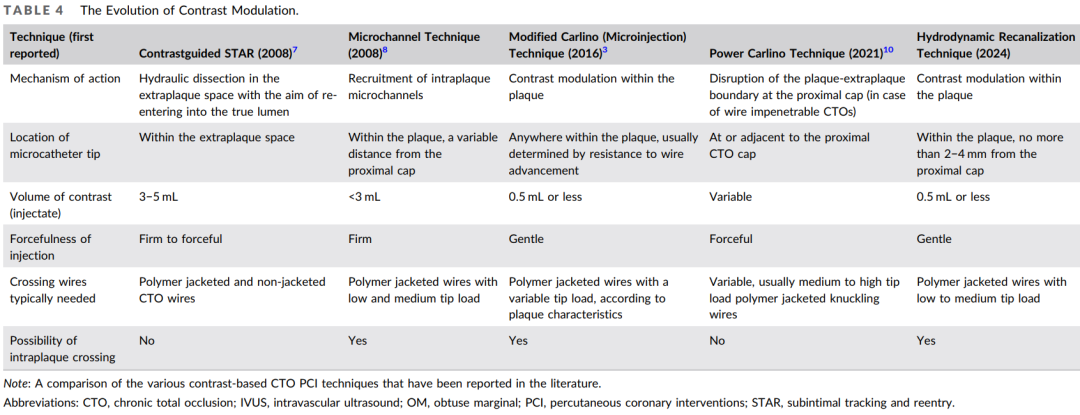
表4造影剂斑块改型技术的演变

07
讨论
本研究首次介绍全新CTO通过策略——HDR。其核心特点:近端纤维帽边界以远斑块内行微量造影剂注射(改良Carlino技术),随后用聚合物涂层导丝开通闭塞病变。
在筛选后的适宜患者中,HDR成功率高、无并发症,无需导丝升级或进入斑块外间隙,侧支保留率高。
IVUS证实所有病例导丝均走行于斑块内。(图3)
这些观察结果表明,HDR是一种有前景的新技术,可能比标准的CTO开通策略具有显著优势。
自Carlino等于2008年首次描述以来,CTO-PCI中造影剂斑块改型技术的作用已经发生了重大演变。
造影剂引导STAR技术(2008):斑块外间隙液压分离,最初的技术被称为造影引导下的内膜下追踪再入(STAR),设计用于术者有意或无意进入斑块外空间之后。它强制性地向内膜夹层平面用力注射大量(3-5mL)造影剂,以创建一个或多个孔洞供导丝再入远端真腔。不幸的是,这种操作在实现血管再入方面不可预测,有可能导致广泛的血管损伤,并且与高再狭窄率相关。注射3–5mL,注射压力大
微通道技术(2008):更精确的穿刺CTO近端纤维帽的方法(以减少进入斑块外空间的机会)和使用适度(<3mL)混合硝酸甘油的斑块内造影剂注射来加以改进他们的技术,其目的是通过冲开CTO内的小血管来为聚合物涂层导丝通过创造路径。注射<3mL,注射压力适中。
改良Carlino技术(2016):后来观察到,即使更小体积的轻柔造影剂注射也能有利地改变斑块特性,从而发展出了微量注射操作,使用微导管在距离近端纤维帽可变距离处向斑块内注射≤0.5mL造影剂。斑块内精准微量注射(≤0.5mL),注射压力轻柔。
强力Carlino技术(2021):球囊锚定辅助造影剂注射。将微导管尽可能推送至近端纤维帽处,在微导管/导丝上方,使用与靶血管管腔1:1大小的球囊充盈,使微导管锚定于血管壁上,通过微导管注射少量造影剂(如0.5mL),球囊的锚定作用使造影剂更集中地作用于近端纤维帽,增强局部压力,从而突破坚硬的纤维帽,破坏近端纤维帽-斑块边界。少量造影剂(如0.5mL),注射压力大。
HDR技术(2024):斑块内改型,微导管距近端纤维帽2–4mm,≤0.5mL轻柔注射,配合低-中穿透力聚合物涂层导丝。
这些形式的造影剂斑块改型与HDR之间的区别在表4中突出显示。
尽管观察性研究中有令人鼓舞的数据表明少量造影剂斑块改型的有效性和安全性,但这种作为CTO-PCI常规策略的方法并未获得广泛接受。这有几个原因,包括源于最初(现已过时)的造影引导STAR技术的血管损伤担忧、对较新的造影剂斑块改型方法不熟悉、微量注射技术缺乏标准化、对该操作在CTO-PCI不同阶段(除近端纤维帽修饰外)的效用认识有限、担心血管破裂限制进一步的开通策略/技术;以及也许最重要的是,对造影剂注射后出现的斑块内染色的不完全理解(可能被误认为是穿孔)。
尽管如此,各种形式的Carlino技术作为辅助操作已在广泛的CTO场景中被报道。目前,CTO-PCI中造影剂斑块改型的主要用途是作为复杂CTO解剖结构的补救策略,以破坏难以穿透的纤维帽和解决血管模糊性的难题。造影剂斑块改型作为早期阶段的首选导丝开通策略的效用尚未被描述。
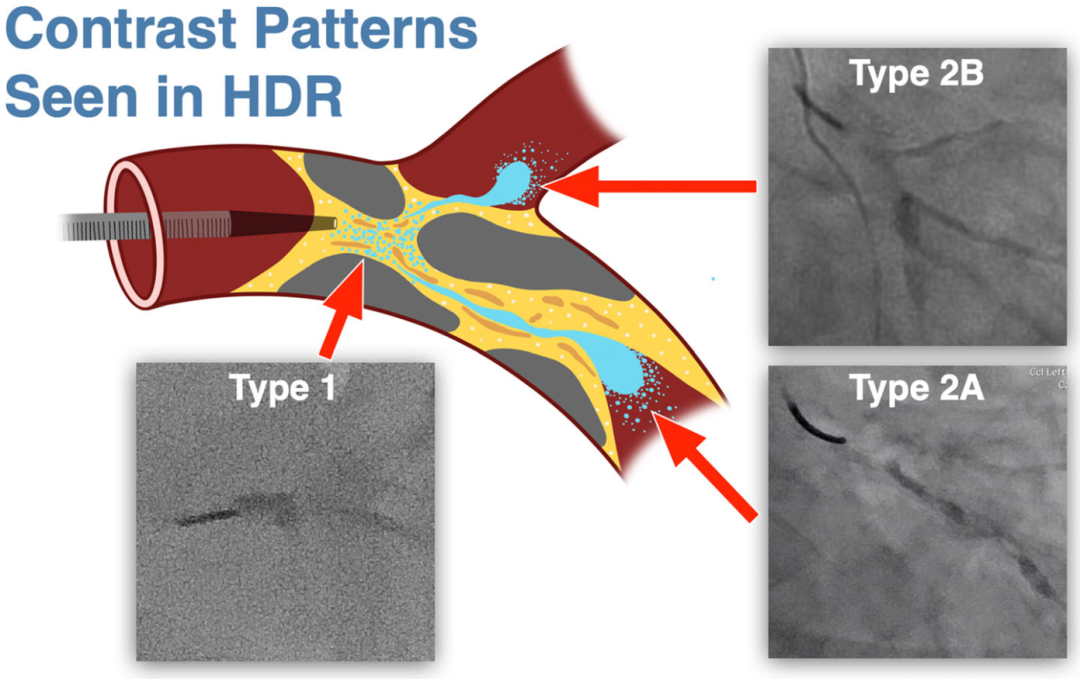
HDR的一个重要方面是识别和解读斑块内造影剂注射后所见的染色。造影剂沉积的外观取决于造影介质与斑块内组织之间的相互作用。根据我们在系列研究中HDR所见染色的形态,确定了三种不同的HDR染色类型(中心示意图):
类型1:具有边缘柔和的斑片状外观,通常在微导管头端附近形成。常见于长(>20mm)闭塞。
类型2:具有更明确(通常是线状)的外观,造影剂末端要么是远端真腔(类型2A),要么是远端侧支(类型2B)。
类型3:兼具类型1和2的形态特征,可见于任何长度和持续时间的闭塞。其起源处呈斑片状,到达远端真腔或侧支时变得更线性、更明确。
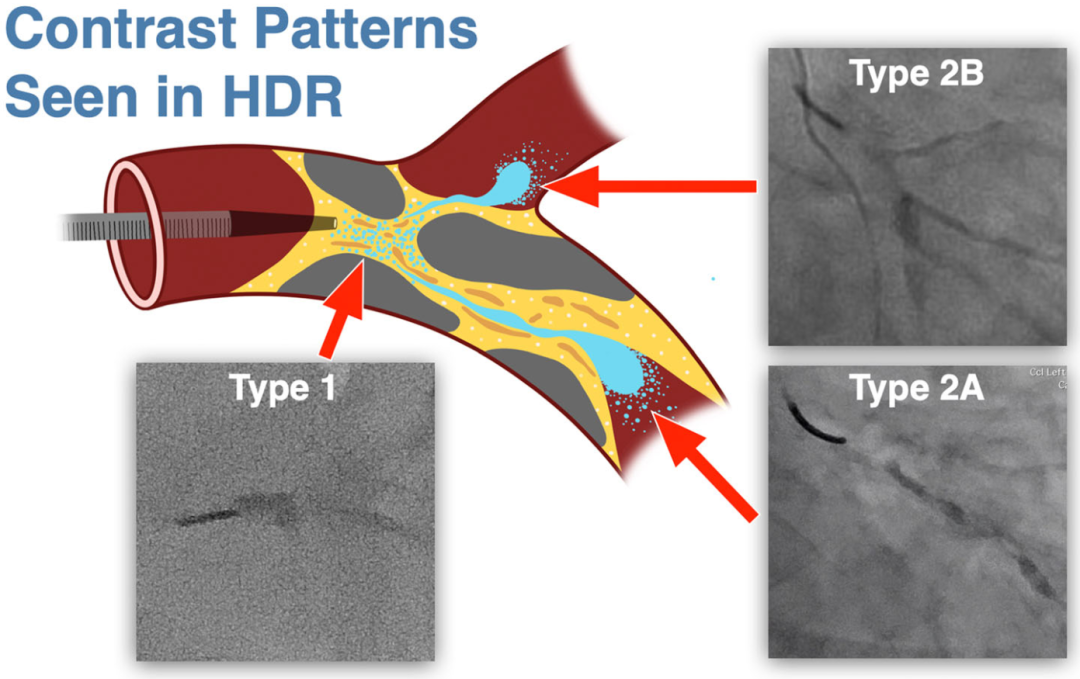
中心示意图 HDR中的造影剂染色类型
图示斑块内注射造影剂后可见的各类染色形态。HDR的潜在机制:冲开斑块内富含脂质的松软区域,形成利于导丝通过的通道。1型:斑片状、边缘柔和,多见于微导管头端附近,常见于长节段(>20mm)闭塞。2A型:线性,终止于远端真腔。2B型:线性,终止于远端侧支。3型:兼具1型与2型特征,近端斑片状,远端连通远端真腔或远端侧支。
HDR的确切作用机制尚待确定。我们推测:
斑片状染色表示造影剂浸润到斑块内富含脂质的松软区域。
线性显影则是当许多相邻的柔软区域被冲开,形成导丝通过的阻力最小路径。
造影剂(机械或化学地)对病变内组织的修饰作用机制得到了以下观察的支持:HDR后的IVUS成像常常显示闭塞斑块内无回声区,但在其近端或远端则没有(图3),从而支持该机制。
与其他开通技术(如前向或逆向导丝升级以及夹层再入)相比,HDR具有多项优势:
操作简单,可快速获取CTO真实长度、斑块成分等关键诊断信息。
多数情况下,HDR后可直接用低穿透力聚合物涂层导丝通过CTO,斑块损伤小。
长段或迂曲病变可按需重复造影剂微量注射。
HDR失败不影响其他CTO-PCI技术使用,反而可有利地修饰斑块,提升其他方法成功率。
支架植入后侧支保留率高(图2),推测因造影剂可同时建立多条斑块内通路,部分与侧支相连(图4),尤其适用于累及主要分支开口的闭塞病变。
本研究中HDR安全性良好,优于早期STAR、微通道技术,与其他通过策略相当。安全性源于改良Carlino技术的操作特点:微量+轻柔注射,压力不足以导致血管穿孔;此外,该操作分步进行,术者可随时停止,以评估微导管头端与造影剂染色形态。HDR学习曲线短,易于掌握推广。
HDR技术的主要优点是:
简单、有效
无需专用设备
适用性广,可用于不同的CTO解剖结构
学习曲线短,不同经验水平术者均可掌握
与其他CTO-PCI策略兼容,可互补使用
研究局限性
本研究为非随机、回顾性病例系列,患者基于解剖适宜性选择性纳入,100%成功率提示存在选择偏倚。
样本量小,无法确定HDR策略可能无效的CTO形态。
缺乏长期临床结局数据,截至投稿时所有患者均存活、症状改善,无再次血运重建。
仅33%病例使用IVUS,限制结果外推。
平均辐射剂量高于当代CTO-PCI,可能与病变/手术复杂程度、射线设置相关,而非HDR技术本身。
本研究为假说生成性研究,HDR的广泛适用性与可重复性,有待更大样本、前瞻性、多中心研究验证。
08
结论
HDR是一种基于造影剂斑块改型原理以促进CTO-PCI中导丝操作的新技术。它为当前CTO-PCI中将造影剂改型从“最后补救手段”转变为早期初始通过策略,是现有理念的重要突破。HDR似乎是一种安全且有前景的新型主要基于造影剂的开通策略,适用于接受CTO-PCI的特定患者。该策略值得在更大规模的前瞻性研究中进一步评估。