
正在进行中的HRS 2026年会突破性研究报道最新发布,无导线起搏从"经静脉起搏备选"迈向"生理性起搏"的技术拐点,已出现人体证据。
研究背景
传导系统起搏(CSP)可维持或恢复接近正常的室间隔激动顺序,减少长期右室起搏相关的心室不同步。左束支区域起搏(LBBAP)因靶区更宽、电参数更优,已成为CSP的主流方向。与此同时,无导线起搏器(LP)技术通过消除导线与囊袋,显著降低了相关并发症。
然而,LBBAP长期依赖经静脉导线系统。无导线器械能否深入室间隔、稳定夺获传导系统,2025年急性期"pass-pull"研究已揭示了该理念的可行性,但依然缺乏慢性植入数据。
LEAP2研究设计
研究类型:前瞻性、单中心、单臂早期可行性研究
地点:捷克布拉格Motol医院
器械:Aveir-CSP(Abbott),较已上市开展应用的AVEIR™ VR相比缩短了机身长度,增设了室间隔固定螺旋及延伸电极(图一)
入组:20例标准起搏适应证患者,经右颈内静脉植入
随访:术前基线CT/超声 → 植入 → 出院前 → 1个月(含CT复查)
主要终点:1个月无严重器械相关不良事件率;电性能(阈值、R波、阻抗)及夺获类型(LBBP/LVSP/DSP)

图一:研究用 无导线CSP与现有器械对比示意 (Aveir-CSP, Abbott公司.)
核心研究结果
植入效率
尝试植入19例,成功18例(95%)
手术时间 36.1 ± 19.5分钟,透视时间10.5 ± 7.2分钟
14例双腔系统均成功建立i2i通信
电学参数稳定性(植入→1个月)

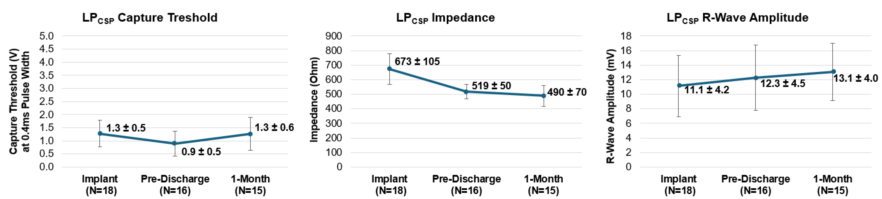
图二: 无导线CSP植入-出院-一个月随访-电学参数趋势
夺获类型的动态演变

6例(40%)发生夺获类型转换,主要与电极-室间隔界面微位移相关。CT显示:LBBP组电极尖端距左室心内膜平均2.3mm(占室间隔厚度81%),DSP组则为6.4mm(40%),穿透深度与夺获质量显著相关。
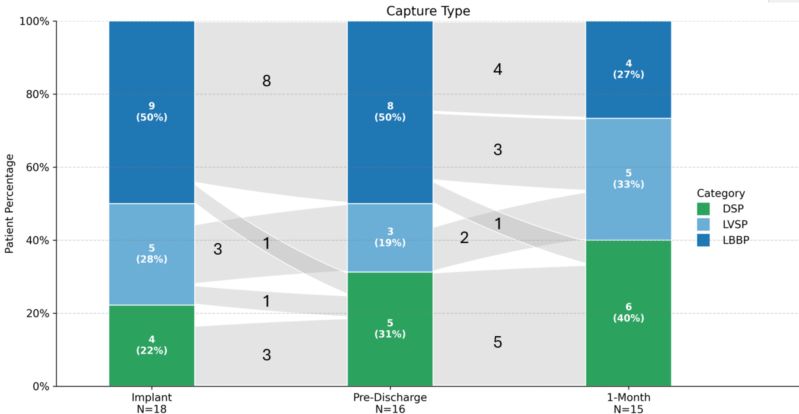
图三:夺获类型演变示意。植入时、出院前和1个月随访时LBBP、LVSP和DSP患者的百分比,不包括已脱位装置。线条表示每次随访之间夺或类型的一致性或变化。
双腔i2i通信
1个月时RV→RA/RA→RV数据互通中位数均为100%
无AV同步不良相关症状
安全性
1个月无并发症率:68.4%
3例术后器械脱位(2例出院前,1例1个月时),均经皮回收后改植入传统无导线起搏器
无室间隔穿孔、无死亡、无系统感染
核心技术解读
1.器械设计的差异化突破
与已上市展开应用的AVEIR™ VR相比,LP CSP的核心改进在于:
缩短设备长度:减少右室腔内占位
远近双螺旋固定:近端螺旋锚定室间隔,远端延伸电极深入心肌
延伸电极:实现深部室间隔穿透,电极为远端螺旋-近端机身间双极配置
这一设计使无导线器械首次具备慢性深部心肌穿透+传导系统夺获的能力。
2.颈内静脉入路的可行性验证
全部病例经右颈内静脉植入,手术时间与经股静脉常规无导线起搏器相当,为解剖入路选择提供了新选项。
3.夺获稳定性的待解问题
40%的夺获类型转换率提示:深部电极-心肌界面在心脏搏动和心肌回缩作用下存在动态变化。无导线CSP 需深入穿透室间隔以实现传导系统夺获,其固定策略与常规的无导线起搏器及目前的经静脉导线系统均有差异,早期回缩脱位或与学习曲线相关;期待进一步观察数据和设备研发改进结果。
4.脱位风险的学习曲线特征
3例脱位的回顾性分析显示,均与早期操作经验相关:
鞘管回退导致支撑不足
植入过深后反旋松脱
Tether模式意外牵拉
这与已上市的第一代无导线起搏器(Nanostim/Micra/AVEIR™)的应用轨迹比较一致:早期脱位率偏高,但随器械迭代和术者经验的积累将显著下降。
临床意义与前瞻
LEAP2首次在人体中证实:无导线器械可实现慢性传导系统夺获,且电参数稳定、双腔通信可靠。这标志着无导线起搏从"消除导线并发症"的功能性替代,向"恢复生理性激动"的疗法升级迈出关键一步。
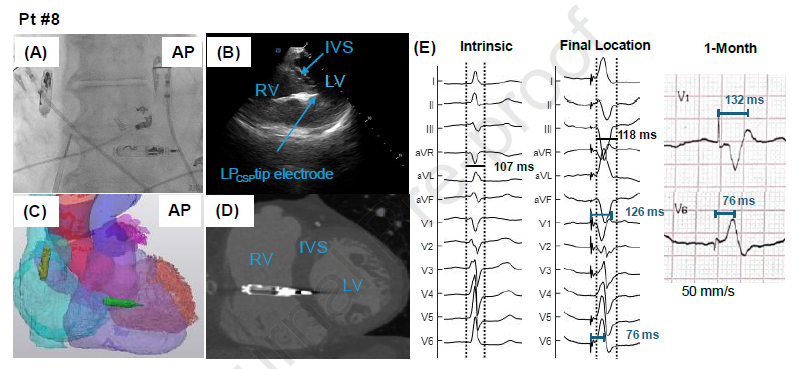
图四:典型病例pt#8 手术影像和心电图

图五:典型病例pt#7 手术影像和心电图
当前数据仍处于早期可行性阶段,样本量小、随访短、脱位率偏高。但方向已经明确:无导线+CSP的融合,有望为需要生理性起搏但存在导线禁忌或高风险的患者提供全新选择。
仍需持续关注:
器械固定机制的迭代优化
更大样本、更长随访的验证
亚洲及中国人群的解剖适应性评估
文献来源
Reddy VY, et al. LEAP2: A First-in-Human Evaluation of a Chronically-Implanted Novel Leadless Pacemaker for Conduction System Pacing. Heart Rhythm. 2026. DOI: 10.1016/j.hrthm.2026.04.014