
在过去,房颤消融的核心问题是:
这台手术能不能做?
而现在,问题已经变成:
这个患者,适合怎么做?
随着房颤导管消融成为一线治疗,患者结构正在发生明显变化——
高龄、合并基础疾病、器官功能储备下降,正在成为常态。
在这样的背景下,能量选择不再只是“术者习惯”,而是一次围绕患者风险的系统决策。
当一台房颤消融手术的规划从“如何做”转向“为谁做”,能量选择便不再只是技术问题,而成为一门关于风险与获益平衡的精准决策。
在电生理门诊中,我们正在面对一类越来越典型的患者:高龄、合并多系统疾病、器官储备功能下降。随着导管消融成为房颤一线治疗手段,射频、冷冻以及脉冲场消融(PFA)三种技术并存,如何基于“患者特征”做出更合理的选择,正成为临床关注的重点。
一种值得参考的思路是:
从“技术能做什么”,转向“患者更难承受什么风险”。
大脑的隐形风险:沉默性脑损伤与微栓塞
在房颤消融中,沉默性脑栓塞事件(SCE)逐渐受到关注。这类病灶通常无明显临床症状,但在MRI中可以被发现,可能与长期认知功能变化相关。
关键风险因素:器械交换次数。
研究显示,不同消融技术在SCE发生率上存在差异。Michifumi Tokuda1 等人的研究提示,不同能量形式及操作流程复杂度可能影响脑栓塞风险,而导管交换等操作被认为是潜在影响因素之一。

在 Vivek Y Reddy 主导的ADVENT2试验中,亚组分析显示,PFA组的SCE发生率达9.1%,而传统温度消融组为0%。
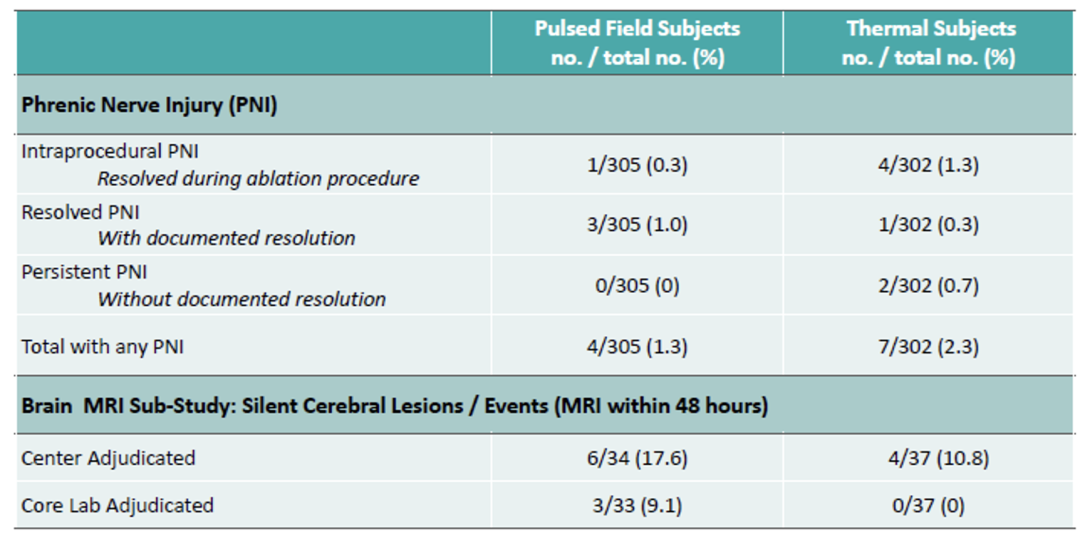
临床启示:在脑血管高风险人群中,减少不必要的器械操作、优化手术流程,可能是重要考量因素。
冷冻消融的“一体化”解决方案:
Nordica系统配合Navigo双向可调弯鞘管,能够一鞘两用,直接完成房间隔穿刺后引导左房导管操作,减少至少1次鞘管交换

适合冷冻的患者画像:
既往脑卒中/TIA病史
轻度认知功能下降
高龄患者(>75岁)
颈动脉粥样硬化明显
脆弱心脏:当安全边际变得尤为关键
心力衰竭患者的心脏结构与功能均处于“边缘状态”,对并发症的耐受能力明显下降。
在ADVENT试验中曾报告个别严重并发症2(如心脏压塞等),提示任何能量形式在复杂患者中均需谨慎选择与操作。
从机制上看,不同能量形式在组织损伤方式上存在差异:
热消融:以温度改变为主
冷冻消融:低温诱导细胞损伤,同时相对保留组织结构
PFA:通过电场作用导致细胞膜不可逆电穿孔
临床启示:在心功能较差患者中,选择“可控性更强、边界更清晰”的消融方式,可能更具意义。
顺应性冷冻球囊为心衰患者提供多重保护:
渐进式损伤:缓慢降温,医生有充足时间观察反应
结构保留:在杀死心肌细胞的同时,最大程度保留细胞外基质,降低穿孔风险
可逆性测试:-30℃左右冷冻标测,出现不良反应可立即回温恢复,组织功能可恢复正常
适合冷冻的患者画像:
左室射血分数(EF)<40%
明显心脏扩大
既往心衰住院史
麻醉策略:当“能不能麻醉”成为前提
在实际临床中,部分患者因基础疾病无法耐受全身麻醉,例如严重呼吸功能不全、困难气道或重度阻塞性睡眠呼吸暂停(OSA)。
目前多数中心在开展PFA时仍倾向于全身麻醉或深度镇静,以保证操作稳定性;而部分传统消融方式在镇静或局麻条件下亦可完成。
临床启示:麻醉方式不只是流程问题,而是部分患者能否接受治疗的前提条件。
适合冷冻的患者画像者:
严重OSA
呼吸功能不全
困难气道
麻醉药物不耐受
冠状动脉:一个容易被忽视的风险点
近年来有研究和临床观察提示,PFA在特定情况下可能诱发冠状动脉痉挛,其机制可能与高电场对血管平滑肌或自主神经的刺激有关,但仍处于研究阶段。
对于已有冠状动脉疾病的患者,这种风险显著增高:
冠心病患者:血管内皮功能不全,对刺激反应性更强
支架术后患者:痉挛可能发生在支架边缘,极难处理
多支病变患者:一旦发生痉挛,后果极为严重
冷冻消融通过低温导致细胞凋亡,其能量以“冷传导”方式缓慢扩散,不会引发血管平滑肌的异常电兴奋,从根本上避免了电刺激诱发的痉挛。
临床启示:当治疗区域邻近重要结构(如冠脉)时,应更加关注能量形式的“外溢效应”。
适合冷冻的患者画像:
冠心病患者
冠脉支架术后
多支血管病变
冠脉痉挛病史
解剖差异:当“标准方案”不再适用
肺静脉解剖的多样性,是房颤消融中长期存在的挑战。
研究显示,不同球囊设计在肺静脉前庭接触方式上存在差异。Liao Y 3等人的影像学研究提示,较大直径球囊在部分解剖结构中可增加接触面积,但其对长期疗效的影响仍需进一步验证。
同时,Kenneth A Ellenbogen4 等人的研究表明,新一代球囊在封堵效率方面具有一定改进。
临床启示:解剖适配性,正在成为影响手术效率和效果的重要因素之一。

适合冷冻的患者画像:
肺静脉共干
前庭宽大
解剖变异明显
既往消融后复发
技术选择的“决策矩阵”:从患者特征到能量匹配
基于上述分析,构建了房颤消融能量选择的临床决策矩阵:
患者特征 | 优先推荐 | 关键理由 | 风险规避 |
脑血管病史/认知障碍 | 冷冻 | 穿刺一体化设计减少器械交换 | 沉默性脑损伤(SCE) |
心衰/低EF值 | 冷冻 | 结构保留,渐进损伤 | 心脏穿孔/压塞 |
麻醉高风险 | 冷冻 | 镇静即可 | 麻醉相关并发症 |
冠状动脉疾病 | 冷冻 | 无电刺激 | 冠脉痉挛 |
当患者合并2项及以上高危特征时,冷冻消融的综合安全边际优势将更加明显。
结语
房颤消融已经进入一个更加精细化的阶段。
技术的进步固然重要,但真正决定治疗质量的,往往是对“患者整体状况”的理解与尊重。
最优的能量选择,并不一定是最新的技术,而是最适合当前患者风险结构的方案。
当临床决策从“征服疾病”走向“保护患者”,
消融治疗的价值,才真正得以体现。
参考文献:
[1] Michifumi Tokuda, et al. Cerebral embolism during catheter ablation of atrial fibrillation. J Cardiovasc Electrophysiol, 2022.
[2] Vivek Y Reddy, et al. Pulsed field or conventional thermal ablation for AF. NEJM, 2023.
[3] Liao Y, et al. PV antrum contact area with dual-sized cryoballoon. Heart Rhythm, 2024.
[4] Kenneth A Ellenbogen, et al. FROZEN AF trial. J Cardiovasc Electrophysiol, 2024.