

复旦大学附属中山医院心内科黄浙勇教授
思辨介入困境
解析手术技巧
梳理中山经验
助您从新手变“心”手
每月15日、30日,严道医声独家发布
CTO成功开通,造影突然发现造影剂外渗,该是怎样的过山车心情?
但外渗并不一定是介入相关性冠脉穿孔,心肌梗死(MI)区域由于微血管毁损并发心室瘘并非个例。因此,究竟是冠脉穿孔还是心室瘘?是个问题。PCI相关穿孔属于急危重症,需要紧急封堵和心包穿刺;而MI心室瘘属于慢性并发症,一般保守治疗即可!把“瘘”当“穿孔”,将过度封堵!把“穿孔”当“瘘”,将延误抢救(图1)。

图1心室瘘接受不必要的弹簧圈栓塞治疗。
A前降支CTO开通后,发现分支血管局部造影剂外渗(圆圈),考虑冠脉穿孔;B立即经微导管弹簧圈封堵(箭头),但渗漏仍然存在(圆圈),且超声心动图未发现心包积液。修正诊断为心室瘘,反思介入封堵并非必须。
2021年我们曾总结MI心室瘘的临床特征[1],本文再次归纳整理其鉴别要点(表1)。
表1 MI心室瘘和冠脉穿孔的鉴别诊断
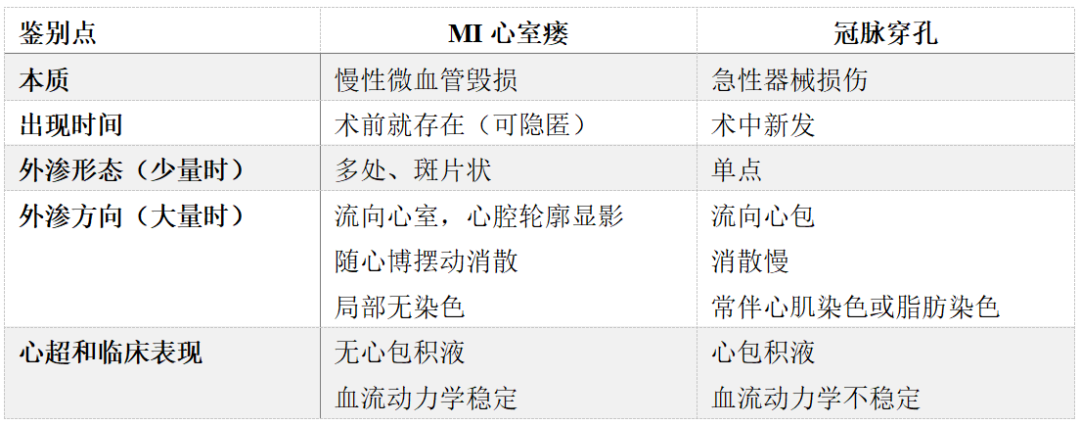
一
超声和临床表现
这是最重要、最优先的判断维度。MI心室瘘不会导致心包积液和心包填塞,不产生急性血流动力学障碍症状。若分流量大,可增加心脏容量负荷,可闻及连续性或收缩期杂音。相比之下,PCI冠脉穿孔属于急性危重并发症,可在短时间内导致心包积液及心包填塞,表现为低血压、晕厥等血流动力学不稳定状态,需紧急处理。
当术中无法立即鉴别时,应优先按冠脉穿孔处理。可采用球囊临时封堵,并严密检测生命体征和床旁心超变化。一旦确认冠脉穿孔,准备永久性封堵(覆膜支架/弹簧圈)和心包穿刺。若患者始终血流动力学稳定且无心包积液,则应结合造影表现和动态心超进一步判断(图2)。
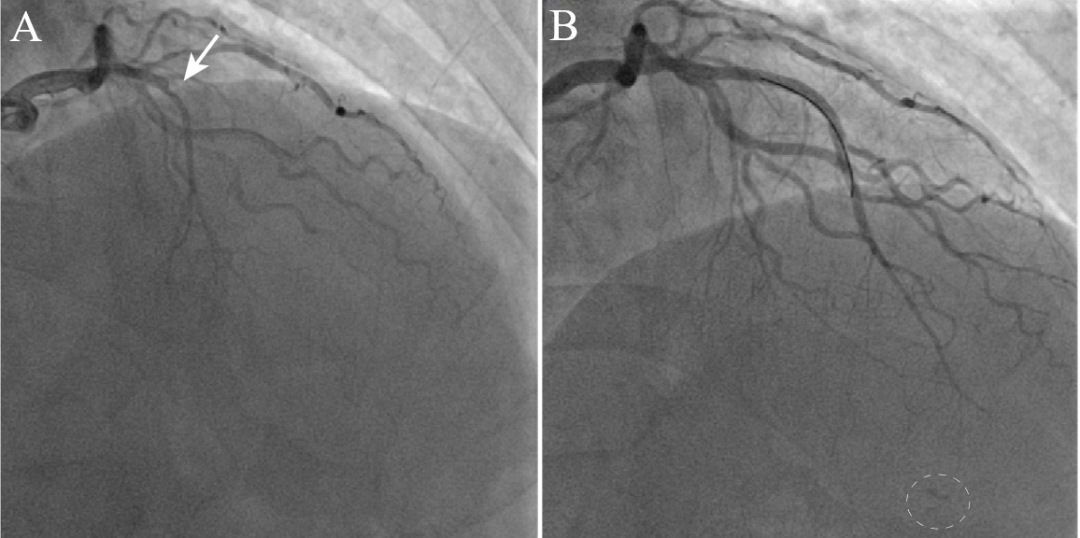
图2 超声鉴别心室瘘和冠脉穿孔。
60岁男性,前降支CTO病变(A,箭头),开通后出现前降支末梢造影剂少量外渗,极似导丝穿孔(B)。由于术中导丝操控良好,未推送过远,故考虑心室瘘,但不敢肯定。即刻及术后多次复查超声均未见心包积液,最终确诊MI心室瘘。
二
形态和方向
“冠脉瘘”和“冠脉穿孔”本质都是血管破裂,但由于病理基础不同,导致造影表现具有显著差异。
MI心室瘘源于梗死区微血管广泛毁损,造影表现多为区域性、斑片状、多发性渗漏(图3)。而冠脉穿孔为器械导致的单点破裂,破口位置通常与导丝或球囊损伤部位一致。

图3 MI心室瘘的血管造影特征:弥散呈斑片状,往往多发。
(A–C)右冠CTO开通后渗出;(D,E)前降支CTO开通后渗出;(F)回旋支CTO开通后渗出。
如分流量大,外渗方向也可成为鉴别点。心室瘘直接进入左室或右室,甚至可见心腔轮廓显影(图4),而且随心动周期博动而迅速冲刷(washout),局部无造影剂潴留和染色。由于瘘管本身属于慢性通道,因此也无造影剂染色/潴留。相反,大量冠脉穿孔时外渗方向是进入心包,呈喷射状进入或者呈墨水样向四周弥散,导致心包内造影剂/血液蓄积,若积聚于心肌内或心外膜下表现为心肌染色或脂肪染色。

图4 MI心室瘘造影剂外渗进入右心室。
75岁女性,陈旧性前壁心肌梗死。造影提示前降支近段闭塞(A),开通后发现大量造影剂进入右心室,可见右心室轮廓显影,证实为心室瘘。
为何MI冠脉瘘与心腔相连,而穿孔一般与心包相通?理论上急性MI后微血管破裂可导致三种结局:局部血肿、向心腔破裂、或向心包破裂。但局限性血肿容易吸收,破入心包者难以存活,经自然选择后能存活到OMI/CTO阶段,只能是冠脉-心室瘘患者!而介入器械接触的冠脉较为粗大,一般位于心外膜下,因此几乎均渗漏至心包,少数可局限于心肌内。
三
出现时间(基线对比)
心室瘘由MI所致,在冠脉介入前已经存在;而冠脉穿孔由介入器械损伤所致,在介入术中出现。因此,只要有清晰的介入前基线冠脉造影,鉴别诊断不是问题(图5)。强烈建议CTO病变介入前行指引导管双侧冠脉造影,这不仅有利于高效安全的开通CTO,也有助于识别潜在的心室瘘,从而避免术后误判。问题是,由于梗死区域血供缺乏,心室瘘在基线造影中表现不典型或难以显影(隐匿型),这是临床误判的重要原因之一(图6)。
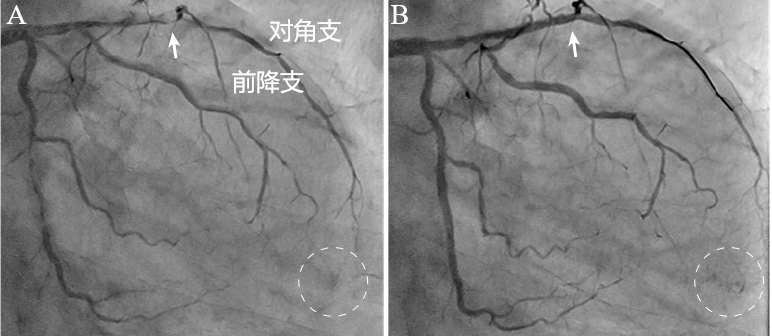
图5 基线造影对比证实心室瘘。
60岁男性,陈旧性MI,心尖部室壁瘤形成。造影提示前降支中段狭窄95%,前降支远段纤细,对角支粗大(A)。前降支-对角支置入支架,术后发现前降支远段分支部位造影剂外渗,怀疑“穿孔”(B,圆圈)。对比发现基线造影业已存在外渗现象(A,圆圈),证实MI心室瘘诊断,避免了不必要的介入封堵。
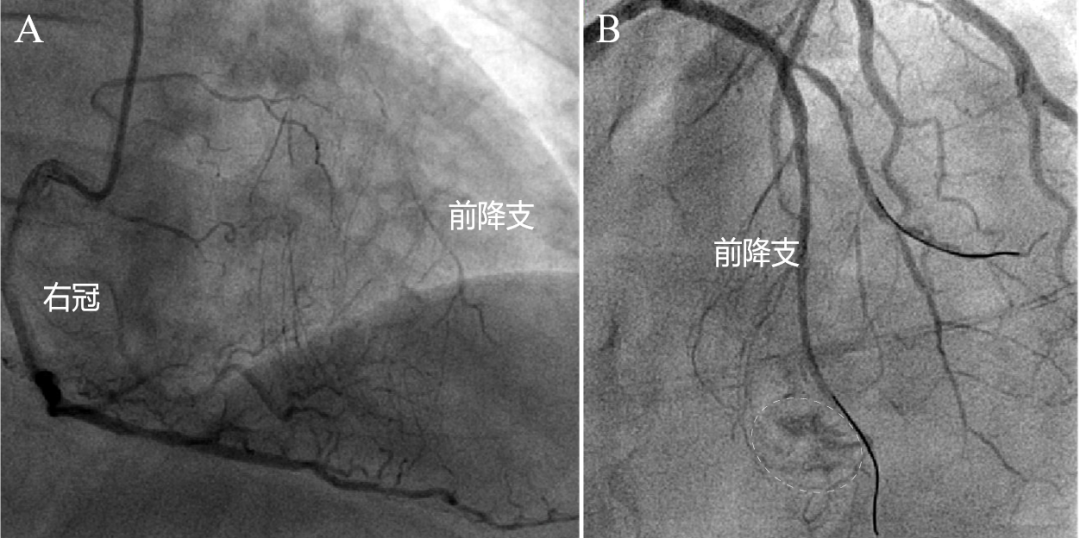
图6 基线造影难以发现心室瘘。
72岁男性,陈旧性前壁心肌梗死,前降支CTO,右冠为前降支提供侧枝,但术前未发现心室瘘(A)。成功开通前降支CTO后,发现前降支远段心室瘘,呈现斑片状造影剂外渗(B,圆圈)。
偶尔的,冠脉穿孔和心室瘘并存,其鉴别诊断显得尤为重要(图7)。

图7 心室瘘和穿孔并存。
79岁女性,前降支近端CTO病变(A,箭头)。前向开通后IVUS示前降支全程弥漫性壁内血肿形成,近中段植入支架,复查造影示支架外远段闭塞(B)。1.5mm小球囊半扩张回拉切割血肿,远段血流恢复(C)。术后1.5h患者突发低血压晕厥,心超示9mm心包积液,心包穿刺引流。回顾最后造影,发现2处造影剂微量外渗:前降支远段附近二点渗出(图D,椭圆形虚线)、前降支末梢段单点渗出(图D,方形虚线)。其中后者存在造影剂潴留(心肌染色)(图E,方形虚线)。综合评估后考虑远段为心室瘘,末梢段为穿孔。弹簧圈只封堵末梢段穿孔(F),心包积液量未再增加。
四
小结
CTO开通后出现造影剂外渗,是“心室瘘”还是“冠脉穿孔”?可遵循“三步法”进行鉴别(图8):先看“命”:血流动力学是否稳定,是否存在心包填塞;再看“像”:外渗形态、方向及是否伴造影剂滞留;最后看“史”:基线造影是否已有类似表现。总体原则是优先排除冠脉穿孔以避免延误抢救,同时警惕将心室瘘误判为穿孔导致过度治疗。
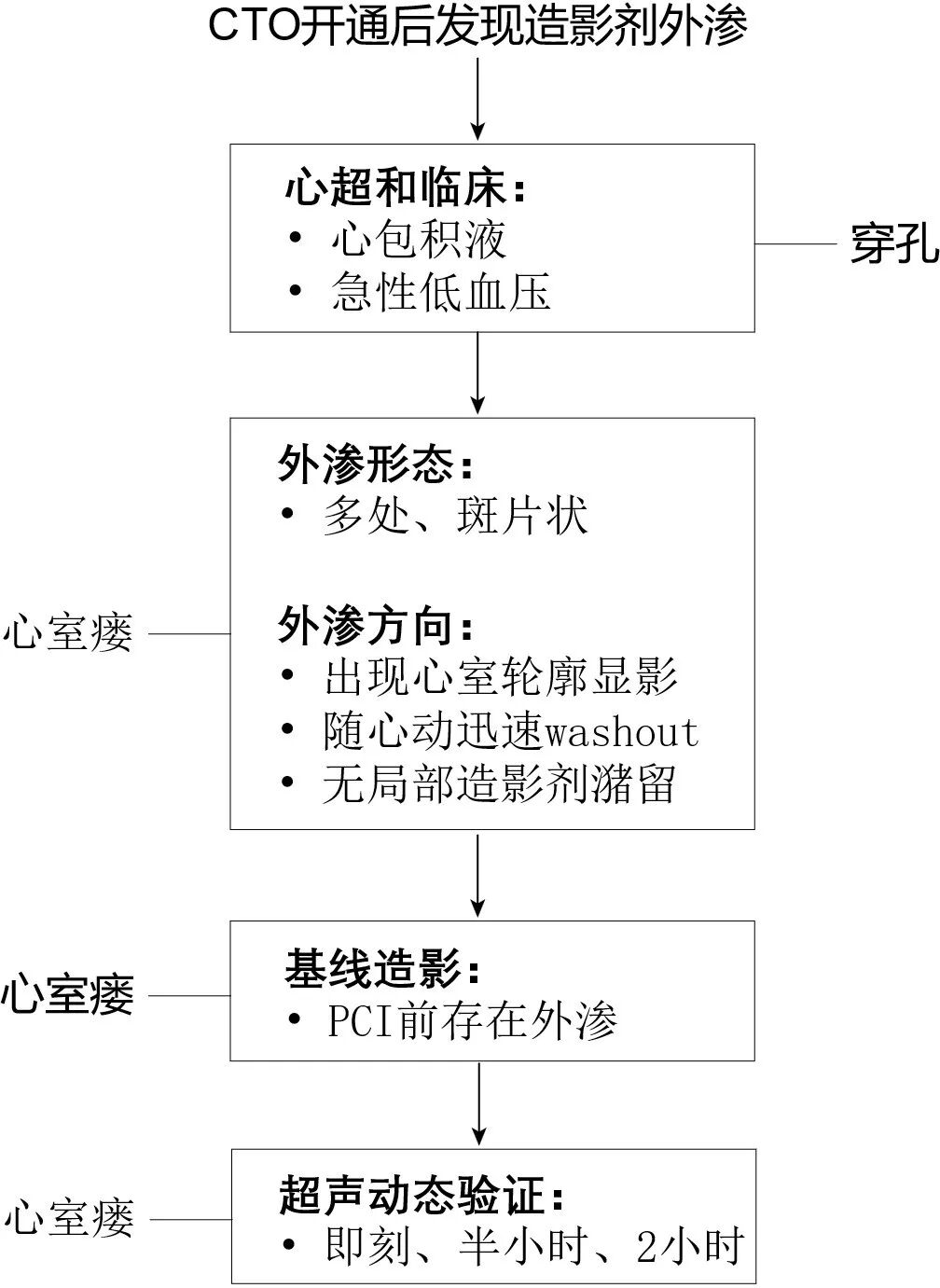
图8 CTO开通后造影剂外渗的鉴别诊断流程图
参考文献:
1. Fan, R., H. Tan, Y. Song, et al., Prevalence and Characteristics of Acquired Coronary Fistulas After Successful Revascularization of Chronic Total Occlusion. Front Cardiovasc Med, 2021. 8: 690890.
“中山PCI解码”下期预告
Knuckle导丝技术的潜在风险
很多介入医生喜欢将导丝Knuckle后潇洒的快速推进。knuckle操作是双刃剑,操作正确是大师,操作错误是魔鬼。对于非CTO病变, Knuckle导丝暴力操作可诱发血管夹层甚至闭塞。


