

动脉粥样硬化性心血管疾病(ASCVD)患者属于心血管事件高风险或极高风险人群,低密度脂蛋白胆固醇(LDL-C)是血脂异常管理的核心靶点,强化降低LDL-C水平是该类患者的重要治疗原则。近年来,血脂管理指南已将ASCVD患者的LDL-C推荐目标从<70mg/dL(1.8mmol/L)下调至<55mg/dL(1.4mmol/L),但针对这一更严格目标获益的证据仍较为有限,临床实践中指南推荐与实际执行也存在明显差距。
在美国心脏病学会年会(ACC.26)上作为最新临床研究(Late-Breaking Clinical Trials)发布,并于2026年3月28日发表于《新英格兰医学杂志》(NEJM)的Ez-PAVE试验(Effects of Ezetimibe Combination Therapy for Patients with Atherosclerotic Cardiovascular Disease — Randomized Comparison),通过头对头比较两种LDL-C目标管理策略对ASCVD患者的影响,为血脂强化达标提供了高质量的循证医学证据,再次印证了对ASCVD患者实施更严格LDL-C目标管理的必要性与可行性。

一、血脂管理目标争议,亟需高质量循证证据
现有指南虽推荐ASCVD患者将LDL-C控制在<55mg/dL,但这一推荐多基于降脂药物疗效的研究,而非直接对比不同LDL-C目标获益的试验。既往随机对照试验主要评估高强度他汀类药物,或他汀联合依折麦布、前蛋白转化酶枯草溶菌素9(PCSK9)抑制剂等降脂方案的效果,证实了强化降脂可降低LDL-C并减少心血管事件风险,但这类研究的核心是验证药物疗效,而非明确具体的LDL-C目标数值。
此前针对缺血性卒中或短暂性脑缺血发作患者的TST试验,虽证实了更低LDL-C目标的心血管获益,但其对比的是<70mg/dL与90~110mg/dL的目标,并非当前指南关注的<55mg/dL与<70mg/dL的对比,无法为最新指南推荐提供直接证据。临床中,ASCVD患者达到<55mg/dL目标的比例不足25%,依折麦布、PCSK9抑制剂等非他汀类药物的使用率也极低,指南推荐与临床实践的脱节,核心原因之一便是缺乏直接对比两种核心目标的高质量研究。
在此背景下,韩国学者开展的Ez-PAVE试验应运而生,该试验旨在明确对于ASCVD患者,将LDL-C目标设定为<55mg/dL是否优于<70mg/dL。
二、研究设计
Ez-PAVE试验是一项由研究者发起的多中心、开放标签、随机优效性试验,研究全程在韩国17个中心开展。
(一)研究人群
研究纳入19~80岁确诊ASCVD的患者,ASCVD的定义为存在以下至少一种疾病:既往急性冠脉综合征(心肌梗死或不稳定型心绞痛)、经影像学或功能检查证实的稳定型心绞痛、冠状动脉或其他动脉血运重建史、卒中或短暂性脑缺血发作、外周动脉疾病。
关键排除标准为未接受他汀治疗时LDL-C已<70mg/dL。
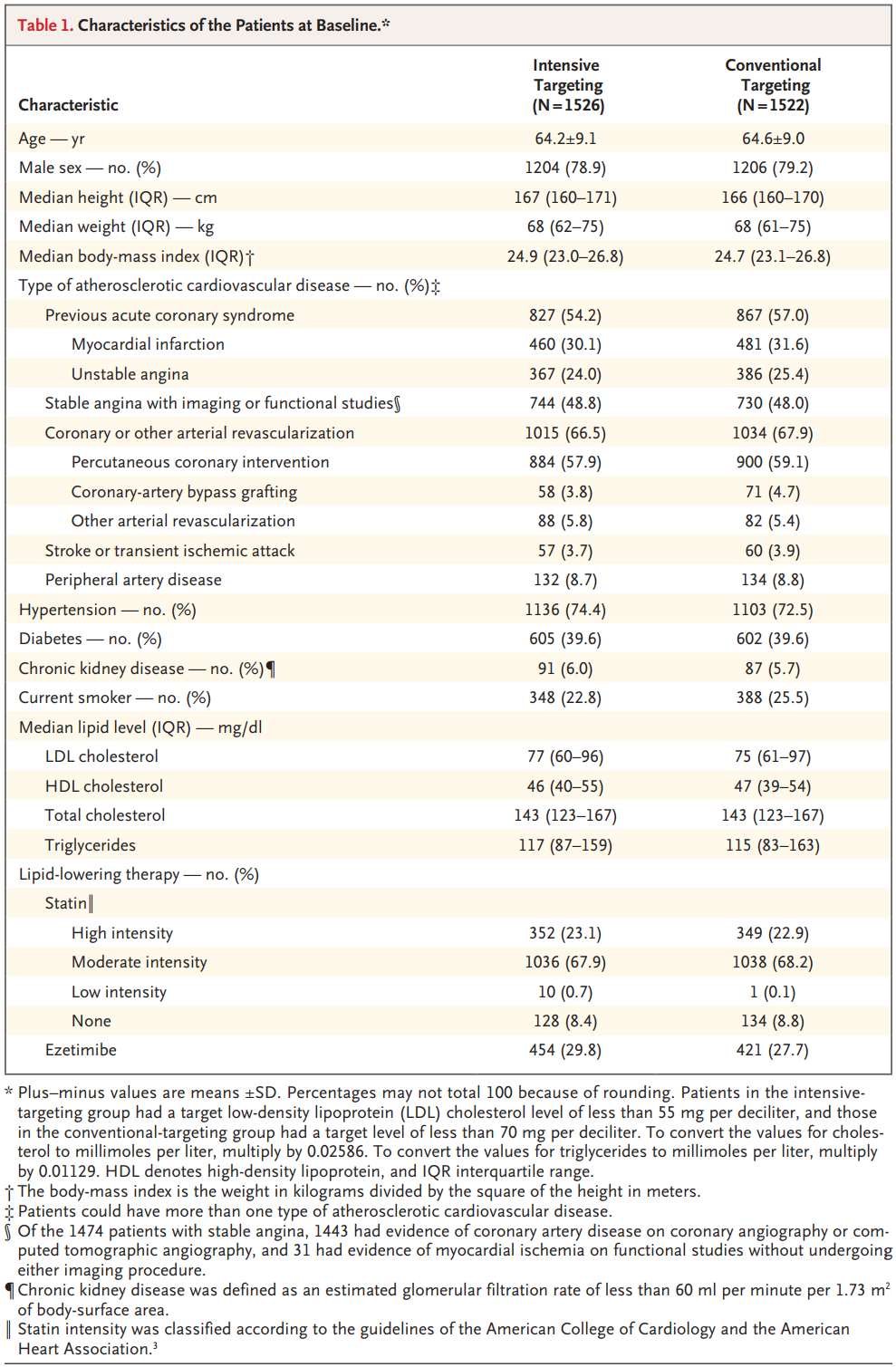
最终共3048例患者完成随机化,其中1526例分配至强化目标组(LDL-C<55mg/dL),1522例分配至常规目标组(LDL-C<70mg/dL)。两组患者基线特征高度均衡,无显著差异:平均年龄64.4±9.0岁,女性占20.9%,中位基线LDL-C为76mg/dL(四分位距61~96mg/dL,2.0mmol/L);基线时两组患者他汀类药物(高强度占23.0%、中等强度占68.1%)、依折麦布的使用率也基本一致(表1)。
(二)随机化与治疗方案
研究采用网络响应系统进行1:1比例随机化,基于既往急性冠脉综合征史(是/否)、糖尿病史(是/否)、基线LDL-C水平(<100mg/dL或≥100mg/dL)进行分层。
为了及时达到指定LDL-C目标并平衡他汀类药物的使用,所有患者在目标随机化后,还进行了二次1:1随机化:分为他汀单药治疗组或他汀联合依折麦布治疗组;他汀单药治疗组进一步1:1随机化,使用瑞舒伐他汀或阿托伐他汀,联合治疗组则均使用瑞舒伐他汀联合依折麦布。
研究者为降脂治疗提供了基础指导原则,降脂药物的强度分类遵循ACC/AHA指南及既往依折麦布相关试验数据。随机化后,患者根据分配的目标组和基线LDL-C水平接受降脂治疗,随访期间根据需要调整药物剂量,优先增加他汀剂量并加用依折麦布,再考虑使用PCSK9抑制剂。
虽有基础指导原则,但治疗决策(如他汀剂量调整、是否加用依折麦布或PCSK9抑制剂)最终由经治医师决定,并详细记录决策依据。
(三)随访与终点指标
患者的随访评估在基线、随机化后1个月、1年、2年、3年进行,每次随访均评估一般健康状况、用药情况、终点事件或不良事件发生情况,并检测血脂谱(包括LDL-C),安全相关的实验室检查在预设时间点完成,患者的生存状态通过韩国国民健康保险数据库交叉验证。
主要终点为随机化后3年内的复合终点,包括心血管原因死亡、非致死性心肌梗死、非致死性卒中、任何血运重建、因不稳定型心绞痛住院。
次要终点分为疗效终点和安全终点:疗效终点包括主要终点的各单独组分,以及心血管原因死亡、非致死性心肌梗死、非致死性卒中的复合终点等;安全终点包括基线无糖尿病患者的新发糖尿病、基线有糖尿病患者的血糖控制恶化、导致治疗剂量或方案改变的他汀相关肌肉症状、癌症诊断、白内障手术,以及转氨酶、肌酐、肌酸激酶水平升高。所有心血管事件、新发糖尿病、血糖控制恶化均由对试验分组和LDL-C水平不知情的独立临床事件委员会判定,其他安全终点通过不良事件数据和实验室检查结果评估。
三、研究结果
研究的中位随访时间为3.0年,期间有3.6%(110名,;强化目标组62名,常规目标组48名)的患者未达到目标却停用或下调降脂治疗强度(其中主要原因为不良事件的有85名患者,占2.8%;强化目标组50名,常规目标组35名),14名患者(0.5%)撤回知情同意,5名患者(0.2%)失访。
(一)降脂治疗实施情况
两组患者的降脂药物使用强度存在显著差异,且这种差异在随访期间持续存在。1个月时,强化目标组使用高强度他汀的患者比例为53.5%,显著高于常规目标组的35.9%;随访3年时,强化目标组高强度他汀使用率仍达48.4%,常规目标组为32.3%。
依折麦布的使用率在两组基线时相近,随访期间强化目标组持续升高:1个月时为49.7%,3年时升至66.6%;常规目标组1个月时为50.0%,3年时为56.7%。
PCSK9抑制剂的使用率在两组中均较低,但强化目标组略高:3年时强化目标组为2.3%,常规目标组为0.9%。
(二)LDL-C达标情况
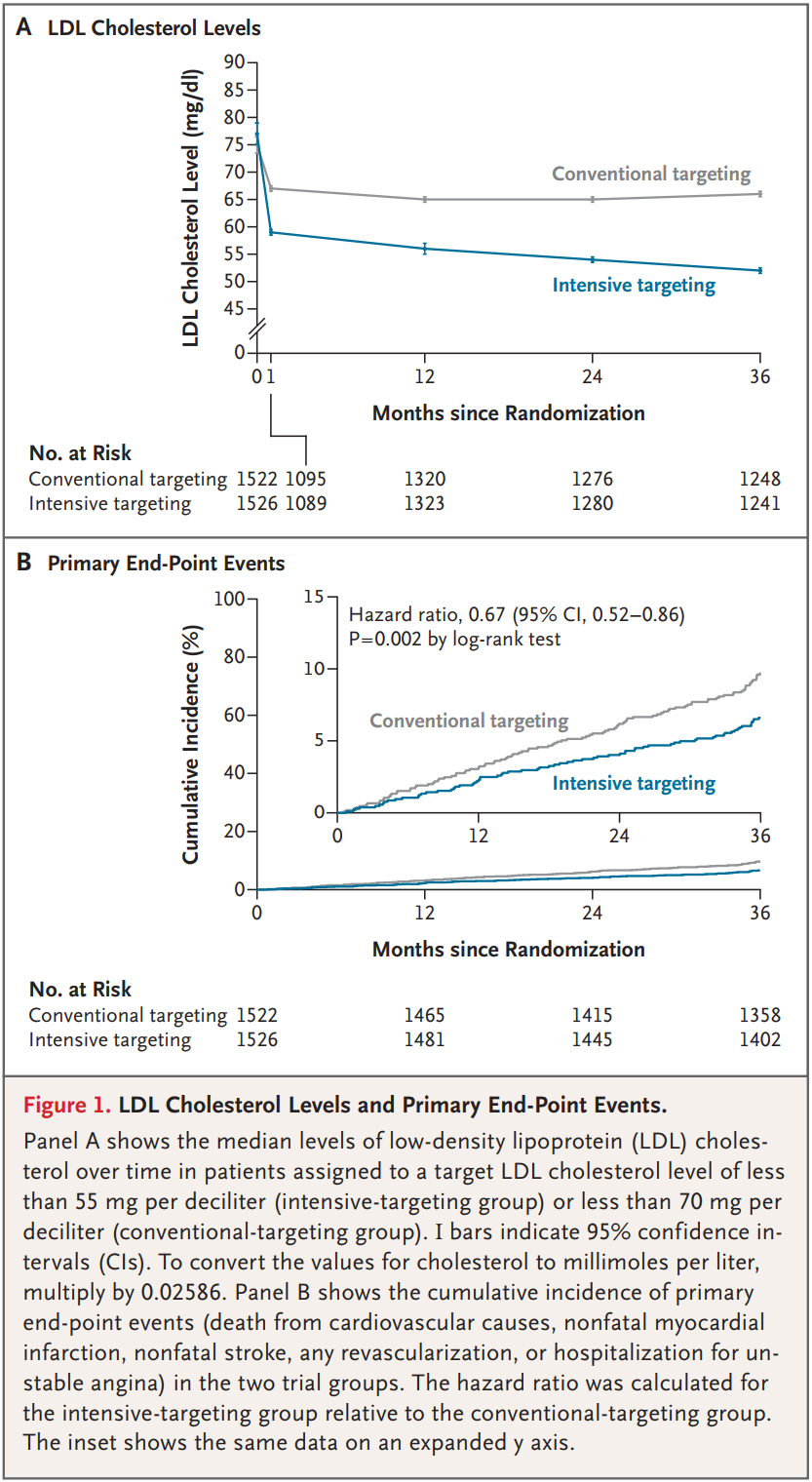
随访期间,强化目标组的中位LDL-C水平始终显著低于常规目标组,且组间差异保持稳定(图1A):试验期间强化目标组的中位LDL-C为56mg/dL(1.4mmol/L,四分位距48~67mg/dL),常规目标组为66mg/dL(1.7mmol/L,四分位距58~76mg/dL),均接近各组的预设目标。
从达标率来看,常规目标组的预设目标达标率始终更高:1个月时常规目标组达标率为59.4%,强化目标组为31.2%;3年时常规目标组达标率为68.1%,强化目标组升至60.8%。
值得注意的是,强化目标组达到常规目标(<70mg/dL)的比例极高,3年时达85.2%,说明强化目标组的患者绝大多数都能达到常规目标,而进一步向更低目标迈进。
(三)疗效终点
3年时强化目标组主要终点事件的累积发生率为6.6%(100例),显著低于常规目标组的9.7%(147例),强化目标组的相对风险降低33%(HR=0.67,95% CI 0.52~0.86,P=0.002)(表2、图1B)。
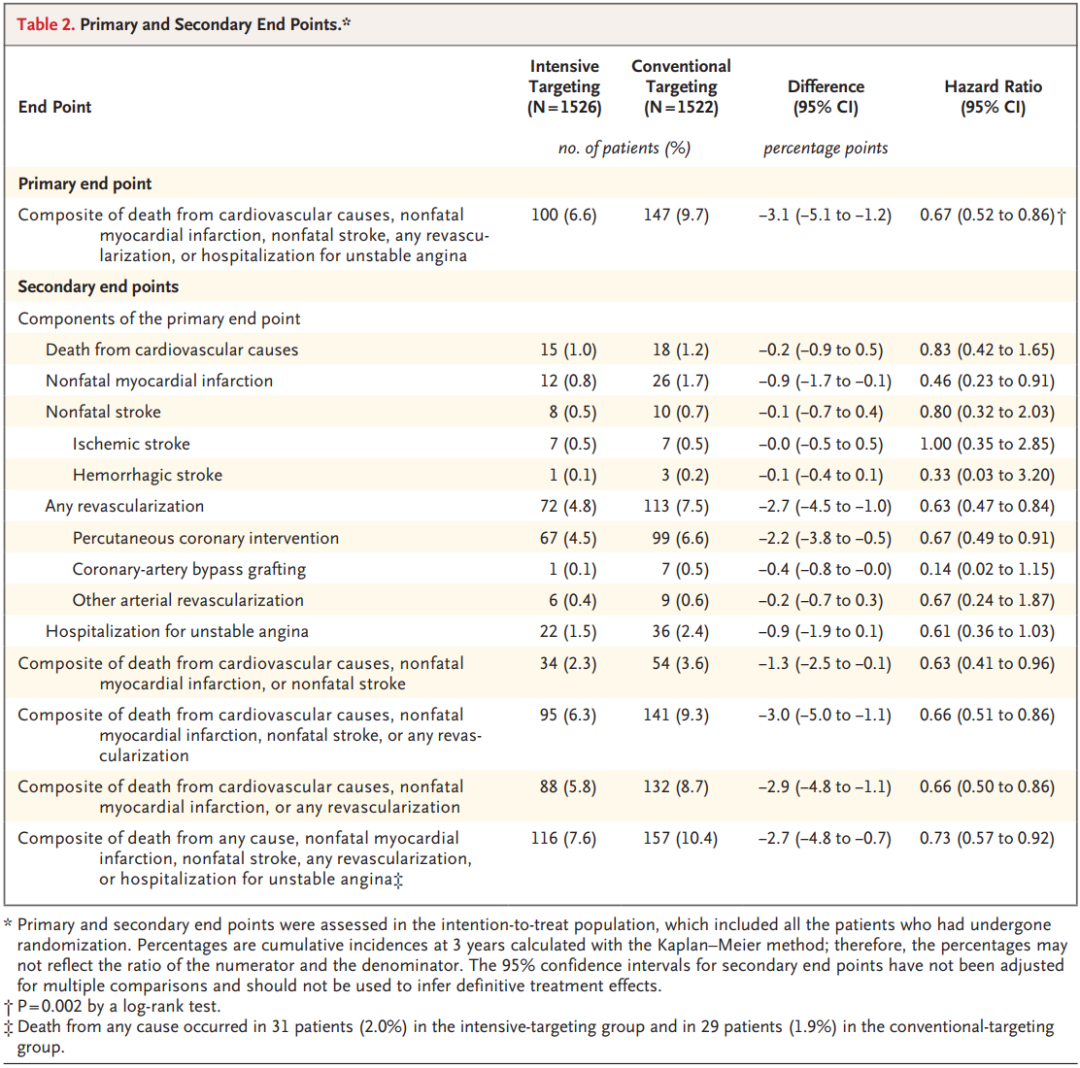
在主要终点的各单独组分中,强化目标组的非致死性心肌梗死、任何血运重建的累积发生率显著低于常规目标组:非致死性心肌梗死的累积发生率分别为0.8%和1.7%(HR=0.46,95% CI 0.23~0.91),任何血运重建的累积发生率分别为4.8%和7.5%(HR=0.63,95% CI 0.47~0.84);其中经皮冠状动脉介入治疗的累积发生率分别为4.5%和6.6%(HR=0.67,95% CI 0.49~0.91),冠状动脉旁路移植术的累积发生率分别为0.1%和0.5%,呈显著降低趋势。
心血管原因死亡、非致死性卒中、不稳定型心绞痛住院的组间差异虽无统计学意义,但强化目标组均呈更低的发生率趋势。在复合疗效终点中,强化目标组心血管原因死亡、非致死性心肌梗死、非致死性卒中的复合终点累积发生率为2.3%,显著低于常规目标组的3.6%(HR=0.63,95% CI 0.41~0.96);纳入全因死亡的扩展复合终点累积发生率也显著更低(7.6% vs 10.4%,HR=0.73,95% CI 0.57~0.92),进一步证实了强化目标管理的全面疗效获益。
(四)亚组分析
预设亚组分析显示,强化目标组相对于常规目标组的主要终点事件风险降低趋势,在绝大多数亚组中均保持一致,未发现明显的效应修饰作用,说明强化目标管理的获益具有广谱性(图2)。
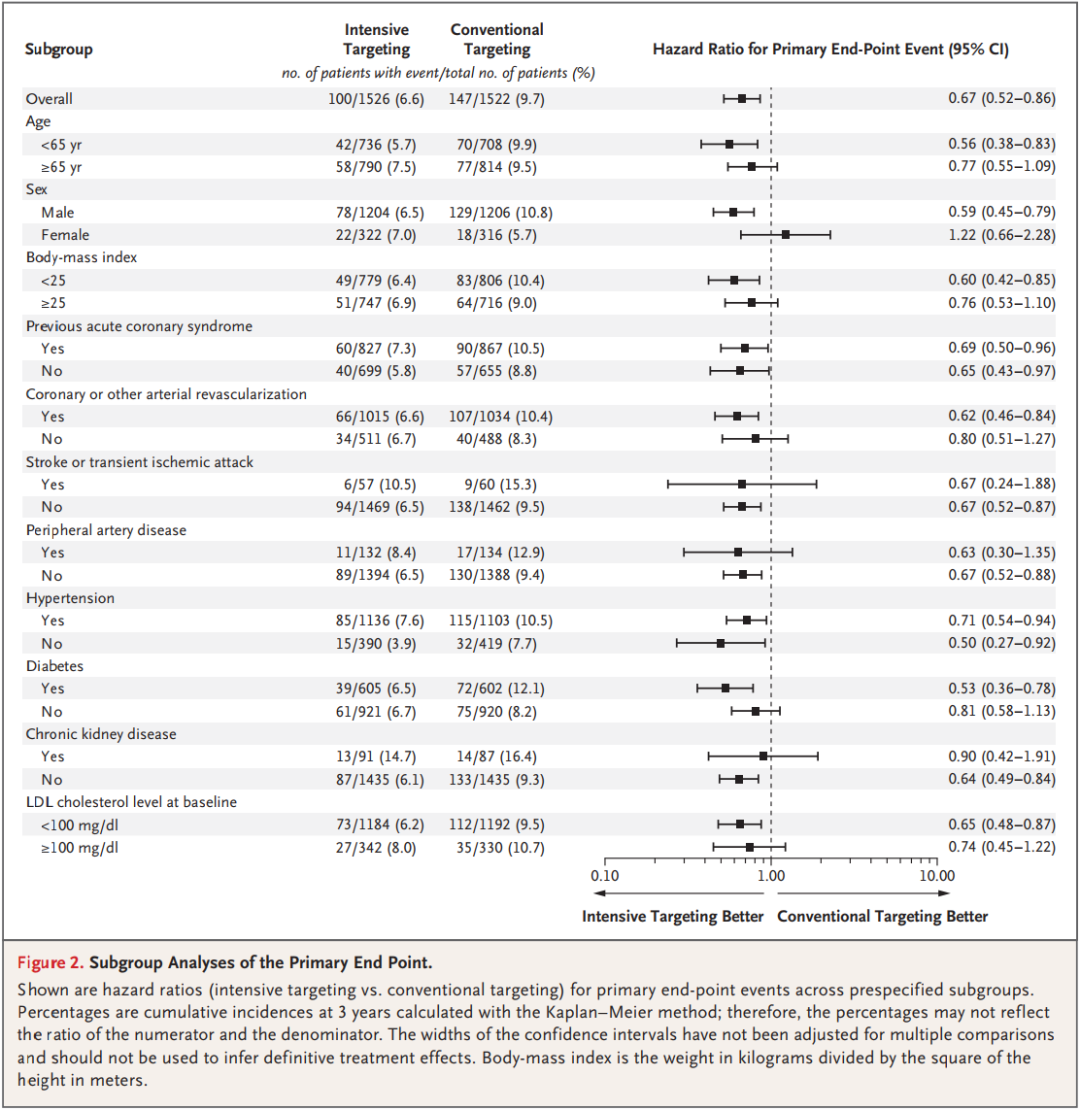
其中,<65岁人群(HR=0.56,95% CI 0.38~0.83)、男性人群(HR=0.59,95% CI 0.45~0.79)、体重指数<25kg/m2人群(HR=0.60,95% CI 0.42~0.85)、糖尿病患者(HR=0.53,95% CI 0.36~0.78)、无慢性肾脏病患者(HR=0.64,95% CI 0.49~0.84)、基线LDL-C<100mg/dL人群(HR=0.65,95% CI 0.48~0.87)的获益更为显著,提示这类人群是强化LDL-C目标管理的重点获益人群。
(五)安全终点
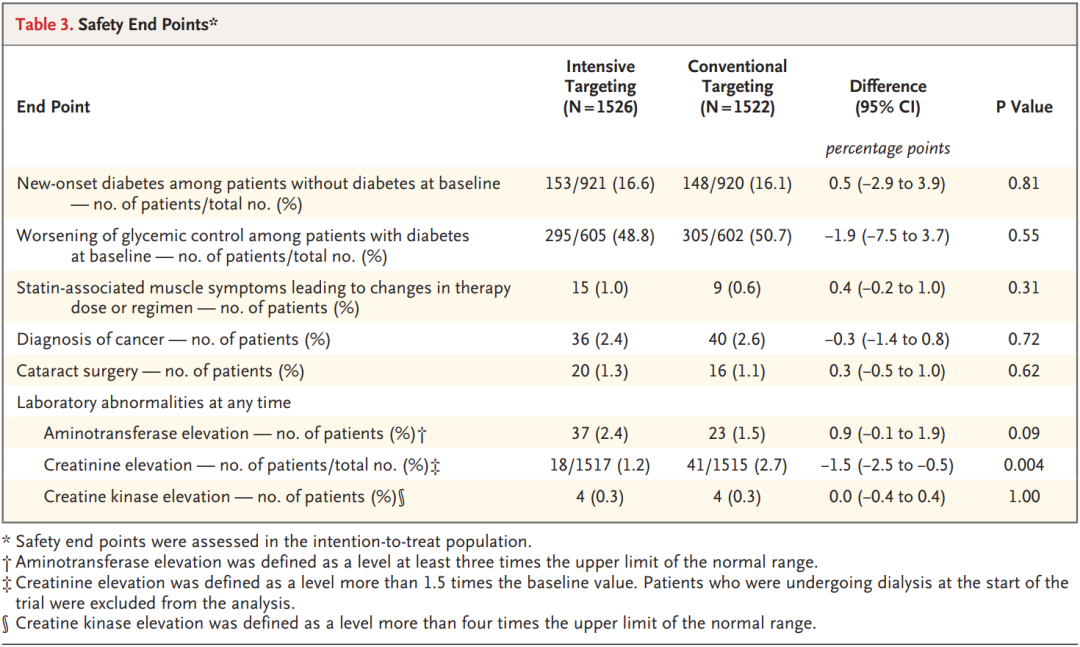
两组患者的预设安全终点发生率总体无显著差异,证实了将LDL-C目标设定为<55mg/dL的安全性(表3)。具体来看,基线无糖尿病患者的新发糖尿病发生率(16.6% vs 16.1%,P=0.81)、基线有糖尿病患者的血糖控制恶化发生率(48.8% vs 50.7%,P=0.55)无显著差异;导致治疗调整的他汀相关肌肉症状(1.0% vs 0.6%,P=0.31)、癌症诊断(2.4% vs 2.6%,P=0.72)、白内障手术(1.3% vs 1.1%,P=0.62)的发生率也无显著差异;转氨酶升高(≥正常上限3倍,2.4% vs 1.5%,P=0.09)、肌酸激酶升高(≥正常上限4倍,0.3% vs 0.3%,P=1.00)的发生率同样无统计学差异。
值得关注的是,强化目标组的肌酐升高发生率(>基线1.5倍)显著低于常规目标组(1.2% vs 2.7%,P=0.004),该分析排除了基线透析患者,提示强化降脂可能对肾功能具有一定的保护作用。
四、讨论
Ez-PAVE试验的结果明确回答了ASCVD患者血脂管理的核心问题:与LDL-C<70mg/dL相比,将目标设定为<55mg/dL可显著降低3年心血管复合事件风险,且安全性良好,为最新血脂管理指南的推荐提供了直接的头对头随机对照试验证据,同时也为临床实践中如何实施严格的血脂管理提供了重要参考。
(一)强化LDL-C目标管理是ASCVD患者二级预防的关键策略
LDL-C降低是ASCVD二级预防的核心,既往指南将<70mg/dL作为初始目标,主要基于高强度他汀类药物的疗效证据,而后续研究证实他汀联合依折麦布、PCSK9抑制剂可将LDL-C降至<55mg/dL,并带来额外的心血管获益,因此欧洲及美国的最新指南均将<55mg/dL作为ASCVD患者的推荐目标。但由于缺乏直接对比两种目标的研究,临床医师对更严格目标的获益仍存疑,这也是导致临床实践与指南脱节的重要原因。
Ez-PAVE试验首次通过随机对照试验证实,直接将LDL-C目标设定为<55mg/dL,相较于<70mg/dL可使ASCVD患者的3年心血管复合事件相对风险降低33%,且获益在多数亚组中一致,这一结果直接验证了更严格LDL-C目标的临床价值,也为指南推荐提供了最直接的循证支持,明确了ASCVD患者血脂强化达标的核心方向。
(二)积极的降脂策略是实现强化目标、获得临床获益的保障
实现LDL-C<55mg/dL的目标,需要积极的降脂治疗策略,Ez-PAVE试验的降脂方案设计为临床提供了重要参考。与既往TST试验中低目标组仅34%使用依折麦布、53%达到<70mg/dL目标不同,Ez-PAVE试验中强化目标组从随机化开始即有50%的患者联合使用依折麦布,优先使用瑞舒伐他汀、阿托伐他汀等强效他汀,随访期间高强度他汀和依折麦布的使用率持续高于常规目标组,最终3年时60.8%的患者达到<55mg/dL的目标,85.2%的患者达到<70mg/dL的目标,显著高于临床真实世界的达标率。
这一结果提示,要实现更严格的LDL-C目标,需要早期、积极地使用强效降脂药物,包括高强度他汀与依折麦布的联合治疗,而非单纯依靠他汀剂量的逐步上调。临床真实世界中达标率低的核心原因,正是非他汀类药物的使用率过低,因此,临床医师应摒弃保守策略,根据患者的基线LDL-C水平和目标要求,早期启动联合降脂治疗。同时,研究中PCSK9抑制剂的使用率较低(3年时2.3%),主要受报销政策限制,而这类药物是实现极低LDL-C目标的重要手段,对于经他汀联合依折麦布治疗后仍未达标的患者,应及时启用PCSK9抑制剂。
(三)强化LDL-C目标管理的安全性得到证实,打消临床医师的顾虑
临床医师对强化降脂的顾虑,主要集中在新发糖尿病、肌肉症状、肝肾功能损伤等不良反应,而Ez-PAVE试验的结果彻底打消了这一顾虑。研究显示,强化目标组与常规目标组的新发糖尿病、血糖控制恶化、他汀相关肌肉症状、转氨酶升高、肌酸激酶升高、癌症、白内障手术的发生率均无显著差异,证实了将LDL-C降至<55mg/dL的安全性。
既往研究提示,高强度他汀可能与新发糖尿病相关,但他汀联合依折麦布、PCSK9抑制剂的进一步降脂,并未增加糖尿病风险,Ez-PAVE试验的结果与之一致,说明降脂治疗的不良反应主要与他汀的剂量相关,而联合非他汀类药物实现强化降脂,可在不增加他汀剂量的前提下降低LDL-C,从而减少不良反应的发生。此外,强化目标组的肌酐升高发生率更低,提示强化降脂可能对肾功能具有保护作用,虽其具体机制仍需进一步研究,但这一结果进一步提升了临床医师对强化降脂的信心。
(四)研究对极端高危患者血脂管理的启示
最新指南已将<40mg/dL作为ASCVD极端高危患者的LDL-C目标,而Ez-PAVE试验的结果为这一更低目标提供了间接支持:既然<55mg/dL相较于<70mg/dL可带来显著获益,那么对于极端高危患者,进一步降低LDL-C目标至<40mg/dL,可能带来更多的心血管获益。研究也指出,对于这类患者,早期联合使用依折麦布、PCSK9抑制剂等非他汀类药物的策略,需要更多专门的研究来验证,这也是未来血脂管理研究的重要方向。
五、严道心得
临床医师应树立“目标导向”的血脂管理理念,摒弃“降脂即可,无需严格达标”的错误认知。Ez-PAVE试验明确显示,将LDL-C从<70mg/dL进一步降至<55mg/dL,可带来显著的心血管获益,且这种获益是明确的、有统计学意义的,对于高风险的ASCVD患者而言,这一获益具有重要的临床价值。
临床真实世界中,ASCVD患者的降脂达标率低,核心原因是依折麦布、PCSK9抑制剂等非他汀类药物的使用率过低,很多医师习惯于逐步上调他汀剂量,直至出现不良反应后才考虑联合非他汀类药物,而这种策略不仅达标率低,还可能增加他汀相关不良反应的发生风险。Ez-PAVE试验的设计和结果提示,早期启动他汀与依折麦布的联合治疗,优先使用强效他汀,是实现<55mg/dL目标的关键,对于基线LDL-C水平较高的患者,更应在治疗初期即采用联合降脂方案,而非单药逐步滴定。
长期以来,对降脂不良反应的过度担忧,是影响临床医师实施强化降脂的重要原因,而Ez-PAVE试验的结果显示,将LDL-C降至<55mg/dL,并未增加新发糖尿病、肌肉症状、肝损伤等不良反应的风险,反而肌酐升高的发生率更低,这一结果彻底打破了强化降脂不良反应多的误区。
血脂管理是一项长期工程,需要医患双方的共同配合。Ez-PAVE试验的中位随访时间为3年,而ASCVD患者的二级预防是终身的,因此临床医师不仅要关注患者的短期达标,更要关注长期的血脂控制,指导患者坚持降脂治疗,避免擅自停药、减药。同时,患者的依从性是长期达标关键,医师应加强患者教育,让患者认识到血脂管理的重要性,了解降脂治疗的获益和安全性,提高患者的治疗依从性。
总之,Ez-PAVE试验为ASCVD患者的血脂强化达标提供了坚实的循证证据,也为临床实践指明了方向。血脂管理的核心是长期达标,这一原则将始终贯穿于ASCVD患者的二级预防中,而Ez-PAVE试验的结果,无疑为这一原则的实施注入了强大的动力。