

引言:从"不得已"到"主动选择"的转变
房颤是临床最常见的持续性心律失常,全球约有6000万患者受其影响,其最严重的并发症——心源性卒中——始终是临床管理的核心挑战。新型口服抗凝药(NOAC)的问世极大改善了房颤患者的抗栓治疗,但依从性不佳、出血风险和长期用药负担仍是制约其临床效果的重要因素。有研究表明,房颤患者在起始NOAC治疗后一年内的停药率高达30%-50%。即使在坚持用药的患者中,NOAC相关的出血事件——从轻微的牙龈出血至危及生命的颅内出血——也是导致患者焦虑、停药和反复就医的重要原因。
经皮左心耳封堵术(LAAC)自PROTECT-AF试验以来,已积累了逾十五年的循证医学证据。从PROTECT-AF(2009,n=707)到PREVAIL(2014,n=407),这两项开创性研究以华法林为对照,证实了初代Watchman在不适合长期抗凝患者中的价值。PROTECT-AF在延长随访中甚至展示了全因死亡的优效性,而PREVAIL则因华法林组表现优于预期而未达到一项主要共同终点——这一教训提醒我们:对照组的表现直接决定了非劣效性试验的成败。
2025年发表于NEJM的OPTION试验标志着LAAC循证基准的进一步提升。该试验在1600例消融术后房颤患者中,首次以现代DOAC(95%为DOAC而非华法林)为对照评估Watchman FLX,展示了效力的非劣效性(5.3% vs 5.8%)和非手术出血的优效性(8.5% vs 18.1%)。值得注意的是,OPTION中缺血性卒中在两组间几乎一致(1.2% vs 1.3%),未出现CHAMPION-AF中的差异信号。

然而,一个核心问题始终悬而未决:对于适合长期抗凝的广泛房颤人群——而非消融术后的特定亚群——LAAC能否成为NOAC的合理替代方案?这正是CHAMPION-AF试验所要回答的问题。

2026年3月28日,ACC2026报道了CHAMPION-AF 3年结果。该结果同期在《新英格兰医学杂志》发表。下面严道医声网带您一起探索该试验的来龙去脉:
CHAMPION-AF试验设计:高质量的循证基石
CHAMPION-AF试验是一项前瞻性、国际多中心、随机对照试验,在16个国家141个中心开展。研究纳入3000例非瓣膜性房颤患者,以1:1比例随机分配至LAAC组(Watchman FLX)或NOAC组。关键入选标准包括:CHA₂DS₂-VASc评分男性≥2分、女性≥3分,且适合长期NOAC治疗。该入选标准为试验设计的核心创新——其刻意选择NOAC的"优势人群"作为目标,直接回答LAAC能否在标准抗凝适应人群中提供等效保护的问题。

基线特征显示两组人群高度匹配:平均年龄71.7±7.5岁,女性占31.9%,平均CHA₂DS₂-VASc评分3.5±1.3分,平均HAS-BLED评分1.3±0.8分。值得注意的是,约69%的患者为阵发性房颤,48%曾接受过房颤消融治疗——这一比例远高于既往LAAC试验,反映了当代房颤管理的临床实际。CHA₂DS₂-VASc评分分布显示,3-4分的中等风险患者占多数(约58%),≥5分的高危患者仅占18.5%。
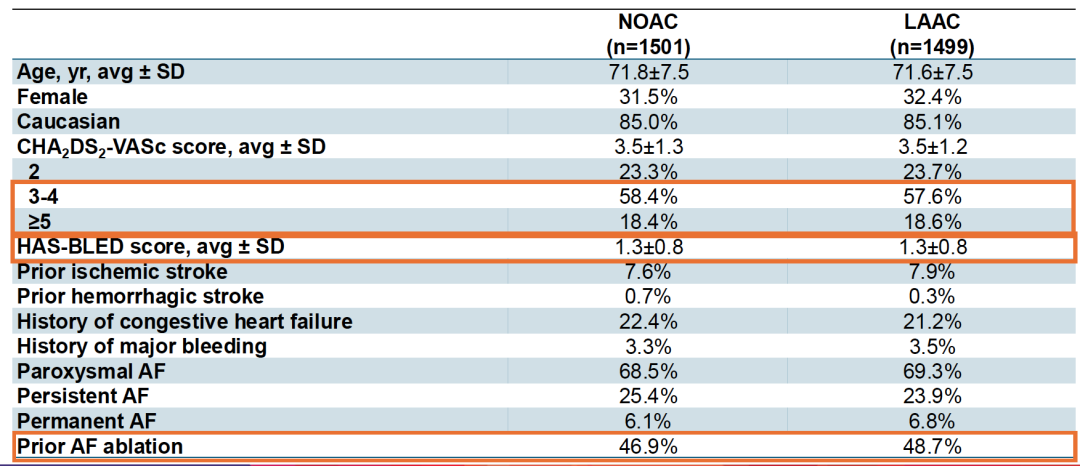
术后抗栓方案方面,LAAC组患者在植入后接受3个月的NOAC±阿司匹林或双联抗血小板治疗,随后转为单药抗血小板治疗至少12个月,此后以阿司匹林维持。NOAC组则按标签剂量持续口服抗凝。试验采用开放标签设计,但所有终点事件由独立临床事件委员会盲法裁定,影像学评估由独立核心实验室完成。
核心结果:双重主要终点全面达标
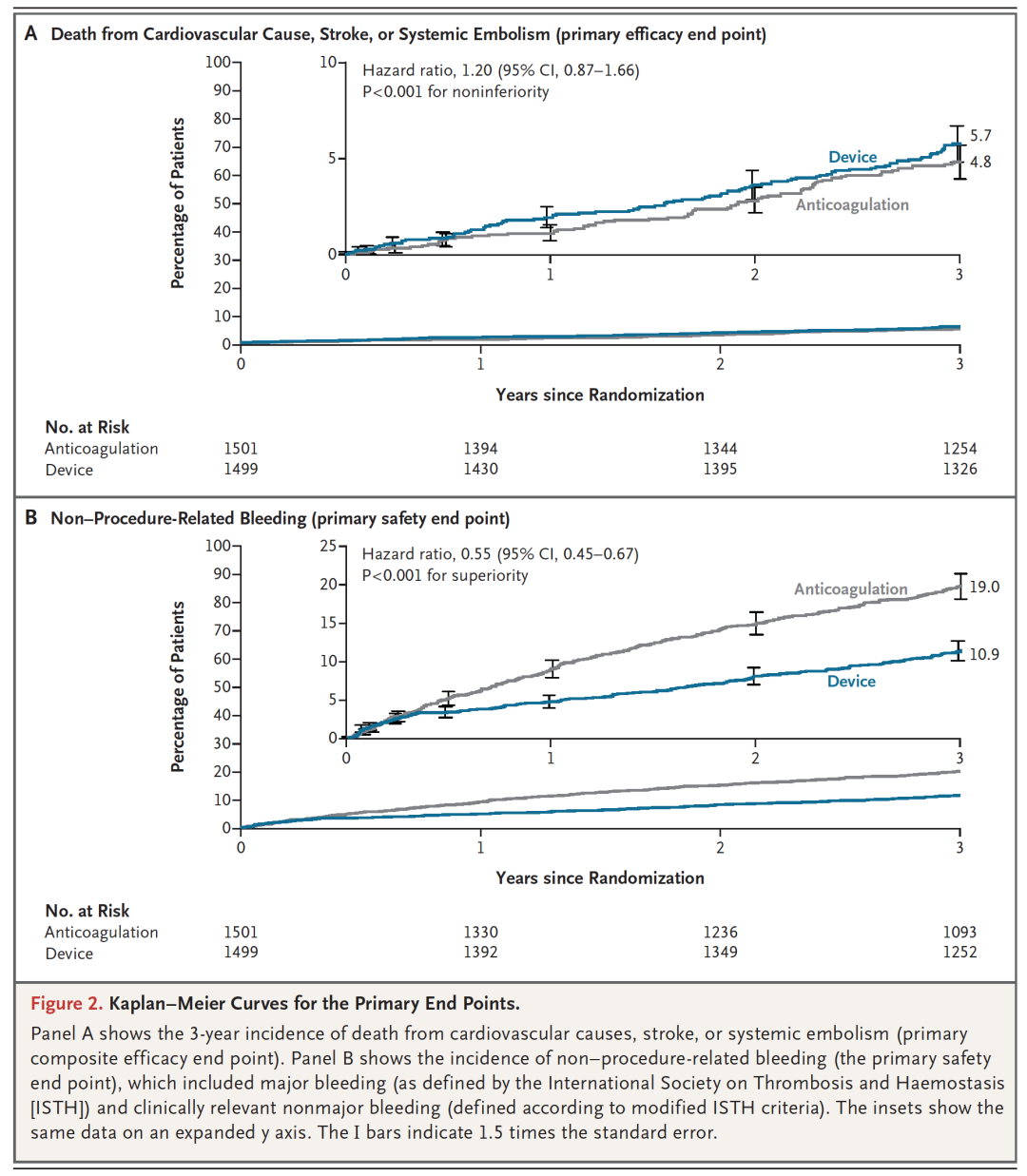
Champion-AF双重主要终点成功
主要有效性终点:非劣效性稳健确立
三年随访时,心血管死亡、卒中(缺血性及出血性)和体循环栓塞的复合主要有效性终点在LAAC组发生81例(Kaplan-Meier估计5.7%),NOAC组发生65例(4.8%),组间差异0.9个百分点(95% CI: -0.8至2.6;非劣效性P<0.001),风险比1.20(95% CI: 0.87-1.66)。97.5%单侧置信上限为2.6%,远低于预设的4.8%非劣效界值,表明非劣效性结论具有充分的统计学余量。
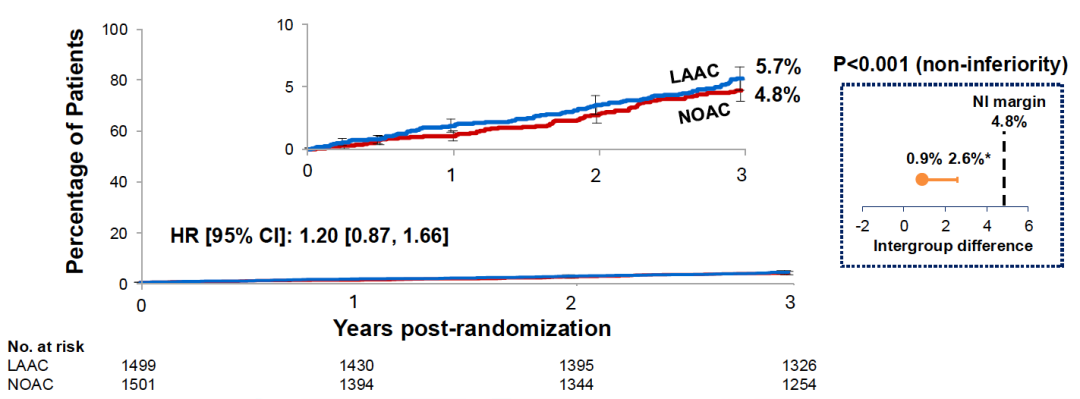
逐项分析各组分:心血管死亡在两组间完全一致(均为2.7%,HR 1.01 [0.64-1.59]),表明LAAC未带来额外的心血管死亡风险。出血性卒中同样无差异(两组均为0.4%,各5例体循环栓塞极为罕见,LAAC组无事件发生,NOAC组仅2例(0.1%)。
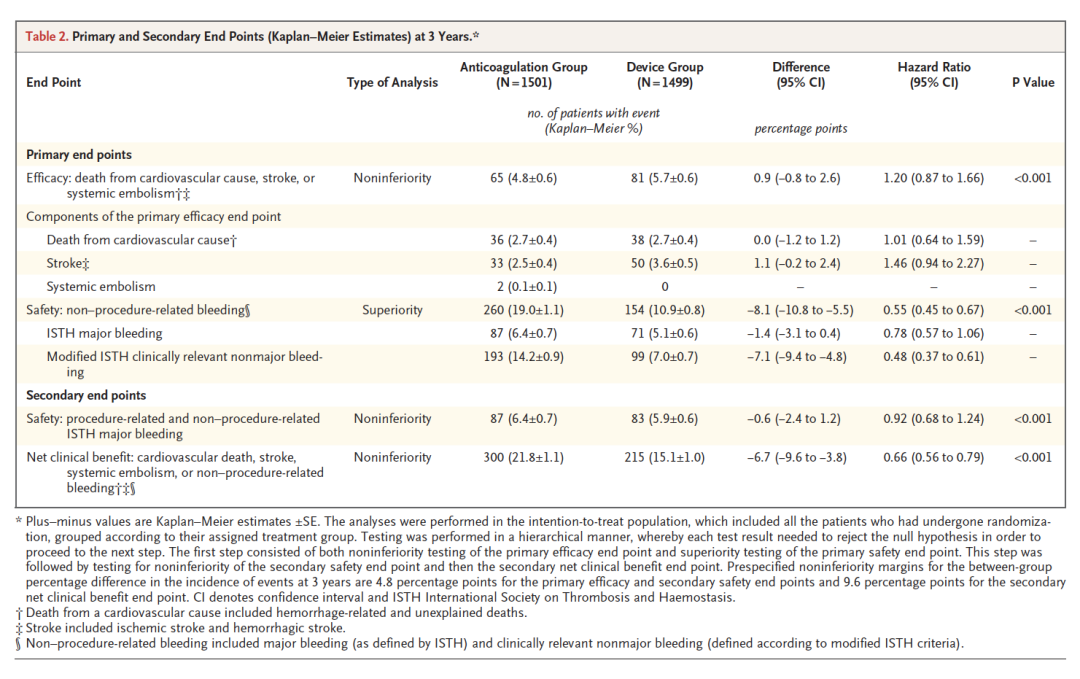
主要安全性终点:出血减少45%,达到优效性
非手术相关出血(ISTH大出血及改良ISTH临床相关非大出血)的发生率在LAAC组为10.9%(154例),NOAC组为19.0%(260例),HR 0.55(95% CI: 0.45-0.67,P<0.001,优效性)。该结果意味着LAAC在三年内将非手术相关出血风险降低了45%。更重要的是,Kaplan-Meier曲线在随访期间持续分离且分离速度随时间加快,提示左心耳封堵的出血获益随着抗凝暴露时间的延长而不断累积。从临床角度计算,每治疗约12例患者即可避免1例出血事件——这一NNT在日常实践中具有切实的临床价值。
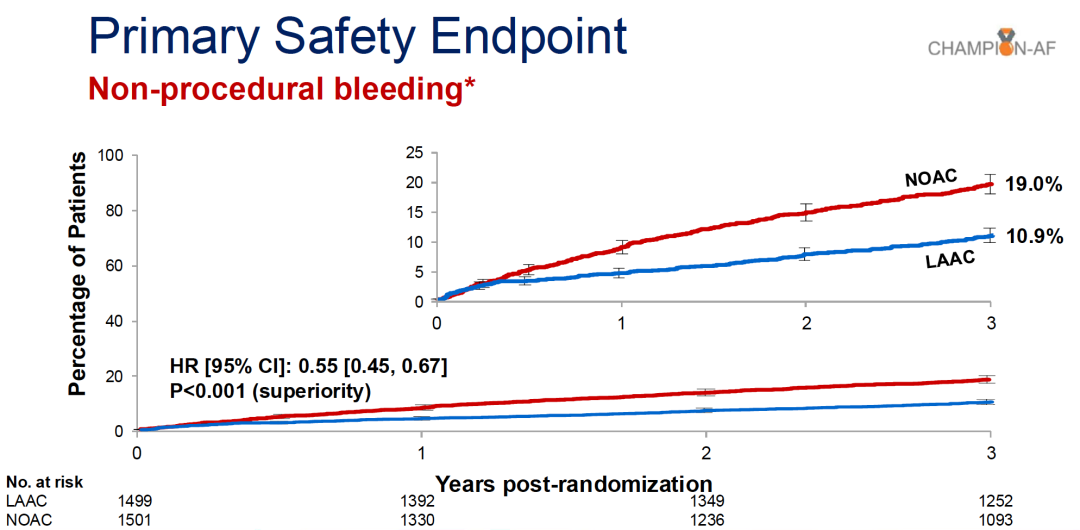
进一步分解出血终点的组分:ISTH大出血在LAAC组为5.1%对比NOAC组6.4%(HR 0.78),虽有数值差异但未达统计学显著性。真正驱动优效性的是临床相关非大出血——LAAC组7.0%对比NOAC组14.2%(HR 0.48),减少幅度超过一半。这些出血事件的定义是"不符合大出血标准但需要住院或增加护理级别"的出血——虽非致命,但每一次都意味着急诊就医、抗凝中断、患者焦虑和生活质量下降。对于长期服药的房颤患者而言,消除这些反复发作的出血事件对其日常生活的改善是深远而实际的。
次要终点与净临床获益
次要安全性终点(包含手术及非手术ISTH大出血)同样达到非劣效性(5.9% vs 6.4%, HR 0.92 [0.68-1.24], P<0.001),即使纳入手术相关的一次性出血风险(心包积液、穿刺点出血等),器械组的整体大出血负担仍不高于药物组。该结果的临床意义在于:手术本身的出血代价在三年的随访尺度上被NOAC的持续出血负担所"追平",且从手术后6个月开始两组曲线已出现交叉趋势——此后器械组的累积出血始终低于药物组。

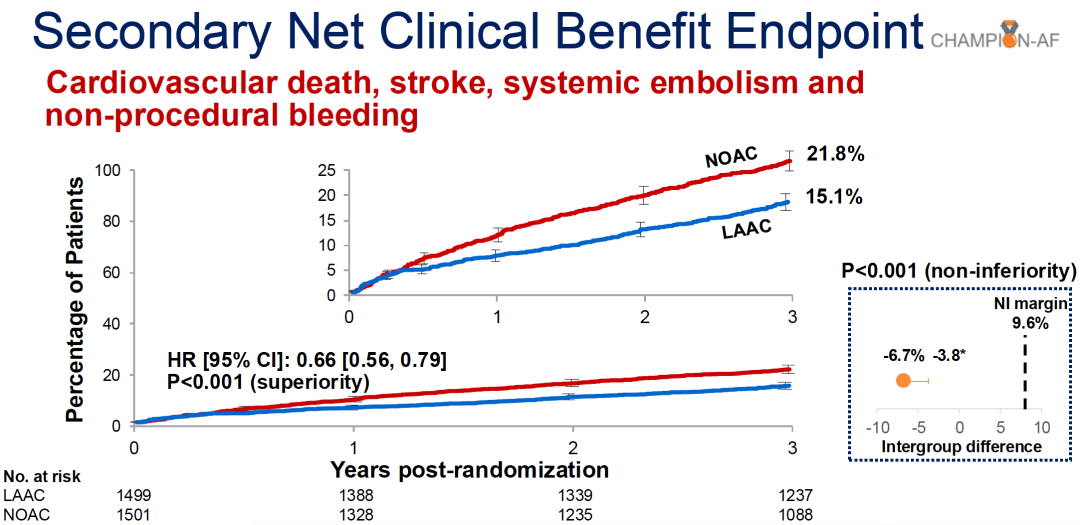
净临床获益终点——心血管死亡、卒中、体循环栓塞和非手术相关出血的复合终点——展现了优效性(15.1% vs 21.8%, HR 0.66 [0.56-0.79], P<0.001)。这一终点综合反映有效性和安全性的平衡,其结果表明当把所有重要的临床事件放在一起考量时,LAAC在整体临床结局上优于NOAC治疗。净临床获益的优效性同时满足了非劣效性检验,97.5%单侧置信上限为-3.8%,远低于9.6%的非劣效界值。
手术安全性与器械表现
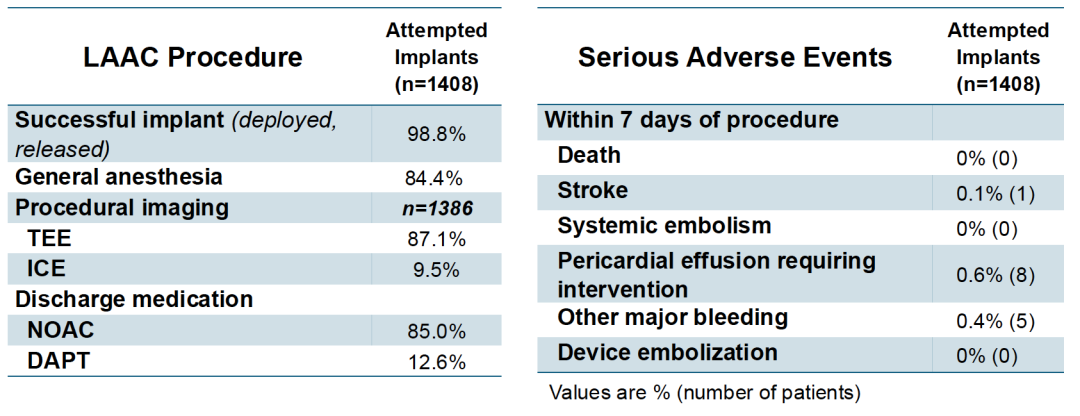
Watchman FLX的植入成功率达到98.8%(1386/1408例尝试植入中成功部署并释放),七日内严重不良事件发生率极低:无死亡、无器械栓塞、卒中仅1例(0.1%)、需干预心包积液8例(0.6%)、其他大出血5例(0.4%)。这些数据与近年来PINNACLE FLX和OPTION试验的手术安全性高度一致,标志着Watchman FLX器械设计和术者操作技术的整体成熟。与PROTECT-AF时代8.7%的手术并发症率相比,改进幅度超过一个数量级。
四个月影像学随访显示有效封堵率(残余漏≤3mm)达98.6%(998/1012),仅14例(1.4%)存在>3mm至≤5mm的残余漏,无一例出现>5mm残余漏。影像学评估由独立核心实验室完成,其中81.7%使用TEE,18.3%使用CT。器械相关血栓(DRT)在1320例完成影像评估的患者中检出63例(4.8%),其中蒂状DRT仅12例(0.9%)。24例(1.8%)患者因DRT需恢复口服抗凝治疗,2例(0.2%)在DRT后发生了卒中。

关于DRT,需要指出的是,CT血管造影较TEE对低密度增厚具有更高的检测敏感性。文献表明,CT发现的部分低衰减增厚实际上可能代表良性的器械表面内皮化过程,而非临床相关的血栓。COVID-19大流行期间对TEE的限制导致了CT使用比例的增加,可能导致了DRT发生率的过度估计。然而,仍需在术后随访中对DRT保持警惕。下一代Watchman FLX Pro(具有HEMOCOAT抗血栓涂层)和正在进行的SIMPLAAFY试验(评估简化术后抗栓方案)有望从根本上改善这一问题。
表1. CHAMPION-AF三年主要及次要终点完整汇总
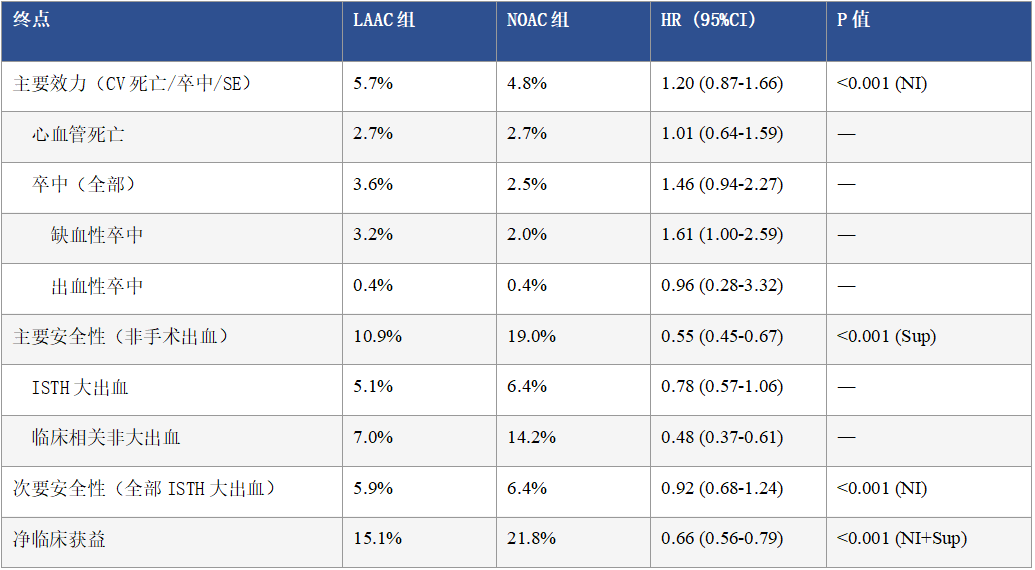
NI=非劣效性;Sup=优效性;SE=体循环栓塞。数据为Kaplan-Meier估计。
亚洲人群的特殊启示
CHAMPION-AF的预设亚组分析中,日本亚组呈现出引人注目的信号——主要有效性终点的HR为0.46(95% CI: 0.14-1.50),虽然置信区间宽泛且包含1.0(日本入组仅120例),但方向性强烈有利于LAAC。这一信号与已知的东亚人群抗凝特征高度契合。

东亚患者面临研究者所称的"东亚悖论":血栓风险相对较低,但抗凝治疗下的出血风险——尤其是颅内出血——显著高于西方人群(约2-4倍)。日本临床实践中普遍采用减量NOAC方案(如利伐沙班15mg替代国际标准20mg,源于J-ROCKET AF试验),且真实世界中NOAC不足剂量使用的问题在亚洲更为突出——GARFIELD-AF注册研究发现NOAC剂量不足在亚洲国家更为常见,这可能在削弱NOAC组卒中保护的同时也降低了出血发生率。这些因素共同决定了东亚患者可能是LAAC获益最大的群体之一——出血获益被放大,而缺血性卒中的代价可能因低体重、不同的血管病理和更高的心源性栓塞占比而被削减。
我国拥有全球最庞大的房颤人群——估计约2000万患者——且抗凝治疗的覆盖率和依从性长期低于欧美水平。多项流行病学研究显示,中国房颤患者的口服抗凝药物使用率虽在近年有所提升,但仍显著低于指南推荐水平,而低剂量NOAC的使用在真实世界中极为普遍。与日本类似,中国患者在抗凝治疗下的颅内出血风险显著高于西方人群,这使得"出血恐惧"成为临床实践中影响抗凝决策的重要因素。CHAMPION-AF所展示的出血获益——HR 0.55的非手术出血减少——对于这一人群而言具有极大的临床吸引力。鉴于中国房颤人群的庞大基数和独特的抗凝治疗现状,未来亟需针对中国人群开展设计严谨的前瞻性随机研究——而非仅依赖国际多中心试验的亚组分析或回顾性注册数据——以真正回答LAAC在中国房颤患者中的获益-风险比问题。
局限性和反思
在欣喜于CHAMPION-AF阳性结果的同时,有责任对试验的局限性进行透明、诚恳的学术观察。唯有正视这些局限,才能在临床实践中审慎地运用这些数据。
第一,缺血性卒中的组间差异值得关注。尽管复合主要终点达到了非劣效性,但缺血性卒中的发生率在LAAC组为3.2%(45例),NOAC组为2.0%(27例),HR 1.61(95% CI: 1.00-2.59),年均差异约0.33%/年。虽然这一差异在绝对值上并不大,但其置信区间下限恰好触及1.00,提示存在统计学边界效应。这一信号与LAAC的既往试验一脉相承——PROTECT-AF中器械组的缺血性卒中同样在早期偏高,但在长期随访中逐渐趋同。在五年随访数据公布之前,我们需持续追踪这一信号是否会随时间放大或趋于平稳。值得注意的是,在OPTION试验的消融术后人群中,LAAC与DOAC的缺血性卒中率几乎一致(1.2% vs 1.3%),提示这一差异可能存在人群异质性——消融手术本身对左房基质的改善可能降低非左心耳来源的栓塞风险。
第二,非劣效性界值的方法学讨论。CHAMPION-AF采用4.8%的绝对非劣效界值,对应40%的相对界值(基于预设对照组事件率12%)。然而,实际观察到的NOAC组事件率仅为4.8%——远低于预期的12%。在绝对非劣效界值框架下,当对照组事件率大幅低于设计预期时,4.8个百分点的绝对界值所允许的相对风险增幅将远超设计初衷的40%,从而使非劣效性结论的临床解释力度被削弱。这一方法学局限是使用绝对界值的非劣效性试验在低事件率时代面临的普遍挑战。
第三,开放标签设计的潜在偏倚。CHAMPION-AF为开放标签设计,虽然终点由独立的临床事件委员会盲法裁定,但患者和临床医师对治疗分配的知晓可能影响出血事件的报告和处理行为。这一偏倚在主要安全性终点的优效性解读中尤为重要:知晓自己在服用抗凝药的患者和医师可能对出血症状更为敏感,更倾向于就医和记录。这一固有局限在所有器械-药物对比试验中普遍存在(包括OPTION和将来报告的CATALYST),但在解读出血减少的幅度时应予以考虑。
第四,主要安全性终点排除了手术相关出血。主要安全性终点定义为非手术相关出血,意味着心包积液、穿刺点出血等与植入操作直接相关的事件被排除在外。虽然这一定义有助于评估LAAC消除长期抗凝后的持续出血获益,但也系统性地有利于器械组。事后分析显示,即使纳入手术相关出血,三年时全部出血事件仍为器械组12.8%对比NOAC组19.0%,曲线在6个月左右交叉后持续分离——但这一"全部出血"分析是事后补充的,并非预设终点。
第五,人群代表性的局限。本试验排除了射血分数<30%的晚期心力衰竭患者,而CHA₂DS₂-VASc≥5分的高危患者仅占18.5%。亚组分析显示,CHA₂DS₂-VASc >5分患者的效力HR为1.44(0.65-3.18),虽然交互检验P值(0.87)未达统计学显著性,但这一数值提示最高危人群的获益-风险比可能不同。正在进行的LAAOS-4试验将专门针对CHA₂DS₂-VASc≥4分的高危人群。
第六,NOAC组的依从性和交叉问题。NOAC组87%的患者在多数随访中保持依从性——这意味着13%的患者在相当比例的随访中未能坚持用药。更值得注意的是,206例(13.7%)NOAC组患者在随访期间交叉至器械组(其中119例在发生主要终点事件前接受了植入)。在ITT分析框架下,这些交叉患者的后续事件仍被计入NOAC组——这一"稀释效应"系统性地低估了两组间的真实差异。五年时如果交叉比例进一步上升,per-protocol或as-treated分析将成为重要的敏感性验证。
对话CLOSURE-AF:互补而非矛盾
就在CHAMPION-AF发表前十天,德国CLOSURE-AF试验在同一期刊公布了其结果:在912例高危高龄房颤患者(平均年龄78岁、CHA₂DS₂-VASc 5.2分、HAS-BLED 3.0分)中,LAAC未能达到预设的非劣效性标准(校正HR 1.28,实际有利于药物治疗组)。NEJM同期社论以"左心耳封堵——又一种心血管内科过度使用的方法?"为题,对整个LAAC领域提出了尖锐质疑。
这一结果初看与CHAMPION-AF矛盾,但两项试验在多个维度上存在根本差异。CLOSURE-AF允许使用多种封堵器械(44% Watchman FLX、42% Amulet及旧代器械),术后多数患者采用双联抗血小板治疗而非NOAC过渡方案,且其主要复合终点将大出血纳入了效力终点——而CHAMPION-AF将出血作为独立的优效性终点分开评估。在入组人群上,CLOSURE-AF恰恰入组的是当前临床实践中LAAC的典型适应人群(高出血+高栓塞风险的老年患者),而CHAMPION-AF针对的是适合长期抗凝的相对低危人群。
从学术角度看,两项试验的对比呈现出一种悖论:LAAC在其当前获批的目标人群中失败了,却在其尚未获批的目标人群中成功了。这一悖论的合理解释是多层次的:高危老年患者的手术风险更高、解剖更复杂、合并症更多,且其卒中来源更可能是多因素的(不仅仅来自左心耳)。CLOSURE-AF的失败恰恰提醒我们不应将CHAMPION-AF的结果不加区分地推广至所有患者亚群。结合两项试验的证据,合理的解读是:LAAC在经过适当筛选的患者中可以提供与NOAC相当的效力保护和更优的出血预防,但精准的患者选择非常关键。
CATALYST试验的设计概况
雅培的CATALYST试验(NCT04226547)于2026年初完成全部约2650例患者的入组,由Vivek Reddy教授领导。这是Amplatzer Amulet封堵器与NOAC的首次大规模正面对决,入组标准与CHAMPION-AF高度一致——适合长期抗凝的非瓣膜性房颤患者。首批结果预计于2028年左右公布。
从试验设计角度看,CATALYST与CHAMPION-AF存在几个值得关注的差异。首先,CATALYST的主要有效性复合终点仅包含缺血性卒中(不含出血性卒中和全部卒中)加体循环栓塞和心血管死亡,评估时点为2年——这是一个更为严格的检验标准。其次,CATALYST采用适应性统计设计,允许根据观察到的事件率动态调整样本量——这一务实的方法学选择正是鉴于CHAMPION-AF等试验中事件率普遍低于预期的教训。第三,在术后抗栓方案上,CATALYST体现了Amulet器械的核心差异化优势:术后仅需双联抗血小板治疗3个月,无需任何口服抗凝过渡——与CHAMPION-AF中85%患者术后仍需NOAC过渡3个月形成对比。
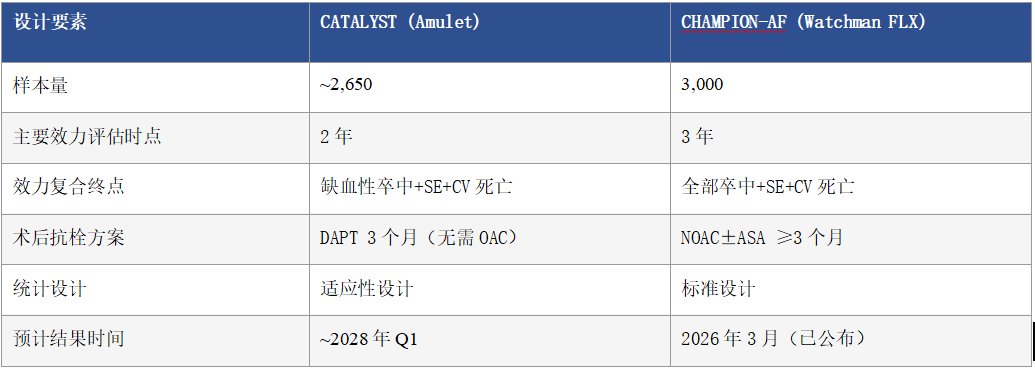
表2 CATALYST与CHAMPION-AF设计对比
Amulet IDE试验的五年随访数据为理解器械设计差异提供了重要线索。在Amulet与Watchman的头对头比较中,虽然缺血性卒中总发生率相似(年化均为1.6%),但致死性或致残性卒中在Amulet组显著更少(22 vs 39例,P=0.030)。与器械因素(DRT或残余漏≥3mm)相关的卒中和心血管死亡事件在Watchman组(63例)是Amulet组(31例)的两倍。五年时仍在使用口服抗凝的比例,Amulet组也显著低于Watchman组(6.0% vs 9.1%,P=0.009),提示Amulet的双重封堵(lobe+disc的两点密封)在长期"去抗凝化"和减少器械相关事件上可能具有结构性优势。
但Amulet的手术操作安全性仍有提升空间。Amulet IDE中手术并发症率为4.5%对比Watchman的2.5%(P=0.02),主要差异来自心包积液和器械栓塞。SWISS-APERO试验三年数据(JACC 2025)在as-treated分析中显示Amulet的复合缺血性终点显著优于Watchman(17.0% vs 31.1%, HR 0.53, P=0.035),但该试验仅221例患者且并非为临床结局设计。CATALYST能否在2650例患者的充分样本量中确认这些信号,将是决定Amulet市场前景的关键。
CATALYST试验结果对于LAAC领域同样重要。如果两种不同设计的器械在不同试验框架下均能展示对NOAC的非劣效性和出血获益,那么这将是支撑LAAC作为一类治疗策略(而非某一特定品牌器械)的最强有力证据,也将为指南更新和适应证扩展提供更为坚实的循证基础。反之,如果CATALYST未能达标,则提示器械设计差异确实影响临床结局,临床决策将需更加关注器械选择而非仅关注LAAC技术本身。
临床实践前瞻
CHAMPION-AF的三年数据为LAAC在适合抗凝的广泛房颤人群中提供了首个以DOAC为对照的阳性随机证据。结合OPTION在消融术后人群的验证,左心耳封堵术的循证基础已跨越了关键门槛。从监管层面看,CHAMPION-AF数据预期将支持FDA补充PMA申请,以扩展Watchman FLX的适应证至适合长期抗凝的患者——这将是自2015年首次获批以来最重要的适应证跃迁。但我们也必须保持清醒,缺血性卒中的组间差异需在五年数据中持续追踪。
在"LAAC替代抗凝"的讨论之外,LAAOS-4试验正在探索一个更为激进的假设——LAAC叠加抗凝是否优于单独抗凝。这一设想源于LAAOS III(NEJM 2021)的里程碑发现:外科左心耳闭合在继续抗凝的基础上额外降低缺血性卒中33%(HR 0.67)。LAAOS-4计划在15个国家纳入4000例CHA₂DS₂-VASc≥4分的高危患者,以经皮LAAC联合口服抗凝对比单独口服抗凝。如果结果阳性,LAAC的定位将从"替代抗凝"拓展至"强化抗凝"——这可能从根本上重塑左心耳管理的治疗哲学。
目前最合理的基于循证证据的实践建议为:将CHAMPION-AF的数据纳入与房颤患者的共同决策对话。对于那些担忧长期出血风险、药物依从性不佳、或偏好一次性手术解决方案的患者,LAAC现在有了充分的循证支持作为NOAC的合理替代。但同时向患者沟通潜在的缺血性卒中差异和器械相关血栓风险,让患者在充分知情的基础上做出符合自身价值的选择。
我们正处于LAAC领域最激动人心也最具挑战性的时代。CHAMPION-AF证明了左心耳封堵术不再只是"没有选择的选择";CATALYST将验证这一结论是否跨越器械界限;而下一代器械的技术创新正在重新定义左心耳管理的可能性。