
功能性二尖瓣反流(FMR)与高死亡率相关,即使是轻度病例也是如此,因此,其治疗管理极具挑战性。有研究曾探讨二尖瓣经导管缘对缘修复术(M-TEER)相较于指南指导药物治疗的获益情况,其结果存在的差异促使研究人员提出假设:FMR存在不同表型,而最新指南尚未对此予以关注。然而又有研究表明,对于有效反流口面积(EROA)较小的中重度FMR患者,M-TEER仍能带来持续获益,这对上述假设提出了挑战。总体而言,目前针对FMR形态学差异的研究仍较为匮乏,左心房应变和左心室应变等新型指标对FMR的预后评估价值也尚未从表型层面进行验证。
FMR的综合形态学表型特征及预后分析
— JACC:Asia —
方法
研究人群与临床数据
本回顾性研究纳入了 2010 年 1 月至 2022 年 7 月期间,在两家三级转诊中心接受经胸超声心动图(TTE)检查,且确诊为中重度FMR的 18 岁及以上患者。所有研究参与者均在TTE检查后 30 天内接受了全面的心脏病学和/或心血管外科评估。
超声心动图与FMR表型分类
所有TTE均由训练有素的超声技师使用商用超声系统完成,随后重新审阅并评估以下指标:左心室大小/容积(双平面圆盘求和法)、左心房容积、二尖瓣反流严重程度、二尖瓣环大小(舒张期心尖四腔心切面二尖瓣开口最大处测量)及右心室功能。
本研究基于Reddy等人的研究将FMR分为3种主要形态学表型,同时由于缺血性心脏病也可能导致心室源性FMR,为避免混淆,对命名进行了修正:
心室源性FMR(VFMR),研究中重命名为对称性束缚型心室源性FMR(VFMRst):因两个乳头肌位移程度相等导致二尖瓣对称性束缚,表现为中心性反流束,主要由左心室整体扩张或室壁运动异常(WMA)引起;
缺血性FMR(IFMR),研究中重命名为不对称束缚型心室源性FMR(VFMRat):二尖瓣不对称束缚,后叶束缚更明显且前叶覆盖,表现为后向性反流束,主要由下侧壁WMA或左心室不均匀重构导致;
心房源性FMR(AFMR):因左心房扩张导致二尖瓣环扩大、二尖瓣中心对合不良而引发的反流。
此外,存在一种由心房重构导致单纯后叶束缚(PML)引起的 AFMR 亚型,表现为后向性反流束,将其归类为后叶束缚型 AFMR。
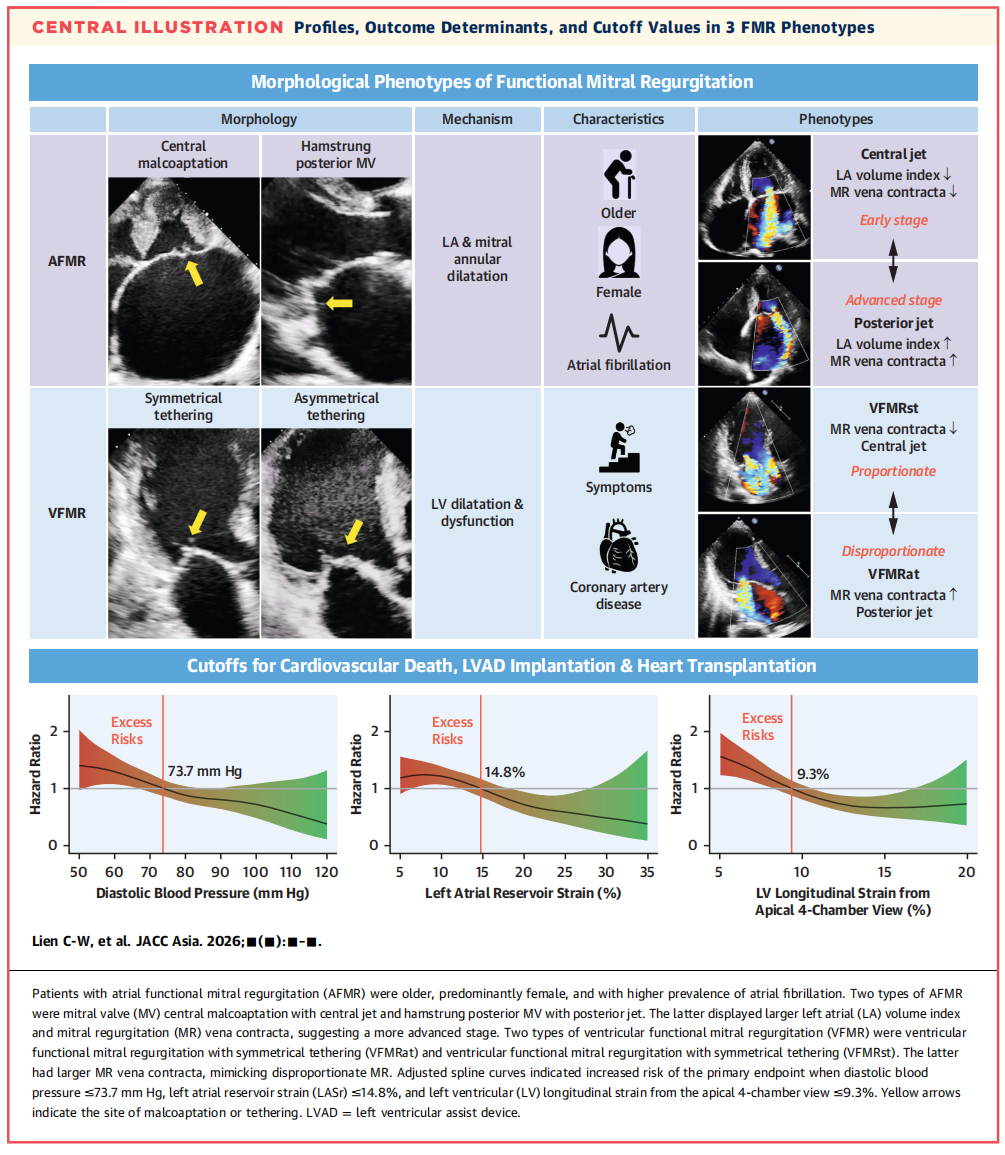
图1 3种FMR表型的特征、预后及临界值
左心室与左心房应变测量
由于部分患者心尖切面图像质量受限,最终分析采用心尖四腔心切面左心室纵向应变(A4C-LVLS)。左心房应变分析以舒张末期为参考点(R-R 间期门控),若心内膜边界追踪不合适则进行修正,采用调整后的数据进行半自动化应变分析。
研究终点
主要复合结局:5年内心血管死亡及死亡等效事件[如左心室辅助装置(LVAD)植入、心脏移植(HTx)]。
次要结局为5年内全因死亡及死亡等效事件(如LVAD植入术或HTx术)。
观察时间:从基线TTE检查日期至患者死亡、接受LVAD植入术/HTx术或最后一次随访(最长随访时间为5年)。
研究结果
基线特征
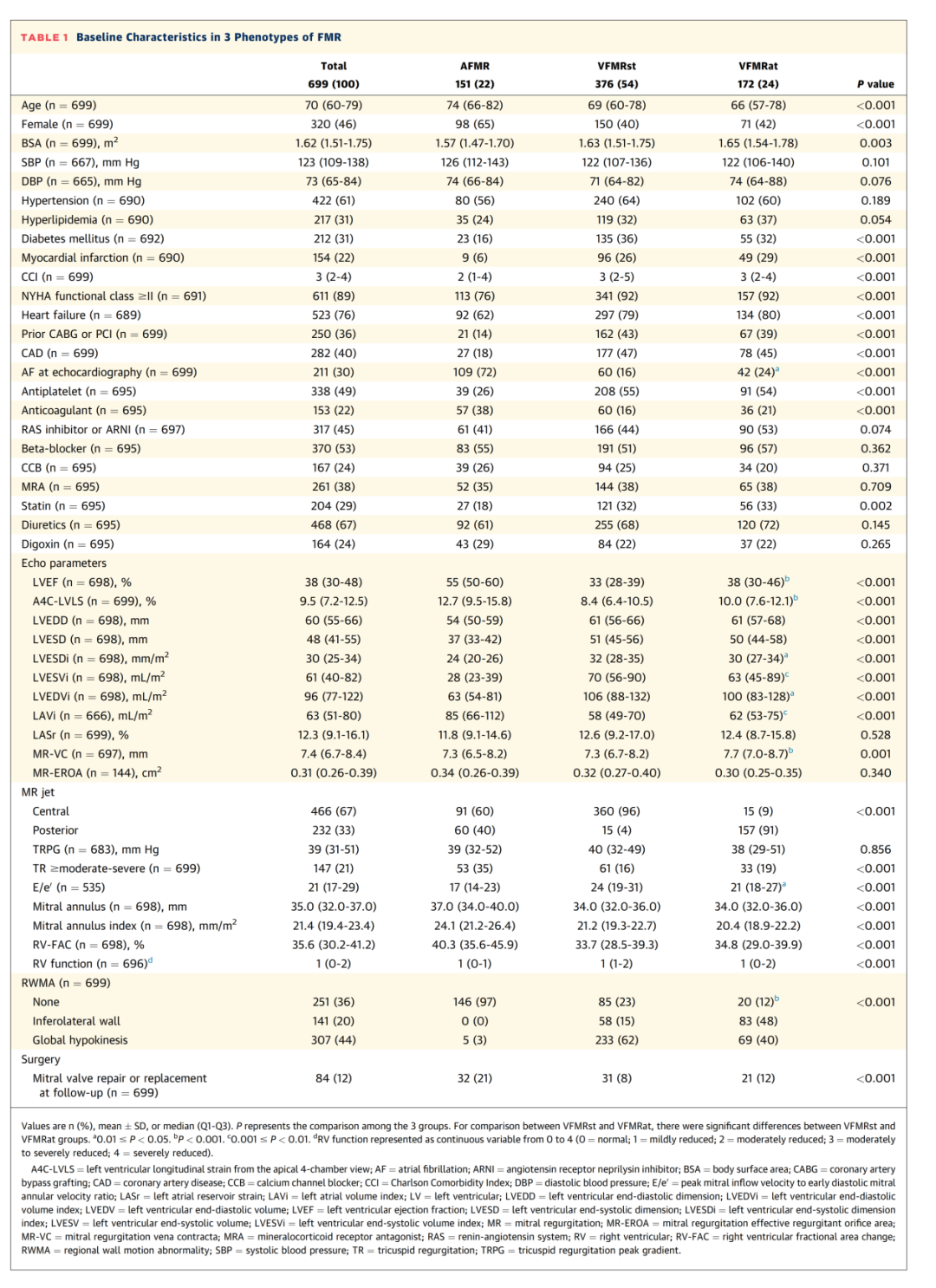
最终队列纳入 699 例中重度FMR患者,中位年龄 70 岁(Q1-Q3:60-79 岁)(表1)。其中,AFMR 151 例(22%),VFMRst 376 例(54%),VFMRat 172 例(24%)。
表1 3种FMR表型基线特征
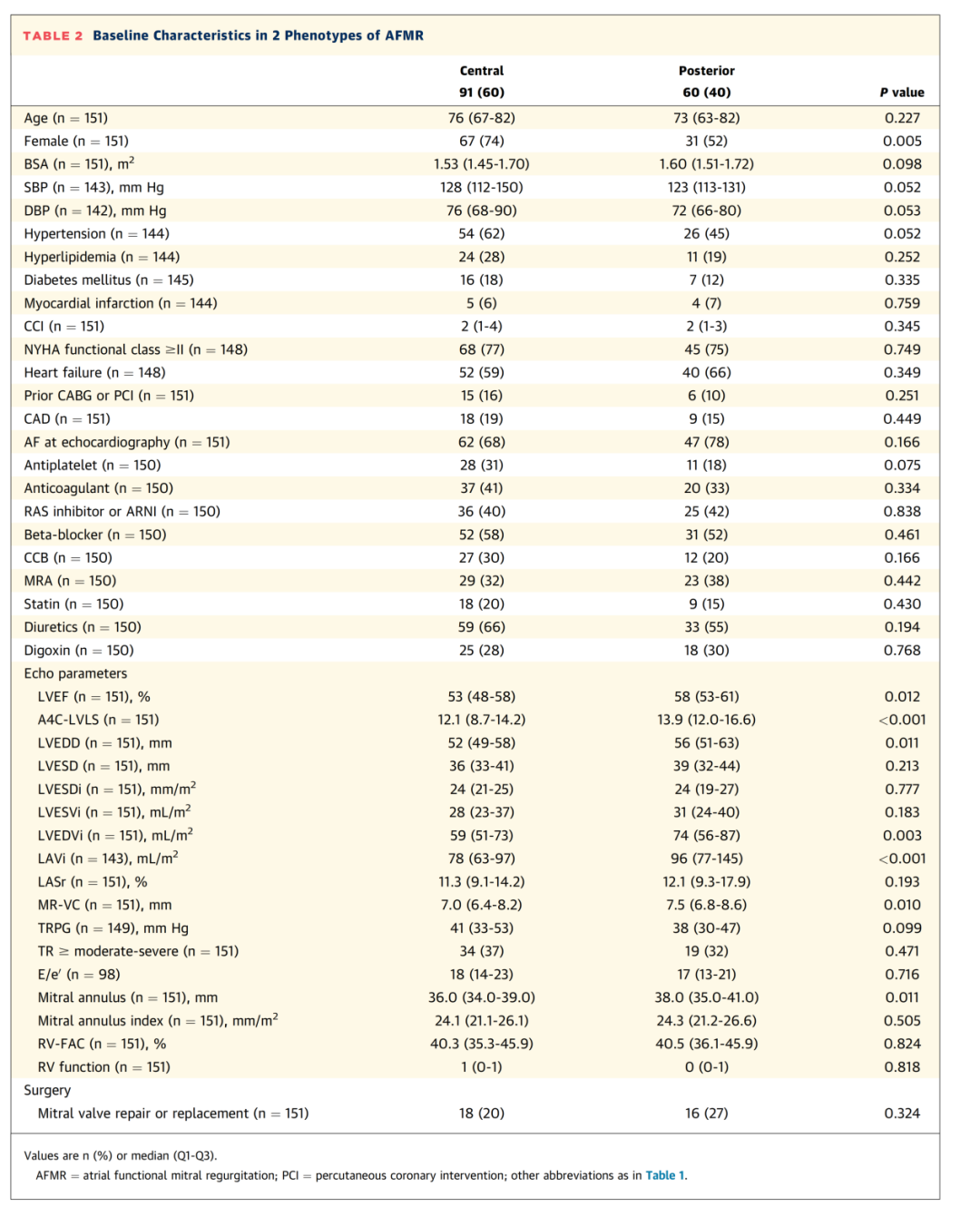
在 AFMR 亚组(n=151,22%)中,91 例(60%)表现为中心性反流束,60 例(40%)表现为后向性反流束(表 2)。与中心性反流患者相比,后向性反流患者以男性为主,且 LVEF、A4C-LVLS、左心室舒张末期容积指数(LVEDVi)、LAVi 和 MR-VC 均更大(均P≤0.012)。
表2 2种AFMR表型基线特征
手术操作
在观察期结束前,即发生死亡、LVAD植入、HTx时或5年随访结束前,84 例患者接受了MVS,平均时间为基线后 3.7±6.8 个月。其中:
53 例(63%)行二尖瓣修复术(含 3 例M-TEER),31 例(37%)行二尖瓣置换术(28 例为生物瓣,3 例为机械瓣);
25 例(30%)患者同期行冠状动脉旁路移植术(CABG),20 例(24%)同期行迷宫手术,34 例(40%)同期行三尖瓣环成形术。
观察期间:
13 例患者单独接受 CABG(未联合MVS),平均时间为基线后 6±14 个月;
29 例(4%)患者接受了 LVAD 植入或 HTx,平均时间为基线后 8.8±7.8 个月。
主要复合终点事件的影响因素
随访率 100%,主要终点中位随访时间为 2.6 年(Q1-Q3:0.9-5 年),共有193 例患者达到主要终点(29 例接受 LVAD/HTx,164 例发生心血管死亡),其中VFMRst 和 VFMRat 的主要终点结果受单变量影响(均 P≤0.030)。
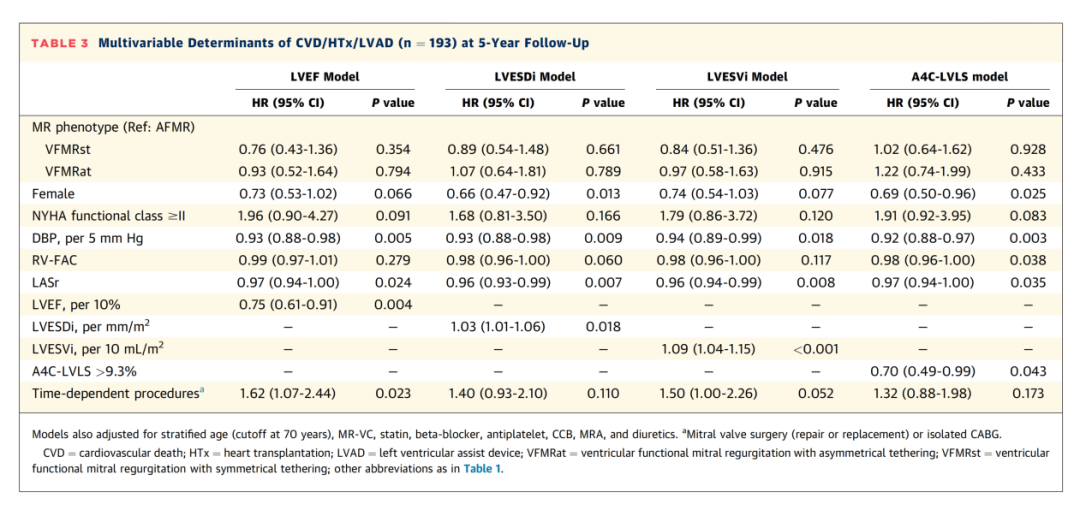
多变量模型分析显示(表 3),男性、舒张压降低、右心室面积变化分数(RV-FAC)降低、LVEF 降低、A4C-LVLS 降低(临界值:9.3%)、LASr 降低,以及LVESDi增大、LVESVi 增大,均与主要结局独立相关(均 P≤0.043)。但经调整后,二尖瓣反流(MR)表型与主要结局无关联(均 P≥0.139)。
表3 5年随访期间心血管死亡/HTx/LVAD多变量因素
未调整的 Kaplan-Meier 曲线显示,AFMR、VFMRat 和 VFMRst 的 5 年无事件生存率分别为 71±4%、63±4% 和 64±3%(AFMR vs VFMRst:P=0.030;AFMR vs VFMRat:P=0.024)(图2)。AFMR 患者中,后向性反流与中心性反流的 5 年无事件生存率无显著差异(HR:1.16;95% CI:0.57-2.33;P=0.678)。
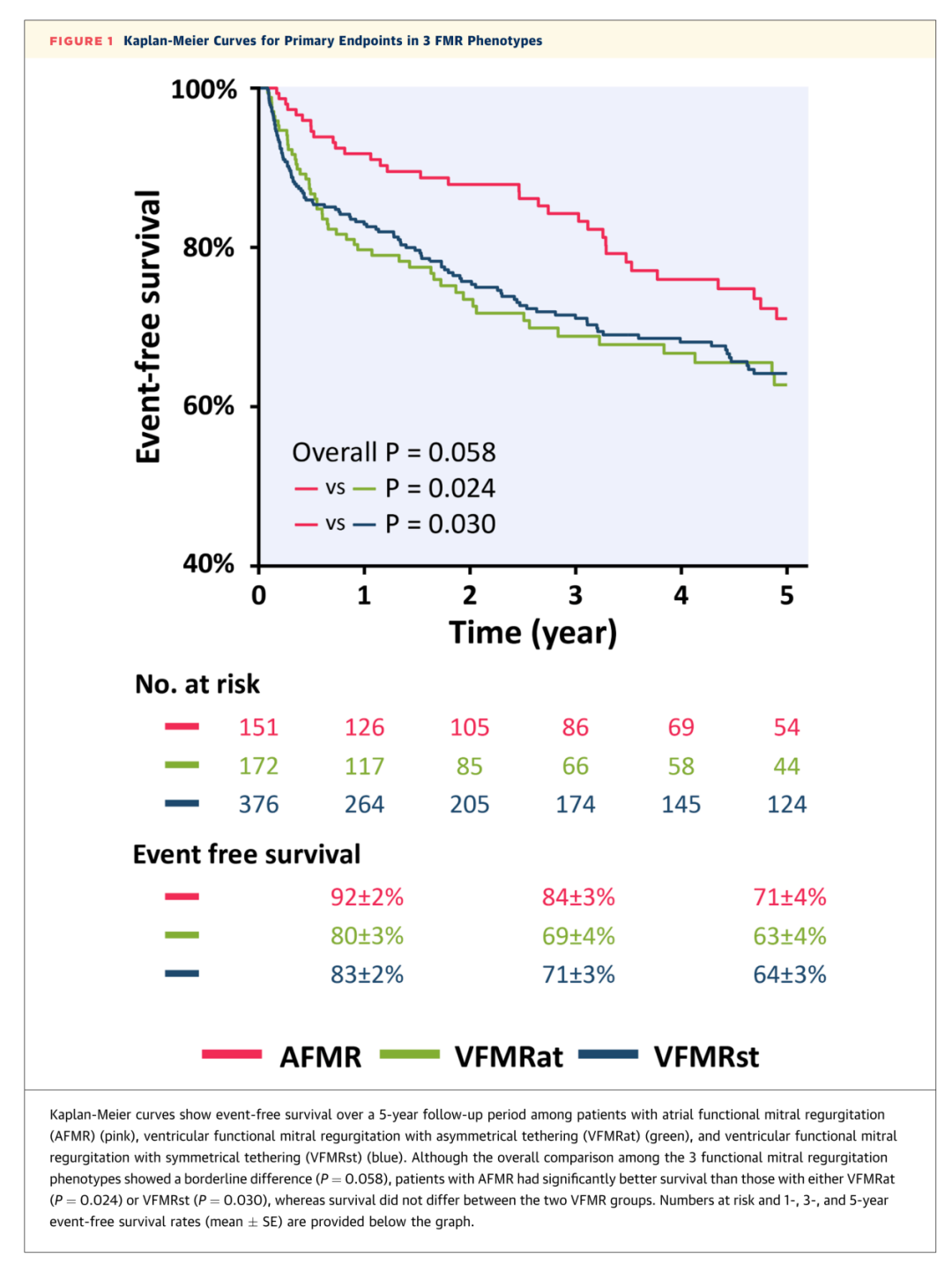
图2 3种FMR表型Kaplan-Meier曲线
主要终点的增量分析
通过向核心模型[MR 表型、分层年龄、性别及纽约心脏病协会(NYHA)心功能分级≥Ⅱ 级]逐步添加舒张压、左心室参数(LVEF、LVESDi、LVESVi、A4C-LVLS)和 LASr 进行增量分析。结果显示:
添加舒张压可显著提升模型的预后价值(P≤0.001);
纳入全部 4 项左心室参数后,预后价值进一步改善(P<0.001);
后续添加 LASr 仍能提供额外预后价值(P≤0.007)。
全因死亡、HTx 及 LVAD 次要终点相关影响因素
在中位随访时间为 2.6 年(Q1-Q3:0.9-5 年)期间,356 例(51%)患者达到次要终点(29 例接受 LVAD/HTx,327 例发生全因死亡)。VFMRst 与次要结局存在单变量关联(P=0.003)。
多变量模型分析显示,查尔森合并症指数(CCI)升高、舒张压降低、RV-FAC 降低、LASr 降低,均与次要结局独立相关(均 P≤0.049);调整后,MR 表型与次要终点无关联。
基于年龄和性别调整后曲线确定终点临界值
整体而言,当舒张压分别低于 73.7 mm Hg 和 72.4 mm Hg 时,主要终点和次要终点的风险逐渐升高,其对应的 LASr 临界值分别为 14.8% 和 15.6%,对应的 A4C-LVLS 临界值分别为 9.3% 和 9.6%(图3)。在头对头比较模型中,A4C-LVLS>9.3% 和 较高的LVEF均与更好的结果相关。
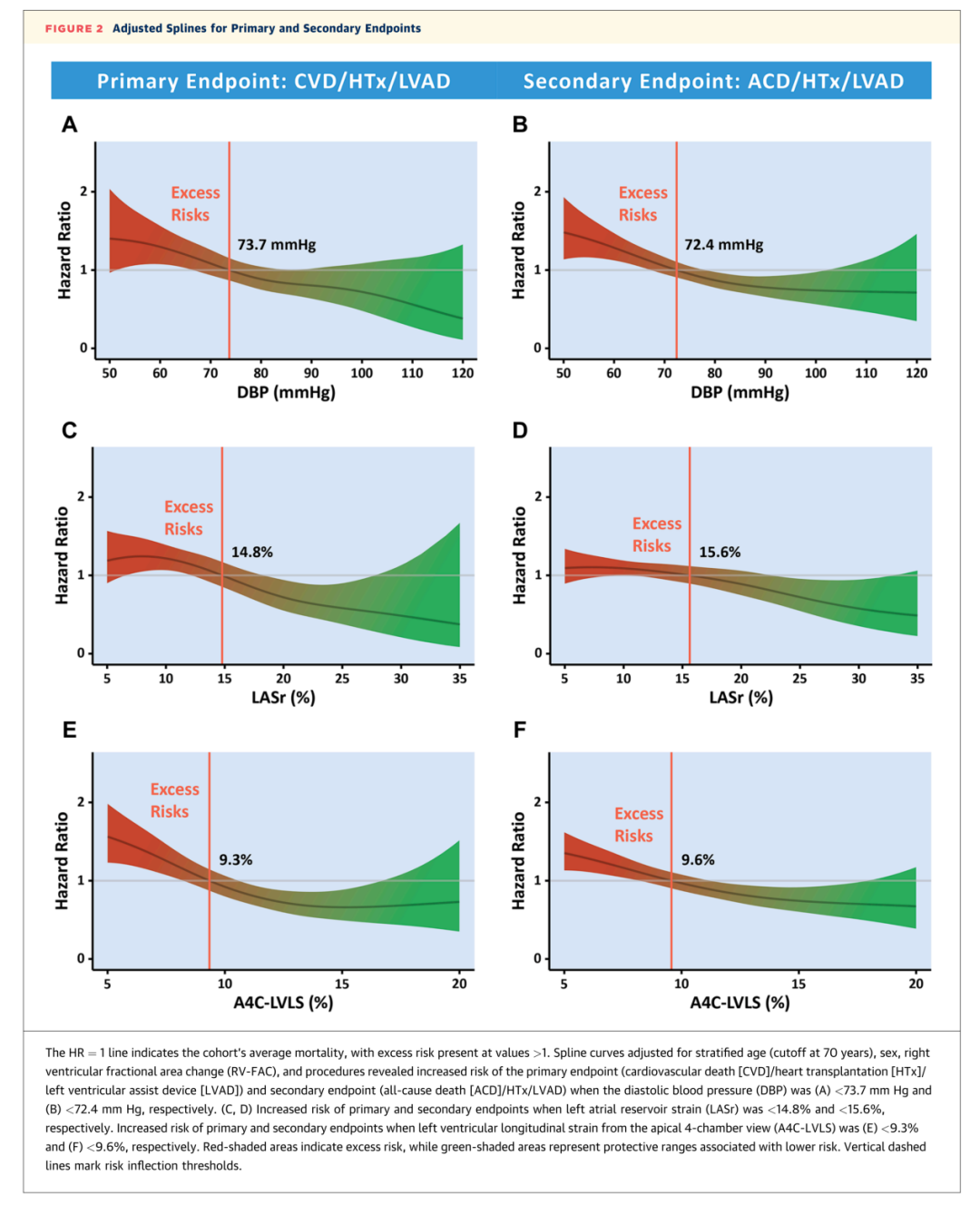
图3 调整后主要终点和次要终点曲线
3种 FMR 亚型的结局影响因素
变量模型中各亚型主要结局的影响因素如下:
AFMR:更大的 MR-VC、更大的 LAVi 及右心室功能受损(均 P≤0.041);
VFMRat:心房颤动、更低的 LVEF、更低的 LASr、更低的 A4C-LVLS 及更大的 LVESVi(均 P≤0.045);
VFMRst:更低的 DBP、更低的 LVEF、更低的 A4C-LVLS、更低的 LASr 及更大的 LVESVi(均 P≤0.041)。
讨论
FMR 的形态学表型
本研究基于二尖瓣形态学特征,提出将 VFMR 分为两种亚型:VFMRat 和 VFMRst。另一方面,既往 AFMR 的分类依赖固定参数,包括 LVEF 临界值、左心室大小/容积或无局部WMA。但在临床实践中,这类患者可能因反流相关容量负荷或心房颤动诱导的心肌病,出现左心室轻度扩张或 LVEF 轻度降低,导致 50% 的 LVEF 临界值可能不可靠。本研究提出的基于二尖瓣形态学的 FMR 表型分类,有助于更全面地理解疾病潜在机制,并更完整地涵盖 AFMR 的疾病谱。
AFMR:一种异质性疾病
尽管本研究通过独特的二尖瓣形态学特征对AFMR进行分类,而非左心室指标,但患者仍表现出相对保留的 LVEF,且平均 LVEDVi 和 LAVi 与既往 AFMR 研究一致。此外,AFMR 患者的症状较 VFMR 患者更轻,这可能是 AFMR 患者易被忽视、就诊时疾病已处于晚期的原因。尽管结果并不理想,但本研究发现AFMR患者的未调整生存率优于 VFMR 患者,这与前者心功能更佳相关,而非表型本身的直接作用。MR-VC 增大、LAVi 增大及右心室功能受损与不良结局相关,这些指标或可帮助识别需要积极二尖瓣干预的高危 AFMR 患者。
本研究还显示,后叶束缚型 AFMR 的患病率较高(40%),且经体表面积标准化后的二尖瓣环大小在两种 AFMR 亚型间无差异,这与近期一项研究结果一致。后叶束缚型 AFMR 患者表现出更大的 LAVi 和 MR-VC。该亚型是否为所有 AFMR 患者的最终共同通路,还是不同心房重构过程的结果,仍需进一步研究证实。
非相称性与相称性 VFMR:基于二尖瓣形态学的视角
“非相称性 FMR”概念用于解释两项标志性试验的结果差异,其核心是乳头肌不对称移位和下侧壁WMA。本研究的 FMR 表型分类与“相称性假设”一致:与 VFMRst 亚组相比,VFMRat 亚组更接近非相称性 FMR,表现为左心室容积显著更小而 MR-VC 更大。然而,两组的二尖瓣反流EROA无显著差异,可能原因包括:1)偏心反流束中,通过近端等速表面积法计算的 EROA 存在低估;2)EROA 数据不完整。
低舒张压与 FMR 不良结局的新见解
低舒张压与多种疾病的不良结局相关,包括射血分数保留的心力衰竭、缺血性心脏病和主动脉瓣反流,其机制可能与冠状动脉灌注减少导致的亚临床心肌损伤或主动脉僵硬度增加有关。本研究首次报道了低舒张压与 FMR 不良结局的关联,其临界值(72.4~73.7 mm Hg)与既往研究结果相似。与其他研究不同,本研究未观察到 J 型曲线现象,这可能是因为 FMR 患者身体状况较弱,且舒张压相较于高血压人群更低。
左心室应变与 LASr 在 FMR 中的作用:左心室-左心房的相互作用
关于 FMR 患者左心室整体纵向应变(LVGLS)的研究较少,本研究证实了其在FMR中的预后价值,发现尽管 AFMR 患者的 LVEF 相对保留,但 A4C-LVLS 却显著降低,可能原因包括:1)反流相关的 LVGLS 降低;2)严重反流时 LVEF 被高估,实际存在收缩功能障碍;3)LAVi 极度增大,反映了左心室-左心房的相互依赖性。简而言之,左心房显著扩大可能限制左心室基底段下移,导致左心室纵向应变(LVLS)降低,而左心室基底段的运动状态又会显著影响左心房储备功能。
本研究还证实了 LASr 作为心房纤维化标志物和不良结局预测因子,是不良事件的强独立影响因素。这可能是因为 LASr 反映了左心室-左心房的相互作用,同时捕捉了两个心腔的功能状态,并能早期检测左心室充盈压升高和左心房功能障碍。但本研究发现,在左心房严重扩大(提示晚期心房功能障碍)的 AFMR 患者中,LASr 的应用价值有限。
总体而言,LASr 展现出了一定的预后价值,但其在指导临床干预中的作用仍不明确,需在未来试验中进一步验证。
研究局限性
本研究为回顾性设计,存在潜在选择偏倚。
难以区分结局影响因素与反流严重程度或潜在心肌疾病的关联。同时,这些影响因素及其临界值是否代表“不可逆转点”,或是否反映对 M-TEER 的潜在反应性,仍不明确。
LVLS仅基于心尖四腔心切面计算。
部分患者的 MR EROA 数据缺失。
指南指导药物治疗的应用不够充分,且由于全民健康保险未覆盖相关费用,仅 2 例患者接受了 M-TEER,无法评估不同表型患者接受治疗后的结局改善情况。
结论
本研究通过提供形态学相关见解,为FMR现有研究文献提供了补充。在三种表型中,AFMR生存率最佳,但仍不尽如人意。后叶束缚型 AFMR 并不少见,可能是 AFMR 的晚期表现形式。与VFMRst相比,VFMRat更接近非相称性MR。除传统的右心室和左心室功能指标外,舒张压、LASr及A4C-LVLS降低,均与 FMR 患者的不良结局独立相关。未来仍需开展进一步研究,以验证表型分类对治疗策略的影响。
JACC: Asia编委会

