
复旦大学附属中山医院心内科黄浙勇教授
思辨介入困境
解析手术技巧
梳理中山经验
助您从新手变“心”手
每月15日、30日,严道医声独家发布
孤立性分支开口病变(Medina 0,0,1))占分叉病变的<5%,相对少见和次要。但如何处理,尚无最优方案[1, 2],药物?球囊?单支架?双支架?讨论空间极大。
由简入繁,走一步看一步,可能是处理孤立性分支开口病变的一种实用策略(图1)。
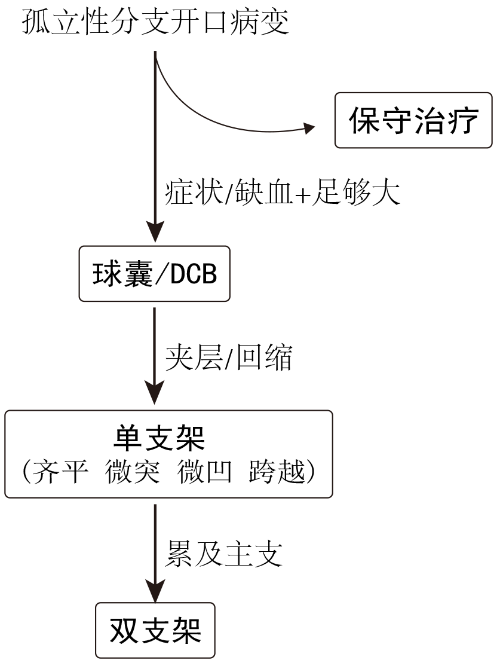
图1 孤立性分支开口病变的处理流程。
一
是否需要介入?
设想一下,前降支支架置入后对角支开口狭窄即使高达90%,也往往不予处理,体现了“怠慢”处理分支开口的合理性。临床研究也发现,孤立性分支开口病变采用药物治疗不劣于甚至优于介入干预[3, 4]。
因此,孤立性分支开口病变,药物治疗是默认选项,介入治疗实际上属于二线选择。原因并非药物疗效卓著,而是介入疗效差强人意。(1)分支支配心肌少,介入获益不大;但可能累及主支,譬如斑块移位、脊移位、主支夹层等,介入风险不小。 “因小失大”,“得不偿失”,是分支开口病变介入治疗的主要顾虑。(2)分支开口支架定位难以精准,尤其是成角小的Y型病变,要么分支开口支架覆盖不全(缺失),要么支架突入主支(冗余)。(3)分支开口弹力纤维丰富,病变容易钙化纤维化,球囊扩张后易弹性回缩,被迫植入支架。即使植入支架,也容易扩张不全或贴壁不良,导致介入再狭窄。
一般认为,只有药物治疗无效的“有症状/缺血+大分支”的患者才需要介入干预。
(1)症状:作为ACS或STEMI的靶血管,PCI没有争议。但稳定性心绞痛患者需要思考症状是否与分支开口狭窄相关,最好参考功能学评估。
(2)缺血:缺血金标准是FFR等功能学评价,冠脉造影和腔内影像只能反映狭窄程度的解剖学改变(图2)。Koo研究[5]支架后分支开口受累情况,若造影<75% ,FFR均无意义;若造影 ≥75%,只有27%(20/73例)FFR有意义。
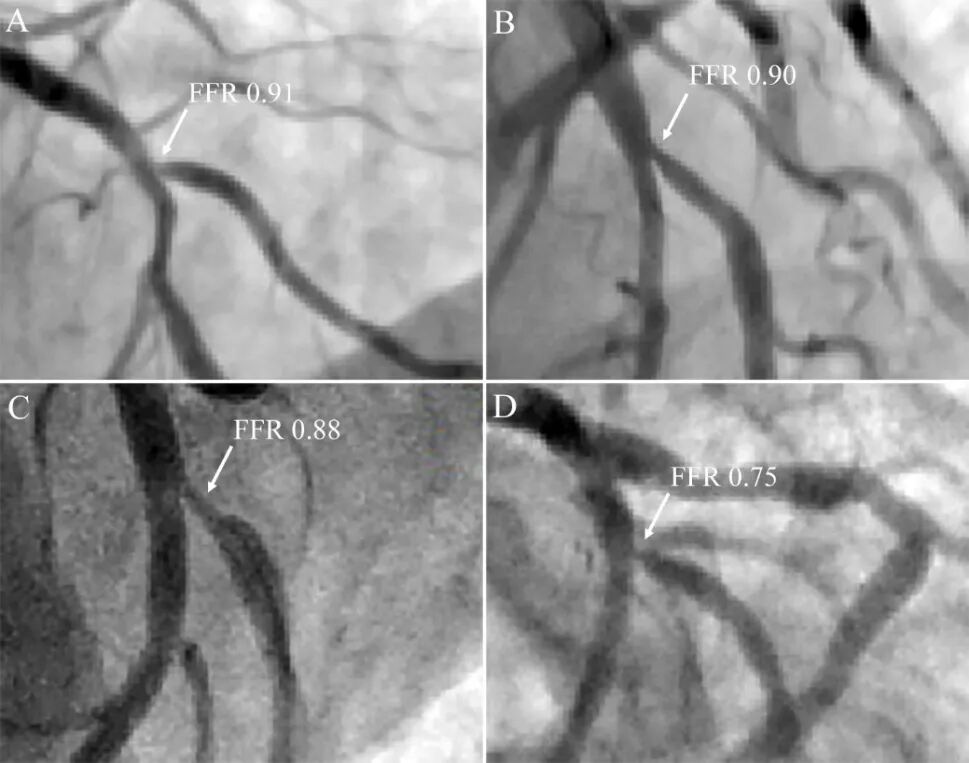
图2 对角支开口病变,造影容易高估狭窄程度
事实上 ,即使是分支开口的解剖学评价,也困难重重。
冠脉造影的局限性。一般血管的狭窄程度可多角度评价,但评价分叉开口的最佳视线是固定的:分叉平面的垂直方向!一方面,假如偏离该方向,冠脉造影容易遗漏孤立性分支开口病变,因此强调需要多体位透照,以寻找最佳体位。另一方面,假如以该方向评估,经常 “评判过重”。为何?成角边支开口呈扁圆形,斑块位于分叉脊对侧面!详见《冠心病介入治疗解码》第15章。
腔内影像的局限性。对分支开口病变,腔内影像对狭窄程度的评价也不尽可靠。一方面,由于分支大小不一,腔内影像缺乏狭窄介入干预的管腔面积绝对值;另一方面,成像切面与超声探头垂直(与导丝长轴垂直),而导丝在分支开口存在弧度和成角,因此最终成像往往是斜截面而不是横切面(图3)。
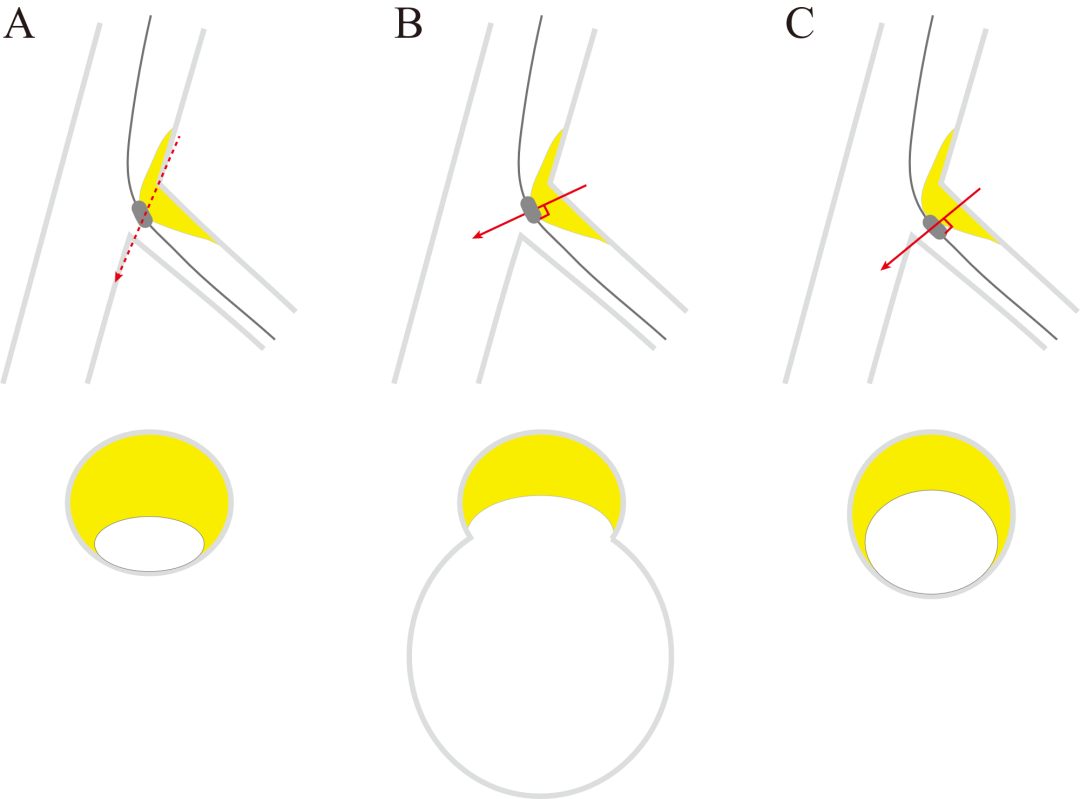
图3 腔内影像评估分支开口病变的局限性。
A 不可能的成像“横”切面;B 开口部成像“斜”切面;C 近端成像“斜”切面
(3)解剖学意义:需要评估分支的重要性,一般认为<2mm分支意义不大,但要结合血管长度、基础心功能等具体情况。另外,腔内影像学评估斑块性质,可预测介入难度和介入风险。对于重度钙化开口病变,要思考有无旋磨等特殊器械。
二
尝试球囊扩张?
药物球囊(DCB)的适应症越来越宽泛,几乎无绝对禁忌[6]。对于孤立性分支开口狭窄,DCB处理的优势是对主支血管影响较小,也无支架植入关于“缺失和冗余”的顾虑,因此是一种广为接受、富有前景的方法(图4-5)。缺点是球囊扩张后容易出现夹层或弹性回缩。若出现严重夹层或弹性回缩,尤其是血管直径≥2.5mm的分支开口病变,可转为支架治疗。Vaquerizo报道[7]DCB治疗后,14%患者需要补入支架;1年后14%患者需要再次靶病变血运重建。
预处理是药物球囊成功的关键。(1)减少夹层形成:建议逐步缓慢增加扩张直径;(2)尽量充分预扩张:可采用高压球囊、切割球囊,钙化严重者采用旋磨或震波球囊预处理[8]。(3)鉴于分支缺血耐受时间较长,因此建议DCB扩张时间尽可能超过90秒。
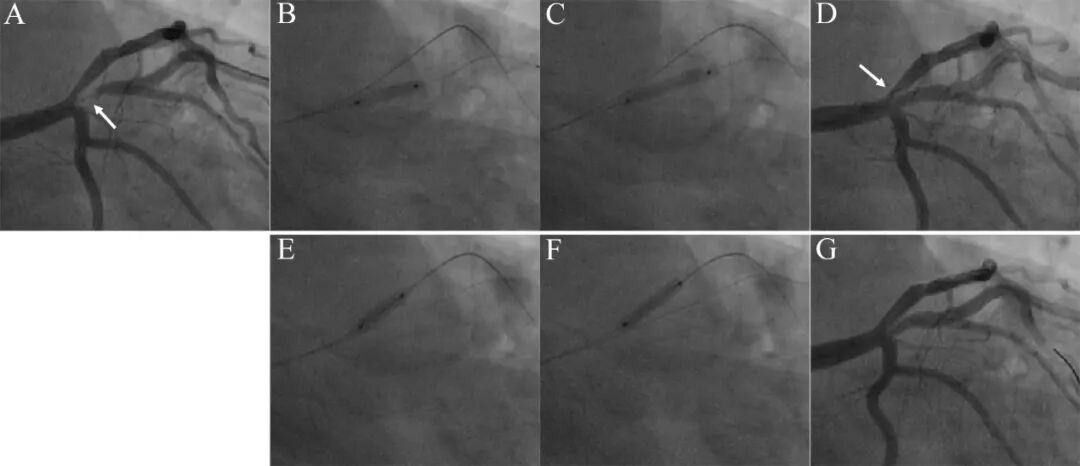
图4 球囊扩张处理中间支开口病变。
55岁吸烟男性,劳力性心绞痛1个月。造影示前降支近段狭窄40%,粗大中间支开口狭窄95%(A)。2.5mm×15mm半顺应性球囊和2.75×10mm切割球囊预处理病变(B),最后2.75×15mm药物球囊10atm×45秒扩张中间支开口病变(C),中间支残余狭窄<50%,但前降支开口狭窄加重(D)。同样流程处理前降支开口病变,先后以2.5×15mm半顺应性球囊、2.75×10mm切割球囊(E)、2.75×15mm药物球囊扩张前降支开口病变(F),造影结果良好(G)。IVUS检查前降支开口和中间支最小管腔面积(MLA)分别为5 mm² 和 4.81 mm²。
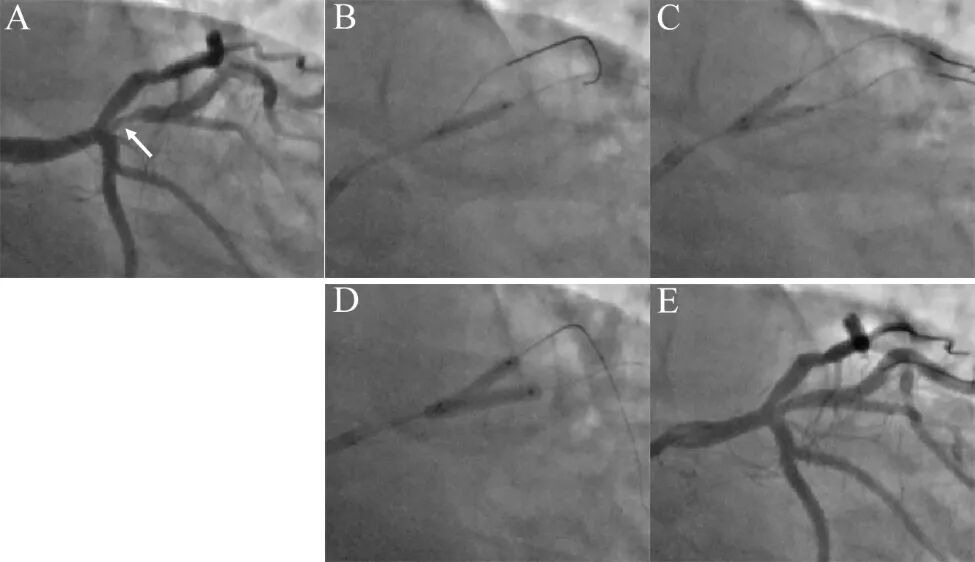
图5 球囊对吻处理中间支开口病变。
图4同一病例11个月后,再次出现劳力性心绞痛,性质同前。复查造影提示中间支开口病变再次加重至90%(A)!分析再狭窄原因,可能与前降支扩张时斑块移位和脊移位有关,也可能与中间支未充分扩张导致斑块弹性回缩有关。决定采用球囊对吻技术,首先2.75×10mm切割球囊预处理病变(B),然后两个2.75高压球囊8atm×20秒对中间支和前降支对吻扩张(C),最后2.75mm×15mm药物球囊12atm×45秒对吻扩张(D),造影结果良好(E)。IVUS检查前降支开口和中间支开口MLA 分别为5.5 mm2和5.6 mm²。随访2年未有心绞痛再发。
三
单支架技术采取哪种术式?
理想的支架定位既要完全覆盖分支开口,又无主支内支架突出,但这种理想模式只有成角90°时才有可能实现。真实世界里,分叉角度并非直角,因此理想定位几乎是不存在的,“冗余和缺失”的矛盾始终存在:支架太远,分支口覆盖缺失;支架太近,主支内支架梁冗余(图6)。
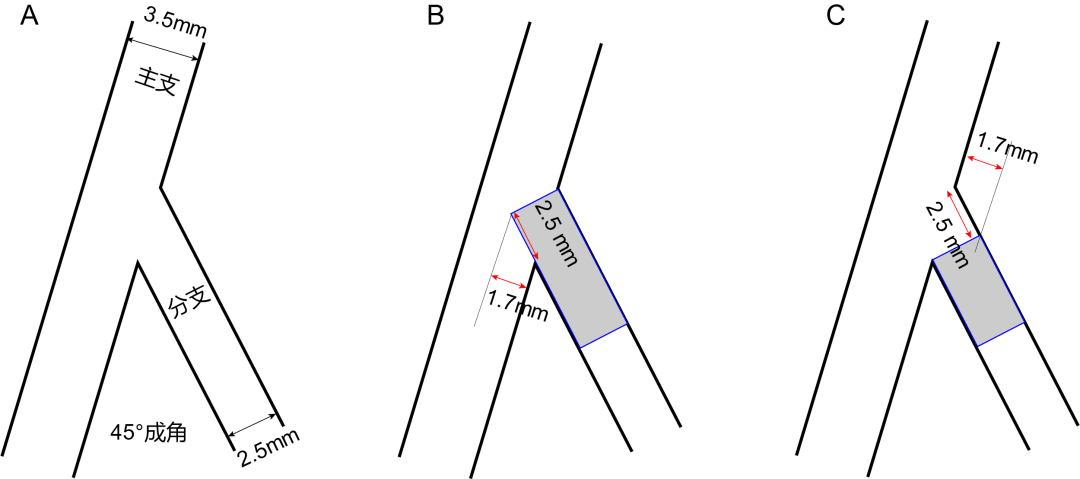
图6 分支开口支架的冗余和缺失[2]。
假设分叉成角45°角,主支内径3.5mm,分支内径2.5mm。若支架齐平分支开口上缘,主支内支架冗余1.7mm;若支架齐平分支开口下缘,分支开口支架缺失缺失2.5mm。
因此,支架定位需要权衡冗余和缺失的利弊,努力实现“冗余+缺失总值”最小化。如分支开口起始部(origin)病变轻、分支不太重要,宁可多缺失一点(精准或微凹);反之,如分支粗大,分支开口病变严重,主支有病变,宁可多冗余一点(微突或跨越)(图7)。

图7 支架定位区间示意图。
蓝色区域为精确定位,支架“冗余+缺失”总值最小化;黄色区域为微突法,支架冗余过多;绿色区域为跨越法(crossover),支架跨越至主干;红色区域为微凹法,缺失过多。
1、 支架精确定位技术
所谓的支架精确定位适合于分叉角度大、分支开口起始部(origon)狭窄不重的病例(图8)。
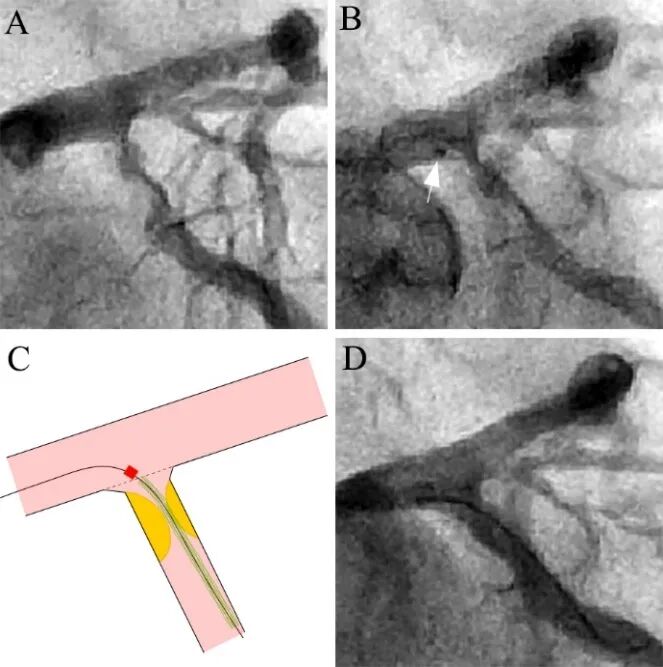
图8 回旋支开口精确定位。
本例回旋支开口严重狭窄有两个特点(A):其一,成角接近90°;其二,起始部呈喇叭形,IVUS证实开口无明显斑块;因此适合精确定位技术。支架定位时将标志点(marker)定位于左主干轮廓内,此时支架刚好平开口位置(B)。C为示意图,注意标志点和支架近段存在一定间隙。最后结果良好(D)。
有一种简单的、粗犷的辅助定位技术,叫做主支球囊辅助下的支架回拉技术[9](图9-10)。要点是主支内放置低压释放的球囊协助分支支架的定位。首先,将分支支架送至远端, 主支放置球囊。然后主支球囊6~8 atm加压膨胀,回撤分支支架,直至主支球囊出现明显的压痕凹陷(dent),此时释放支架。缺点是主支球囊有可能损伤主支血管。另外,回拉力量不同和凹陷大小不同将影响支架位置,最后结果有可能是精准定位,也有可能是微突或微凹。
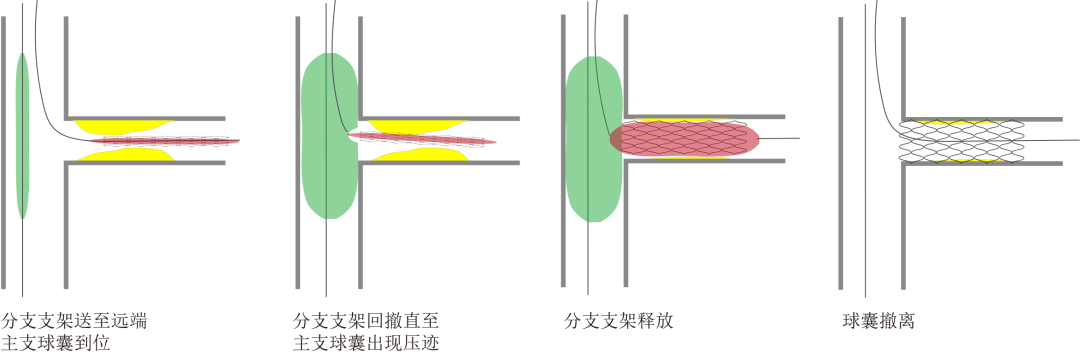
图9 支架回拉技术定位支架
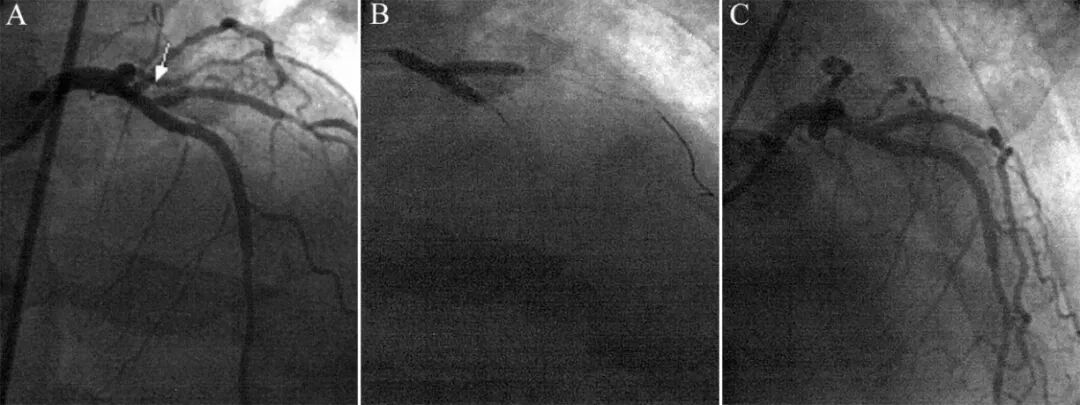
图10 支架回拉法处理对角支开口病变[10]。
对角支开口狭窄80%,前降支狭窄20%(A)。前降支4.0×20mm球囊4atm低压扩张,同时对角支3.0×13mm支架回拉,遭遇阻力并出现压迹时,16atm释放支架(B),最后结果良好。
还有一种相对复杂一点的操作,支架尾端用导丝锚定的Szabo定位技术(图11)。详见《冠心病介入治疗解码》第20章和21章。
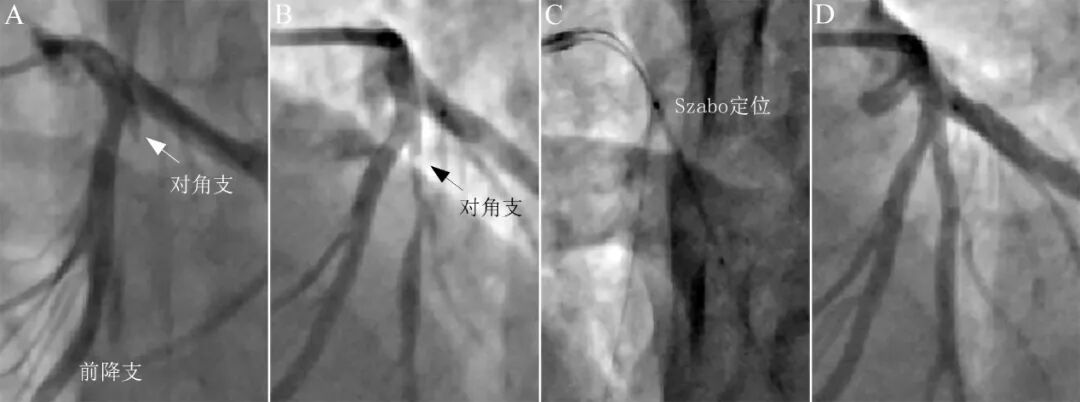
图11 Szabo精确定位处理对角支开口病变。
40岁吸烟男性,胸痛1天,心电图诊断为急性高侧壁心肌梗死。造影显示前降支近中段狭窄40%,第一对角支开口完全闭塞(A)。Sion导丝顺利通过,预扩张后提示对角支粗大,近段残余狭窄90%,开口部1-2mm基本正常,决定采用Szabo技术。齐平对角支开口植入支架(C),造影结果良好(D)。
2、支架微突技术
为确保对分支开口的完全覆盖,有术者强调支架微突入主支,所谓支架微突技术。由于分支开口病变或多或少会累及主支血管,万一分支支架植入后主支加重或夹层,微突支架基础上可丝滑变换为双支架术式。
突出到主支内的支架需要加以挤压贴壁,根据挤压方式,可以分为T处理(冗余支架梁挤压于血管脊部位)、Crush处理(冗余支架梁挤压于分支开口四周血管壁)和Culotte处理(冗余支架梁挤压于主支四周血管壁)(图12),方法学类似于双支架技术时对分支支架的处理方式。
后续处理根据具体情况灵活进行,如主支球囊扩张、球囊对吻扩张、主支药物球囊扩张、甚至双支架植入等。

图12 微突支架的挤压方式。
注意重置导丝的方式和支架梁最后的分布位置。
(1)T处理。冗余支架梁挤压于血管脊部位,成为额外的金属脊。
(2)Culotte处理。冗余支架梁挤压于主支四周血管壁。最极端的例子是将最近端的一个支架梁挤压于主支四周血管壁,形状呈现花瓣样,简称花瓣技术[11]。
(3)Crush处理。将冗余支架梁挤压于分支开口四周血管壁,为避免支架梁阻挡分支开口,建议重置导丝后扩张对角支开口[12](图13)。最复杂者当属2023年报道的Osdokina 技术,但不推荐。
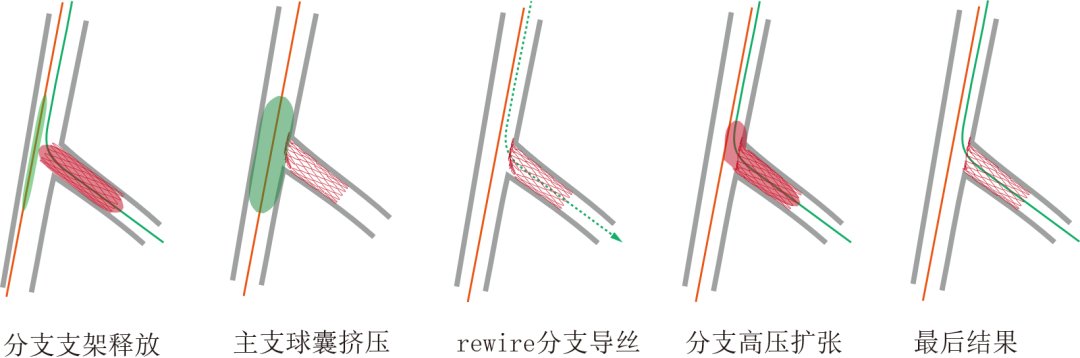
图13 微突+Crush处理的基本流程
关于花瓣技术和Osdokina 技术,笔者将撰写专门章节简单介绍。
3、支架微凹技术
按照一般定义,开口病变指距离开口起始部3mm之内的病变,因此部分所谓开口病变的起始部可以基本正常。此时支架不一定要覆盖起始部,只要覆盖病变即可(图14)。事实上,这已经不是严格意义上的分叉开口病变。
另一种情况是真正的分叉开口病变,但无意中支架定位失败,导致开口支架覆盖不全(缺失);或者为了避免损伤主支,有意将支架保守定位,导致开口支架覆盖不全(缺失)。此时也并非不可接受,可在缺失部位药物球囊扩张加以补偿。
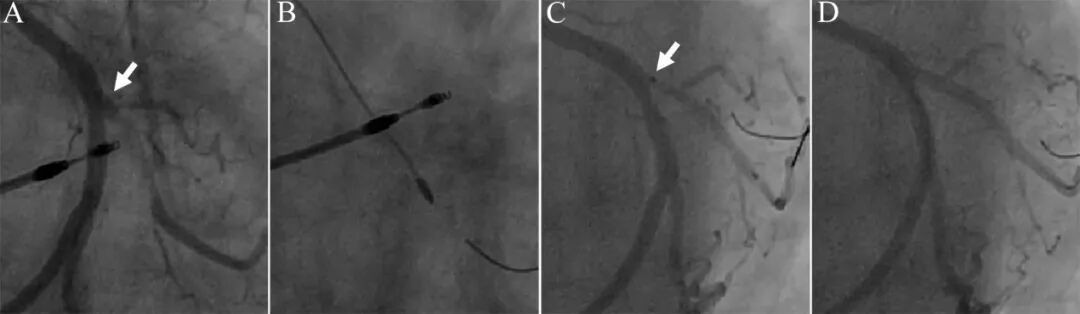
图14 钝缘支开口微凹定位。
钝缘支开口严重钙化病变,起始部血管尚可(A,箭头),因此适合微凹技术。普通球囊不能扩张,启动1.25mm磨头旋磨治疗(B)。鉴于钝缘支粗大,微凹法置入支架。支架定位时将标志点(C,箭头)定位于回旋支主支轮廓边缘,此时支架距离钝缘支开口1-2mm。最后结果良好(D)。
4、单支架跨越技术
单支架跨越(Crossover)术式或称为必要时支架术式(Provisional stenting)是分叉病变最常用的、最成熟、甚至是默认的术式。操作时,自主支近段至主支远段进行单支架置入,跨越分支开口。
若孤立性分支开口狭窄采用单支架跨越技术,需要自分支到主支近段支架植入,因此有人称之为反向单支架技术(Inverted provisional stenting)(图15-18)[13]。其优点是保证分支覆盖完全,保证了分支的利益,但潜在的损害了主支的利益,可能“因小失大”:(1)额外增加主支支架负荷;(2)分支和主支落差过大,难以选择合适支架,主支支架很可能贴壁不良;(3)主支分叉口狭窄加重(斑块移位和脊移位),若对吻后存在一定的夹层和血肿风险。因此,仅适用于分支直径粗大的患者。Brunel等[13]完成小样本量试验,手术成功率高。
操作注意事项:(1)主支支架贴壁问题。由于主分支落差较大,必须选择扩张性好的支架,另外支架植入后充分POT处理,尽量保证主支贴壁。(2)主支远端受累问题。支架置入后,主支远端或多或少受累,通常需要扩张网孔,必要时高压球囊对吻、药物球囊等处理,甚至转变为双支架。
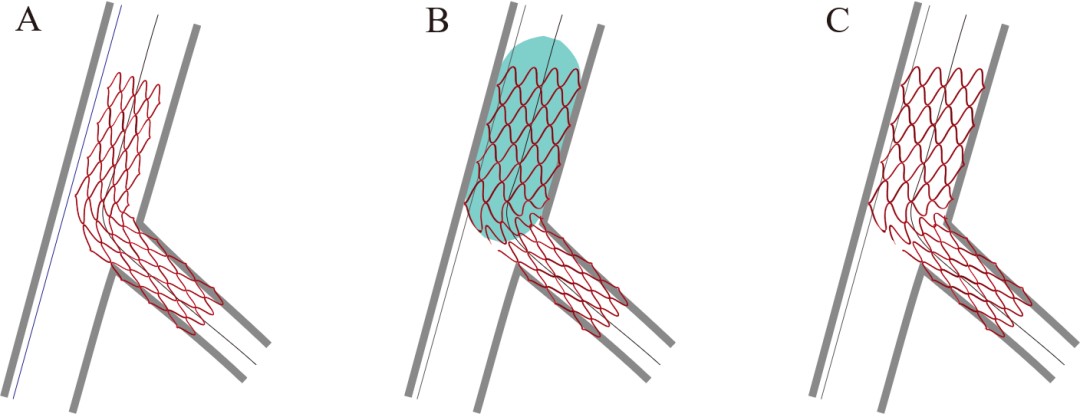
图15 单支架跨越技术。
A根据分支血管选择支架直径;B 植入后POT优化;C评估主支受累情况,必要时主支球囊扩张、球囊对吻、药物球囊、双支架等处理。
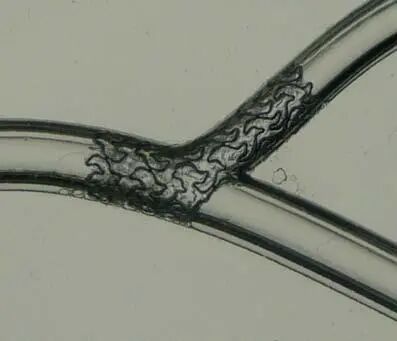
图16 单支架跨越式植入+球囊对吻的体外实验结果(TAXUS支架)[13]。
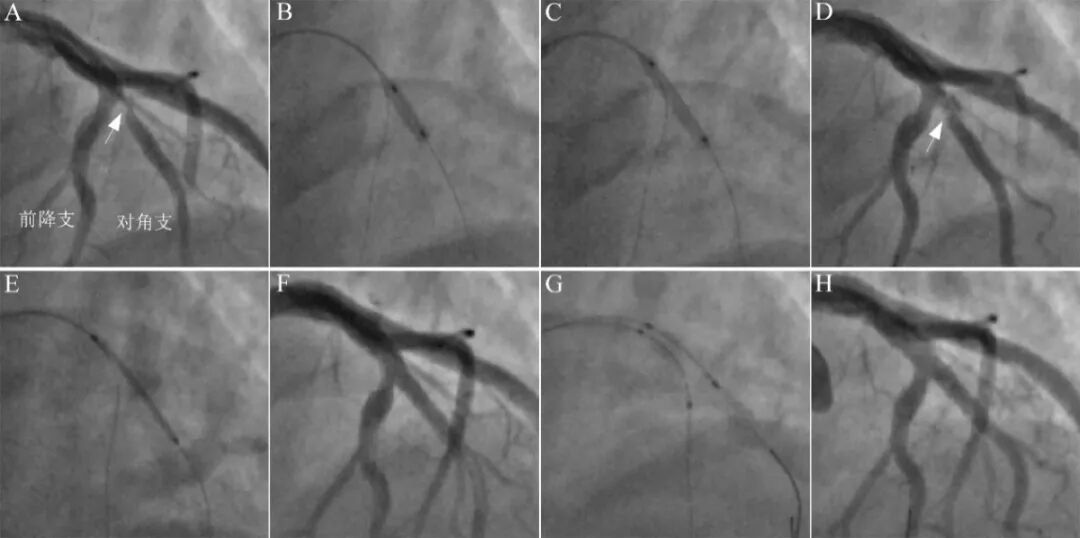
图17 单支架跨越技术处理对角支开口病变。
48岁女性,运动后胸痛3年,加重2周,肌钙蛋白轻微升高,诊断为NSTEMI。造影提示前降支中段狭窄50%,第一对角支开口狭窄95%(A)。对角支为靶病变。首先尝试球囊处理,2.5×10mm切割球囊处理后(B),2.5×15mm药物球囊扩张60秒(C),造影提示对角支开口明显夹层形成(D)。鉴于对角支比较粗大,夹层累及开口部,决定采用单支架Crossover置入。前降支近段-对角支近段植入3.0×18mm药物洗脱支架(E),近端POT。造影提示前降支狭窄有所加重(F),提示脊移位或斑块移位可能。二个3.0mm高压球囊对吻扩张(G),然后前降支局部3.0×15mm药物球囊扩张30秒处理。最后结果良好(H)。
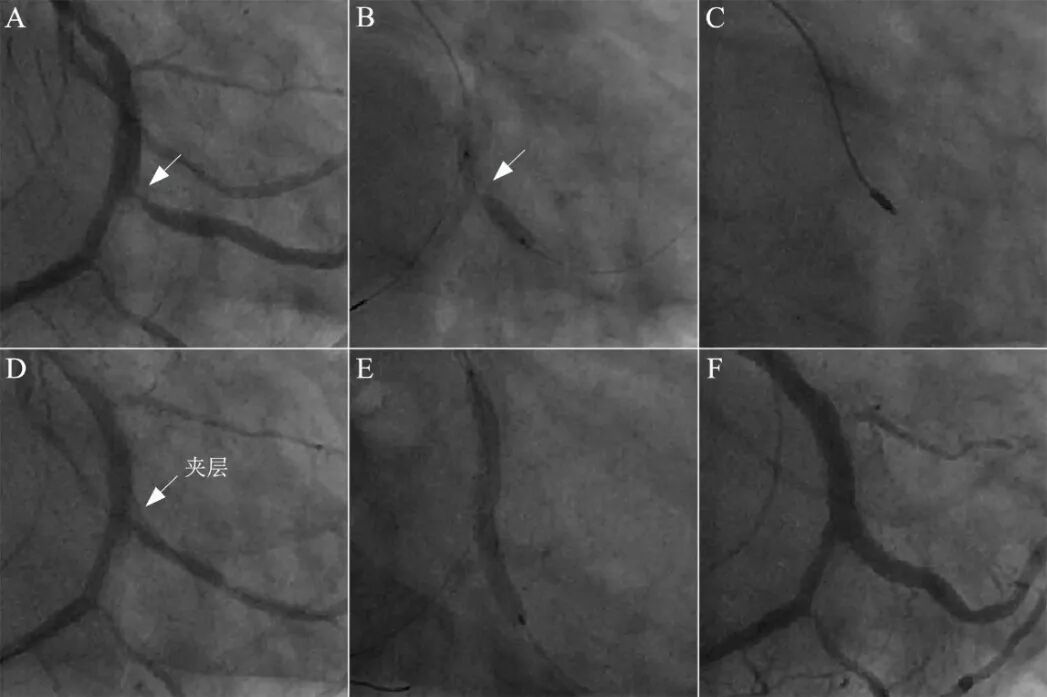
图18 单支架跨越技术处理钝缘支开口病变。
钝缘支开口钙化性狭窄95%(A),球囊16atm膨胀不全(B),启动旋磨治疗,1.25mm磨头尝试3次后顺利通过(C),球囊扩张后可见明显夹层形成(D)。鉴于钝缘支粗大,直接跨越法置入支架(E),结果良好(F)。
四、兜底的是双支架技术
若DCB处理分支开口病变出现严重夹层,可补入支架,这并非手术的失败;同理,若单支架后出现主支并发症,主支可补入支架(双支架),这也不是手术的失败!因此,走一步看一步、随机应变是处理001病变的技术策略。研究发现001型分叉病变双支架技术疗效和单支架技术并无差别[14],说明双支架可作为最后兜底的选择(图19)。
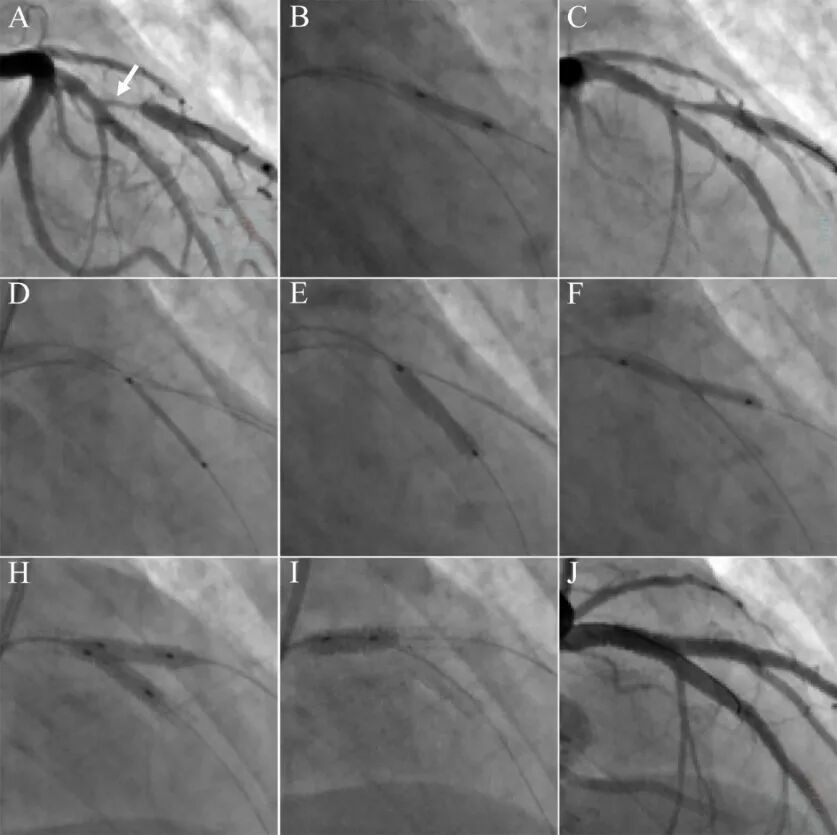
图19 Szabo双支架处理分支开口病变。
60岁女性,胸痛2个月。造影提示前降支近中段狭窄40-60%,粗大对角支开口狭窄95%(A)。首先尝试球囊处理,2.0mm半顺应性球囊和2.5mm切割球囊处理(B),对角支开口夹层形成,残余狭窄60%(C),决定直接采用双支架技术。鉴于对角支粗大,反观前降支略小+中段肌桥,决定采用反转Szabo双支架技术。主支远段(前降支中段)采用Szabo技术置入3.0×15mm药物洗脱支架(D-E),主支近段-对角支近段置入3.5×24mm药物洗脱支架(F),高压球囊对吻扩张(H),近端POT(I),最后结果良好(J)。
五
小结
手在分支,心在主支;主次分明,切忌因小失大。孤立性分支开口病变的介入处理原则比较保守,“有症状、有缺血、直径较大”才介入干预。简言之,能不介入就尽量药物治疗,必须介入就尽量DCB处理,必须支架尽量单支架,能精确定位就尽量避免主支突出和主支kissing,最后双支架技术兜底(图1)。
原则只是原则,实践中要结合分支大小、分支角度、分支开口病变特性等情况灵活处理。
参考文献:
⇅ 向上滑动阅览
“中山PCI解码”下期预告
花瓣技术
2005年Szabo提出一种专门针对开口病变精确定位的支架置入方法:支架尾端导丝锚定技术,即Szabo技术。在此基础上,2013年Cayli提出支架尾端球囊锚定技术,即花瓣技术(Flower petal technique)。我们对此做一介绍。


