QICC2017 | 沈法荣:CIED围手术期感染预防策略
2017-09-13 19:14
浙江绿城心血管病医院 沈法荣
植入性心脏电子装置(CIED)围手术期感染的发生是临床遇到的最为棘手的问题之一。通常会导致囊袋发红、破溃,伤口反复不愈。严重的必须拔除植入装置,包括电极导线和整套植入装置。因此了解CIED围手术期感染的发生、造成的原因以及预防的措施对于临床有着非常重要的意义。
一、CIED围手术期感染的现状
CIED感染的临床表现包括起搏器囊袋部位有局部炎症和浓肿形成,起搏系统的一部分露出皮肤表面而伴有继发性感染,发热和血培养阳性,伴或不伴有感染灶。CIED感染的分类1包括囊袋浅表皮肤感染、囊袋感染、菌血症以及感染性心内膜炎。其中,感染性心内膜炎又分为两类,一类是电极导线及心腔内赘生物,另一类是瓣膜赘生物。CIED感染的类型包括切口感染(I型)、囊袋浅表炎症(Ⅱ型)、囊袋破溃,装置外露(Ⅲ型)、导线赘生物或瓣膜赘生物(Ⅳ型),以及发热和血培养阳性,伴或不伴有感染灶(Ⅴ型)。I型和Ⅱ型为早期(<1个月);Ⅲ- Ⅴ型为中晚期。(如表1)
表1 CIED感染类型
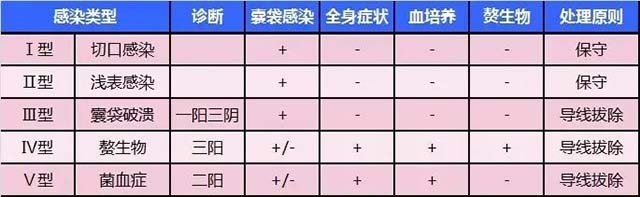
美国流行病学调查显示2,CIED感染的发生率自1993年开始,感染的比率整体亦成增长的趋势,2008年CIED感染的发生率为2.4%。美国流行病学调查显示,自2003年开始,感染的例数整体成增长的趋势。红色代表导线拔除的例数。(如图1)

图1 美国CIED感染发生率及导线拔除例数
CIED感染发生率增多的原因有很多3,包括CIED植入指征拓宽、老年患者比例增加、合并其他疾病增多、升级及更换比例增加,以及ICD或CRT/D增加。
美国流行病学调查显示,自2003年开始,CIED感染的死亡率在4%以上。导线拔除伴随囊袋感染的死亡率远远高于单纯的导线拔除,死亡率高达4%以上。NCDR研究4对CIED感染数据进行了分析。此研究对2006-2009年期间植入ICD患者(n=200909)感染情况分析。共有3390位患者发生感染,1.7%。初次植入患者感染率为1.6%;ICD更换感染率为1.9%。P<0.0001。感染发生时期为早期(0-28天)有25%,晚期(29-364天)有33%,延迟(>365天)有42%。感染相关因素包括术后血肿、电极移位,先前瓣膜手术,器械升级,肾脏衰竭透析患者等。
二、CIED围手术期感染的原因
CIED围手术期感染的原因包括器械因素、围手术期因素、患者因素,以及医生因素。器械因素包括导线数量多、器械类型复杂和装置更换/升。围手术期因素包括术前使用临时起搏器、围术期使用中央静脉或股静脉导管和围术期未使用预防性抗生素。患者因素包括长期使用免疫抑制剂及类固醇激素、长期使用抗凝剂、抗血小板药、慢性疾病,以及年龄大、体瘦,长期摩擦囊袋。医生因素包括术者经验不够丰富、手术时间长,以及囊袋靠外、表浅。
CIED感染的处理分为保守治疗和拔除。抗生素的保守治疗适用于囊袋浅表皮肤及切口感染,以及不适宜拔除的囊袋感染。拔除的适应证包括囊袋感染、血行感染,以及感染性心内膜炎。在确诊后,单纯抗生素保守,治疗几乎100%失败。需要尽早进行整体拔除感染装置。
感染的高危因素包括年龄与性别、伴有多重疾病、植入装置的类型、CIED更换/升级/调整,以及囊袋血肿。在年龄与性别方面,美国流行病学调查显示5,男性的感染比例高于女性,65-79岁群体的感染人数虽然最高,但同时也是CIED的主要植入年龄段,反而是64岁之前的患者感染风险更高,高龄并不是感染的高危因素。伴有多重疾病方面。包括心衰、糖尿病、血栓栓塞、晚期肾病、慢性肾病,以及营养不良。植入装置的类型方面,CRT植入的感染风险最高,可能与植入装置的大小、植入的时间、导线植入的数量有关。CIED更换/升级/调整方面,多项研究6带来的结果指出CIED的更换/升级/调整增加感染的风险。囊袋血肿方面,Vidal等7的研究,对照感染研究入选病人659例,1年随访期总体感染率为2.4%(16 of 659),同时伴有囊袋血肿史的感染率为11% (7 of 66),不伴有囊袋血肿史的感染率为1.5%(9 of 593)。研究同时发现,囊袋血肿是术后感染的独立预测因子。
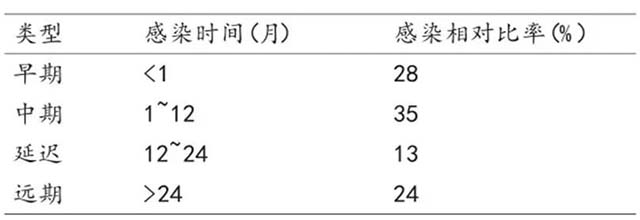
CIED感染的时间如下表2,分为早期、中期、延迟和远期。心律植入装置感染与处理的中国专家共识 2013指出,CIED 围手术期的感染预防很重要。
表2 植入装置感染发生时间的分类
三、CIED围手术期感染的预防
CIED感染的预防包括抗生素的应用、术前皮肤准备、囊袋的处理、起搏抗菌膜的使用,合适的CIED装置,以及术前全身情况的准备。
1 抗生素的应用
REPLACE研究8是一项前瞻性,单盲,多中心研究。入组72家中心,共计1744名CIED更换患者。所有患者术前静脉滴注抗生素、68.7%的患者术后应用抗生素。结果现实,22名患者6个月内发生术后感染,感染率1.3%(低于2.4%),5名曾有囊袋血肿的病人发生感染,感染率为22.7%(5 of 22)。研究结论表明,术前应用抗生素可以显著降低术后感染发生率,囊袋血肿是术后感染的独立预测因子。
Rabih等9的研究也提示,术前一小时应用抗生素可以有效降低感染风险。目前共识中 I类推荐术前应给予针对葡萄球菌的抗生素,可选择一代头孢菌素(头孢唑林)或万古霉素,对一代头孢或万古霉素均过敏时,可选用达托霉素和利奈唑胺。
CIED手术抗生素的预防性使用原则是按照《抗菌药物临床应用管理办法》(卫生部令第84号)规定(2012年5月8日发布,自2012年8月1日起施行)。原则上不预防使用抗菌药物(介入手术等)。Ⅰ类切口(CIED等)手术患者预防使用抗菌药物时间控制在术前30分钟至2小时,预防使用抗菌药物时限不超过24小时。Julio等10进行的首个大型,随机,双盲,安慰剂对照研究,连续入选1000例行CIED植入或更换患者,随机分为两组,Ⅰ组术前接受头孢唑啉1.0g静脉滴注,Ⅱ组术前接受安慰剂治疗。随访时间为术后10天,1月,3月,6月。入选至649例患者时提前终止。结果显示,接受头孢唑啉组感染发生率明显降低(0.64% VS 3.28%,P=0.016)。
2010年AHA《心血管置入电子装置感染和处理最新共识》建议,可预防性使用针对葡萄球菌的抗生素头孢唑啉,术前1小时静脉注射(Ⅰ,A类)MRSA,感染高危患者,可预防性使用万古霉素,术前2小时 静脉注射(Ⅰ,A类)。植入CIED患者进行牙科或其他手术时,不推荐预防性使用抗生素以防止CIED感染(Ⅲ,C类)。
2 术前皮肤准备
术前要求患者清理囊袋处皮肤。现在有不少医疗机构会在术前于手术区域应用无菌手术薄膜。
3 囊袋的处理
囊袋出血的原因通常包括锁骨下静脉穿刺处出血、小动脉破裂出血、头静脉结扎不牢出血、抗凝、抗血小板药物应用、中药,以及全身疾病引起等。预防及处理的原则包括术前评价凝血功能停阿斯匹林等1周;停低分子肝素12小时;停华法林并调整INR在<1.5-1.8, 48h后服用;术中压迫及结扎止血;术后伤口加压包扎;出现血肿后,少量不需处理;中量可在无菌下穿刺抽吸;如持续出血切开清除结扎出血血管,不留置引流条。同时需要制作合适囊袋大小,保持适当的张力。(如图2)
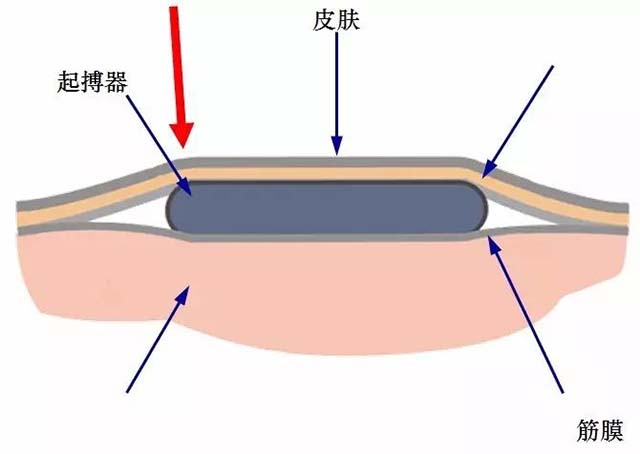
图2 起搏器囊袋示意图
4 选择合适的CIED装置
对于CIED感染的高危病人,皮肤纤薄的病人,在装置选择时应为其选择合适的植入CIED植入装置及电极。
5 起搏器抗菌保护套应用
2013年FDA批准的起搏器抗菌保护套(AIGISRx R)可以降低70-100%的感染风险,同时能够保障CIED在囊袋的稳定性。Matthew等11进行的一项大样本量的临床研究,入组TYRX-A(生物可吸收型抗菌保护套)135例、TYRX(非可吸收型的抗菌保护套)353例、对照组(未使用抗菌保护套)636例。在超过300天的随访跟踪之后,结果显示,TYRX-A组感染率为0%, TYRX组感染1例,感染率0.3%,对照组感染20例,感染率 3.1%。研究结论表明,生物可吸收型抗菌保护套及非可吸收型的抗菌保护套能显著的降低CIED的感染发生率。
在五项研究共计4769名患者中,其中使用TYRX抗菌保护套的患者共计2214例,发生感染14例,感染率为0.63%,对照组为2565例,发生感染60例,感染率为2.3%。应用抗菌保护套可以显著降低感染风险。
6 术前全身情况的准备
术前一般身体状况的评估包括低蛋白血症、贫血等。其它脏器有否感染情况。出凝血功能的评估,尤其是应用相关药物及肝脏疾病者。胸部畸形者的评估。更换/升级的评估。感染者起搏系统再次植入前的评估等。
四、小结
CIED感染率呈逐年增加。CIED感染的原因包括病人、术者、器械及围手术期的各种因素。降低CIED的感染需采取综合的措施。
参考文献
[1] 中国生物医学工程学会心律分会.心律植入装置感染与处理的中国专家共识[J].临床心电学杂志.2013;22(4):241-253.doi:10.3969/j.issn.1005-0272.2013.04.001.
[2] Sridhar AR, Lavu M, Yarlagadda V, et al. Cardiac Implantable Electronic Device-Related Infection and Extraction Trends in the U.S. [J].PACE. 2017;40(3):286-293. doi: 10.1111/pace.13009. Epub 2017 Feb 15.
[3] Greenspon AJ, Patel JD, Lau E,et al. 16-year trends in the infection burden for pacemakers and implantable cardioverter-defibrillators in the United States 1993 to 2008[J]. JACC. 2011;58(10):1001-6. doi: 10.1016/j.jacc.2011.04.033.
[4] Messenger JC, Ho KK, Young CH, et al. The National Cardiovascular Data Registry (NCDR) Data Quality Brief: the NCDR Data Quality Program in 2012[J]. JACC. 2012 16;60(16):1484-8. doi: 10.1016/j.jacc.2012.07.020. Epub 2012 Sep 19.
[5] Joy PS, Kumar G, Poole JE, et al. Cardiac implantable electronic device infections: Who is at greatest risk[J]? Heart Rhythm. 2017 ;14(6):839-845. doi: 10.1016/j.hrthm.2017.03.019. Epub 2017 Mar 16.
[6] Polyzos KA, Konstantelias AA, Falagas ME. Risk factors for cardiac implantable electronic device infection: a systematic review and meta-analysis[J]. Europace. 2015;17(5):767-77. doi: 10.1093/europace/euv053.
[7] Essebag V, Verma A, Healey JS, et al. Clinically Significant Pocket Hematoma Increases Long-Term Risk of Device Infection: BRUISE CONTROL INFECTION Study[J]. JACC. 2016;67(11):1300-8. doi: 10.1016/j.jacc.2016.01.009.
[8] Uslan DZ, Gleva MJ, Warren DK, et al. Cardiovascular implantable electronic device replacement infections and prevention: results from the REPLACE Registry[J]. PACE. 2012;35(1):81-7. doi: 10.1111/j.1540-8159.2011.03257.x. Epub 2011 Nov 11.
[9] Darouiche R, Mosier M, Voigt J. Antibiotics and antiseptics to prevent infection in cardiac rhythm management device implantation surgery[J]. PACE. 2012;35(11):1348-60. doi: 10.1111/j.1540-8159.2012.03506.x. Epub 2012 Sep 4.
[10] de Oliveira JC, Martinelli M, Nishioka SA, et al. Efficacy of antibiotic prophylaxis before the implantation of pacemakers and cardioverter-defibrillators: results of a large, prospective, randomized, double-blinded, placebo-controlled trial[J]. Circ Arrhythm Electrophysiol. 2009;2(1):29-34. doi: 10.1161/CIRCEP.108.795906. Epub 2009 Feb 10.
[11] Kolek MJ, Patel NJ, Clair WK, et al. Efficacy of a Bio-Absorbable Antibacterial Envelope to Prevent Cardiac Implantable Electronic Device Infections in High-Risk Subjects[J]. J Cardiovasc Electrophysiol. 2015;26(10):1111-6. doi: 10.1111/jce.12768. Epub 2015 Sep 6.