
经桡动脉介入治疗因其穿刺部位并发症少、出血风险低而广受欢迎。这些介入治疗也提高了患者的舒适度并缩短了下床活动时间。桡动静脉瘘(AVF)是经桡动脉途径进行经皮冠脉介入治疗(PCI)的一种极其罕见的并发症。大型注册研究发现,医源性AVF的发生率低至0.08%-0.04%,使其成为与桡动脉入路相关的最罕见并发症之一。由于其罕见性,对于桡动脉入路后医源性AVF的最佳处理方案尚无普遍共识。

大多数报道的病例要么采用保守治疗,要么采用经皮介入或外科手术治疗。《JACC Case Rep》报告一例经桡动脉PCI后并发AVF,并采用经右侧远端桡动脉入路(dTRA)经皮治疗的病例。据我们所知,这是首例通过在并发症同侧使用dTRA植入冠脉覆膜支架(GS)成功闭合AVF的病例。
核心信息
介入医生必须保持警惕,以识别和处理即使是最罕见的并发症,例如桡动静脉瘘。
dTRA因其可能降低桡动脉闭塞率而广受欢迎。
熟悉这项技术为有效处理医源性桡骨并发症提供了独特的机会,且能保证患者的安全、提高效率并提升患者的舒适度。
在某些情况下,dTRA可能是比肱动脉或股动脉入路更安全的替代方案,特别是对于需要持续抗栓治疗的患者。
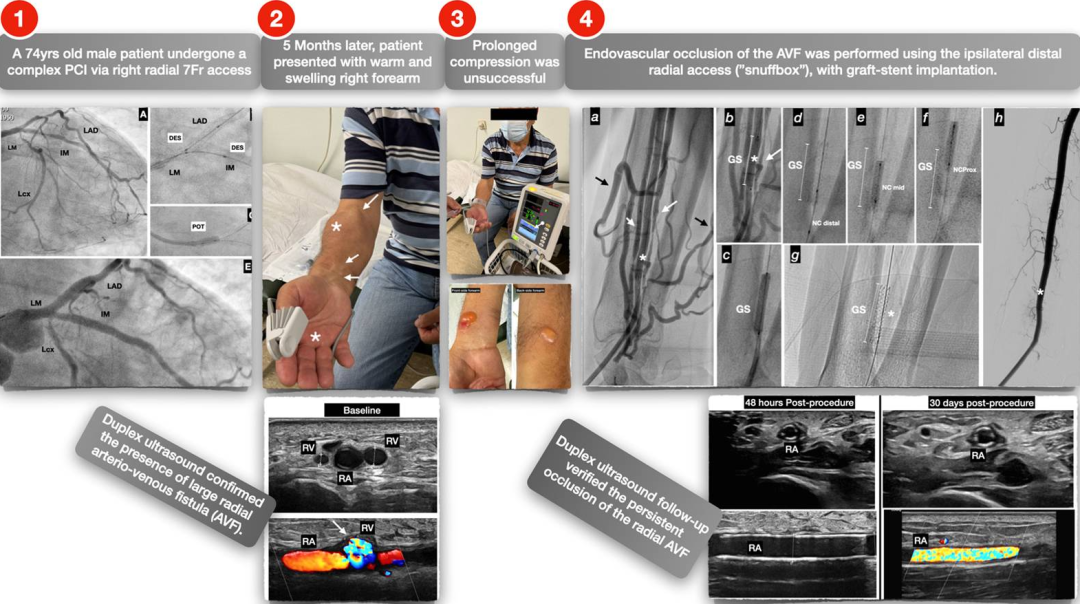
病史与临床表现
一名74岁男性因不典型胸痛就诊,拟行择期经皮冠脉造影,冠脉CTA显示严重三支冠脉病变。通过右侧dTRA进行诊断性冠脉造影,证实了前降支(LAD)近端、中间支(IM)和回旋支(LCx)近端存在严重狭窄,以及右冠脉(RCA)后侧支闭塞(图1)。
与患者讨论后,决定对LAD、IM和LCx进行PCI。二十天后,患者接受了成功的IVUS引导下PCI,在无保护左主干、LAD近端和IM中段植入了支架,并在LCx近端使用药物球囊进行了血管成形术(图2)。
使用右侧桡动脉作为穿刺部位,植入7F桡动脉鞘管,采用7F XB3.5指引导管。术后使用双气囊压迫装置进行桡动脉压迫6小时,并逐渐减压。患者次日出院,接受双联抗血小板治疗,无任何并发症。出院前常规触诊显示桡动脉搏动良好,无震颤或明显的局部并发症迹象。
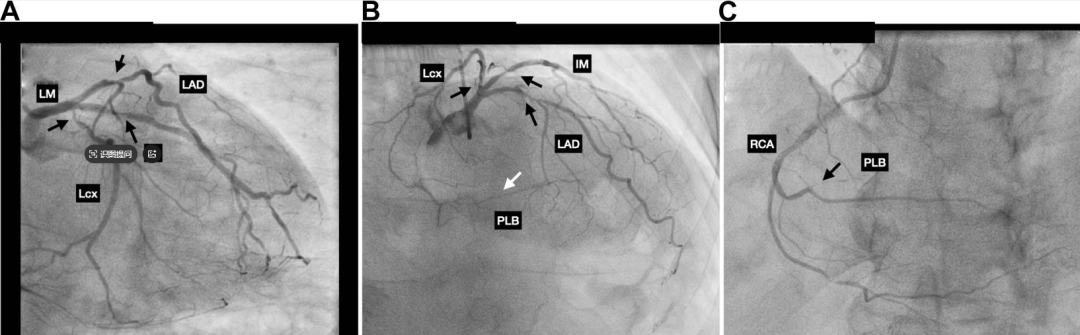
图1.基线冠脉造影显示三支病变
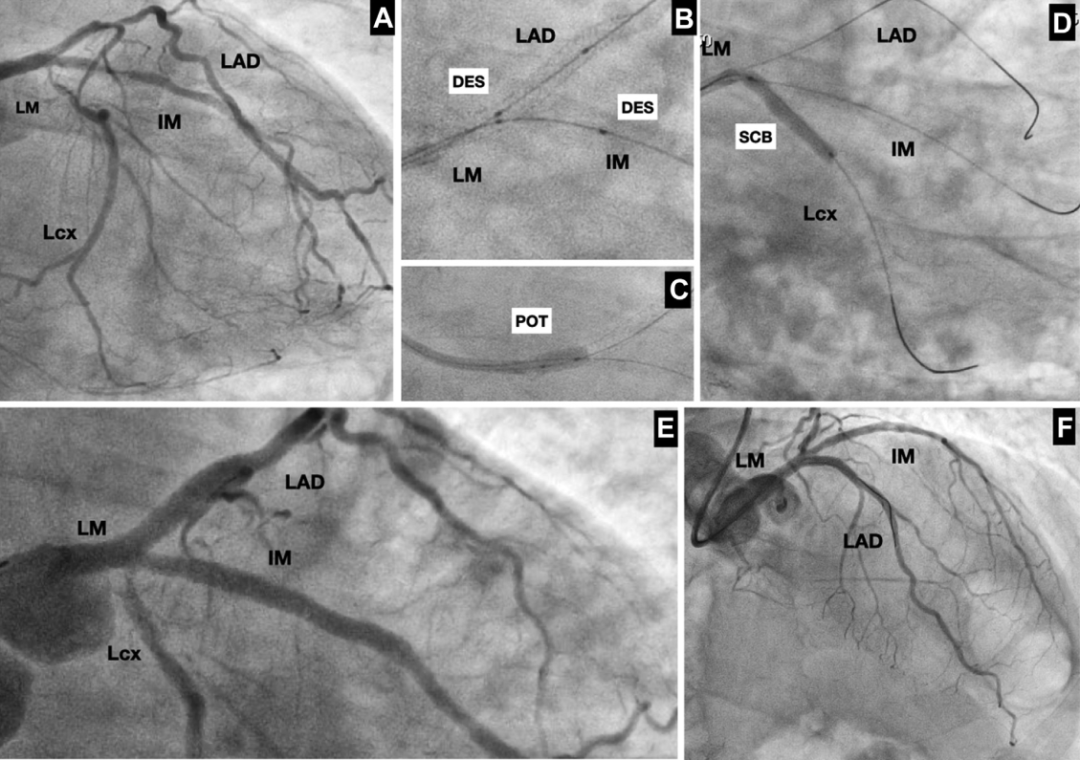
图2.PCI手术过程造影图像
五个月后,患者出现右前臂发热且明显肿胀。除右前臂严重不适外,无其他症状。体格检查发现前臂温热、发红,可触及震颤并可闻及明显的血管杂音。
既往史
患者既往无心脏事件史。曾吸烟,有高血压和高脂血症病史,均通过药物控制良好。
检查
临床怀疑AVF,前臂超声(图3)迅速确认了AVF的诊断。
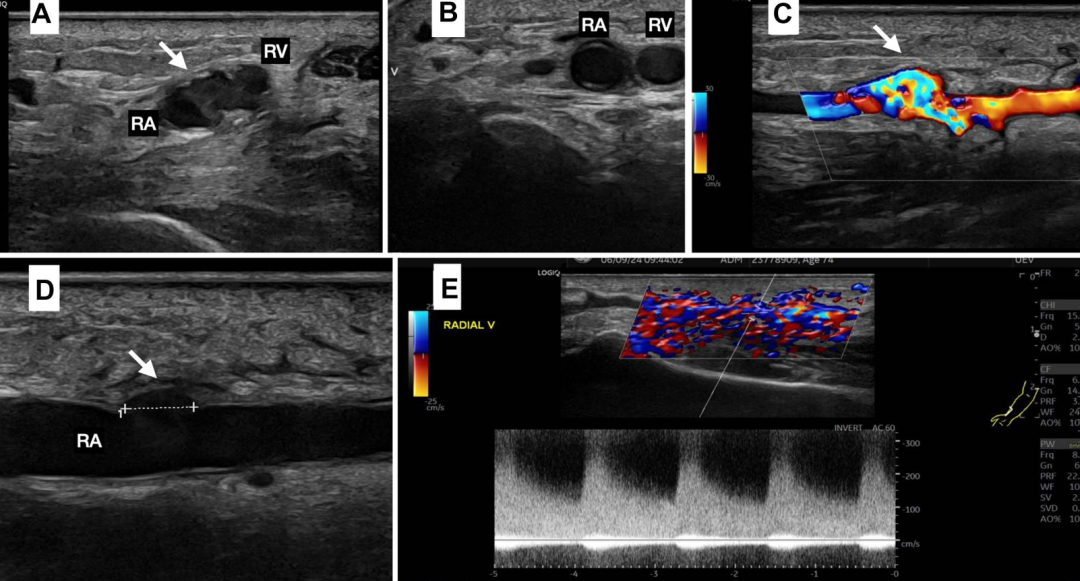
图3.桡动静脉瘘的基线超声图像
(A)桡动脉(RA)与静脉(RV)之间的瘘口(箭头);(B)RA和RV的横断面超声图像;(C)瘘口的湍流;(D)RA侧的瘘口;(E)桡静脉血流“动脉化”及彩色伪影。
治疗
最初尝试使用标准止血器进行长达24小时压迫以闭合AVF。持续压迫12小时后,患者因手臂不适加剧而返回。不幸的是,没有明显迹象表明瘘口成功闭合;前臂仍然温热且可闻及响亮杂音。此外,压迫部位出现了大面积皮肤溃疡伴广泛水疱,使得再次尝试延长压迫不可行(图4)。
患者接受了抗生素和局部皮肤治疗20天,并计划采用有创闭合AVF的治疗方案。在与血管外科医生深入讨论后,决定采用介入治疗,使用dTRA进入AVF瘘口并用覆膜支架将其闭合。
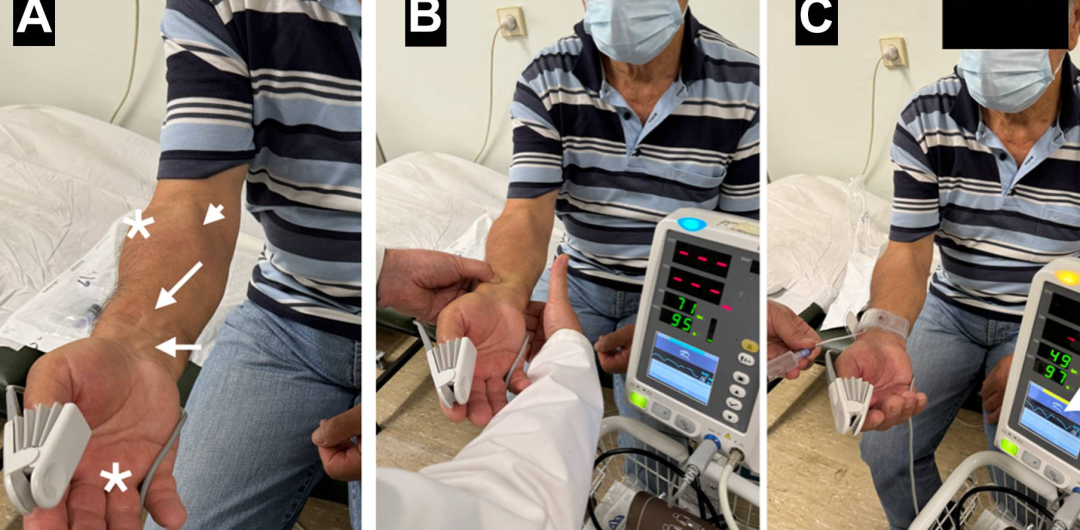
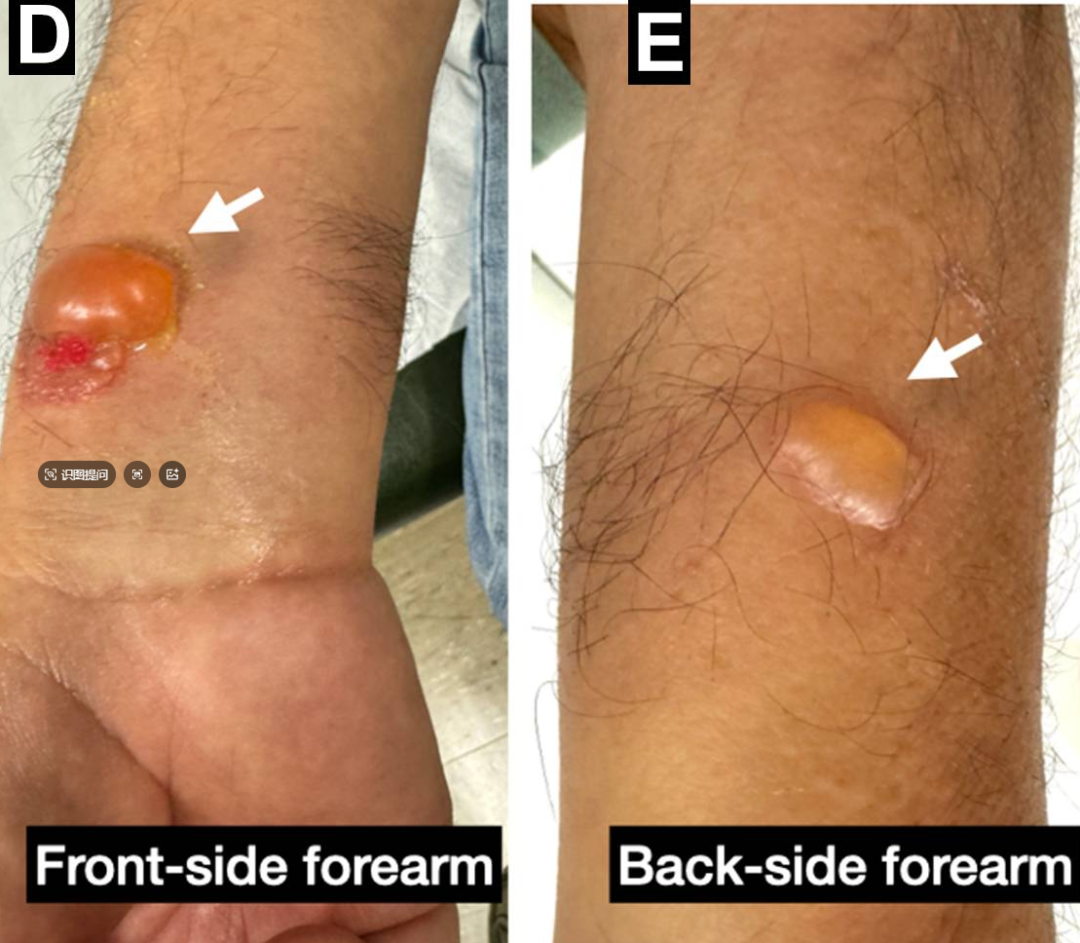
图4.尝试用长时间压迫闭合AVF失败
选择右侧dTRA入路。使用20G针成功穿刺远端桡动脉,插入0.025in导丝,随后植入一根12cm长的6F桡动脉鞘管。撤出0.025in导丝,将一根0.014in冠脉导丝(Choice Floppy)推进至肱动脉近端;静脉内注射5000 IU肝素。
基线血管造影显示桡动脉通畅,同时可见增粗扩张的桡深静脉与浅表的头静脉和贵要静脉相通(图5)。为达到最大血管舒张,动脉内注射硝酸甘油后,获取了多幅血管造影图像,以评估桡动脉的合适尺寸并确定AVF瘘口的确切位置。
根据初始超声测量结果,选择了一枚冠脉覆膜支架(3.5×21mm,ePTFE覆膜),将覆膜支架置于瘘口部位,并以标称压力(11atm)扩张,实现即刻封堵。
使用3.5×15mm非顺应性球囊进行了再次扩张,特别是在支架边缘,以确保完全隔绝。最终血管造影显示桡动脉完全通畅,无静脉循环显影,表明AVF闭合成功(图6)。
dTRA穿刺部位止血采用常规桡动脉气囊压迫止血装置,压迫4小时。
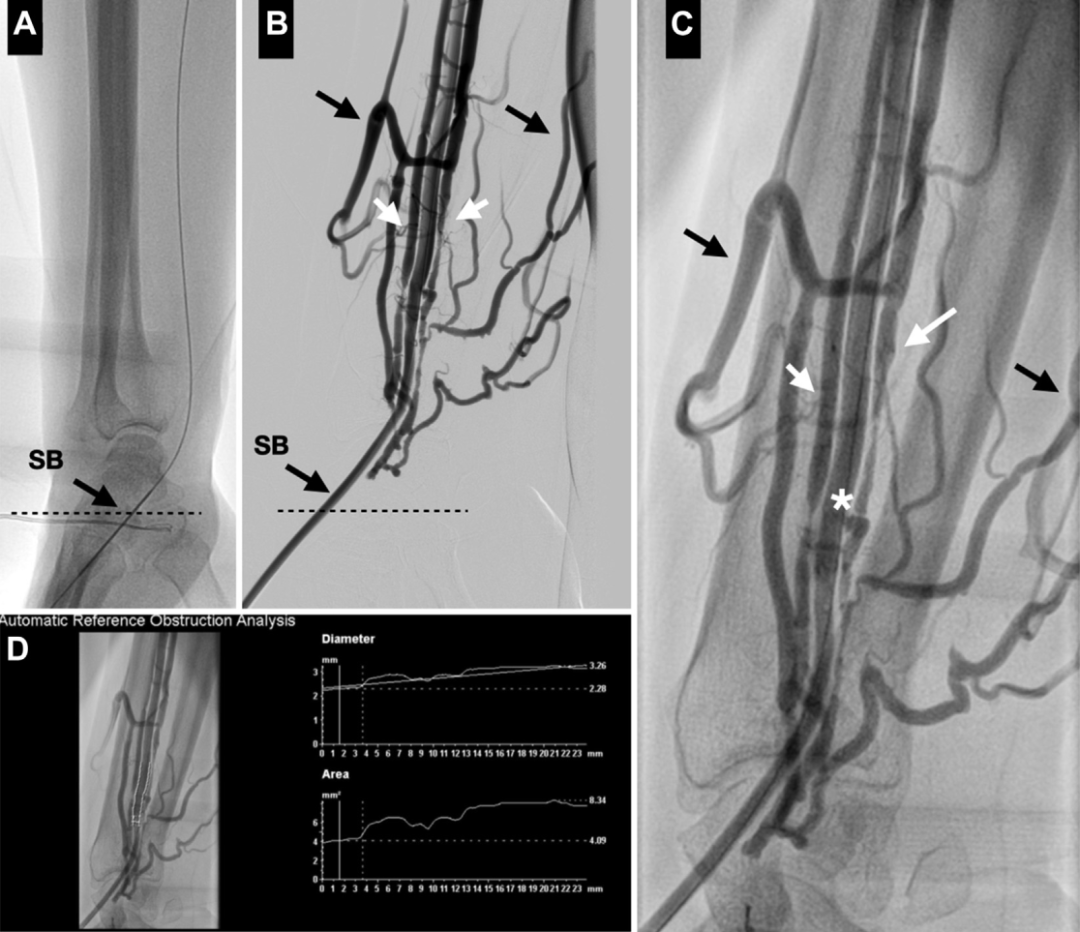
图5.通过右侧远端桡动脉(dTRA)的基线血管造影
(A)通过20G针,插入0.025in导丝,植入6F桡动脉。(B,C)基线造影显示静脉系统明显显影,近端静脉循环扩张,使桡深静脉(白色箭头)与浅静脉系统(头静脉和贵要静脉;黑色箭头)之间形成连通。(D)注射硝酸甘油后,验证桡动脉的确切直径,以便选择合适尺寸和长度的覆膜支架(最小直径2.3mm,最大直径3.2mm)。星号指示AVF瘘口。
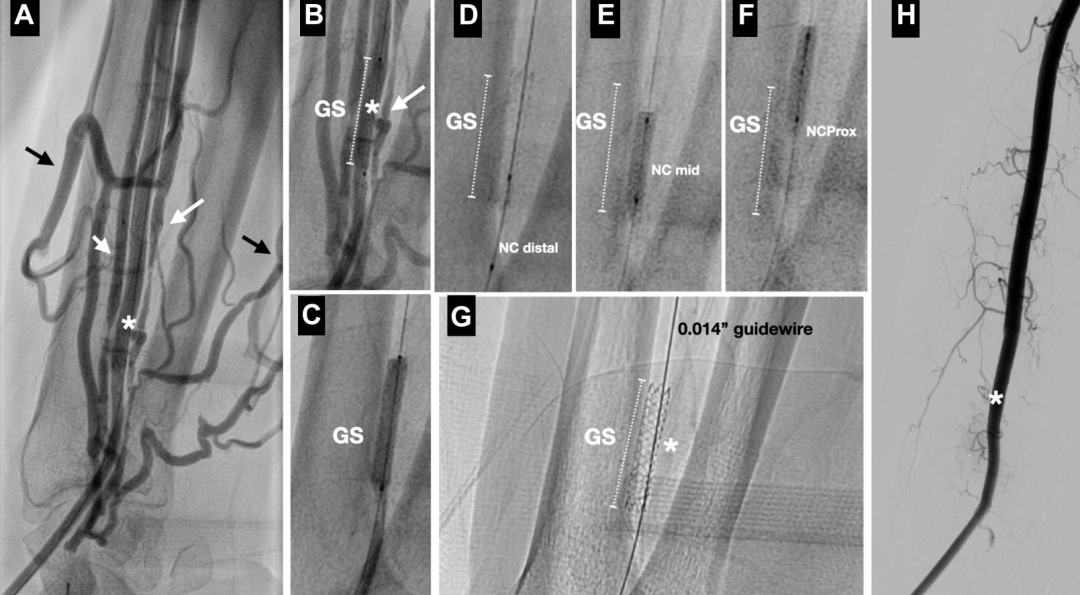
图6.AVF闭合手术步骤详解
(A)基线图像。黑色箭头指示增粗扩张的前臂浅静脉、头静脉和贵要静脉。(B)在瘘口(白色箭头)放置覆膜支架。(C)覆膜支架在12atm压力下扩张。(D至F)使用非顺应性球囊进一步扩张,特别是在覆膜支架边缘以确保覆膜支架完全贴壁。(G)已释放覆膜支架的增强影像图像。(H)最终血管造影图像显示AVF瘘口完全被封堵。
结果与随访
术后第二天,患者报告症状完全缓解。前臂外观正常,无温热迹象,杂音也已消失。
48小时后,再次超声证实AVF已闭合,其中一条伴行的桡静脉出现血栓性闭塞(图7)。
患者出院,手术前、中、后均未中断双联抗血小板治疗。
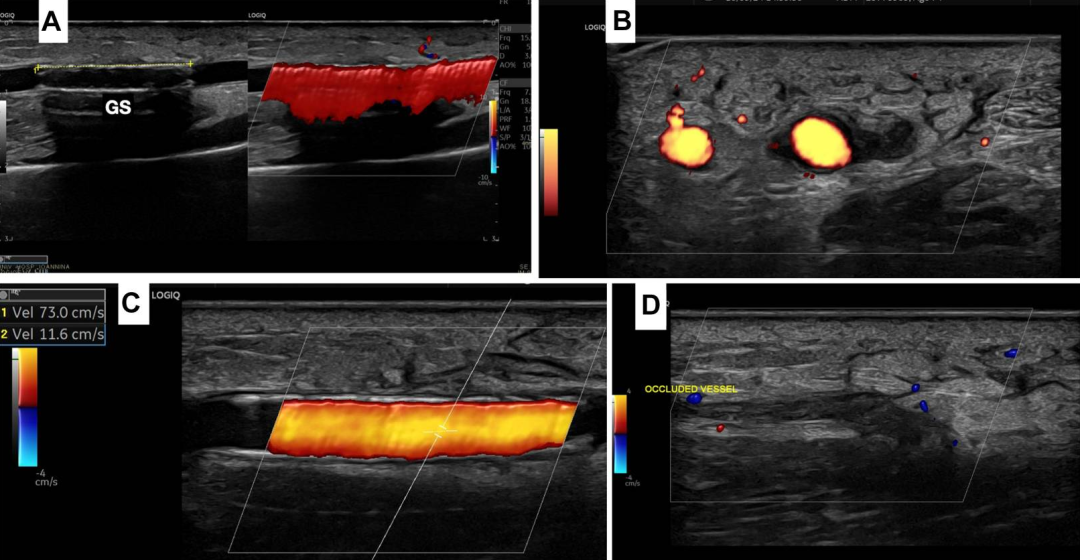
图7.术后48小时超声图像
(A)扩张良好的覆膜支架。(B,C)桡动脉通畅。(D)其中一条桡静脉血栓性闭塞。
术后1个月随访,患者右前臂无温热或肿胀迹象。随访超声证实桡动脉通畅,无再狭窄、血栓形成或AVF复发的迹象。
术后4个月随访,患者临床状况稳定,无症状,无任何AVF复发的迹象。
术后基线、48小时和30天的超声图像见图8。
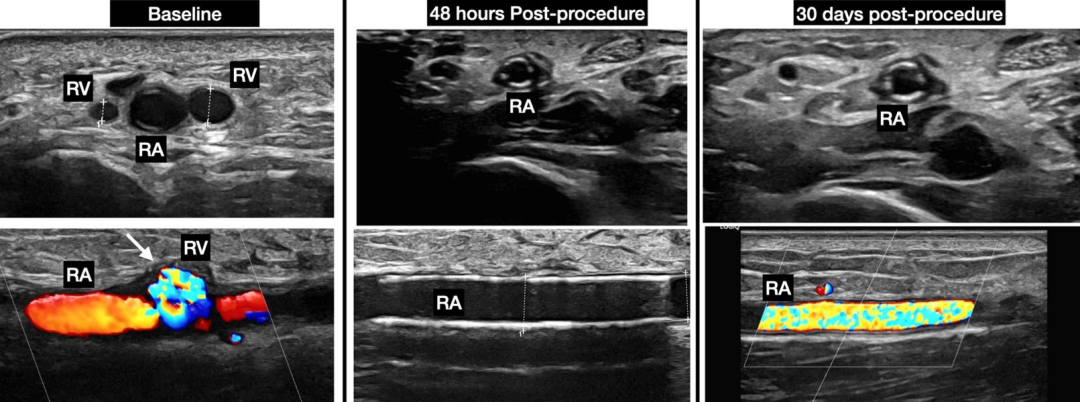
图8.系列超声随访对比图像
讨论
医源性桡AVF是桡动脉PCI手术中极其罕见的并发症。此类AVF可能长期未被诊断,并且在大多数情况下可能无症状。在罕见情况下,可能形成大的瘘口,导致症状,尤其影响前臂。如本病例所示,患者通常主诉前臂肿胀和温热。若无症状且存在血流动力学上不显著的分流,桡AVF可采取保守治疗。然而,当症状持续存在、逐渐加重或增加患者不适时,应考虑闭合AVF。
迄今为止,已有三种基本技术来闭合桡AVF:延长桡动脉压迫、外科修复和使用覆膜支架进行血管内闭合。Hashimoto等人报道了通过使用止血带连续压迫左桡动脉穿刺部位24小时,完全闭塞了一例左桡AVF。然而,本例同样的技术失败了:患者因前臂显著不适和皮肤溃疡在12小时提前返回,且无任何AVF成功闭合的迹象。
有几个因素可能导致此次失败。压迫时间较短(本病例为12小时,而非建议的24小时)以及手术与AVF诊断之间的间隔时间显著较长可能是其中原因。Hashimoto等人报告AVF在术后第20天变得明显,这表明AVF形成时间短,使得延长桡动脉压迫可能成功。然而,本例患者症状出现得晚得多,表明AVF可能已充分成熟,使得延长压迫无效。此外,鞘管尺寸(本例为7F)可能也起了反面作用,而Hashimoto等人的报告为6F。更大的鞘管口径可能造成了更宽的瘘口,导致更大的AVF,对延长压迫的闭合效果较差。
先前的报告大多通过外科手术成功治疗AVF,即结扎AVF部位并在需要时修复桡动脉。在一例病例中,使用NBCA组织胶进行球囊辅助栓塞成功闭合了桡AVF。然而,在初次手术后,另一条引流静脉形成,需要进行第二次手术以实现AVF的完全闭合。值得注意的是,NBCA粘附在球囊上或NBCA远端栓塞的风险,远端栓塞可能导致严重手部缺血甚至可能会手指坏死。因此,我们认为经皮覆膜支架技术对患者更合适。
有几份报告使用覆膜支架闭合AVF。Reguiro等人使用了一种与本例相似的技术来封堵一例保守措施(外部压迫)失败后出现的迟发性医源性桡AVF。与本例不同,他们使用经肱动脉入路接近AVF部位,他们还不得不使用额外的覆膜支架,因为第一个支架对于桡动脉尺寸来说太小,需要第二个更大的覆膜支架才能成功闭合AVF。这强调了在术前超声和术中动脉内注射硝酸甘油后,精确仔细测量桡动脉尺寸的重要性。这些测量对于选择合适的覆膜支架尺寸至关重要。此外,使用经肱动脉穿刺可能伴随相对较高的并发症风险。
在Petrov等人的一项大型研究中,包括847名经肱动脉入路的患者,7.3%的患者出现轻微并发症,2.2%出现需要手术干预的严重并发症,如假性动脉瘤或血栓形成。
由于数据有限,对覆膜支架在桡动脉位置的长期通畅性提出了担忧。在冠脉应用不同类型覆膜支架的数据表明,由于可能的内皮化延迟,存在较高的血栓形成风险,并最终可能导致支架内血栓和支架闭塞。显然,目前没有关于覆膜支架在桡动脉位置长期通畅性的数据。然而,来自犬髂股动脉的实验数据表明,ePTFE覆膜支架在6个月内几乎完全内皮化。因此,在此类病例中,通常建议延长双联抗血小板治疗以减轻晚期覆膜支架血栓形成的风险。
本例通过dTRA独特入路提供了一种替代方案,与外科手术和其他经皮穿刺部位相比,出血并发症发生率更低,特别是对于需要不间断双联抗血小板治疗的患者,如本例中复杂无保护左主干PCI术后患者。除了出血问题外,广泛的局部皮肤感染也促使本例选择血管内介入而非局部外科手术。
本例技术可能存在一个重要限制,覆膜支架在该部位的存在可能会妨碍未来可能的穿刺入路。然而,替代的穿刺部位,如对侧桡动脉入路或同侧dTRA入路,可以克服这个问题。
