
国家结构性心脏病介入技术医疗质量控制中心 中国超声心动图学会瓣膜病与介入组
DOI:10.3760/cma.j.cn131148-20251007-00537
前 言
二尖瓣反流(mitral regurgitation,MR)是临床最常见的心脏瓣膜疾病之一,重度MR与心力衰竭进展及全因死亡率显著增加直接相关,严重威胁患者心血管健康[1]。传统外科二尖瓣修复或置换术虽是标准疗法,但高龄、左心室功能低下或合并多重并发症的高危患者因手术风险过高难以耐受,临床亟需微创治疗手段。经导管二尖瓣缘对缘修复术(mitral valve transcatheter edge-to-edge repair,M-TEER)作为核心介入技术,通过模拟外科Alfieri缝合原理夹合二尖瓣前后叶,为上述高危患者提供了安全有效的微创治疗新选择[2]。M-TEER的成功实施高度依赖于精确、全面的超声评估,尤其是经食管超声心动图(transesophageal echocardiography,TEE)凭借实时动态成像能力,贯穿患者筛选、手术策略制定、器械导航、即刻疗效评价及术后随访全流程,是M-TEER开展的核心支撑。
然而,当前国内各中心在M-TEER超声评估的图像采集、测量方法及结果判读上尚存差异,缺乏统一标准,制约了该技术规范化推广、疗效客观比较以及术者团队的培养。鉴于此,本规范集结国内该领域专家临床经验与共识[3-5],参考国际指南与最新循证医学证据[6-8],系统明确M-TEER术前、术中及术后超声评估的标准化操作流程与关键技术要点,旨在建立科学、实用、可重复的超声影像评估体系,为超声医师及心脏团队提供清晰技术指导,以期提升我国M-TEER诊疗的标准化与同质化水平,保障患者获益,推动技术健康、有序发展。
术语和定义
1.MR
指二尖瓣装置(包括瓣叶、腱索、乳头肌及瓣环)中的一个或多个结构发生异常,导致二尖瓣在心室收缩期不能完全关闭,使左心室的血液逆流回左心房的一种心脏瓣膜病。
2.二尖瓣修复术
二尖瓣修复术是指恢复二尖瓣正常功能且无需置换该瓣膜的任何手术操作。该术式通常用于治疗MR或二尖瓣狭窄。
3.M-TEER
用于治疗MR的微创技术,通过夹合装置抓取二尖瓣前叶和后叶,使两者对合,其原理类似于心脏外科中的Alfieri缝合术。
缩略语
ASD:房间隔缺损(atrial septal defect)
ASE:美国超声心动图学会(American Society of Echocardiography)
CDS:二尖瓣夹导管输送系统(clip delivery system)
CMR:心血管磁共振(cardiovascular magnetic resonance)
COAPT:功能性二尖瓣反流患者MitraClip治疗的心血管结局评估(cardiovascular outcomes assessment of the MitraClip percutaneous therapy)
CW:连续多普勒(continuous wave Doppler)
EROA:有效反流口面积(effective regurgitant orifice area)
EVEREST:血管内瓣膜缘对缘修复研究(Endovascular Valve Edge-to-Edge Repair Study)
EXPAND G4:第四代MitraClip系统的安全性和有效性上市后评价(A Post-Market Study Assessment of the Safety and Performance of the MitraClip G4 System)
FMR:功能性二尖瓣反流(functional mitral regurgitation)
GDMT:指南指导的药物治疗(guideline-directed medical therapy)
IASD:医源性房间隔缺损(iatrogenic atrial septal defect)
LVEDD:左心室舒张末期内径(left ventricular end-diastolic diameter)
LVEDV:左心室舒张末期容积(left ventricular end-diastolic volume)
LVEF:左心室射血分数(left ventricular ejection fraction)
LVESD:左心室收缩末期内径(left ventricular end-systolic diameter)
LVOT:左心室流出道(left ventricular outflow tract)
MAC:二尖瓣环钙化(mitral annular calcification)
MPR:多平面重建(multi-planar reconstruction)
MR:二尖瓣反流(mitral regurgitation)
M-TEER:经导管二尖瓣缘对缘修复术(mitral valve transcatheter edge-to-edge repair)
MVA:二尖瓣口面积(mitral valve area)
MVP:二尖瓣脱垂(mitral valve prolapse)
mPG:平均跨瓣压差(mean pressure gradient)
NYHA:纽约心脏病协会(New York Heart Association)
PASP:肺动脉收缩压(pulmonary artery systolic
pressure)
PISA:近端等速表面积(proximal isovelocity surface area)
PW:脉冲多普勒(pulsed wave Doppler,PW)
RF:反流分数(regurgitant fraction)
RVFAC:右心室面积变化分数(right ventricular fractional area change)
RVOT:右心室流出道(right ventricular outflow tract)
RVol:反流容积(regurgitant volume)
SGC:可操控导引导管(steerable guide catheter)
SLDA:单侧瓣叶夹合器脱位(single leaflet device attachment)
TAPSE:三尖瓣环收缩期位移(tricuspid annular plane systolic excursion)
TTE:经胸超声心动图(transthoracic echocardiography)
TEE:经食管超声心动图(transesophageal echocardiography)
TR:三尖瓣反流(tricuspid regurgitation)
VCW:缩流颈宽度(vena contracta width)
VSD:室间隔缺损(ventricular septal defect)
2D:二维(two-dimensional)
3D:三维(three-dimensional)
超声图像采集设备及患者准备
(一) 仪器准备
高端彩色多普勒超声诊断仪,包括2D/3D TTE和TEE探头。
(二) 检查前准备
检查前准备应包括但不限于以下内容:
1.依次录入患者的姓名、出生年份、日期、性别、身高及体重,进入检查界面进行超声图像存储;
2.连接心电图,常规患者留存3个心动周期,房颤或心律不齐患者为5个心动周期;
3.PW与CW的频谱扫描速度应设置为75~100 mm/s;
4.调节对比度及二维增益设置,使其能清晰显示心内膜及瓣叶结构;
5.调节彩色多普勒标尺速度至50~70 cm/s。
(三) 检查方法
TTE和TEE兼用。
超声图像采集要求
(一) TTE
1.常规TTE标准切面见表1。
2.聚焦于MR的TTE标准切面扫查见表2。

表1 常规TTE标准切面
注:AV为主动脉瓣,MV为二尖瓣,AAO为升主动脉,IAS为房间隔,IVS为室间隔,LA为左心房,LAA为左心耳,LPA为左肺动脉,LV为左心室,LVOT为左心室流出道,PA为肺动脉,RA为右心房,RPA为右肺动脉,RV为右心室,RVOT为右心室流出道,TR为三尖瓣反流,TV为三尖瓣,IVC为下腔静脉

表2 聚焦于二尖瓣反流TTE标准切面(放大模式)
注:EROA为有效反流口面积,IAS为房间隔,LA为左心房,MR为二尖瓣反流,MV为二尖瓣,MVP为二尖瓣脱垂,AV为主动脉瓣,PISA为近端等速表面积,RF为反流分数,RVol为反流容积,VCW为缩流颈宽度,VTI为速度时间积分,CW为连续多普勒
(二) 2D、3D TEE
1.TEE在M-TEER术前评估和术中指导中具有重要价值。TEE可通过多角度、多切面的成像方式,提供二尖瓣及邻近结构的清晰解剖图像,比较准确地诊断二尖瓣结构异常类型、反流机制。2D与3D TEE的联合应用,能够更全面地展示瓣叶病变位置、夹合靶点及治疗效果。
2.常用标准切面扫查
术前与术中TEE检查中,建议至少获取4个标准的食管中段切面以全面评估二尖瓣结构与功能。这些切面包括食管中段四腔心切面、食管中段二尖瓣交界区联合切面、食管中段两腔心切面及食管中段长轴切面。各切面的扫查方式及关键解剖结构识别要点见表3。

表3 TEE评估二尖瓣标准切面
注:A1为二尖瓣前叶A1区,A2为二尖瓣前叶A2区,A3为二尖瓣前叶A3区,AV为主动脉瓣,IAS为房间隔,IVS为室间隔,LA为左心房,LV为左心室,LVOT为左心室流出道,P1为二尖瓣后叶P1区,P2为二尖瓣后叶P2区,P3为二尖瓣后叶P3区,RA为右心房,RV为右心室,AAO为升主动脉
3.食管中段实时双平面系列切面模式评估二尖瓣
以标准食管中段二尖瓣交界区联合切面为基础,通过向左(内侧)或向右(外侧)移动取样线,同时获取对应的左心室长轴切面来分别清晰显示二尖瓣A3-P3、A2-P2及A1-P1区,在一幅图像中完成对四个方向的判断,从而完成对二尖瓣解剖及反流的详细评估(图1~3)。

图1 实时双平面模式评估二尖瓣外侧(1区)病变 A:在食管中段二尖瓣交界区联合切面(主切面)中将取样线置于1区(左图),对应的正交切面左心室长轴切面则显示1区前、后叶结构及运动情况(右图);B:在食管中段二尖瓣交界区联合切面(主切面)结合彩色多普勒超声观察二尖瓣反流束分布范围,将取样线置于1区(左图),对应的正交切面左心室长轴切面则显示1区二尖瓣反流情况(右图)

图2 实时双平面模式评估二尖瓣中央区(2区)病变 A:在食管中段二尖瓣交界区联合切面(主切面)中将取样线置于2区(左图),对应的正交切面左心室长轴切面则显示2区前、后叶结构及运动情况(右图);B:在食管中段二尖瓣交界区联合切面(主切面)结合彩色多普勒超声观察二尖瓣反流束分布范围,将取样线置于2区(左图),对应的正交切面左心室长轴切面则显示2区二尖瓣反流情况(右图)

图3 实时双平面模式评估二尖瓣内侧(3区)病变 A:在食管中段二尖瓣交界区联合切面(主切面)中将取样线置于3区(左图),对应的正交切面左心室长轴切面则显示3区前、后叶结构及运动情况(右图);B:在食管中段二尖瓣交界区联合切面(主切面)结合彩色多普勒超声观察二尖瓣反流束分布范围,将取样线置于3区(左图),对应的正交切面左心室长轴切面则显示3区二尖瓣反流情况(右图)
4. 3D影像评估二尖瓣病变
采用3D聚焦ZOOM模式获取二尖瓣“外科视野”立体显示二尖瓣前后叶,将主动脉瓣置于屏幕顶部12点钟的位置,此时二尖瓣内、外交界应处于平齐状态,左心耳在大约9点钟的位置,结合3D彩色多普勒超声可以更加准确地评估MR的部位、机制及程度,帮助制定手术策略(图4)。

图4 三维外科视野显示二尖瓣后瓣脱垂导致重度二尖瓣反流 A:经食管超声心动图三维外科视野显示二尖瓣后叶P2区脱垂;B:三维外科视野结合彩色多普勒超声模式显示二尖瓣后叶P2区脱垂引起的重度二尖瓣反流
5.可采用3D MPR模式确定二尖瓣瓣口面积,通过移动蓝线、绿线和红线,最终定位二尖瓣口,描记瓣口并获得术前瓣口面积(图5)。
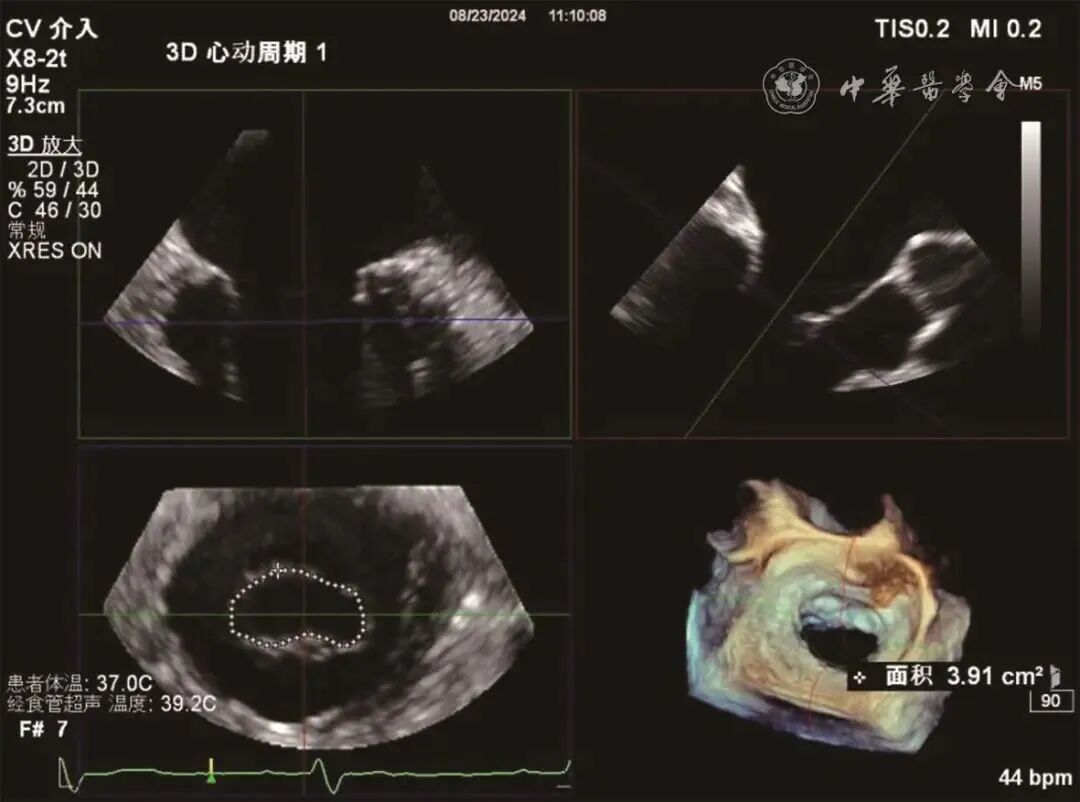
图5 多平面重建评估测量二尖瓣口面积
6. M-TEER相关的二尖瓣数据测量
M-TEER术前的2D与3D TEE检查,应系统获取与二尖瓣解剖、反流机制和治疗路径密切相关的定量与定性参数。核心测量内容包括瓣环尺寸、瓣叶长度与对合情况、脱垂特征、反流束特征(如VCW、PISA半径、反流速度、肺静脉血流谱等指标)。此外,应特别关注与手术路径选择密切相关的结构参数,如左心耳完整性、房间隔长度与穿刺可行性。3D MPR模式对于瓣口面积的准确测量与夹合靶点规划具有重要价值。常用的M-TEER相关超声测量指标、扫查切面及其诊断意义见表4。
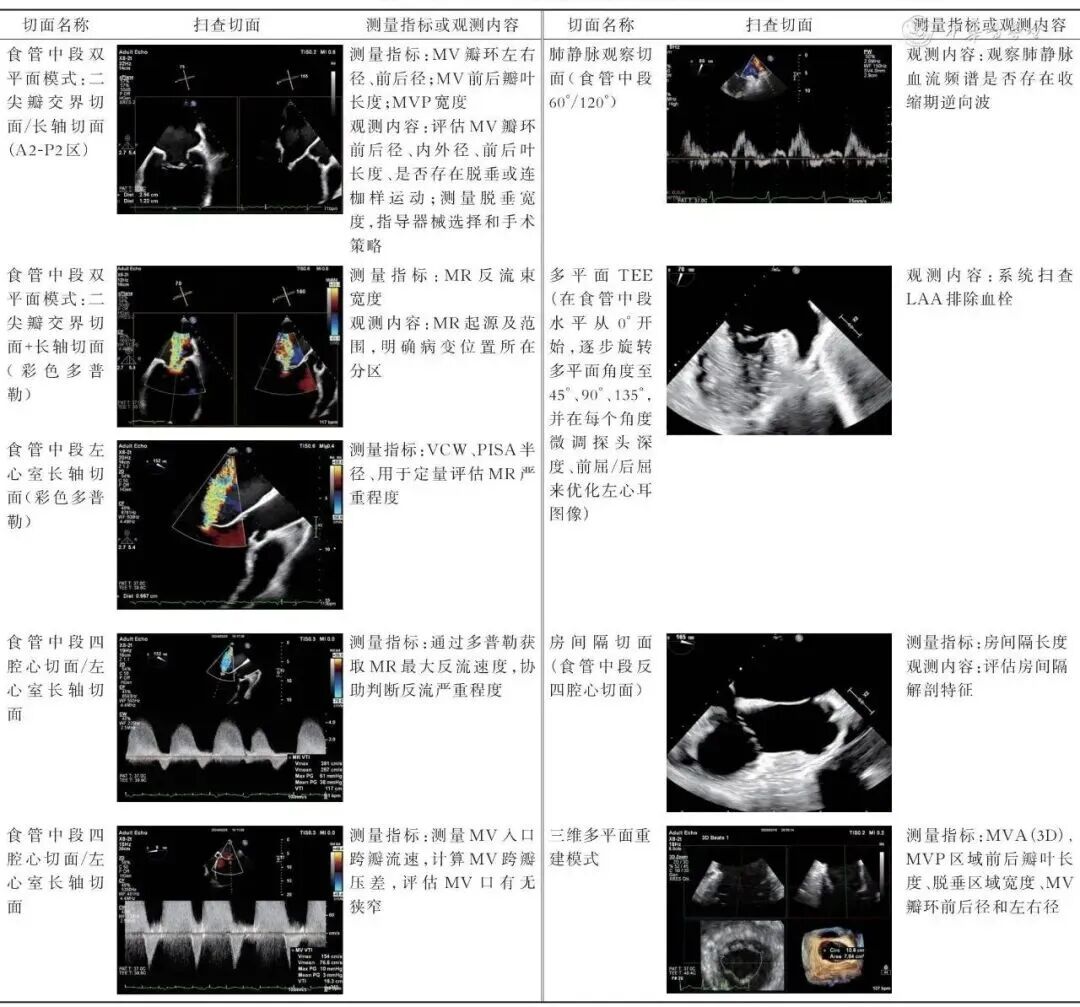
表4 M-TEER相关的二尖瓣数据测量
注:3D为三维,MR为二尖瓣反流,MV为二尖瓣,MVA为二尖瓣口面积,PISA为近端等速表面积,M-TEER为经导管二尖瓣缘对缘修复术,VCW为缩流颈宽度,LAA为左心耳,MVP为二尖瓣脱垂
M-TEER术前评估
(一) 超声心动图对MR程度的判断
1.MR功能分型
MR的干预策略以Carpentier分型为核心依据[9],基于瓣叶活动度分为3型(表5)。
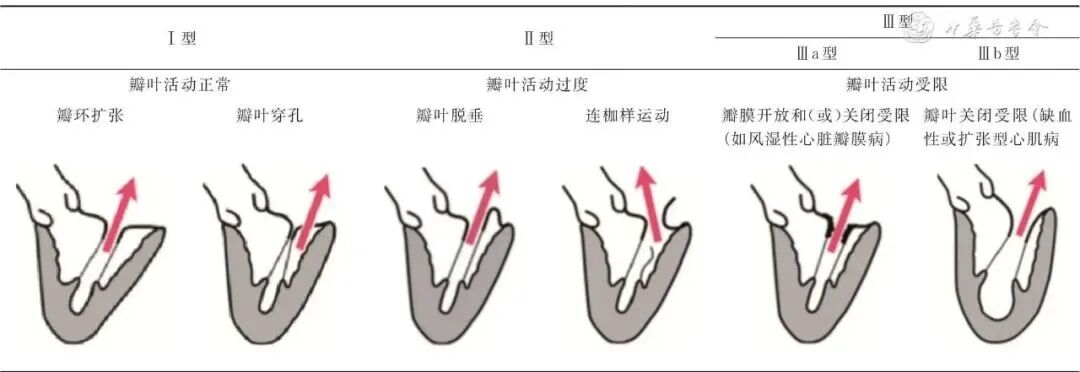
表5 二尖瓣反流功能分型(Carpentier 分型)
(1)Ⅰ型(瓣叶活动正常)病理机制:瓣环扩张(如心房颤动、心肌病导致左心房扩大,致瓣叶对合面积不足)或瓣叶局部缺损(如穿孔);
(2)Ⅱ型(瓣叶活动过度)病理机制:收缩期瓣叶游离缘运动超越瓣环平面,凸向左心房(如腱索断裂引起的“连枷样”运动、乳头肌功能不全或瓣叶脱垂);
(3)Ⅲ型(瓣叶活动受限)病理机制:①Ⅲa型[瓣叶开放和(或)关闭受限]:瓣膜或瓣下装置增厚钙化(如风湿性心脏病、自身免疫性瓣膜炎),导致一个或多个瓣叶的运动在瓣叶开放(舒张期)或关闭时(收缩期)受限,产生不同程度的狭窄或反流;②Ⅲb型(瓣叶关闭受限):左心室扩张(如缺血性或扩张型心肌病),瓣下结构牵拉瓣叶,致瓣叶关闭(收缩期)受限。
2. MR严重程度分级
参考2025年版心脏瓣膜病管理指南[10],对MR严重程度分为4级:轻度(1+),中度(2+),中重度(3+)和重度(4+)MR,分级情况见图6。

图6 二尖瓣反流(MR)定量评估流程 (CMR:心血管磁共振成像;CW:连续多普勒;EROA:有效反流口面积;PISA:近端等速表面积;RF:反流分数;RVol:反流容积;TEE:经食管超声心动图;TTE:经胸超声心动图;VCW:缩流颈宽度)
3.超声心动图定量评估指标
MR严重程度的定量评估应采用多参数综合判断的方法,推荐流程见图6。包括但不限于以下内容:
(1)核心初步指标:VCW在反流束最窄处(即缩流颈)测量其宽度,此参数是进行初步分级的首选指标。
(2)关键定量指标:PISA半径和基于PISA法计算EROA、RVol和RF。
(3)重要辅助指标:CW MR频谱形态,二尖瓣口前向血流频谱,左心房与左心室内径/容积和肺静脉血流频谱,观察收缩期(S)波是否减弱或出现逆向波(提示重度MR)。
(4)成像方式选择:评估主要基于TTE。当TTE成像质量不佳或彩色多普勒显示不清,无法可靠评估MR严重程度时,应使用TEE或CMR进行辅助和精准量化分析。
4. VCW测量方法
(1) 测量规范
VCW测量切面应包括但不限于以下内容:①放大模式TTE胸骨旁左心室长轴切面;②放大模式TEE食管中段左心室长轴切面;③反流最严重的标准切面。
(2) 操作步骤
VCW测量操作步骤应包括但不限于以下内容:①预设参数:适当调节彩色速度标尺至50~70 cm/s,调节增益,局部放大图像;②切面优化:调整探头角度使声束垂直于反流束方向,逐帧回放收缩期图像,选取反流量最大帧;③测量方法:在血流汇聚区最窄处(缩流颈)测量血流束宽度。
(3) 技术局限性
VCW测量具有包括但不限于以下局限性:①多束反流不适用:由于多束反流的路径和形态较为复杂,单纯测量某一束反流的VCW不能全面代表整个反流的严重性,也无法简单地将各束反流的VCW进行相加等操作来综合判断;②偏心性反流有偏差:在评估偏心性反流时由于声束角度偏差导致VCW高估(贴壁射流)或低估(涡流),对反流严重程度的判断出现偏差;③非圆形反流口:椭圆形反流口(常见于继发性MR)单平面测量值会低估真实的EROA。
5. 定量指标评估方法
MR的定量评估通常使用PISA法,在TTE或TEE四腔切面进行,操作流程如下。
(1)预设条件:①局部放大MR区;②调整Nyquist极限(混叠速度Val:30~40 cm/s);③调节增益使血流汇聚区清晰显示。
(2)关键参数获取:①PISA半径:收缩中期测量半球形等速面至反流口的垂直距离;②反流峰值速度(Vreg):CW获取完整频谱(避免声束夹角>20°);③MR时间速度积分(velocity-time integral,VTI):描记反流频谱。
(3)计算公式:①EROA=(2πr2×Vav)/Vreg;②RVol=EROA×VTI,在无主动脉瓣反流时,可用多普勒连续方程法计算:RVol=SVMV-SVLVOT;③RF=(RVol/MIVol)×100%(MIVol为二尖瓣前向血流容积)。
6. M-TEER的选择及二尖瓣解剖适用性评估指标
依据多项关键性临床试验入选标准及国际专家共识[11-13],并结合中国2022版临床路径[9],建立M-TEER解剖适用性评估标准体系(见表6)。

表6 M-TEER解剖适用性评估指标
注:M-TEER为经导管二尖瓣缘对缘修复术,MVA为二尖瓣口面积,FMR为功能性二尖瓣反流,SLDA为单侧瓣叶夹合器脱位,MAC为二尖瓣环钙化,mPG为平均跨瓣压差,TEE为经食管超声心动图。1 mmHg=0.133 kPa
7.功能性MR除符合解剖学外的其他条件
除解剖适配外,应满足包括但不限于以下内容:
(1)药物难治性心力衰竭:经过优化GDMT、血运重建或心室同步化治疗≥3个月仍症状持续[纽约心脏病协会(心功能)分级(NYHA),Ⅱ~Ⅳ]。
(2)左心室功能:LVEF介于20%~50%且LVESD≤70 mm(COAPT标准)。
(3)血流动力学:PASP≤70 mmHg(1 mmHg=0.133 kPa)。
(4)反流程度:重度MR(EROA≥0.4 cm2或RVol≥60 ml)且与左心室扩大不成比例。
注:目前有学者提出根据EROA和LVEDV的比值关系将FMR分为成比例型(EROA/LVEDV<0.14)和非成比例型(EROA/LVEDV≥0.14)。成比例型FMR主要指MR继发于左心室扩大;非成比例型FMR指MR严重程度不能完全用左心室重构扩大解释,且对血流动力学或预后产生显著影响,但目前相关理论以及界定的标准需要进一步研究证实。采用此种理论有利于筛选适合M-TEER的FMR患者,避免对晚期心力衰竭患者过度干预。
M-TEER术中超声图像方案
(一) 术中常用切面及操作设置
常用切面包括但不限于食管中段四腔心切面(0°~10°)、食管中段交界联合部切面(40°~80°)、食管中段两腔心切面(30°~80°)、食管中段长轴切面(130°~140°)、3D二尖瓣外科视野(EnFace)切面、食管中段大动脉短轴切面(30°~60°)、食管中段上下腔静脉切面(80°~120°)、食管中段反四腔心切面(140°~160°)。在图像质量方面的优化调整,术中要求与术前筛查的要求是一致的,但是术中采集图像应当设置为回顾性存图,采集周期常规设置为3个心动周期或3 s,在记录夹持器捕捉瓣叶时,存储时长应当增加为7个心动周期或7 s,以确保能够及时记录术中产生的影像用于评估手术。
(二) 术中的基线数据采集
应在手术当天患者麻醉后再次对心脏进行TEE评估,以避免患者的心脏参数发生变化。在彩色超声诊断仪中输入完整的患者基本信息、留存好基线影像资料,以供术中及术后参考对比。
(三) 确定手术方案
由于患者间存在个体差异,如上、下腔静脉的入右房夹角大小、主动脉窦部是否扩张、腔静脉内是否有血栓等异物、右心房内是否有异常结构等不同情况,超声医生应在手术正式开始前与手术者沟通好手术过程中的图像显示特点、各种可能遇到的挑战及解决方案。
(四) M-TEER手术流程
1.应基于经股静脉入路的M-TEER技术体系,操作流程见表7。经心尖入路M-TEER的超声引导原则与经股静脉入路基本一致,但入路建立阶段(如心尖穿刺定位)的影像导航存在差异;而夹合器捕获、释放等核心操作环节的超声评估技术具有高度通用性,手术流程总结见表8。
2.经股静脉行M-TEER是目前最常见的手术方式,操作流程及超声引导切面见表7和图7~14。

表7 经股静脉M-TEER手术规范流程及超声引导切面
注:CDS为二尖瓣夹导管输送系统,IASD为医源性房间隔缺损,IVC为下腔静脉,LUPV为左上肺静脉,MPR为多平面重建,SGC为可操控导引导管,SVC为上腔静脉,M-TEER为经导管二尖瓣缘对缘修复术。1 mmHg=0.133 kPa

图7 房间隔穿刺TEE引导切面 A:TEE X-plane双平面引导房间隔穿刺,双房上下腔切面确定穿刺点上、下方向的位置(左图),大动脉短轴切面确定穿刺点前、后位置(右图);B:TEE食管中段反四腔心切面测量房间隔穿刺点距离瓣环的垂直距离:中央区病变3.5~4.5 cm,内侧病变及DMR穿刺点较高(4.0~4.5 cm),外侧病变或FMR穿刺点偏低(3.5~4.0 cm);C:3D EnFace切面(主动脉瓣位于12点方向)穿刺点位于3点方向(AO:主动脉;LA:左心房;RA:右心房;LV:左心室;RV:右心室;SVC:上腔静脉;IVC:下腔静脉;TEE:经食管超声心动图;3D EnFace:三维成像外科视野)

图8 经导管二尖瓣缘对缘修复术(M-TEER)手术中交换超硬支持导丝至肺静脉 A:X线下观察房间隔穿刺导管鞘管经超滑导丝引导进入左上肺静脉;B:X线下观察撤回超滑导丝,交换超硬支持导丝;C:3D TEE观察导丝进入左心房方向和位置(LAO:X线左前斜位投照体位)

图9 经导管二尖瓣夹导引导管进入左心房 A:X线监测SGC进入左心房;B:TEE大动脉短轴切面监测SGC进入左心房;C:TEE观察SGC进入左心房方向和位置;D:3D TEE实时成像观察SGC进入左心房方向和位置
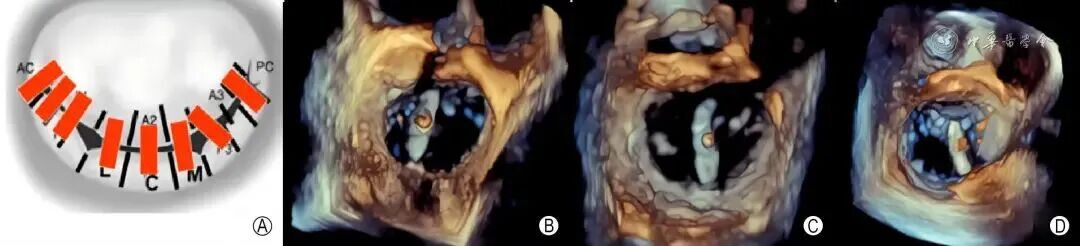
图10 TEE 3D EnFace切面指引夹合器在左心房调整方向 A:夹合器和二尖瓣对合缘垂直;B:1区病变夹合器方向为1~7点;C:2区病变夹合器方向12~6点;D:3区病变夹合器方向为11~5点

图11 应用TEE的MPR模式调整夹合器轴向 A:通过MRP切取二尖瓣交界联合切面(绿线)观察CDS的方向和位置;B:沿夹合器双臂最长方向(红线)切取左心室长轴切面观察夹合器夹合瓣叶过程;C:在夹合器水平切取二尖瓣短轴观察夹合器的轴向;D:用于二尖瓣3D MPR影像

图12 缘对缘钳夹前确认夹合器的方向和位置 A:二尖瓣交界联合切面可观察到夹合器两臂重合垂直于瓣环进入左心室,夹合器位于目标夹合的位置;B:通过X-plane模式垂直于取样线在A图中垂直瓣膜夹切取观察左心室长轴切面上两臂展开夹合瓣叶;C:在3D EnFace切面观察(减少增益)评估夹合器的轴向和位置

图13 通过观察肺静脉血流频谱特征观察二尖瓣反流严重程度变化 A:重度MR患者术前肺静脉血流频谱可见收缩期逆向波;B:M-TEER术后复查肺静脉血流频谱可见收缩期逆向波消失

图14 缘对缘钳夹时第二枚夹合器的方向和位置 TEE X-plane切面观察第二枚夹合器与第一枚夹合器平行紧靠(左图)及两枚夹合器置入后残余二尖瓣反流(右图)
3. 经心尖M-TEER手术规范流程及超声引导切面
经心尖入路M-TEER的超声引导原则与经股静脉入路基本一致,但入路建立阶段(如心尖穿刺定位)的影像导航存在差异;而夹合器捕获、释放等核心操作环节的关键工作切面和超声评估技术与经股静脉M-TEER类似,手术流程和超声引导切面总结见表8,图15~19。

表8 经心尖M-TEER手术规范流程及超声引导切面
注:M-TEER为经导管二尖瓣缘对缘修复术,TEE为经食管超声心动图,TTE为经胸超声心动图,MPR为多平面重建,3D为三维。1 mmHg=0.133 kPa
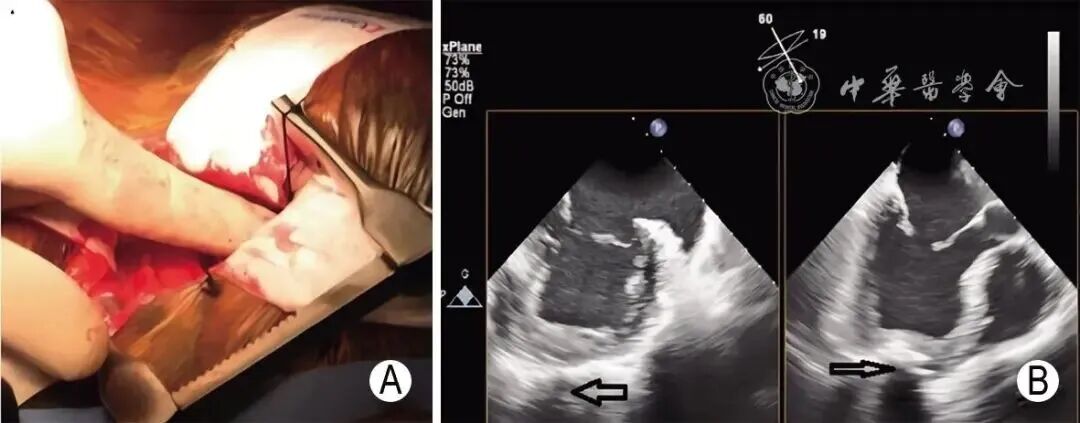
图15 经心尖入路选择最佳穿刺点 A:指尖按压法选择经心尖入路最佳穿刺点;B:经TEE X-plane切面显示指尖压迫点

图16 TEE X-plane双切面观测导丝经心尖送入左心室方向 二尖瓣联合切面(左图)和左心室流出道切面(右图)可见导丝经心尖进入左心室后的强回声影

图17 经心尖二尖瓣缘对缘修复系统导管鞘系统置入过程 在TEE X‑plane模式通过二尖瓣交界区联合切面+左心室长轴切面指导下操作。A:跨瓣器进入左心室;B:跨瓣器跨过瓣环进入左心房;C:跨瓣器导引导管鞘跨瓣环;D:退出跨瓣器,保留导引导管鞘在左心房

图18 夹合器在左心房内调整方向和位置 A:TEE 3D EnFace切面显示夹合器双臂垂直于瓣叶对合线;B:二尖瓣交界联合切面示夹合器的下夹呈现一条“直线”;C:左心室长轴切面显示下夹呈“V”字形

图19 经心尖二尖瓣缘对缘钳夹过程:在TEE任意双平面(X‑plane)模式通过二尖瓣交界区联合切面+左心室长轴切面指导下操作 A:夹合器下夹轻轻托起瓣叶;B:回拉上夹夹住瓣叶;C:前推闭合环收紧夹住;D:夹合器完全夹合瓣叶后评估稳定性
M-TEER术后超声随访要点
(一) M-TEER术后超声随访时间
M-TEER术后患者需要按以下时间节点接受系
统超声心动图随访:
1.常规复查时间点:出院前,术后1个月、3个月、6个月、12个月;
2.中长期随访:术后2年、3年、4年、5年;
3.症状驱动复查:若出现新发呼吸困难、心力衰竭体征等临床变化,应立即行超声评估。
随访方案依据M-TEER患者心脏康复[14]和围术期管理专家共识[15]的推荐框架。
(二) 影像学随访方法
M-TEER术后随访常规应用TTE,当TTE成像受限或可疑器械并发症,MR加重需要精准评估病理机制时,可进一步行TEE,并与术中数据进行对比。
(三) 核心评估内容
1.术后MR程度评估见表9。

表9 M-TEER术后二尖瓣反流分级指标
注:EROA为有效反流口面积,PISA为近端等速表面积,RF为反流分数,RVol为反流容积,M-TEER为经导管二尖瓣缘对缘修复术,VCA为缩流颈面积(3D测量),VCW为缩流颈宽度。*PISA法EROA术后评估受限:因为置入瓣膜夹合器后近端血流汇聚形态改变,假设为半球形准确性下降;在有多个反流束或非常偏心的反流束时,PSIA通常会低估二尖瓣反流严重程度
2. 术后MR机制分析
(1)反流来源定位:识别反流束源自夹合器侧方、中央或瓣叶间隙。
(2)病理机制判断:区分瓣叶捕获不全、夹合器移位、新发瓣叶脱垂/连枷。
(3)器械稳定性评估:夹合器稳定性是M-TEER
术后评估的重要内容,其评估要点见表10。

表10 M-TEER术后随访器械稳定性评估要点
3. 术后并发症筛查
M-TEER术后主要并发症及评估要点见表11。

表11 M-TEER术后并发症及超声特征
注:平均跨瓣压差测量应排除心动过速/高心排状态,临床症状为肺水肿/新发心房颤动等。1 mmHg=0.133 kPa
4. 术后心脏结构与功能评估
M-TEER术后心脏重塑的逆转以及心功能的改善是决定患者近期和远期预后的关键,其评估要点见表12。

表12 M-TEER心脏结构及功能变化评估
注:LA为左心房,LAVI为左房容积指数,LEVDD为左心室舒张末期内径,LVESD为左心室收缩末期内径,LVEDV为左心室舒张末期容积,LVEF为左心室射血分数,TAPSE为三尖瓣环收缩期位移,RVFAC为右心室面积变化分数,PASP为肺动脉收缩压,TRVmax为三尖瓣反流峰值流速
5. 术后随访重点
M-TEER术后短、中期和长期随访超声心动图评估要点见表13。

表 13 M-TEER术后随访策略重点
综上,本规范作为既往相关共识的更新与补充,系统涵盖二尖瓣解剖结构、MR病因及功能分型、MR定量评估以及M-TEER超声适应证,并重点规范经股静脉与经心尖M-TEER术中超声操作及术后随访内容,弥补了2022年共识术中导航监测阐述不足的问题。相较于以往类似指南,本规范更聚焦M-TEER全流程超声指导,强调多切面联合与精准量化评估,为临床提供更具体的实操依据。未来需进一步开展研究,进一步优化MR评估指标,同时积累国产M-TEER器械临床数据,持续完善超声评估体系,推动我国M-TEER技术更安全、规范地发展。
利益冲突声明
所有作者声明不存在利益冲突
编写组成员
组长:段福建(中国医学科学院阜外医院)
专家顾问:王浩(中国医学科学院阜外医院);潘湘斌(中国医学科 学院阜外医院)
主要执笔人:段福建(中国医学科学院阜外医院);孟欣[空军军医大 学第一附属医院(西京医院)];王艺(武汉大学中南医院);李 伟(复旦大学附属中山医院);邓冰清(中山大学孙逸仙纪念医 院);卢志南(中国医学科学院阜外医院)
编写专家(按姓氏汉语拼音排序):
曹媛(山东大学齐鲁医院);陈少敏(北京大学第三医院);丛娟 (阜外华中心血管病医院);邓冰清(中山大学孙逸仙纪念医院); 邓荷萍(河北医科大学第三医院);邓燕(广西医科大学第一附 属医院);杜鑫(天津医科大学总医院);段福建(中国医学科学 院阜外医院);范怡婷(上海市第一人民医院);房芳(中国医学 科学院阜外医院);方凌云(华中科技大学同济医学院附属协和 医院);方跃华(上海交通大学医学院附属瑞金医院);冯杰莉 (北京大学第三医院);富华颖(天津医科大学第二医院);付明 (广东省人民医院);苟中山(苏州市立医院);关欣(天津市胸 科医院);何锦霞(新疆维吾尔自治区人民医院);何亚峰(武汉 亚洲心脏病医院);黄季江(新疆维吾尔自治区人民医院);江勇 (中国医学科学院阜外医院深圳医院);康文英(中国医学科学院 阜外医院);科雨彤(首都医科大学附属北京安贞医院);赖宝春 (福州大学附属省立医院);郎志斌(阜外华中心血管病医院); 李贺(华中科技大学同济医学院附属协和医院);李慧(中国医 学科学院阜外医院);李楠(中国医科大学附属第一医院);李瑞 (华中科技大学同济医学院附属同济医院);李天亮(山西省心血 管病医院);李伟(复旦大学附属中山医院);梁玉佳(四川大学 华西医院);刘艳(山东大学齐鲁医院);刘永太(中国医学科学 院北京协和医院);卢志南(中国医学科学院阜外医院);骆志玲 (云南省阜外心血管病医院);孟红(中国医学科学院阜外医院);孟庆龙(中国医学科学院阜外医院);孟欣[空军军医大学第一附 属医院(西京医院)];潘湘斌(中国医学科学院阜外医院);蒲 朝霞(浙江大学医学院附属第二医院);苏茂龙(厦门大学附属 心血管病医院);孙旭东(福建医科大学附属协和医院);唐海霞 [海南省人民医院(海南医科大学附属海南医院)];王蓓(浙江 大学医学院附属邵逸夫医院);王斌(武汉大学中南医院);汪芳 (北京医院);王贺男(北京中医药大学第三附属医院);王建德 (中国医学科学院阜外医院);王晶(解放军总医院第六医学中 心);王霜(武汉大学中南医院);王顺(西安交通大学第一附属 医院);王吴刚(河北医科大学第一医院);王湘竹(北京中医药 大学第三附属医院);王胰(四川省人民医院);王艺(武汉大学 中南医院);魏薪(四川大学华西医院);向帆(中南大学湘雅二 医院);修丽丽(哈尔滨医科大学附属第二医院);杨冬妹(中国 科学技术大学附属第一医院);姚凤娟(中山大学附属第一医 院);叶晓光(首都医科大学附属北京朝阳医院);叶振盛(福州 大学附属省立医院);张涵(首都医科大学附属北京安贞医院); 张娟(南京市第一医院);张茗卉(首都医科大学附属北京友谊 医院);钟优(北京医院);周炳元(苏州大学附属第一医院)
参考文献
略

Ultrasound assessment technical guidelines for transcatheter edge-to-edge mitral valve repair (2025 edition)
National Structural Heart Disease Interventional Technology Medical Quality Control Center; Chinese Society of Echocardiography, Valvular Heart Disease and Interventional Group

引用本文: 国家结构性心脏病介入技术医疗质量控制中心,中国超声心动图学会瓣膜病与介入组.经导管二尖瓣缘对缘修复术超声评估技术规范(2025版)[J].中华超声影像学杂志,2025,34(11):932-949.
National Structural Heart Disease Interventional Technology Medical Quality Control Center;Chinese Society of Echocardiography, Valvular Heart Disease and Interventional Group.Ultrasound assessment technical guidelines for transcatheter edge-to-edge mitral valve repair (2025 edition)[J].Chin J Ultrasonogr,2025,34(11):932-949.
通信作者:段福建,中国医学科学院阜外医院超声科,北京 100037,Email: duanfujian@aliyun. com;王斌,武汉大学中南医院心血管超声医学科,武汉 430071, Email:wangbin87098429@126. com;苏茂龙,厦门大学附属心血管病医院超声科,厦门 361000,Email:sumaolong@xmu. edu. cn
基金信息: 中国医学科学院临床与转化医学研究专项(2023-I2M-C&T-B-056);中国医学科学院医学与健康科技创新工程(2024-I2M-ZH-003);中央高水平医院临床科研业务费(2022-GSP-GG-18);湖北省重点研发项目(2025BCB019);武汉大学中南医院科技成果转化基金临床研发基金(LCYFMS2023008)
收稿日期:2025-10-07
出版日期:2025-11-25