

点击图片进入TCT 2025学术专栏
当地时间2025年10月25日,第37届经导管心血管治疗年会(TCT 2025)于美国旧金山莫斯康中心(Moscone Center)隆重召开。在刚刚结束的TCT WorldLink Forum环节传来中国创新之声,高超教授代表中国人民解放军空军军医大学西京医院陶凌教授及REC-CHIPMCS多中心研究团队在大会上首次报告了该随机对照试验结果。

研究背景
常见的MCS包括介入式心室辅助装置(pVAD,如Impella,CorVad®),IABP和动静脉体外膜肺氧合装置(VA-ECMO)。pVAD主要是基于微轴流泵(mAFP)将左心室血液通过入血口泵送至升主动脉处。相比于IABP的循环支持能力不足与ECMO的高侵入性,研究团队及部分国际专家均推测mAFP可能是较优选择;然而。目前尚无相关大型临床试验验证pVAD和VA-ECMO相比,对HR-PCI患者的支持效果。

研究方法
REC-CHIPMCS试验采用前瞻性、多中心、非劣效、随机对照设计(NCT06373120),旨在评价CorVad®介入式心室辅助系统(CorVad®)与VA-ECMO相比在HR-PCI术中为患者提供循环支持的安全性及有效性。主要评价指标为30天和90天主要不良事件(MAE)发生率(MAE包括:死亡、卒中、心肌梗死、心肺复苏、严重器械相关不良事件、大出血、急性肾损伤、血运重建和心血管原因再入院),此外,本试验也通过Win Ratio分析(胜率分析),进一步评估试验器械在主要终点方面的优效性。

本试验主要纳入人群为:左室射血分数(LVEF)≤35%或LVEF≤40%且NYHA心功能分级为III级和IV级的复杂PCI患者。主要排除标准为:(1)7天内的急性心肌梗死或接受溶栓治疗;(2)心原性休克;(3)24小时内进行过心肺复苏;(4)pVAD和ECMO无法置入或存在应用禁忌症;(5)1个月内出现过活动性内脏出血;(6)需行透析治疗;(7)严重肺动脉高压;和(8)严重右心功能衰竭或严重三尖瓣反流。

研究结果
基线资料
本试验在全国23家中心进行,共计纳入262例患者。其中mAFP组134例,VA-ECMO组128例。通过严格的随机化,本试验mAFP组及VA-ECMO组受试者基线期各指标均无显著性差异,组间具有良好的可比性。糖尿病(mAFP组:51.2%,VA-ECMO组:54.9%)和慢性肾脏疾病(mAFP组:31.2%,VA-ECMO组:30.8%)作为患者自身合并症的重要危险因素,在两组比例均较高。mAFP组基线期LVEF值为(32.4±6.1)%,VA-ECMO组基线期LVEF值为(31.3±5.5)%。术前SYNTAX评分mAFP组为36.3±10.7,VA-ECMO组为35.7±10.9,术后SYNTAX评分mAFP组为12.4±11.2,VA-ECMO组为13.0±9.9。在STS评分方面,mAFP组为5.8±6.0,VA-ECMO组为5.7±5.6。

造影资料
以mAFP组为例,本试验纳入的患者88.7%为三支血管病变,30.1%为左主干合并三支血管病变,43.6%为至少两支慢性完全闭塞病变(CTO),两组在入组人群中,进行血管内影像的比例均较高(mAFP组 vs. VA-ECMO组:76.3% vs. 77.5%)。

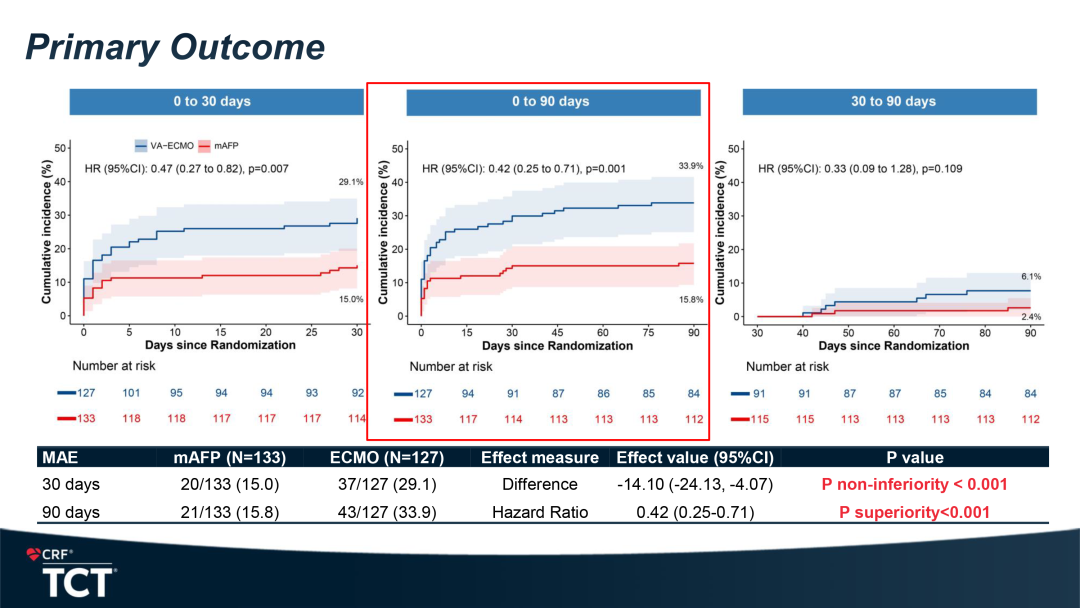
主要终点
30天时,mAFP组MAE发生率为15.04%(20/133),VA-ECMO组29.13%(37/127),率差(试验组-对照组)为-14.10%,95% CI为(-24.13%, -4.07%),差异具有统计学意义(P非劣 <0.001)。90天时,和VA-ECM0组相比,mAFP组能够降低MAE事件的发生(15.8% vs. 33.9%; HR: 0.42; 95%CI: 0.25-0.71; P优效<0.001)。
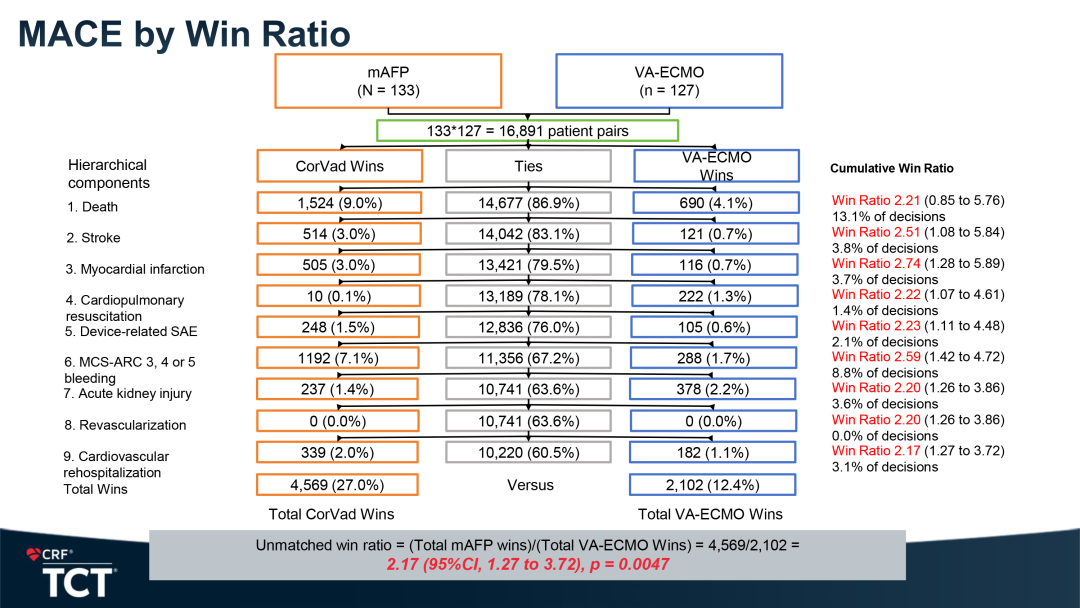
胜率分析
通过对MAE事件分层进行胜率分析,mAFP组的总体胜率(27.0%)高于VA-ECMO组的总体胜率(12.4%),赢率为2.71(95%CI: 1.27-3.72;P =0.047)。
次要终点
对全因死亡,心肌梗死和卒中的复合硬终点进行分析,结果发现,30天时,mAFP组发生率为6.0%,VA-ECMO组为15.7,两组在复合硬终点率差为-9.73%(95%CI: -17.79,-2.28, P=0.011),终点事件差异在90天时仍存在(6.8% vs. 16.5%; HR: 0.39; 95%CI: 0.18-0.85; P=0.018)。

研究结论
本研究首次通过随机对照试验,证实CorVad®在缺血性心肌病患者中进行复杂高危PCI操作时,在30天和90天的MAE事件方面,展现出非劣于VA-ECMO的支持效果。
CorVad®作为中国首个全自主研发的微轴流泵(mAFP)心室辅助系统,与国外同类产品相比,拥有在同一尺寸导管下提供更大流量支持,具备更优的血液相容性和更长的支持时间的特点。其更小的介入尺寸便于微创操作,减少血管损伤,在为血运重建提供流量支持的同时,可改善体循环血流与心肌灌注,并减轻心室负荷,从而提高手术安全性与患者耐受性。
专家点评
蒋峻教授,浙江大学医学院附属第二医院
2021年ACC/AHA/SCAI冠状动脉血运重建指南推荐对于特定的高危经皮冠状动脉介入治疗(HR-PCI)人群,通过机械循环辅助(MCS)支持PCI手术是合理的(推荐等级:IIB)。
几种MCS技术的相关研究中,IABP因在某些情况下可能无法提供充足流程支持,BCIS-1研究并未证明IABP在预防性支持HR-PCI中的临床获益;VA-ECMO在一项兰州大学第一附属医院的单中心随机对照试验中显示能够降低HR-PCI患者的手术相关并发症(Pan, C. et al. JACC: Advances ,2025)。然而VA-ECMO创伤较大。因此,pVAD可能是高危PCI人群更加合适的选择。
pVAD的临床价值虽已获多项研究支持,但既往证据体系仍存在重要空白。例如,Impella的PROTECT系列研究未能证明其相较于传统IABP具备显著优势,亦尚无相关严格设计的临床试验对比微轴流泵(mAFP)和VA-ECMO支持HR-PCI的临床疗效。在此背景下,这项研究具有重要突破意义——试验将全因死亡率,心肌梗死(MI)、卒中及因心血管事件再住院等关键临床结局作为复合终点(MAE事件),CorVad®组在30天MAE事件发生率非劣于甚至优于VA-ECMO组的结果,相对风险降低48.45%,且其影响效果在90天时仍存在。其结果首次证实了中国首个原研微轴流泵心室辅助系统在缺血性心肌病患者中展现出明确的临床优效性,也为pVAD的全球发展提供了新的高级别临床证据。
研究者总结
陶凌教授,中国人民解放军空军军医大学西京医院
该研究入组的两组人群的平均SYNTAX评分均超过了35,冠脉病变的复杂性都很高,研究所涉及的CorVad®装置在实现更小介入尺寸的同时,保持了出色的血液相容性和更大的流量支持,这一技术特点为其临床优势提供了有力支撑。
当前研究的样本量仍存在一定局限,未来有必要通过更大规模、多中心的随机对照试验进一步验证该结论的稳健性与普适性。

CorVad®是由深圳核心医疗开发的介入式心室辅助装置。产品采用内置电机技术的创新设计,保障了系统稳定高效运行,同时实现低功耗、低温升,进一步降低血液破坏风险。该产品已于2023年7月纳入创新医疗器械特别审查程序,目前已在多家顶尖医学中心应用超300例。本次公布的试验结果再次证明了CorVad®产品的安全性及有效性,这些扎实的循证证据,正推动中国创新在国际心血管学术领域确立其不可或缺的声音。