
心肌梗死或心肌缺血伴非阻塞性冠状动脉疾病(MINOCA/INOCA)一直是诊断难题。这类患者往往表现为典型的心绞痛症状,甚至危及生命的心律失常,但冠状动脉造影却显示血管“正常”。传统的经验性治疗可能延误真正病因的发现,导致患者长期受困于症状反复。近日,《JACC: Case Reports》发表的一则案例,通过全面的冠状动脉生理学和成像技术,揭示了一例以心室颤动为首发表现的MINOCA的罕见病因——心肌桥合并微血管功能障碍。

非阻塞性冠状动脉疾病的评估一直是临床实践的挑战。当患者出现反复胸痛或急性冠脉综合征(ACS)表现,但冠状动脉造影未见显著狭窄时,诊断往往陷入僵局。功能性异常,如血管痉挛、微血管功能障碍或心肌桥,可能是缺血的关键驱动因素。然而,这些病变在常规影像学中难以捕捉,尤其当多种机制共存时,经验性治疗常如盲人摸象,效果有限甚至适得其反。
心室颤动是心源性猝死的主要原因,多数由阻塞性冠状动脉疾病引发的ACS触发。但有一小部分患者,在血管造影正常的情况下仍发生致命性心律失常,这提示功能性或解剖性异常可能扮演关键角色。2023年和2024年欧洲心脏病学会(ESC)关于ACS和慢性冠脉综合征管理的指南强调,对MINOCA/INOCA患者需进行系统性有创评估,以明确病理生理机制。本文所述的案例正是这一理念的生动体现:通过光学相干断层扫描(OCT)和冠脉生理学检查,揭开了长达十年的误诊迷雾。
从十年误诊到生命危急
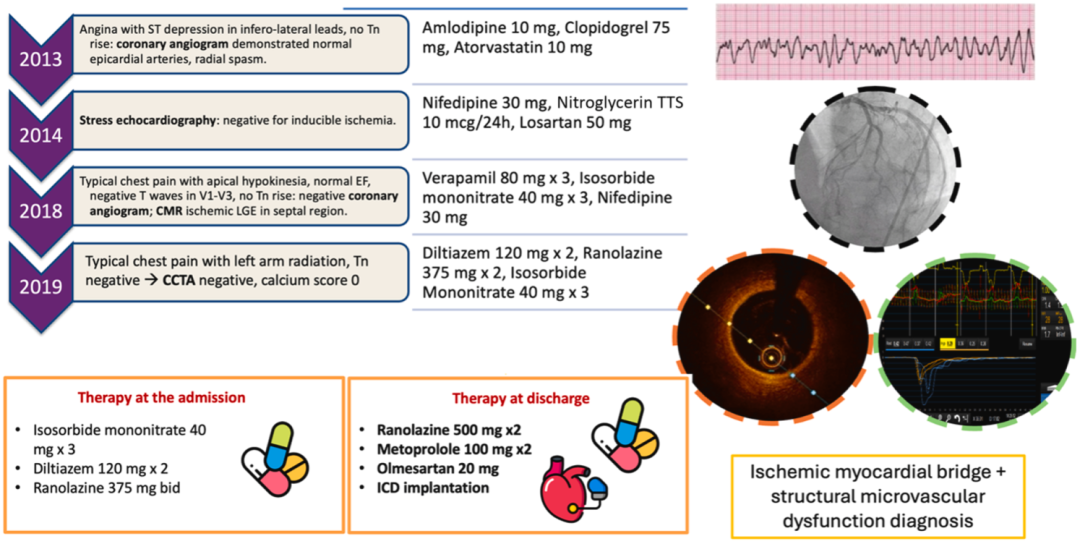
患者男性,57岁,有高血压、血脂异常和吸烟史等心血管风险因素。自2013年起,他反复发作胸痛,最初被归因于冠状动脉痉挛(基于症状和一次造影中观察到的桡动脉痉挛)。十年间,他接受了经验性治疗,包括钙通道阻滞剂和硝酸酯类药物,症状控制时好时坏。无创检查如负荷超声心动图和心脏磁共振成像,曾提示室间隔缺血性晚期钆增强和心尖部运动减弱,但始终未明确病因。
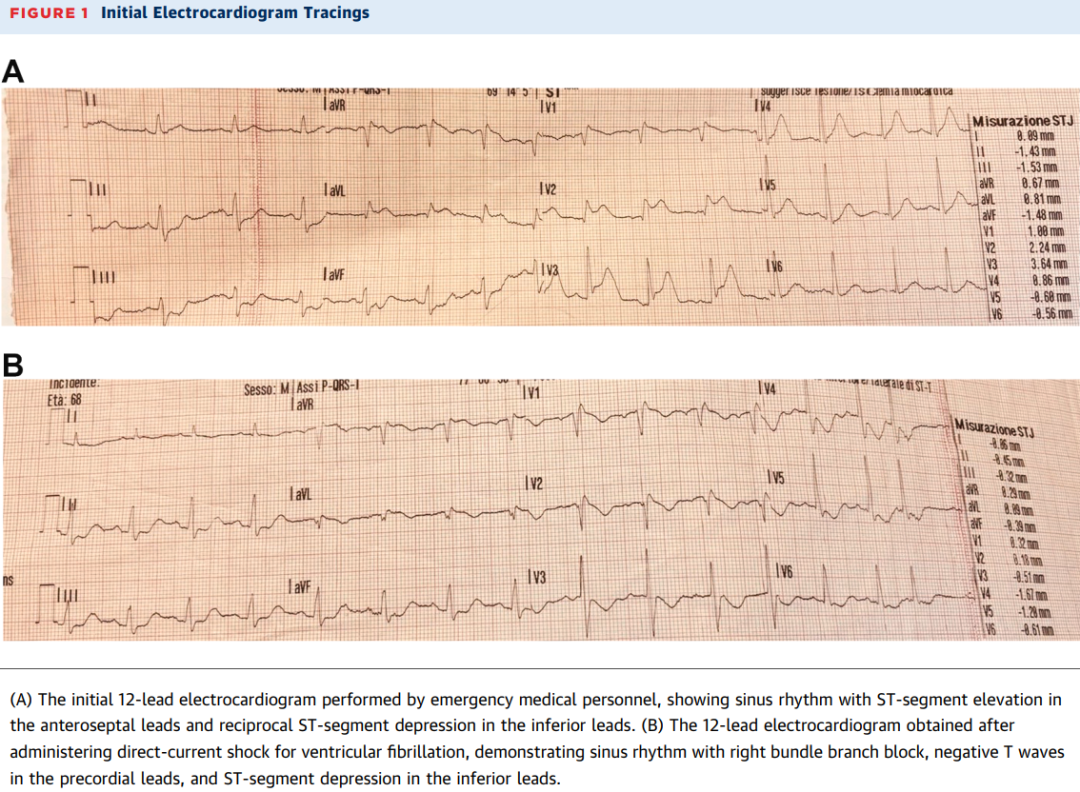
转折点发生在一次急性事件中:患者因胸痛呼叫急救,心电图显示前壁ST段抬高伴下壁对应性压低。在转运至导管室途中,他突发心室颤动,经电除颤后恢复。复苏后心电图出现新发右束支传导阻滞、前壁和侧壁T波倒置,以及持续性ST段压低(图1)。紧急冠状动脉造影显示心外膜冠状动脉正常,呈右优势型,无阻塞性病变。患者被转入重症监护室,但病因仍未明朗。
回顾历史,2019年患者曾因类似症状就诊,冠脉CTA确认血管正常且钙化积分为零。治疗方案调整为地尔硫卓和雷诺嗪,但症状依旧反复。
此次危急事件促使医疗团队进行彻底评估:鉴于患者年轻、症状慢性化、影像学异常和肌钙蛋白升高(峰值165 pg/mL),决定采用有创冠脉内成像和生理学评估,以排除血管造影隐匿性ACS的潜在不稳定斑块,并评估功能学异常。
有创技术揭开双重病理机制
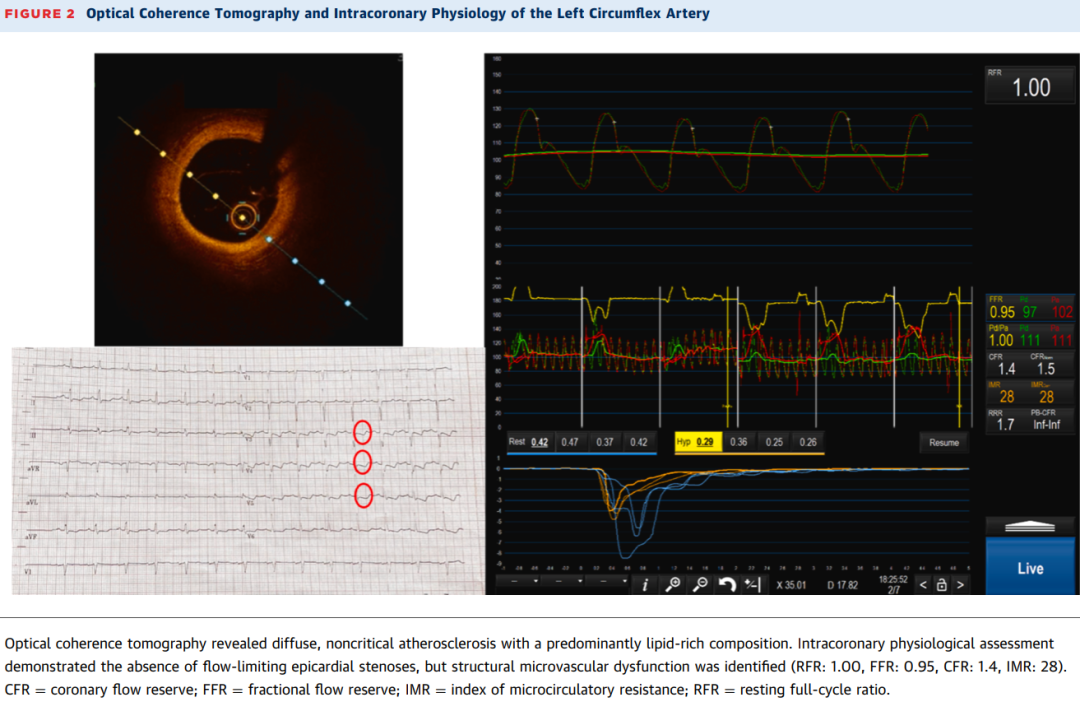
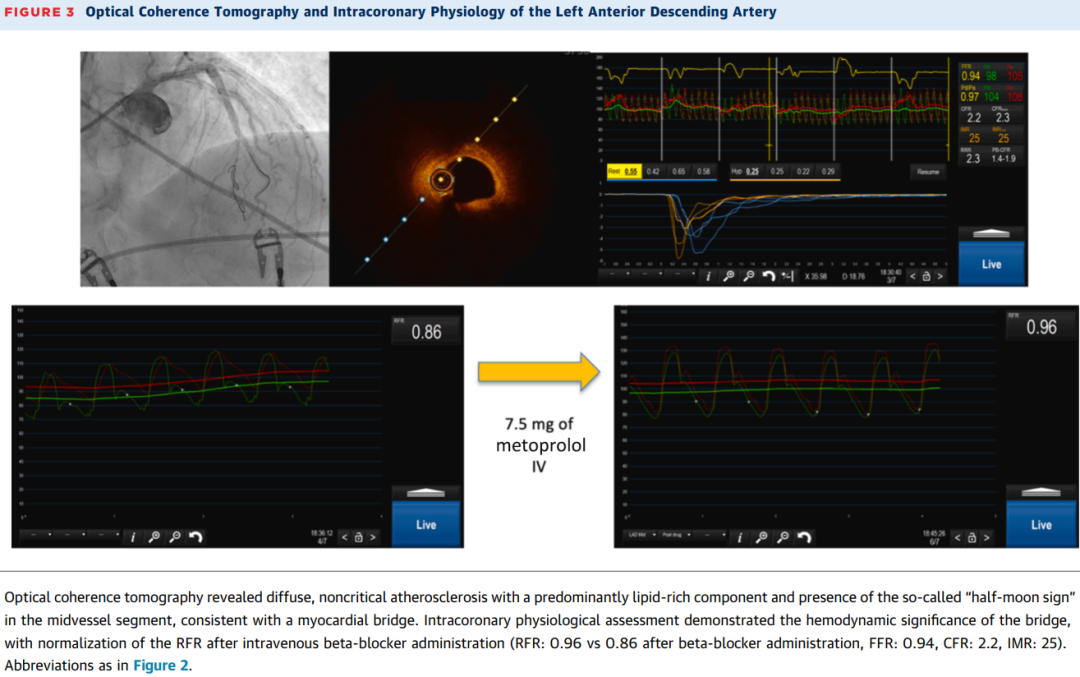
医疗团队按如下步骤进行。首先,通过光学相干断层扫描(OCT)对前降支和回旋支进行成像,发现弥漫性动脉粥样硬化,以脂质成分为主,,但无不稳定斑块特征。在前降支中段可见一中间亮度带环绕血管壁,符合心肌桥的“半月征”表现(图2和图3)。
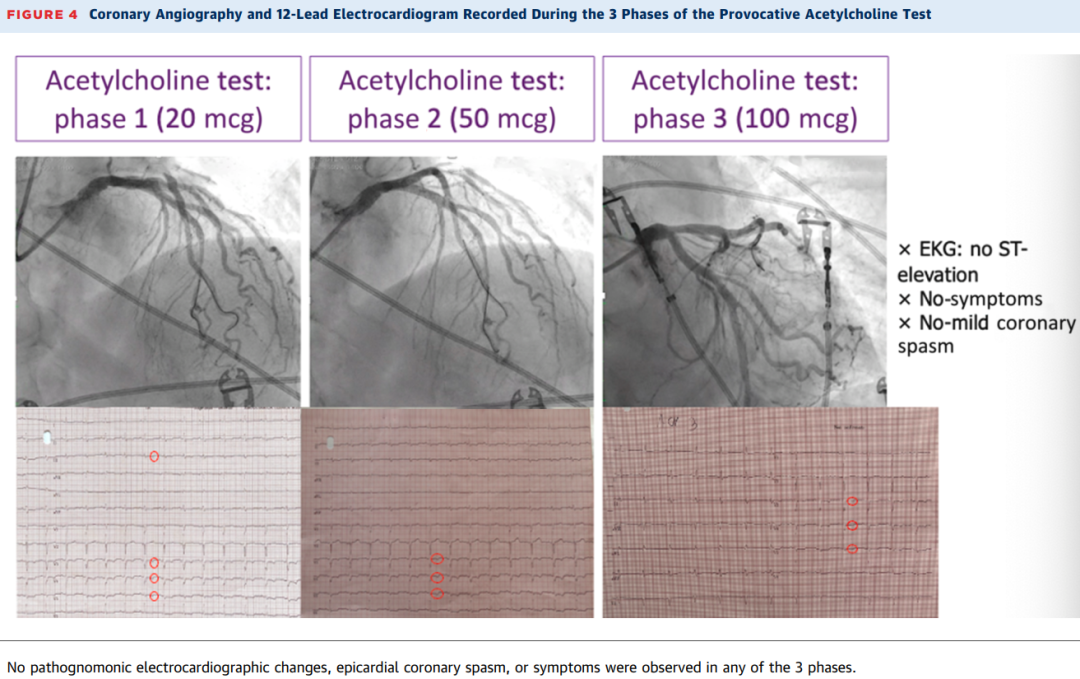
随后,进行乙酰胆碱激发试验(剂量递增至100μg),结果显示轻度弥漫性痉挛,但无典型心电图改变或症状。注射硝酸盐后,前降支中段出现“挤奶效应”,进一步支持心肌桥的诊断(图4)。
使用压力导丝进行了生理学评估。在回旋支(因血管尺寸和心肌灌注范围适宜)测量非充血和充血指数(通过静脉注射腺苷诱导充血)以及通过团注热稀释法获得的微循环功能,显示冠状动脉血流储备(CFR)降低(1.4)和微血管阻力指数(IMR)升高(28),提示结构性微血管功能障碍。静息全周期比率(RFR)为1.00,血流储备分数(FFR)为0.95,排除了血流限制性狭窄(图2)。
为评估心肌桥的血流动力学影响,压力导丝被置于前降支心肌桥段远端,基线RFR为0.86(表明缺血)。静脉注射美托洛尔后,RFR逐步改善至0.96,证实β受体阻滞剂可缓解肌桥相关缺血(图3)。
最终诊断为心肌桥和结构性微血管功能障碍所致的心肌缺血。
从经验性到个体化治疗
基于上述发现,治疗方案彻底调整:停用可能加重心肌桥的硝酸酯和地尔硫卓,将雷诺嗪加量至500 mg每日两次,并加用美托洛尔100 mg每日两次。同时,为预防猝死,植入心律转复除颤器(ICD)。出院后6个月随访,患者症状完全消失,心电图和超声心动图检查结果均正常。
长达十年的经验性治疗,经验性药物治疗意图控制血管痉挛,却忽略了心肌桥和微血管功能障碍的核心作用。尤其硝酸酯类药物,可能通过增加心肌收缩力和增快心率,加剧肌桥的压迫效应。而β受体阻滞剂通过负性肌力和频率作用,有效缓解了缺血。
讨论
本案例深刻体现了有创生理学和腔内影像在MINOCA管理中的核心地位。ESC指南已将其列为推荐,但临床实践中的落地仍存挑战。尽管心外膜血管痉挛和微血管功能障碍的评估方法已标准化,但关于如何、何时评估心肌桥,以及如何避免与用于评估血管痉挛和微血管功能的药物发生相互作用,目前仍缺乏统一的指南。
众所周知,考虑到心肌桥引起的血流阻塞为动态性,传统FFR因测量整个心动周期,可能低估肌桥的动态压迫作用,似乎并非此情况下最合适的指标。在小型系列研究中,已观察到在多巴酚丁胺给药后测量的舒张期FFR(dFFR),以0.76为界值,与症状和IVUS识别的心肌桥有更直接的相关性。该指标避免了在整个心动周期中测量的负性冠脉内压力梯度所产生的误导性影响。鉴于dFFR的可用性有限,其他非充血指数已被采用,例如瞬时无波比率(iFR)和RFR。在最近一项纳入64名患者的队列中,这两种指数在与多巴酚丁胺输注后的dFFR比较中均显示出良好的相关性,且RFR表现出更优的诊断准确性。
我们选择RFR来评估心肌桥,是在完成流程最后一步后进行的:仅在乙酰胆碱、硝酸酯类和腺苷的作用消退后才评估心肌桥。考虑到这些药物的半衰期较短,我们认为基线时异常的RFR值是可靠的,在静脉注射美托洛尔后恢复正常也证明了这一点。
尽管心肌桥是致命性心脏事件的相对罕见原因,且通常无症状,但研究发现它是ICD患者中发生危及生命的室性心律失常的独立危险因素。此外,进行OCT检查,不仅是为了排除ACS潜在的其他原因,也是为了提供前降支心肌桥的详细解剖特征,这可能对未来潜在的血运重建策略提供了依据。
然而,有创评估也面临争议:成本、操作复杂性。本团队通过分步评估(先腔内影像、后痉挛评估、再生理学评估),避免了相互干扰。此外,ICD植入的决策基于肌桥相关心律失常的风险证据,提醒我们MINOCA并非总是良性。
严道心得
阅读此案例,笔者深感医学的复杂与谦卑。一名患者辗转十年,终获明确诊断,背后是诊断技术的进步与临床思维的革新。首先,它警示我们:症状与造影不匹配时,切忌满足于经验性判断。血管痉挛、心肌桥、微血管障碍常交织存在,需系统性排除。
其次,个体化治疗不止于药物选择,更在于病理生理的深度解构。β阻滞剂对肌桥的效益、雷诺嗪对微血管的改善,体现了机制导向的精准性。但笔者也存有疑问:微血管功能障碍的成因未明(是否与高血压、血脂异常相关?);OCT发现的富脂质斑块是否需强化降脂?长期预后仍待观察。
最后,技术普及与卫生经济平衡是关键。有创诊断增加短期成本,但可能减少反复住院和误治损失。在控费背景下,需证明其成本效益。同时,无创替代方案(如CT-FFR、心脏MR)的发展,或可部分替代有创检查。
总之,此案例提醒临床医生:在正常造影背后,可能隐藏着功能与解剖的交响曲。唯有借助先进工具与细致思维,才能奏出精准医疗的强音。