
在心血管疾病诊疗领域,亚临床冠状动脉粥样硬化的早期识别一直是改善患者预后的关键环节。冠状动脉CTA作为当前主流的无创检测手段,虽能有效发现无症状人群的早期粥样硬化病变,但如何精准筛选出需要接受CTA检查的高风险个体,仍是临床实践中的一大难题。
近年来,越来越多的研究提示视网膜微血管变化与全身微循环障碍存在密切关联。视网膜微血管在生理结构和解剖特征上与冠状动脉系统具有高度相似性,这使得通过评估视网膜微血管状况来间接反映冠状动脉健康状态成为可能。视网膜光学相干断层扫描血管造影(OCTA)作为一种新型无创影像学技术,能够清晰显示视网膜浅层毛细血管丛(SCP)和深层毛细血管丛(DCP),并精准量化黄斑区及中心凹旁区域的血管密度(VD),为视网膜微血管评估提供了更细致、更客观的工具。

既往研究已观察到冠心病患者存在视网膜血管密度降低的现象,但这些研究多缺乏大样本量的验证,且未深入探讨OCTA参数与冠状动脉CTA关键指标之间的关联。鉴于全身疾病负担可通过视网膜微血管得到良好反映,而OCTA又能对视网膜微血管进行精细化评估,有理由假设,OCTA参数或可成为辅助诊断冠状动脉粥样硬化的有效工具。
为此,来自韩国首尔峨山医疗中心的研究团队开展了一项大样本横断面队列研究,旨在分析无症状高心血管风险人群中视网膜微血管变化与冠状动脉CTA的相关性,为亚临床冠状动脉粥样硬化的早期筛查提供新的思路。
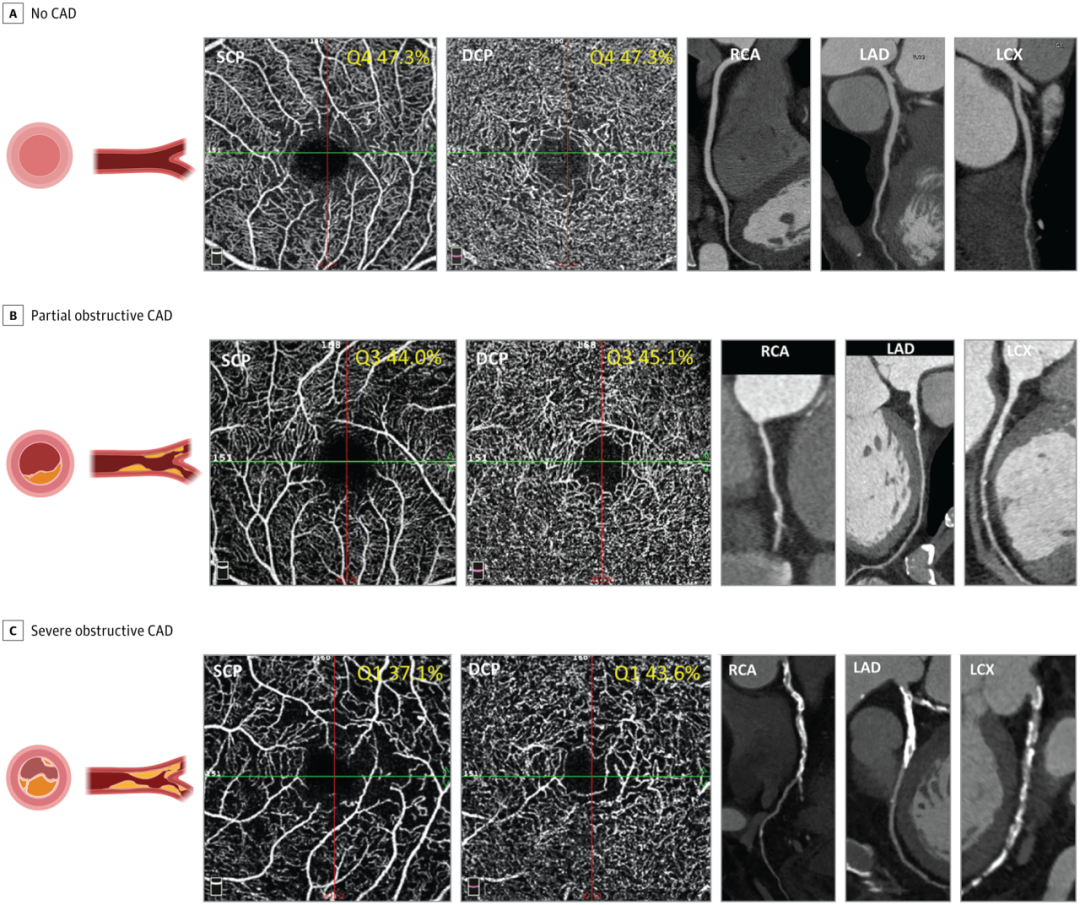
OCTA与冠状动脉CTA之间存在关联的代表性案例
方法
研究人群
研究纳入2015年10月至2020年12月期间在韩国首尔峨山医疗中心参与自愿健康筛查项目的无症状个体。所有参与者均同时接受了冠状动脉CTA检查和OCTA检查。
纳入标准:年龄≥18岁;无症状但存在心血管风险升高(基于动脉粥样硬化性心血管疾病风险评分评估);自愿参与健康筛查并接受冠状动脉CTA和OCTA检查;签署书面知情同意书。
排除标准:年龄<18岁;有心绞痛或心肌梗死病史;因心脏直视手术或经皮冠状动脉介入治疗导致冠状动脉结构异常;医疗记录不完整。
在OCTA评估中,选择最佳矫正视力(BCVA)最较的眼睛。如果双眼BCVA相同,则选择右眼。当眼睛有明显黄斑病变病史时,对另一眼进行研究。有玻璃体内注射、玻璃体切割术病史,或患有黄斑水肿、玻璃体出血、外伤等眼部疾病且信号强度指数(SSI)低于50的眼睛被排除在外。此外,高度近视(等效球镜度数>6.0屈光度或眼轴长度>26毫米)以及有明显双侧黄斑疾病、眼内感染、葡萄膜炎、外伤或青光眼病史的参与者也被排除。
纳入组和排除组参与者的BCVA比较无显著差异,表明与视觉功能相关的选择偏倚极小。最终,共有1286名参与者(1286只眼)被纳入分析。
临床及实验室指标采集
通过查阅医疗记录,收集参与者与冠状动脉CTA检查时间最接近的临床资料,包括:人口统计学特征、吸烟史、合并症、用药史、体格检查指标。实验室检查指标均由峨山医疗中心认证实验室采用标准化方法检测。
冠状动脉CTA检查与分析
所有参与者均采用第二代或第三代双源CT(Siemens SOMATOM Definition)进行冠状动脉CTA检查,扫描方案遵循标准化流程。由3名具有执业资格的放射科医师根据已建立的解读指南独立分析冠状动脉CTA图像,最终由1名心血管放射科医师(D.H.Y.)汇总分析结果。
伴有明显狭窄的阻塞性冠心病定义为狭窄程度达到50%或更高。总动脉粥样硬化斑块负荷采用冠状动脉斑块评分进行评估:包括节段受累评分(SIS)和节段狭窄评分(SSS)。严重冠心病定义为符合以下标准之一:累及左前降支(LAD)近段的双支血管病变;②三支血管病变;③左主干病变;
OCTA检查与分析
采用Optovue RTVue XR Avanti光学相干断层扫描仪(配备AngioVue软件)进行OCTA检查,获取黄斑区3mm×3mm立方体扫描图像,每幅图像包含304组重复B扫描,每组B扫描包含304条A扫描线。
采用设备默认设置,SCP定义为从内界膜下方3μm至内丛状层下方15μm的区域;DCP定义为从内核层下方15μm至外丛状层下方70μm的区域;
测量的视网膜微血管参数如下:包括黄斑无血管区(FAZ)面积(单位:mm²)、SCP和DCP的黄斑中心凹血管密度(1mm直径区域,基于糖尿病视网膜病变早期治疗研究网格中心亚区定义)、SCP和DCP的中心凹旁血管密度(PFVD,基于3mm直径内圈4个亚区的平均值,不包括中心亚区)、视网膜中央厚度(从内界膜到视网膜色素上皮层的距离,单位:μm)。
结果
人群特征
纳入的1286名参与者中(表1),平均年龄为64.2±9.9岁,女性482例(37.5%);
体重指数中位数为24.60(22.64~26.56),其中超重(25~30)者503例(39.1%),肥胖(≥30)者74例(5.8%);
吸烟状态分布为当前吸烟135例(10.5%)、既往吸烟349例(27.1%)、从不吸烟802例(62.4%);
收缩压平均值为130.19±10.04mmHg。
合并症方面,糖尿病552例(42.9%)、高血压675例(52.5%)、高脂血症930例(72.5%)、脑卒中80例(6.2%)、肾病94例(7.3%);
用药情况为阿司匹林260例(20.2%)、氯吡格雷337例(26.2%)、他汀类药物803例(62.4%)、胰岛素108例(8.4%)、二甲双胍376例(29.2%)。
实验室指标:
HbA1c平均值为6.25±1.18%,其中≥7%者294例(22.9%);空腹血糖平均值为124.21±43.04mg/dL;甘油三酯平均值为129.33±75.73mg/dL;HDL-C平均值为50.27±14.02mg/dL;LDL-C平均值为102.85±32.49mg/dL;CRP平均值为0.80±2.35mg/dL;eGFR中位数为85.00(71.25~95.00)mL/min/1.73m²,其中≤59mL/min/1.73m²者147例(11.4%)。
OCTA参数:
BCVA(log MAR)平均值为0.37±0.44;FAZ面积平均值为0.35±0.48mm²;SCP黄斑中心凹血管密度平均值为18.95±10.16%;SCP中心凹旁血管密度(SCP PFVD)平均值为45.00±7.32%;DCP黄斑中心凹血管密度平均值为32.28±10.04%;DCP中心凹旁血管密度(DCP PFVD)平均值为49.08±7.16%;中心视网膜厚度平均值为264.35±63.44μm;OCTA信号强度平均值为63.24±6.86;OCTA与冠状动脉CTA检查间隔中位数为4.4(2.0~7.7)个月。
冠状动脉CTA结果:
CACS中位数为0.00(0.00~98.70),其中>400者136例(10.6%);存在任何斑块者804例(62.5%),其中钙化斑块685例(53.3%)、非钙化斑块234例(18.2%)、混合斑块320例(24.9%);阻塞性CAD 300例(23.3%),其中单支血管病变148例(11.5%)、双支血管病变88例(6.8%)、三支血管病变63例(4.9%)、左主干病变23例(1.8%);存在左主干或左前降支近段阻塞性CAD者145例(11.3%);严重CAD120例(9.3%);SSS平均值为5.10±7.18,其中≥10者261例(20.3%);SIS平均值为2.53±2.81,其中≥5者220例(17.1%)。
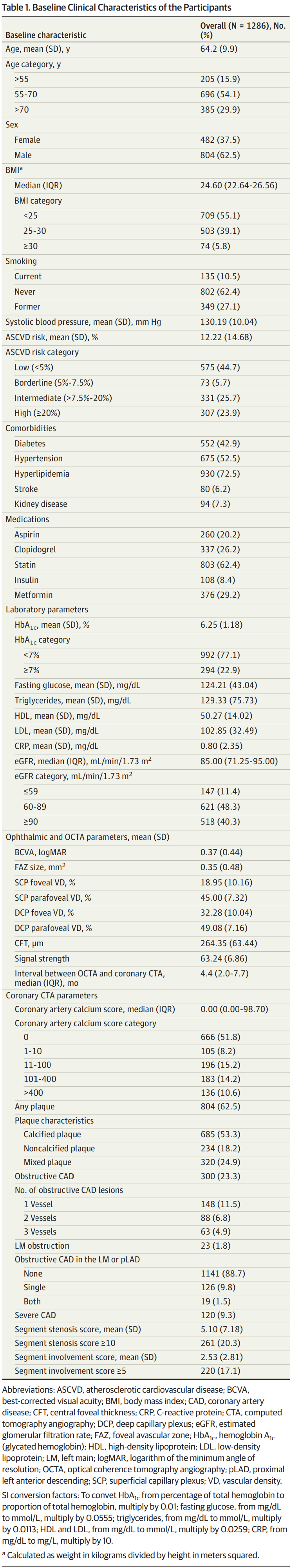
视网膜PFVD与亚临床动脉粥样硬化的关联
结果显示,随着视网膜浅层和深层PFVD四分位数的降低,冠状动脉钙化积分(CACS)、斑块及其亚型的存在率、阻塞性CAD、严重CAD、节段狭窄评分(SSS)以及节段受累评分(SIS)均显著升高。表2为按SCP和DCP的PFVD四分位数展示参与者的基线特征。
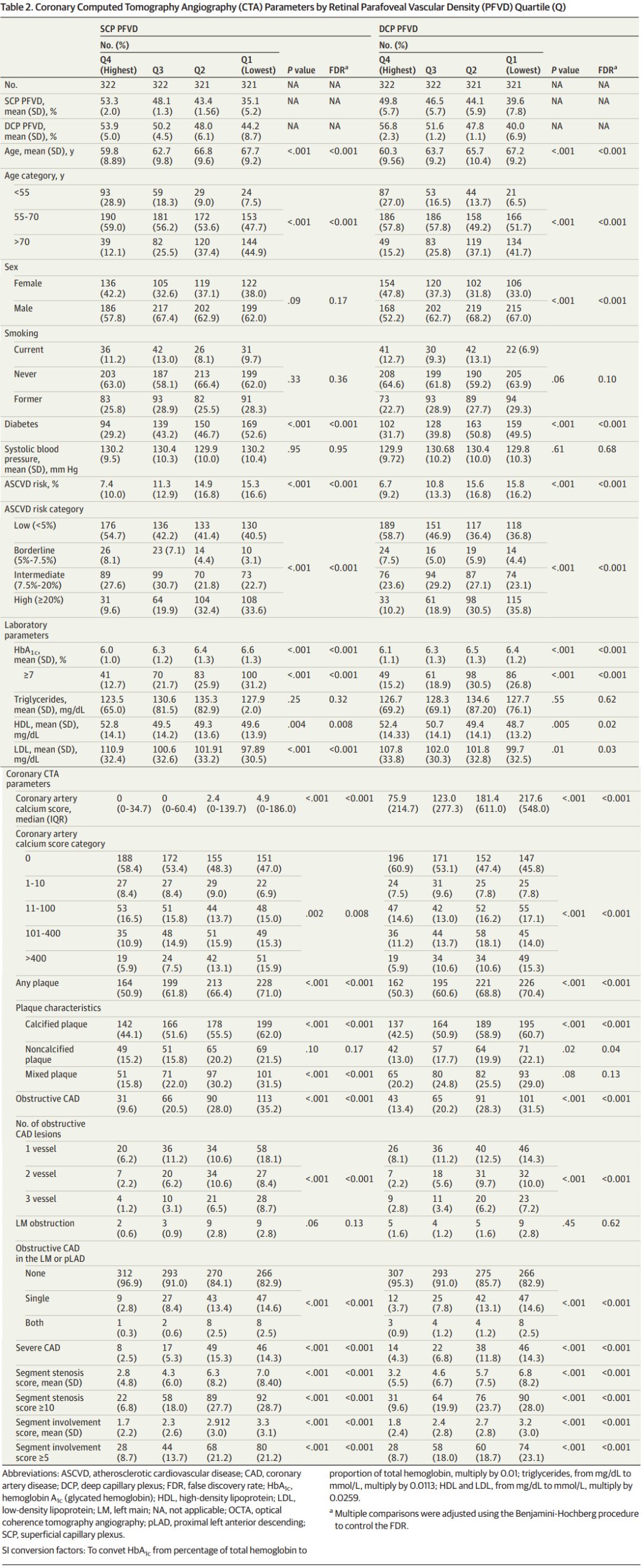
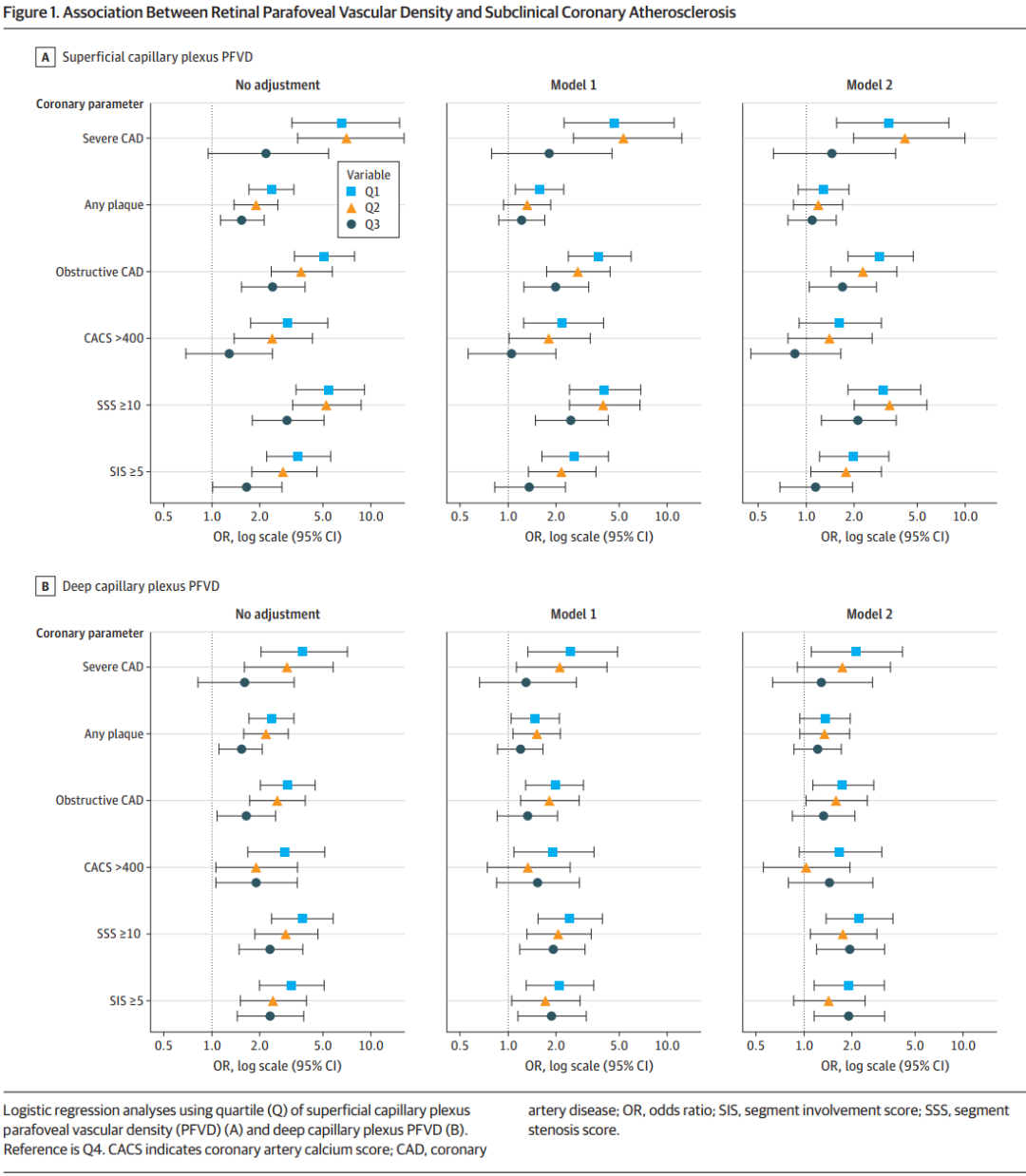
亚临床动脉粥样硬化的比值比见图1。当将SCP和DCP的PFVD作为连续变量纳入模型分析时,二者是与冠状动脉相关指标关联最显著的指标,且均与CACS、受累冠状动脉血管数量、SSS及SIS存在相关性。与SCP PFVD最高四分位数组相比,SCP PFVD最低四分位数组(最低血管密度)发生阻塞性CAD(aOR2.91,95%CI 1.83~4.73)、严重CAD(aOR 3.30,95% CI 1.55~7.91)的风险显著更高,且SSS和SIS评分也显著升高。
DCP PFVD与上述冠状动脉指标也存在类似关联,但关联强度相对较弱。对PFVD单位增量进行比值比(OR)的连续变量分析显示,PFVD降低与冠心病负担增加之间存在线性关联。纳入PREVENT风险评分的敏感性分析得出了与整个队列一致的结果。
视网膜PFVD的增量预后价值
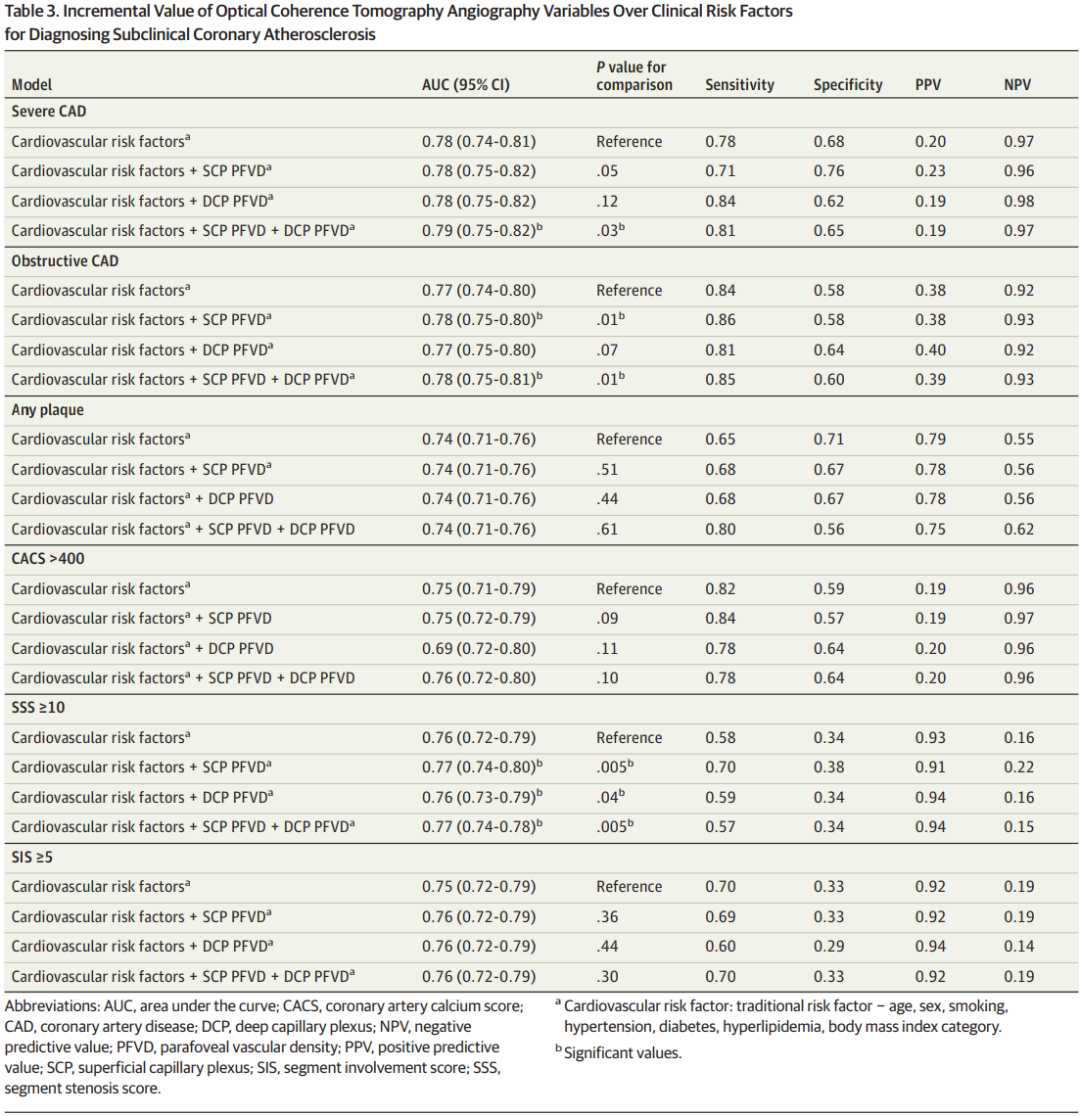
在纳入心血管危险因素的模型中加入PFVD后,模型的阴性预测值(NPV)显著提升(表3),模型对严重CAD(AUC 0.79,95% CI 0.75~0.82)、阻塞性CAD(AUC 0.78,95% CI 0.76~0.81)及SSS≥10(AUC 0.77,95% CI 0.74~0.80)的识别效能显著提升,且SCP PFVD的表现优于DCP PFVD。采用logistic回归训练模型和随机森林模型进一步验证,结果显示,纳入OCTA参数(尤其是SCP PFVD)的模型对严重CAD和阻塞性CAD的鉴别效能显著优于仅包含传统风险因素的模型,其中随机森林模型的敏感性和特异性更高(如对严重CAD的敏感性为0.81,特异性为0.65)。
OCTA参数诊断亚临床CAD的最佳临界值
SCP PFVD诊断阻塞性CAD和严重CAD的最佳临界值为46.3%,DCP PFVD的最佳临界值为49.6%。以临界值为界将参与者分为“低PFVD组”和“正常PFVD组”,结果显示:
低SCP PFVD组发生严重CAD的校正OR为3.13(95% CI:1.93~5.24,P<0.001),发生阻塞性CAD的校正OR为1.89(95% CI:1.39~2.57,P<0.001);
低DCP PFVD组发生严重CAD的校正OR为2.25(95% CI:1.38~3.68,P=0.001),发生阻塞性CAD的校正OR为1.56(95% CI:1.15~2.12,P=0.005);
同时存在低SCP和低DCP PFVD的参与者,发生严重CAD和阻塞性CAD的风险最高(OR 分别为4.02和2.38,均P<0.001)。
讨论
本研究通过大样本横断面队列设计,首次系统探讨了OCTA评估的视网膜中心凹旁血管密度(PFVD)与冠状动脉CTA量化指标之间的关联,核心发现如下:SCP和DCP PFVD与冠状动脉粥样硬化负担(CACS、斑块数量、SSS、SIS)呈显著负相关,且这种关联具有剂量依赖性——PFVD越低,发生阻塞性CAD和严重CAD的风险越高。其中,SCP PFVD的关联强度显著高于DCP PFVD,提示视网膜浅层毛细血管丛的血管密度变化可能更敏感地反映冠状动脉粥样硬化状态。
在传统心血管风险因素(如年龄、性别、糖尿病、高血压、血脂异常)基础上加入PFVD,可显著提升对严重CAD和阻塞性CAD的诊断效能(AUC最高升至0.79),且模型具有高NPV(>0.9)和高PPV(>0.9)。这意味着,对于OCTA显示PFVD正常的个体,其发生严重CAD的可能性极低(可通过高NPV排除);而对于PFVD降低的个体,需警惕高粥样硬化负担(可通过高PPV提示)。这种特性使OCTA有望成为冠状动脉筛查工具——在眼科常规检查中通过OCTA初筛,再对PFVD降低的个体进一步行冠状动脉CTA检查,可提高筛查效率并降低医疗成本。
研究发现SCP PFVD在关联强度和诊断效能上均优于DCP PFVD,可能的机制在于:SCP包含更多的动脉和小动脉,而DCP以毛细血管和静脉为主;冠状动脉粥样硬化的本质是动脉血管壁的病变,其病理生理过程(如内皮功能障碍、炎症反应、脂质沉积)可能与视网膜动脉系统的变化更具同源性。此外,既往研究显示视网膜动脉功能障碍优先表现于SCP,这也解释了为何SCP PFVD能更敏感地反映冠状动脉状态。
本研究纳入的参与者多为无症状高心血管风险人群(如42.9%合并糖尿病、52.5%合并高血压),这类人群往往因眼部疾病(如糖尿病视网膜病变)就诊于眼科,而OCTA是评估视网膜病变的常规检查。若能在眼科检查中同步关注PFVD,可实现心血管风险的机会性筛查——无需额外增加检查项目,即可为临床医生提供心血管风险的额外信息,尤其适用于医疗资源有限、难以普及冠状动脉CTA的场景。
结论
本研究证实,在无症状高心血管风险人群中,视网膜OCTA评估的中心凹旁血管密度(尤其是SCP PFVD)与亚临床冠状动脉粥样硬化显著相关。PFVD降低是亚临床CAD的独立危险因素,且在传统心血管风险因素基础上具有增量预测价值。因此,视网膜PFVD可作为亚临床冠状动脉粥样硬化的潜在生物标志物,辅助临床医生识别需要进一步冠状动脉评估的高风险个体。
严道心得
本研究的创新点在于将眼科的OCTA技术与心血管领域的冠状动脉CTA技术结合,通过“视网膜-冠状动脉”的微血管关联,为亚临床疾病的早期识别提供了新视角。这提示我们,不同学科的技术交叉可能产生突破性的临床应用——眼科检查不仅能评估眼部疾病,还能成为全身血管健康的窗口,这种“一检多评”的模式符合精准医学和高效医疗的发展趋势。
本研究为亚临床冠状动脉粥样硬化的早期筛查提供了新的无创工具,也为跨学科合作推动临床诊疗进步提供了宝贵经验。随着研究的深入,OCTA有望成为连接眼科与心血管科的桥梁技术,为实现心血管疾病的早期预防和精准管理贡献力量。