PART.01

病例寻踪

病例直击
患者为65岁女性,6年前因病态窦房结综合征植入双腔起搏器。3年前开始出现颜面肿胀,颈静脉怒张,视物模糊。1年前于外院行上腔静脉造影,提示上腔静脉闭塞综合征,行上腔静脉球囊扩张,颜面水肿略减轻。1月前因颜面水肿再发并加重前来就诊,经诊断确诊患者为上腔静脉阻塞综合征,且反复多次出现相关症状,足以证明如果不拔除整套起搏系统,无法完全解决该患者的上腔静脉综合征。
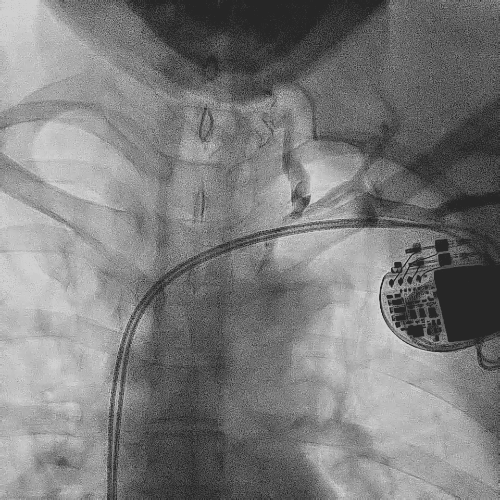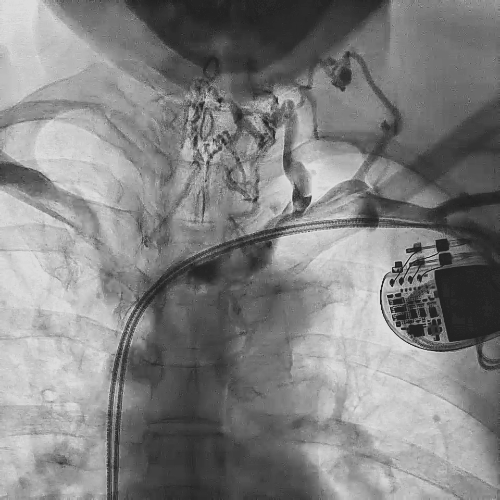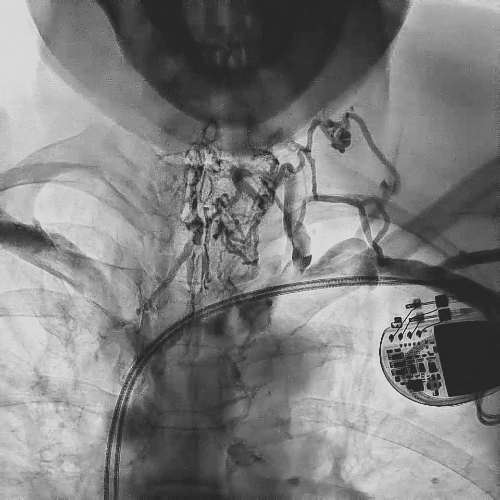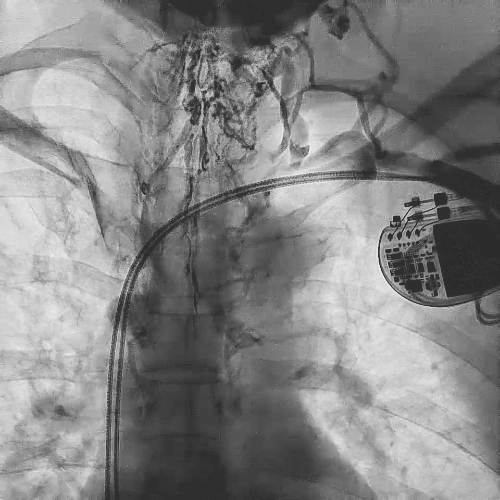

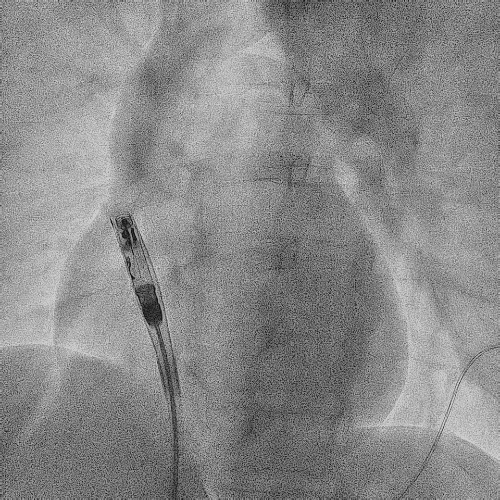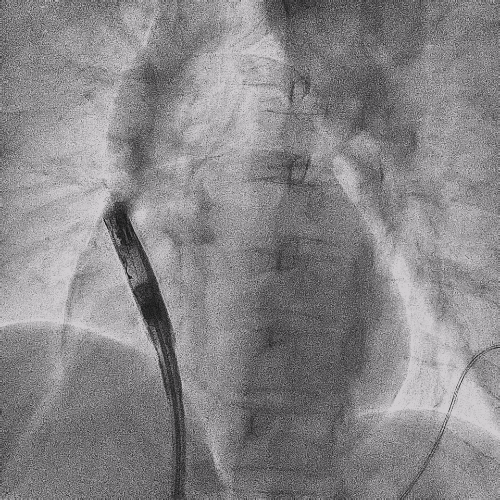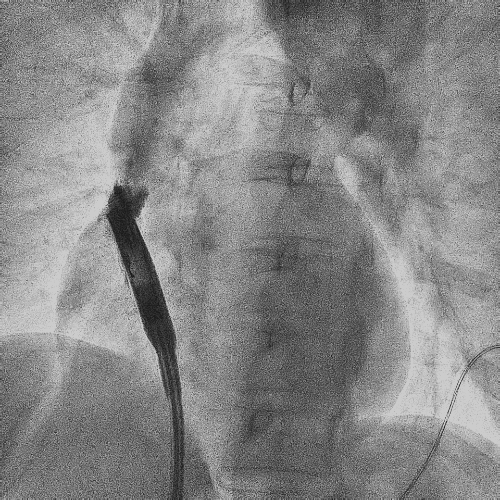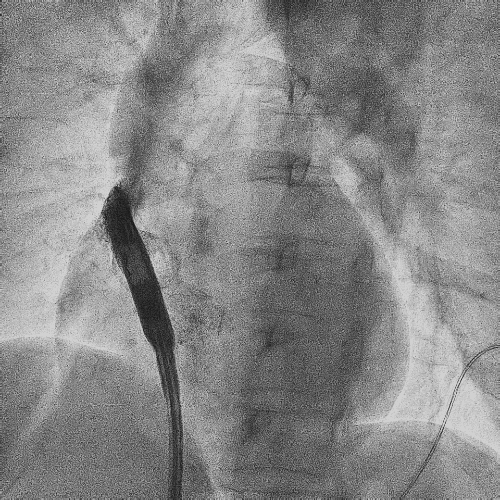
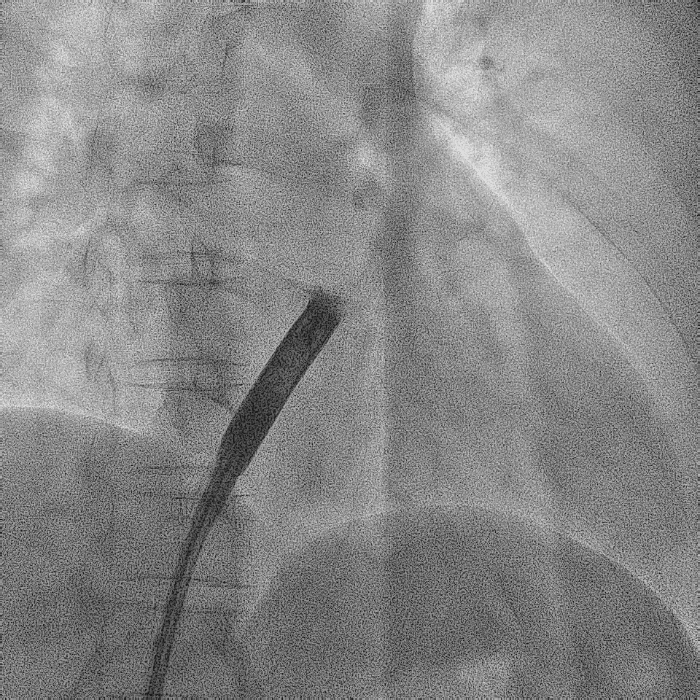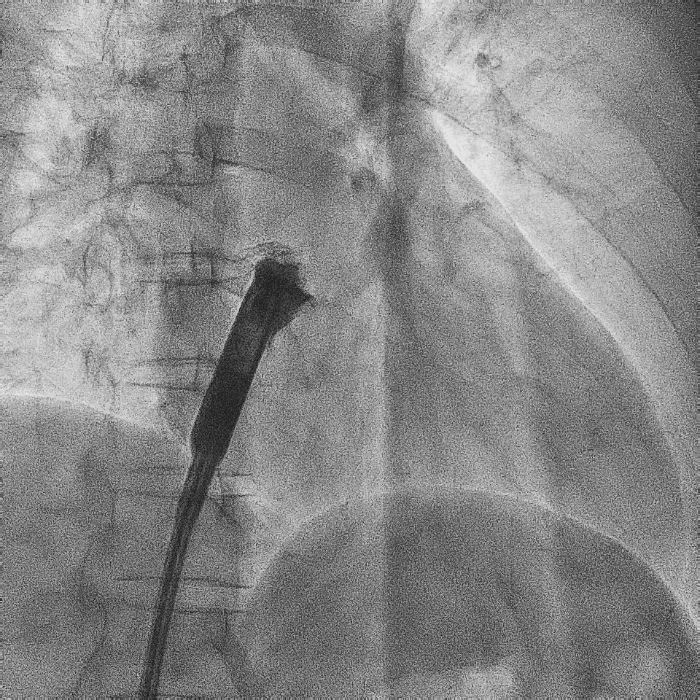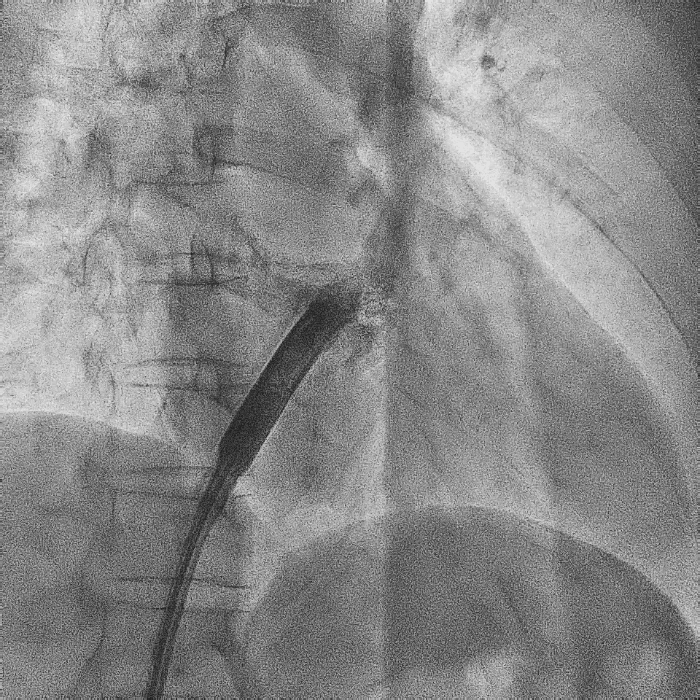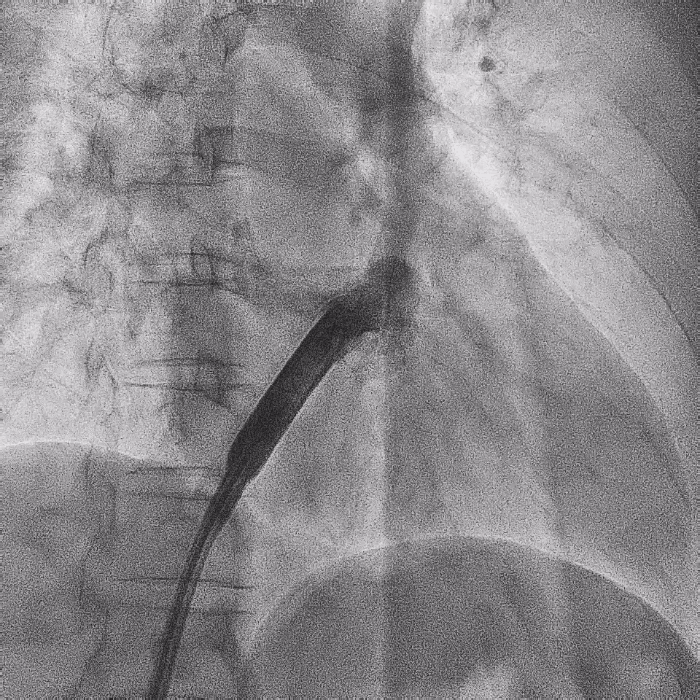
造影显示左侧无名静脉和上腔静脉交汇后
明显狭窄和闭塞
电极拔除前
颈静脉怒张明显


精准决策
入院后行心脏超声和体表心电图等基础检查,通过检查原起搏器起搏比例确认房室传导正常,体表心电图提示工作模式始终为”AAI”。当将患者之前植入的起搏器程控为VVI起搏模式,发现患者对单心室起搏不耐受,有起搏器综合征症状。且患者本身没有其他入路可以选择,如从对侧植入还会有更严重的上腔静脉阻塞问题。结合患者个人植入无导线起搏器意愿,经李学斌教授团队全面考虑后,给患者确定手术对策——①从锁骨下静脉拔除整套起搏系统。②右侧股静脉做入路,利用外周球囊扩张上腔静脉。③同台植入AVEIR™ AR心房无导线心脏起搏器,为患者提供相应治疗。
PART.02

手术概况

右心耳造影
拔除前进行猪尾造影,提前确认原右房导线位置为右心耳中部,心耳空间较大,解剖位置正常。为后续AVEIR™ AR植入做好计划,确认有足够空间避开原起搏导线所在位置。

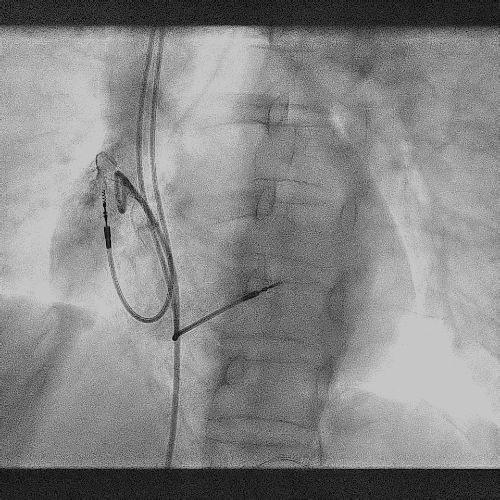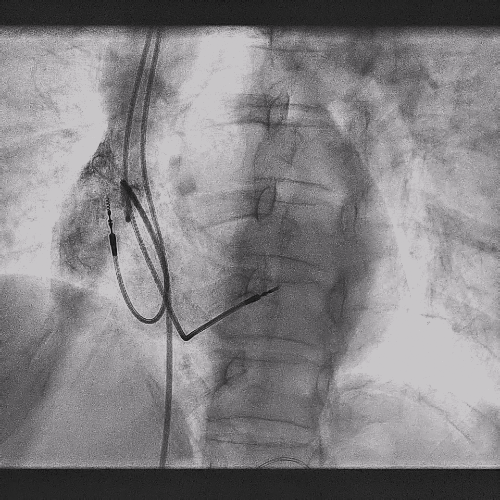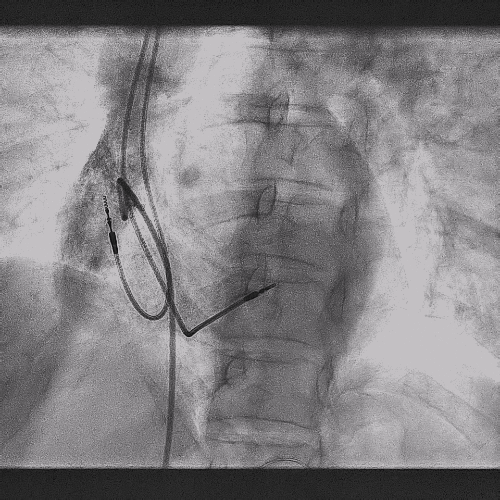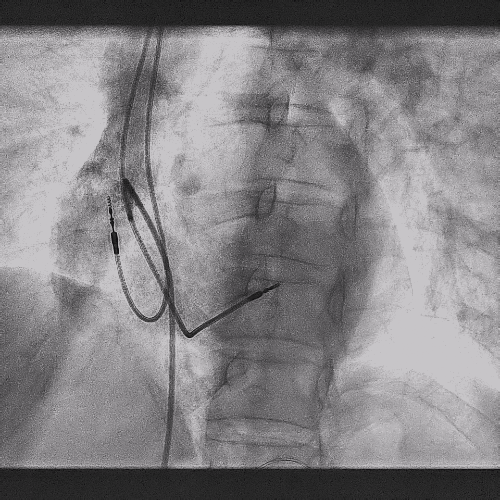
RAO 30°造影
LAO 30°造影


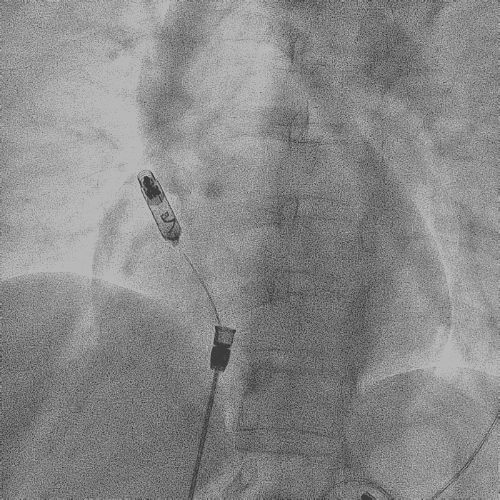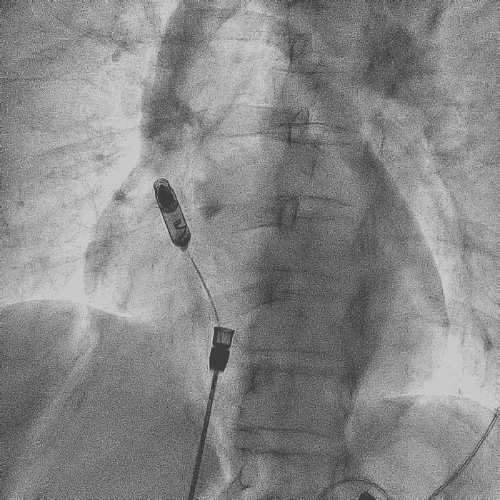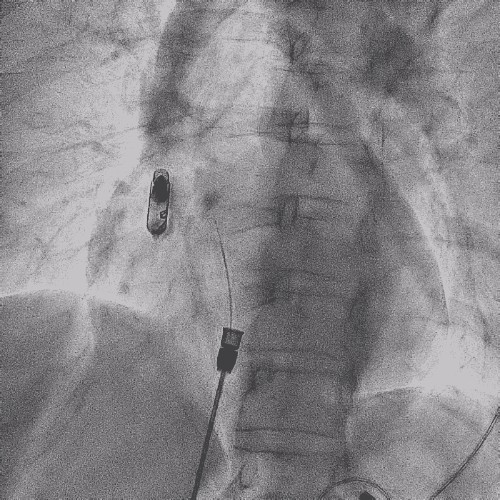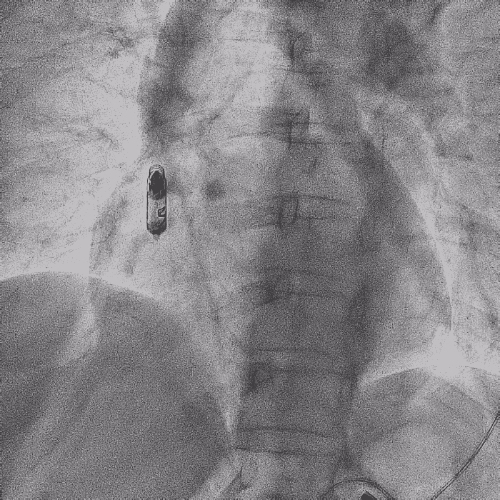
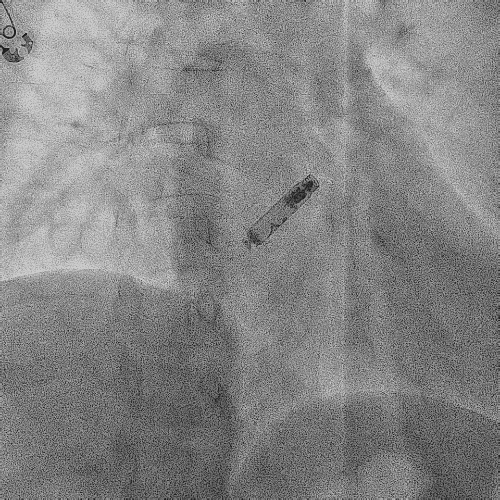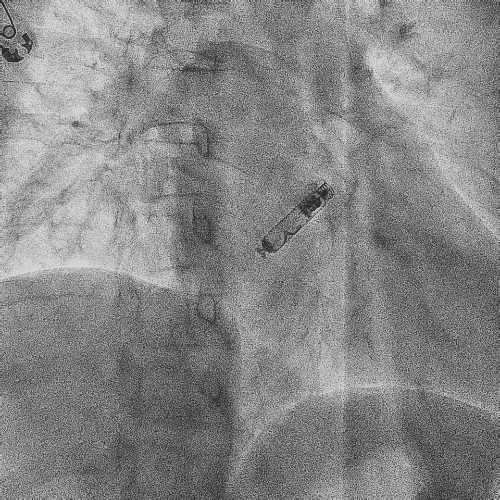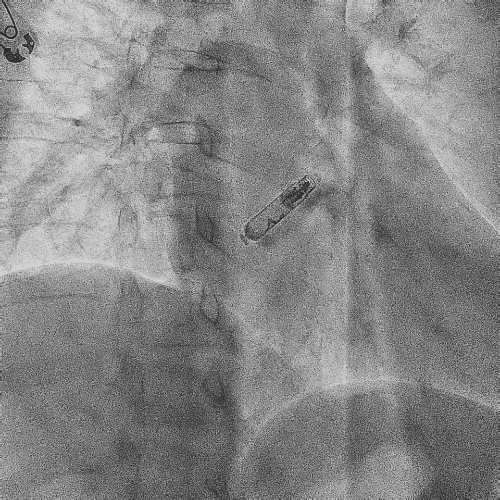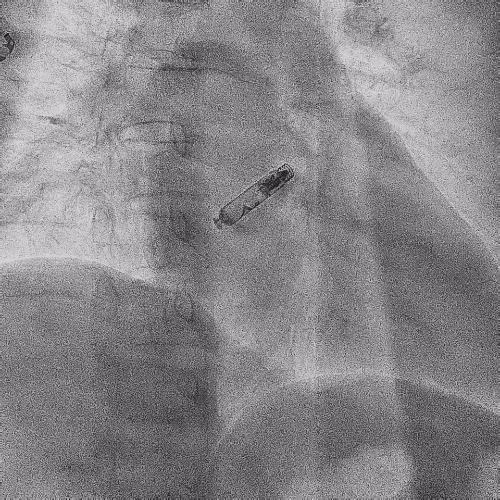
电极拔除
打开囊袋取出原起搏器后,使用锁定钢丝锁定分别锁定两根导线,备用激光鞘并未使用。直接徒手顺利拔除两根导线。
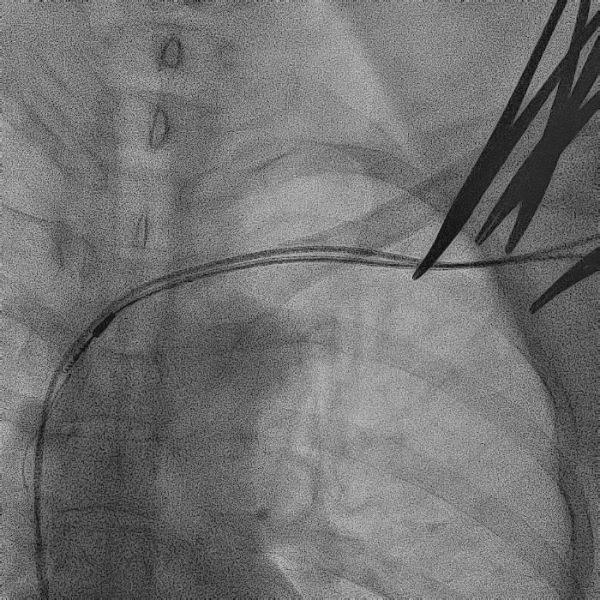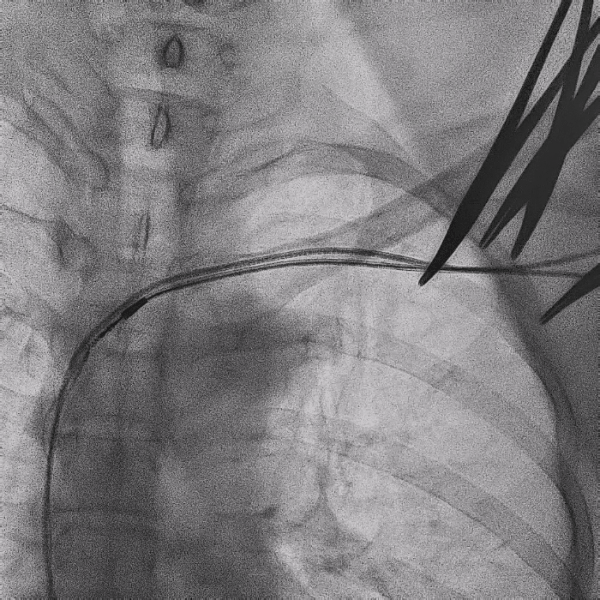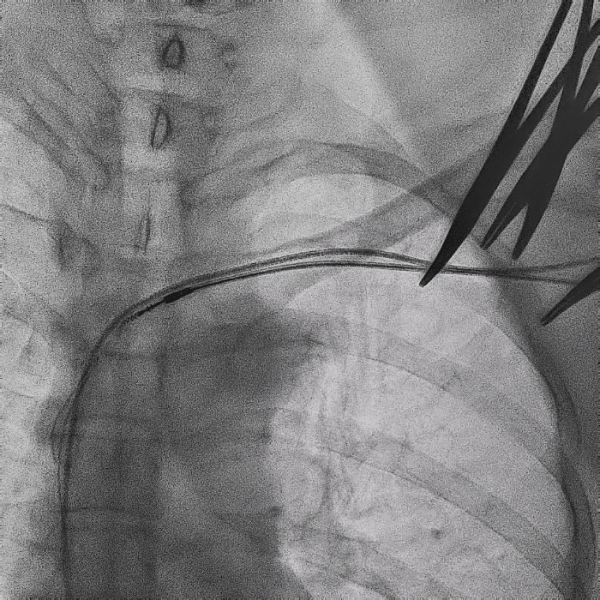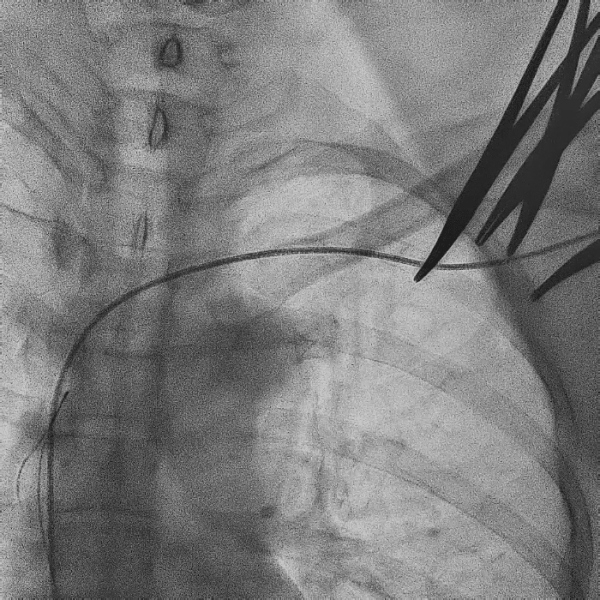
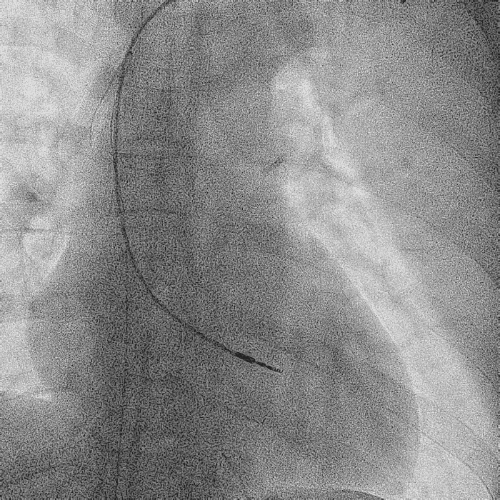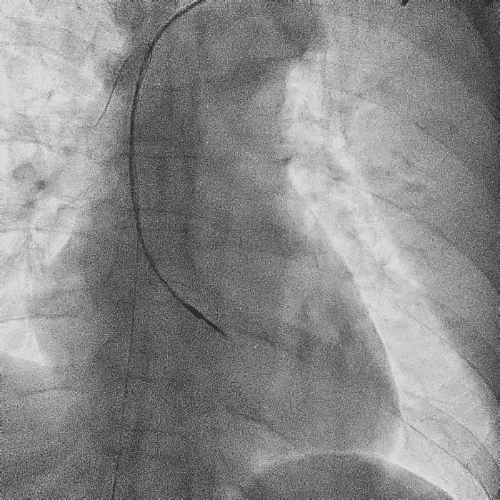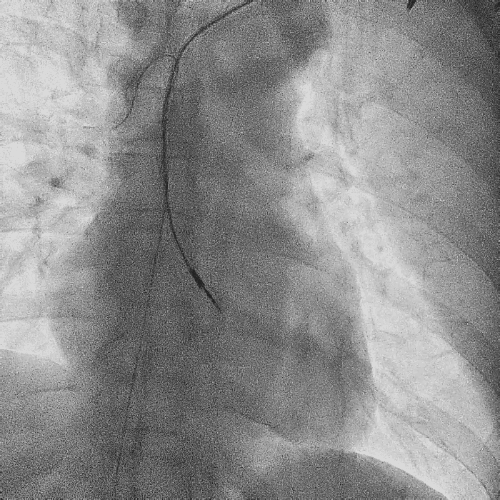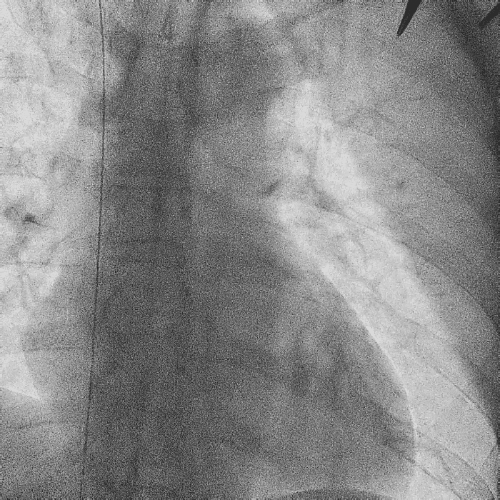
电极拔除过程
在心房和心室电极成功拔除后,患者立刻感觉“眼前一亮”,颜面肿胀感缓解,此时颈静脉怒张相比术前也明显缓解。再次复查上腔静脉造影,狭窄明显减轻,无需再使用上腔静脉扩张球囊进行扩张。

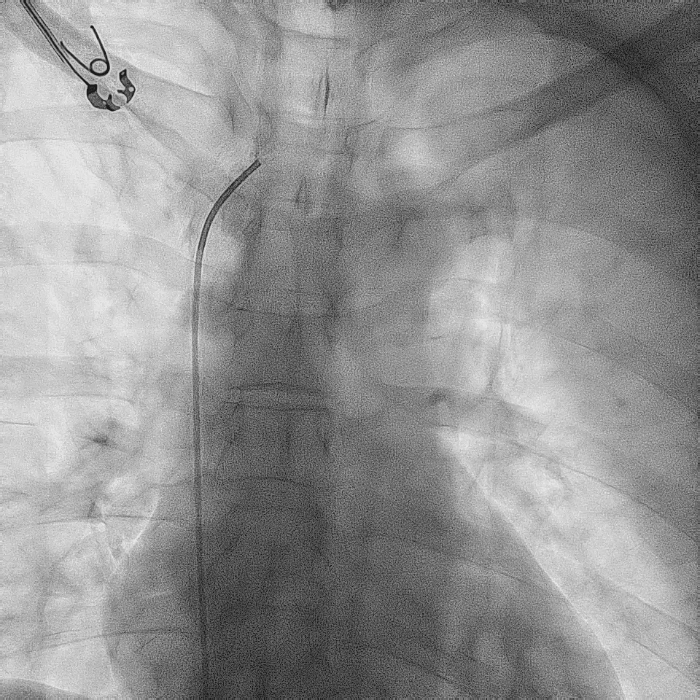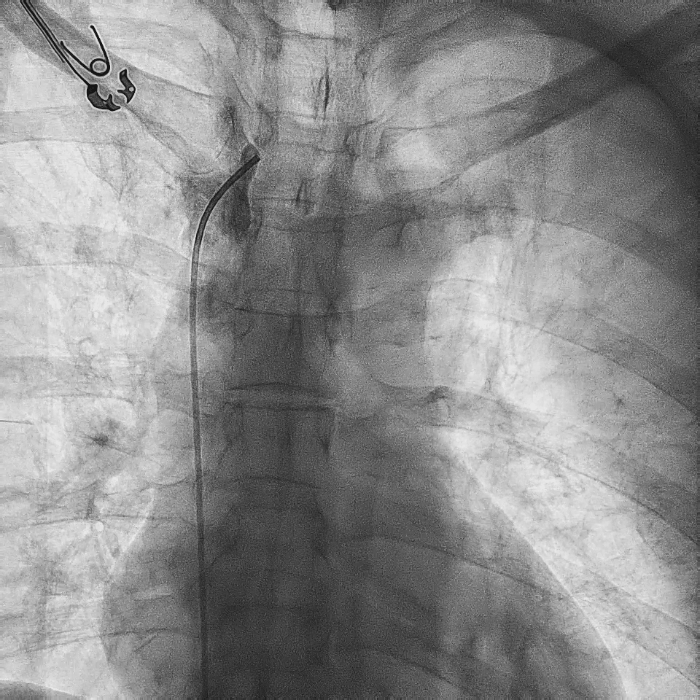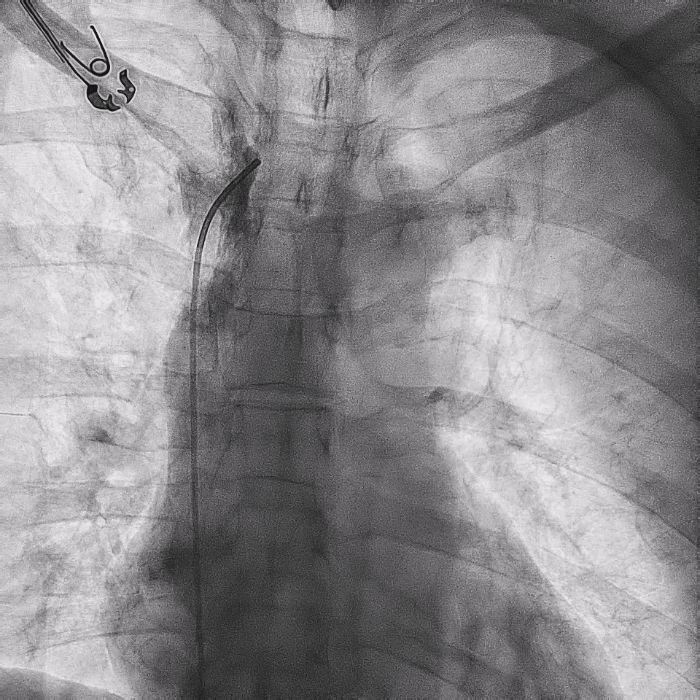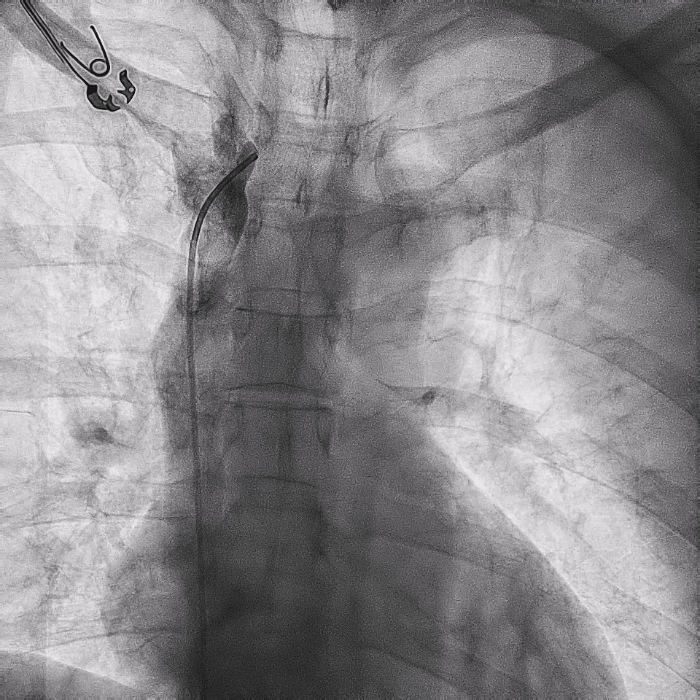
电极拔除后
颈静脉怒张
明显缓解
电极拔除后
上腔静脉狭窄
明显缓解


AVEIR™植入过程操作要点
对于AVEIR™ AR,CEGM的变化以及张力测试后机器的稳定程度更有参考意义。在旋入后右心耳基底部后,由于心肌损伤,可能会出现心房阈值升高,且不同于右室心肌,需要较长时间恢复到低阈值。术中仍可选择稍作等待,若阈值有下降趋势,且CEGM与阻抗在旋入过程中符合要求,可选择释放。该患者为例,等待过程中阈值由3.75/0.4ms下降至3.0/0.4ms。顺利释放后参数与释放前比较稳定,撤台前,阈值已下降至2.75v/0.4ms。
返回病房24小时后测试阈值参数明显下降为阈值:0.75V/0.4ms,阻抗:350Ω,感知:1.4mV,达到理想数值。
PART.03

无线洞察






扫码进入【雅培】全新一代AVEIR™植入式无导线心脏起搏器 学术专栏