
复旦大学附属中山医院心内科黄浙勇教授
思辨介入困境
解析手术技巧
梳理中山经验
助您从新手变“心”手
每月15日、30日,严道医声独家发布
处理极度成角的分叉病变时,2008年Kawasaki等[1]提出的反转导丝技术目前已经成为常规操作。但反转导丝技术操作学习曲线较长,即使是富有经验的术者,也有20%的失败率,失败的原因主要是分叉病变合并其余复杂情形,包括主支血管重度狭窄、钙化、迂曲、小血管等。本文主要探讨情形是:极度成角病变大多合并有分叉近端主支血管的重度狭窄,这可能妨碍“微导管+反转导丝”整个系统的输送。怎么办?
传统的解决方案有:(1)反转导丝塑形时,将反折处预先做成锐角[2],比钝角更容易通过狭窄区域,缺点是反转导丝进入分支后前送会存在一定困难。(2)选择使用小球囊(直径< 1.5 mm)进行预扩张处理。不管采用哪种方法,均存在斑块夹层/移位和脊移位导致分支开口闭塞的风险。
为解决该问题,2020年Hasegawa等[3]人提出了一种简化的反转导丝技术(Streamlined reverse wire technique, SRWT)。不同点为导丝反转不在体外形成,而是借助靶血管对侧或附近的分支,在体内形成导丝反折,笔者称之为体内反转导丝技术。与传统的体外反转技术相比,该技术更容易通过近端狭窄病变,血管损伤和分支闭塞的风险下降,从而提高输送效率。
一
内反转导丝技术的操作流程
(1)第一根导丝(主支导丝)通过分叉病变进入主支远端,双腔微导管沿主支导丝推送越过靶分叉。
(2)第二根导丝(反转导丝)体外预先二处塑形,距离前端2~4cm处反折弯(方便体内反转,根据需要调整导丝长度),前端5mm节段常规塑形(前送时能进入非靶分支,回撤时能反转进入靶分支。)
(3)反转导丝经双腔微导管OTW腔送至靶分叉以远的某一分支(非靶分支),将导丝的反折处和双腔微导管OTW腔出口(侧孔)同时调整到非靶分支的开口处。
(4)固定主支支撑导丝,前送双腔微导管,反转导丝在前送力作用下在体内形成反转,继续前送微导管直至反转导丝脱离非靶分支,其后操作同经典的反转法(图1)。
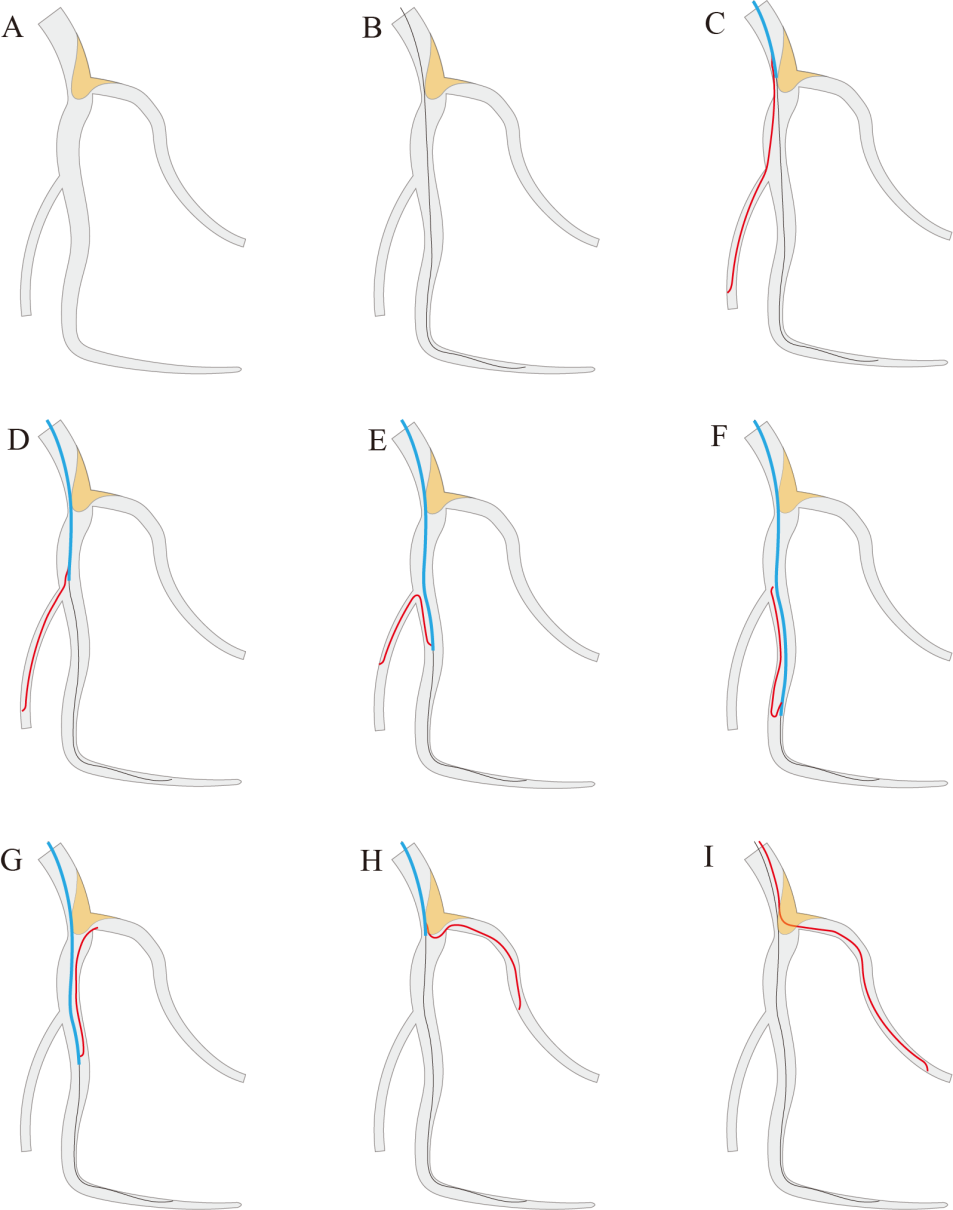
图1 体内反转导丝技术操作示意图[3]:A严重成角病变。B导丝通过分叉病变进入主支远端。C双腔微导管推送越过靶分叉;反转导丝体外预塑形,沿OTW腔送至靶分叉以远的某一分支(非靶分支)。D-F将双腔微导管的中心腔出口(侧孔)送至非靶分支的开口,同时将反转导丝的反折点也调整到非靶分支的开口处。E前送双腔微导管,反转导丝在前送力作用下逐渐反转,直至反转导丝脱离非靶分支。G-I其后操作同经典反转法。
二
内反转导丝技术的评价
优点:(1)无需球囊扩张。双腔微导管单独通过狭窄病变,而不是和反转导丝一起输送,因此很少需要球囊预扩张狭窄部位,血管损伤的风险也随之降低。(2)方便反复尝试。如果反转导丝失败,不管是不能顺利进入非靶分支,还是不能反转进入靶分支,均可自由方便的取出再塑形或换入新的导丝。由于反转导丝技术往往需要多次尝试,自由更换无疑可缩短手术时间。
前提:(1)靶分叉远端需要有分支血管存在,需要有足够长度(>30mm)。(2)靶分叉远端的主支血管需要有足够的空间和长度,可以同时容纳“反转导丝+双腔微导管”。(3)分叉病变近端能通过双腔微导管(无反转导丝)。极少数情况下分叉病变极重,单独的双腔微导管通过都困难,用小球囊(直径< 1.5 mm)预扩张即可。
技术要点:该技术有两次反转。其中,完成第一次反转(成功构建反转导丝)是技术关键。远端非靶分支成角越大,内反转越容易,因此需要选择角度大一些的远端分支。主支血管越大越直,内反转越容易成功,因此可选择靶分叉近端的分支血管。另外,需要更细的超滑导丝(譬如XT系列)、更大的体外预反折弯、更强的大腔支撑和主支导丝支撑(譬如SION blue)。
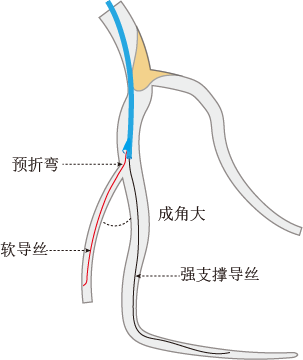
图2 导丝体内反转的技术4要点:分支成角大,分支软导丝,分支软导丝预折弯,主支硬导丝
三
体内反转导丝技术的拓展
体内分叉构建部位一般在靶分叉的远端(图3-4)。但是,有时候靶分叉近端的分支血管也可以使用,譬如前三叉。由于近端血管粗大,更容易反转(图5)。
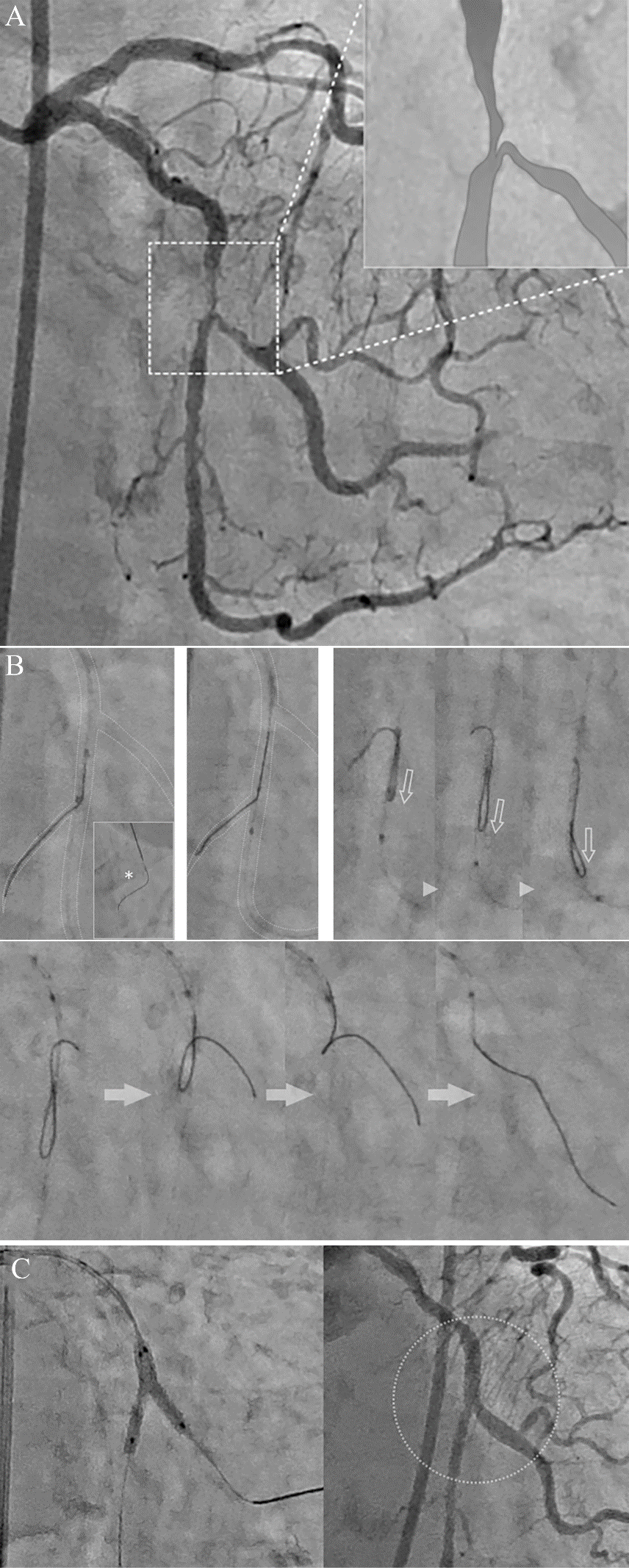
图3 体内反转导丝技术辅助回旋支分叉病变PCI [3]。85岁女性,糖尿病和高脂血症,不稳定性心绞痛。造影示回旋支中段严重狭窄,累及极度成角的钝缘支(A)。右股动脉径路7 F AL1.5 指引导管到位,SION blue回旋支主支,钝缘支导丝难以进入。经典反转导丝技术难以施行,因为“反转导丝+双腔微导管”无法通过回旋支严重狭窄。 尝试进行体内反转导丝技术:双腔微导管(无反转导丝)推送越过靶分叉,沿OTW腔送入预塑形的反转导丝(距离前端25mm处90°反转弯,前端5mm正常塑形),送至靶钝缘支以远的心房支。将导丝的反折处和双腔微导管中心腔出口同时调整到心房支开口处,将“反转导丝+双腔微导管”作为一个整体同时前送,体内形成反转袢,直至反转导丝脱离心房支。其后操作同经典反转法:逐渐回撤“反转导丝+双腔微导管”,并微调反转导丝方向进入靶钝缘支。最终回旋支-钝缘支置入2.75×20mm支架并最终球囊对吻。
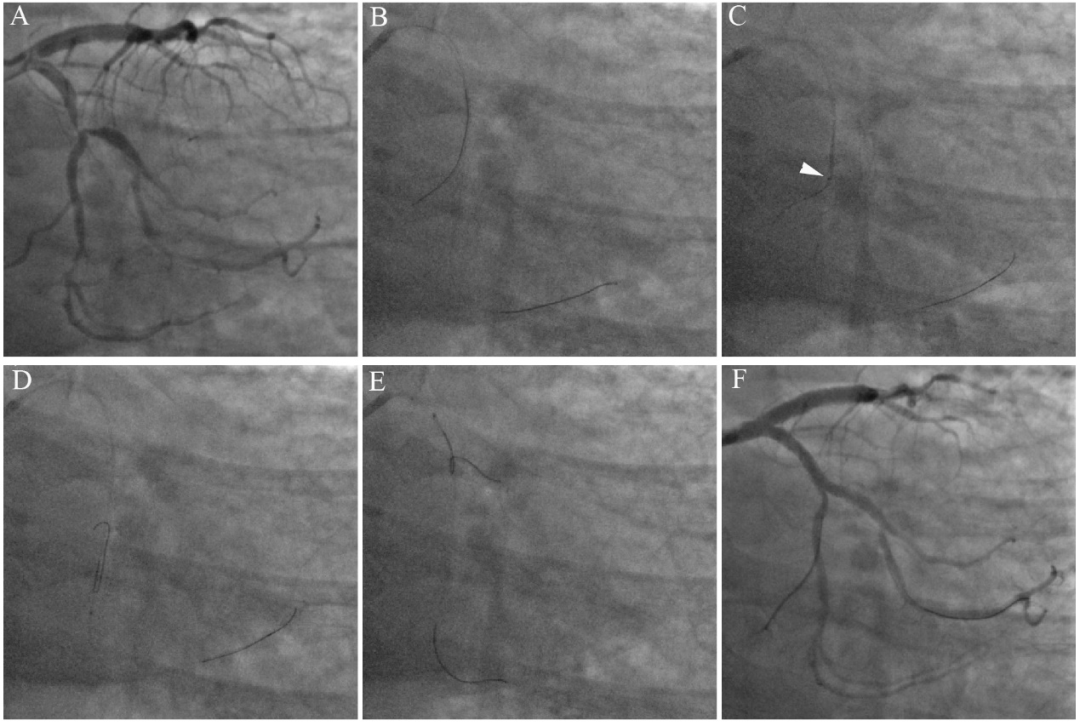
图4 体内反转导丝技术辅助回旋支分叉病变PCI。62岁男性,劳力性心绞痛。右桡动脉径路造影示回旋支中段严重狭窄,累及极度成角的钝缘支开口(A)。6 F EBU3.5指引导管到位,Runthrough导丝进入回旋支主支,Sion导丝反复尝试难以进入钝缘支,包括双腔微导管辅助下正向导丝操控技术均未能成功。最后采用体内反转导丝技术:经双腔微导管的OTW腔送入反转导丝(SION black,未塑反折弯,前端4mm正常塑形),送入靶分叉钝缘支以远的心房支约25mm(B)。将双腔微导管中心腔出口送至心房支开口处(C),将“反转导丝+双腔微导管”作为一个整体同时前送,SION black体内形成反转袢(D),直至反转导丝脱离心房支。其后操作同经典反转法:逐渐回撤“反转导丝+双腔微导管”,并微调反转导丝方向进入靶钝缘支(E)。最终回旋支-钝缘支置入支架并最终球囊对吻,结果良好(F)。
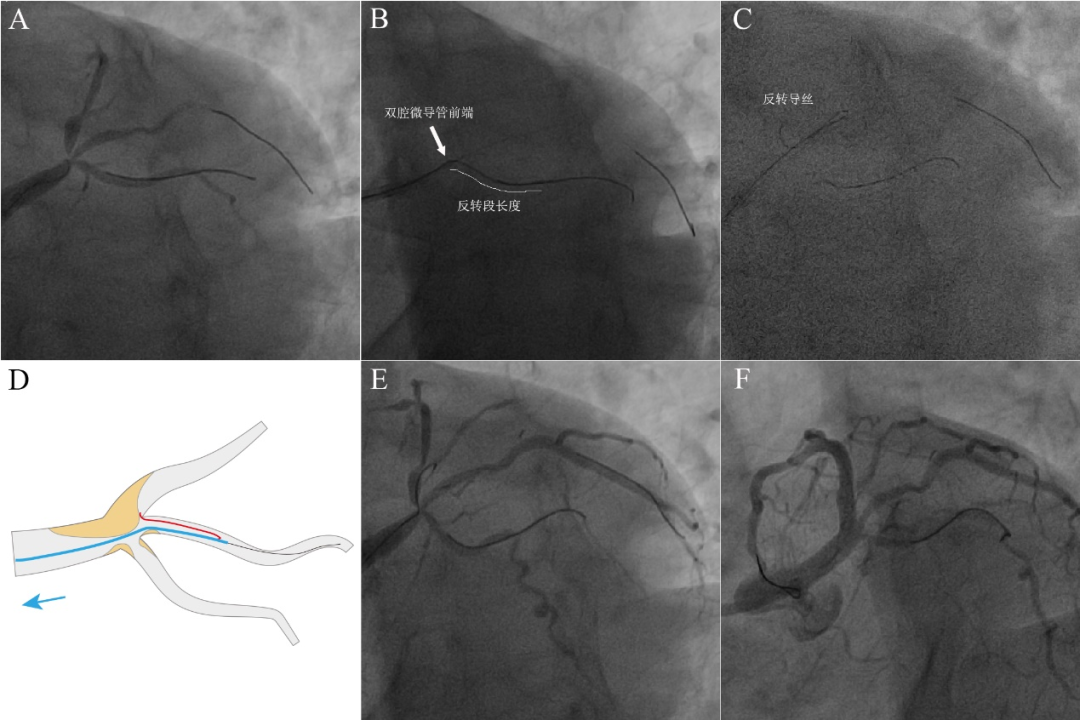
图5 体内反转导丝技术辅助左主干四分叉病变PCI。56岁吸烟男性,反复活动后胸闷1月。冠脉造影示前四叉病变,前降支开口狭窄95%。7F EBU 3.5指引导管到位,Fielder XTR导丝反复尝试无法进入前降支开口。沿中间支Sion导丝送入Crusade双腔微导管,沿双腔微导管OTW腔送入Fielder XTR,反复尝试也未能送入前降支开口(A)。仔细观察前降支开口疑似极度成角,尝试体内反转导丝技术。直接将双腔微导管OTW腔的XTR导丝(反转导丝)送入回旋支约30mm,然后将双腔微导管中心腔出口送至中间支开口处(B),将“反转导丝+双腔微导管”作为一个整体同时前送,XTR导丝体内形成反转袢,直至反转导丝脱离回旋支。其后操作同经典反转法:逐渐回撤“反转导丝+双腔微导管”(C-D),并微调反转导丝方向进入前降支(E)。最终前降支-左主干植入支架,结果良好(F)。
四
反转导丝技术失败的其他原因
2025年Murasato等[4]分析了单中心病例,发现反转导丝技术的成功率为80%,失败的原因主要是分叉病变合并其余复杂情形,包括钙化、迂曲、小血管等。对于此类病变,可尝试球囊阻挡技术(balloon blocking technique,BBT)。
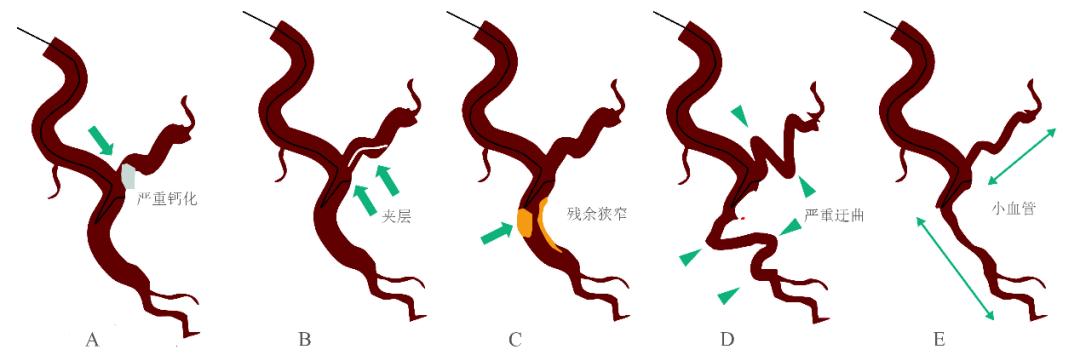
图6 导丝反转技术失败的常见原因
“中山PCI解码”下期预告
球囊拘禁技术改进版:长程球囊保护技术解码
通过分析可以发现,传统的球囊保护技术,在支架置入阶段可有效保护分支通畅,但在支架后扩张阶段,分支并无球囊保护,可通过斑块移位、脊移位、斑块夹层水肿、导丝重置意外等机制导致分支开口闭塞(图1A)。因此传统球囊保护的残余闭塞风险源自无保护的后扩张,可谓“善始不善终”(图2)。尽管导丝重置(rewire)可部分开通闭塞分支,但导丝掏分支是个技术活,不少病例出现分支开口夹层血肿、次全闭塞进展为完全闭塞等尴尬局面。怎么办?


