

肺栓塞(pulmonary embolism,PE)是指外来栓塞物堵塞肺动脉及其分支,引起肺循环障碍的临床和病理生理综合征。其中最主要、最常见的种类为肺动脉血栓栓塞,还包括其它非血栓性栓子栓塞,如脂肪栓塞、羊水栓塞、空气栓塞和肿瘤栓塞等。本节主要讨论血栓性PE。
一、病理与病理生理
(一)病理与病理分型
PE绝大多数系血栓栓塞,其中90%继发于下肢、盆腔等深静脉的血栓形成,其高危因素主要来自创伤、下肢手术和常年卧床者。历时较久的高空旅行者亦是深静脉血栓的高危人群。另外,深静脉血栓的风险还可来自某些先天性因素,如遗传性抗凝血酶-Ⅲ缺乏、凝血酶原基因G20210A变异及先天性纤溶异常等。
据文献报道,单发性PE占34%,多发性占66%,其中53%累及双侧。右下肺动脉受累最多(48%),其次为左下肺动脉(29%),左、右上肺动脉受累相对较少。
肺梗死是PE最常见、最危急的并发症,多发生在肺周围组织。梗死多为单发,也可为多发。急性梗死呈暗红色、实性,肺膜有纤维素渗出,局部肿胀。切面梗死区呈尖端指向肺门的楔形,肉眼或镜下可见血栓阻塞的肺小动脉,肺动脉壁均扩张、变薄(图10-1-1)。
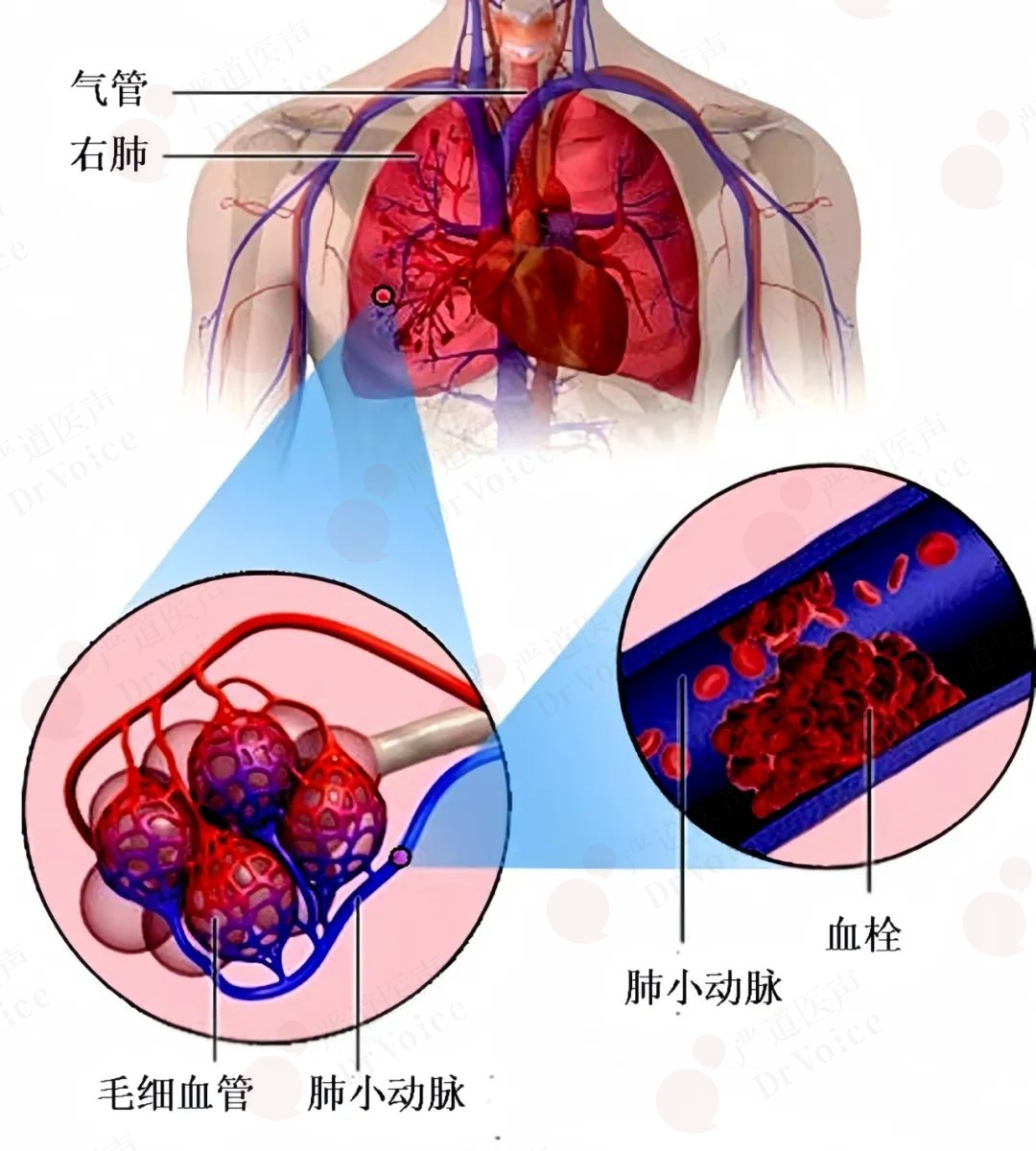
图10-1-1PE模式图
由于肺动脉血流灌注减少,相应部位的毛细血管血流亦减少,出现通气-血流比例失调。
根据栓塞发病时间和阻塞程度,PE分为以下四型:
1. 急性大面积栓塞:急性发生,栓子阻塞肺动脉的面积超过50%。
2. 急性小面积栓塞:急性发生,栓子阻塞肺动脉的面积小于50%。
3. 亚急性大面积栓塞:反复发生的小面积或中等面积栓塞,时间超过数周,栓子阻塞肺动脉的总面积超过50%。
4. 慢性栓塞:病史长达数月以上,病情逐渐加重,出现慢性肺动脉高压,多系反复小面积栓塞逐渐阻塞中等肺动脉,或大面积PE患者存活而仍遗留中等以上PE者。
(二)病理生理
病理生理变化取决于PE的发病速度、程度、范围、持续时间和原有心肺功能状态。
1. 急性大面积栓塞
栓塞使肺动脉压力急剧升高、肺血流量减少;同时神经-体液反射及局部释放的血管活性物质使肺动脉发生痉挛,加重阻塞程度。右心室的继发性扩张导致室间隔左移,加上周围血管扩张,可严重影响左心室充盈,使其舒张末容量减小,心排血量和动脉压明显下降,影响重要脏器血液供应,可导致患者迅速死亡。栓塞部位的肺组织丧失气体交换功能,无效腔增加,通气血流比例失调;而其他部位的肺血管扩张,侧枝血管开放,加之心排血量降低和支气管痉挛等因素,可以导致严重低氧血症(图10-1-2)。
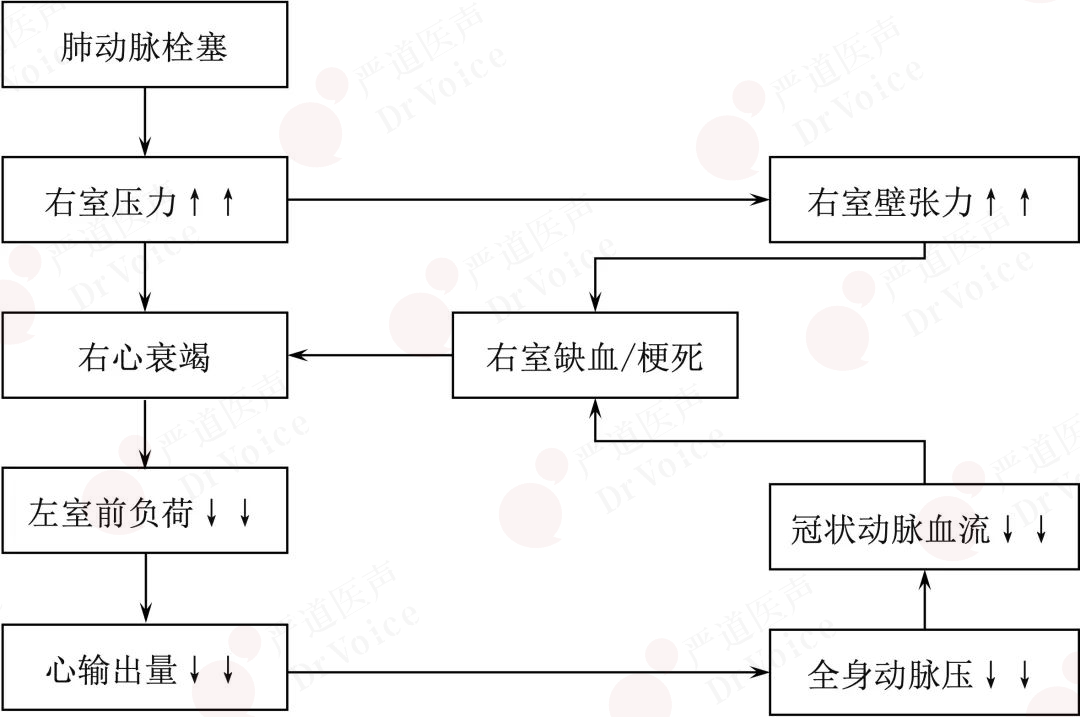
图10-1-2 急性大面积PE的病理生理变化
2. 急性小面积栓塞
静息状态下,多数无明显的血流动力学变化,但在活动时,将会出现类似急性大面积栓塞的变化。
3. 亚急性大面积栓塞
栓子逐渐阻塞中小肺动脉,右心室和肺动脉压力升高后可逐渐形成右心室肥厚,其血流动力学改变介于急、慢性栓塞之间,心排血量一般正常,多数有低氧血症,尤以运动时加重。
4. 慢性栓塞
反复小面积栓塞或大面积栓塞后遗留明显肺动脉阻塞,通常出现慢性肺动脉高压、右心室肥厚和右心室衰竭,形成慢性肺源性心脏病。
二、超声心动图检查
临床可疑PE者,其确诊有赖于心电图、实验室及影像学等检查。其中超声心动图安全、非侵入性、可移动至床旁进行,并且能够直接获得其它可能病变的证据,是最主要的影像学筛查手段之一。由于PE的临床表现缺乏特异性,可酷似急性心肌梗死和主动脉夹层,因此在进行超声检查时,应特别予以鉴别。
(一)M型超声心动图
M型超声可用于检出栓塞后的各种间接征象。如主动脉波群可显示右心室流出道增宽;心室波群可以显示右心室增大,室间隔收缩期运动幅度减低、收缩期增厚率减小或与左室后壁呈同向运动(图 10-1-3)。
正常人下腔静脉(inferior vena cava,IVC)内径随呼吸变化,PE患者因右心系统压力升高,这种规律变化减弱或消失。通过M型超声心动图测量三尖瓣环收缩期位移(tricuspid annular plane systolic excursion,TAPSE)还可以评估右心室收缩功能,PE患者TAPSE<16 cm/s(图10-1-4)。
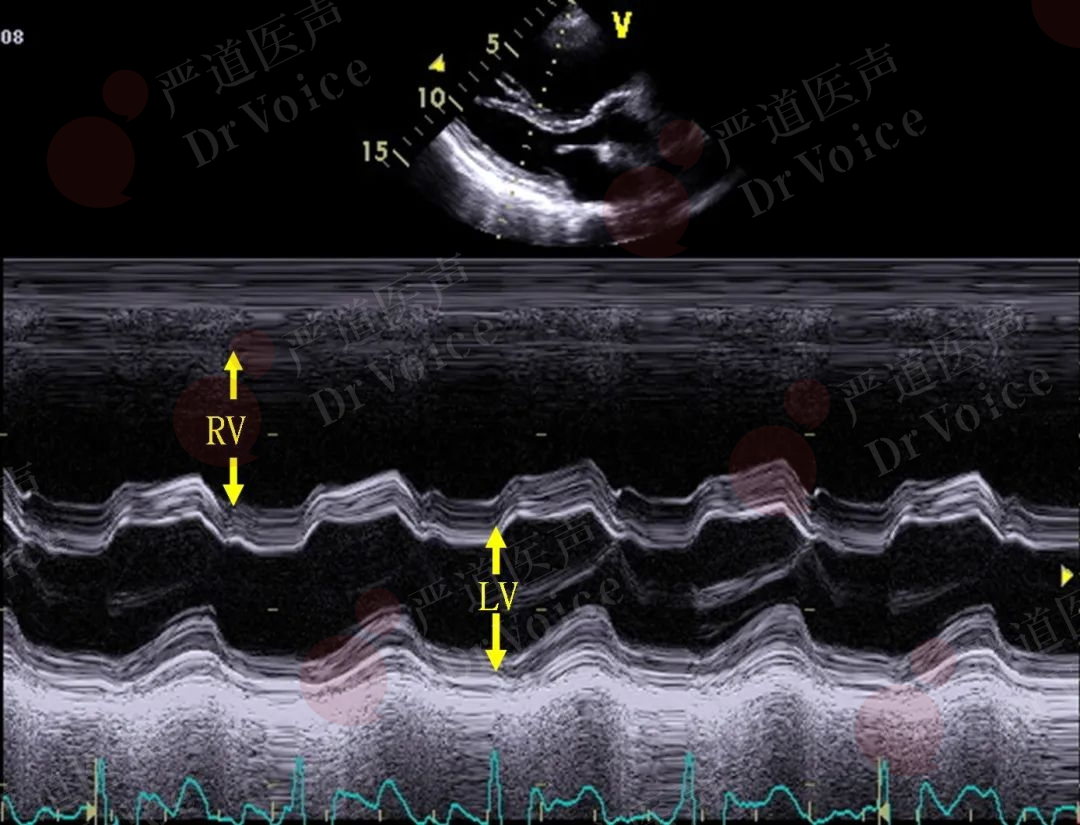
图10-1-3 心室波群示右心室(RV)增大,室间隔与左心室(LV)后壁呈同向运动
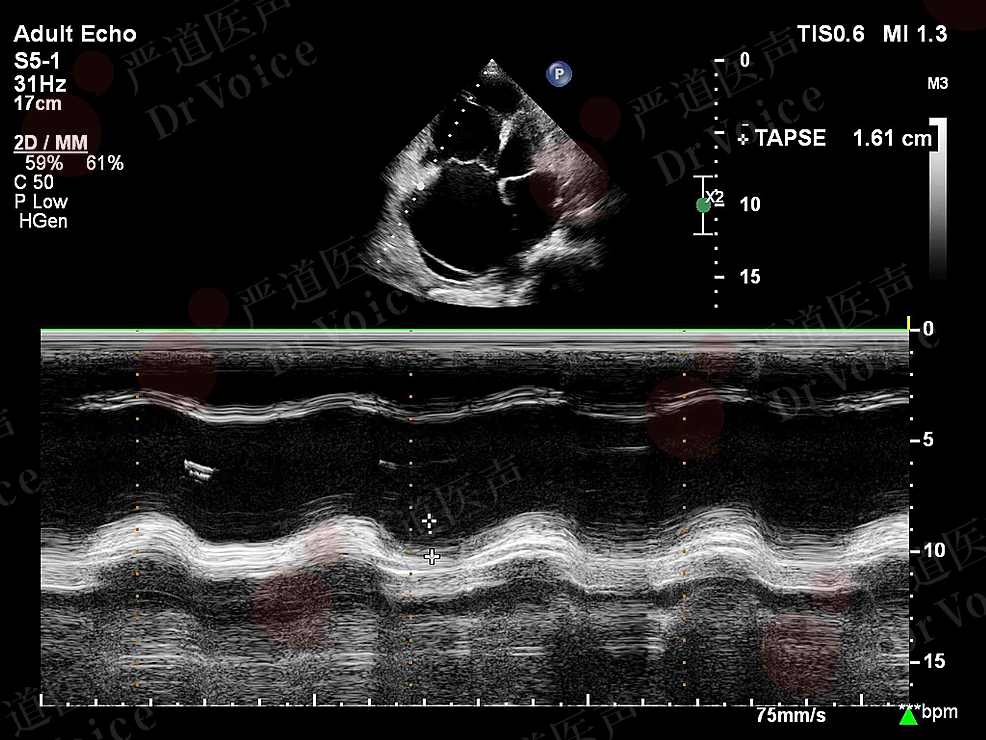
图10-1-4 PE患者TAPSE测值降低
(二)二维超声心动图
PE的直接征象是二维超声检出血栓声像。取胸骨旁或剑突下大动脉短轴切面探查主肺动脉血栓(图10-1-5、图10-1-6)。旋转探头可观察主肺动脉远端及分支内有无血栓回声。新鲜血栓回声低、活动度较高;陈旧性血栓形态多不规则,回声较强,活动度差,临床上多有慢性肺动脉高压的症状和体征。
当考虑PE时,应特别注意探查右心房及下腔静脉,部分患者可能发现血栓残留,该部位血栓容易再次脱落造成新的PE(图10-1-7、图10-1-8)。
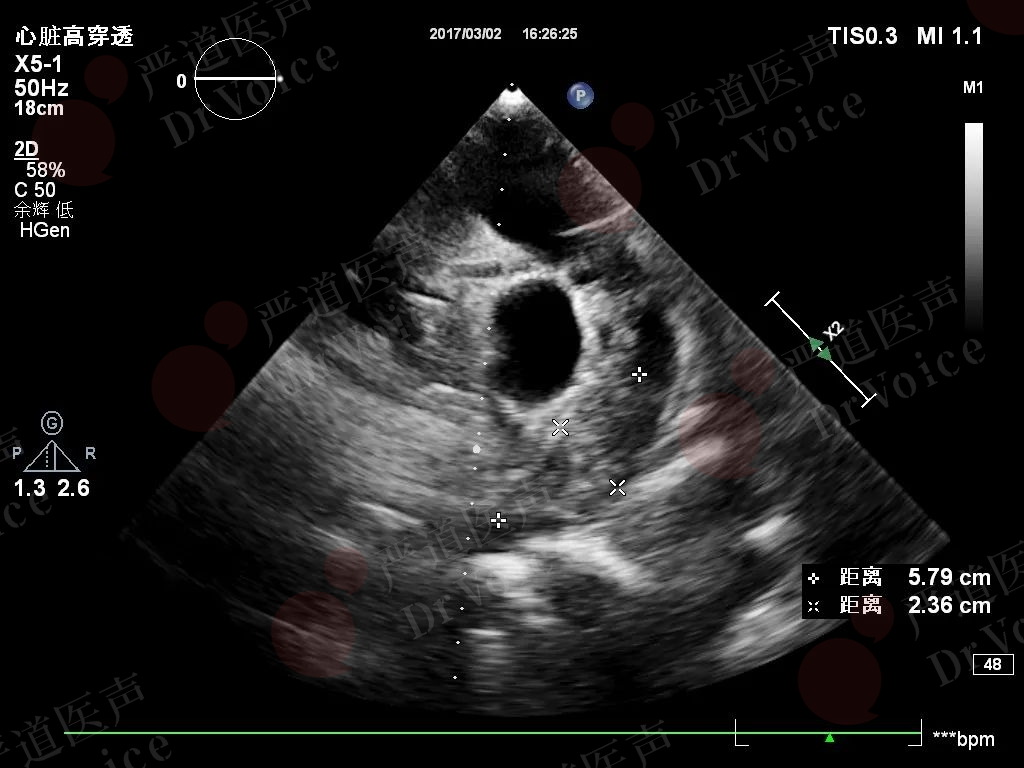
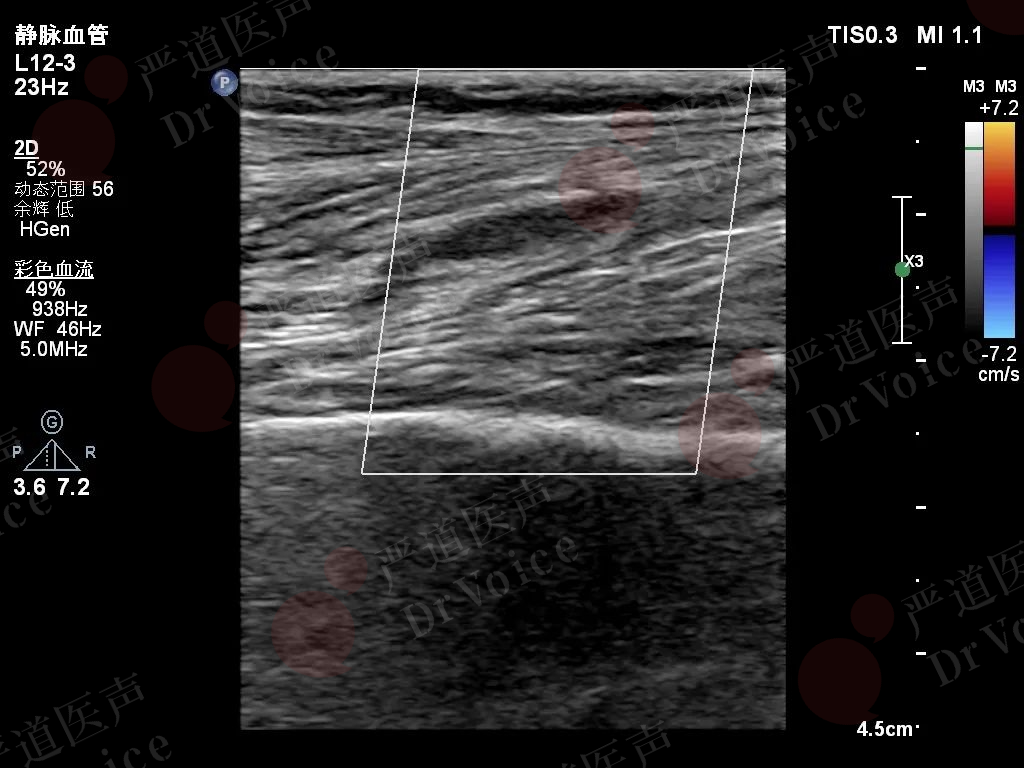
图10-1-5 PE二维超声表现:右肺动脉起始处血栓(图A),下肢深静脉血栓(图B)。
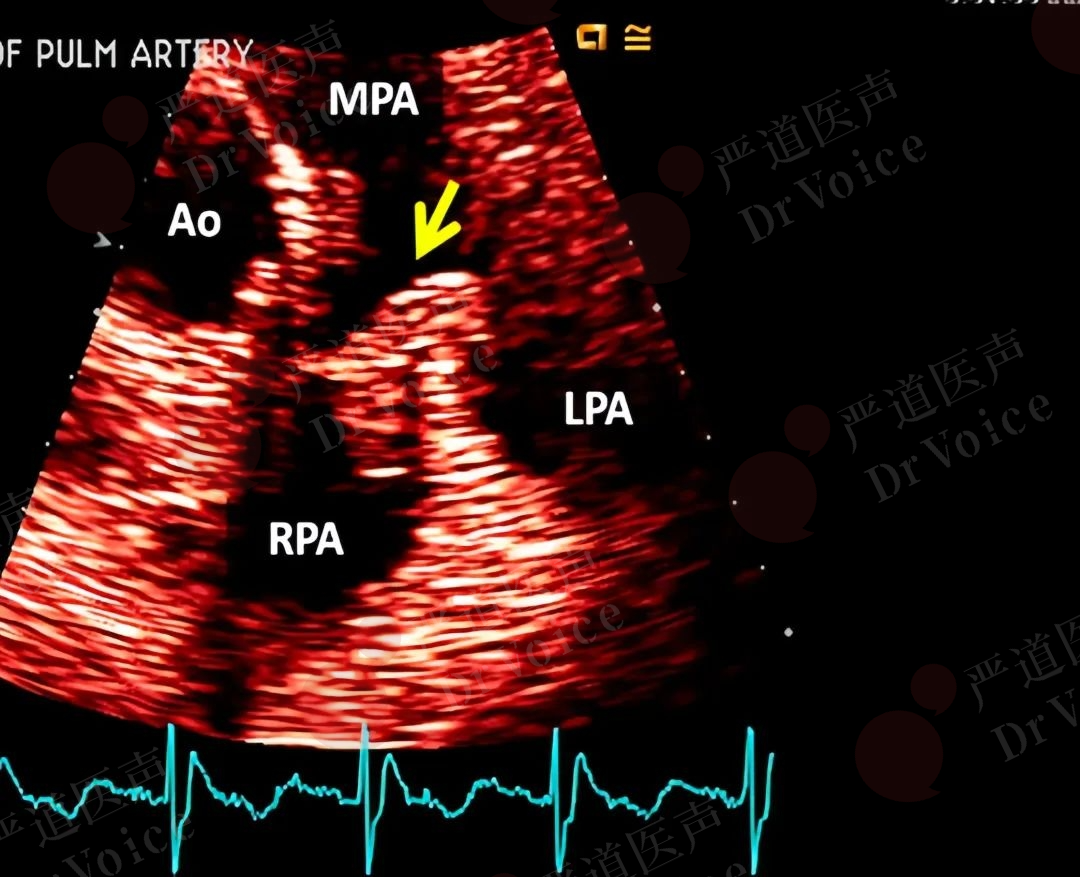
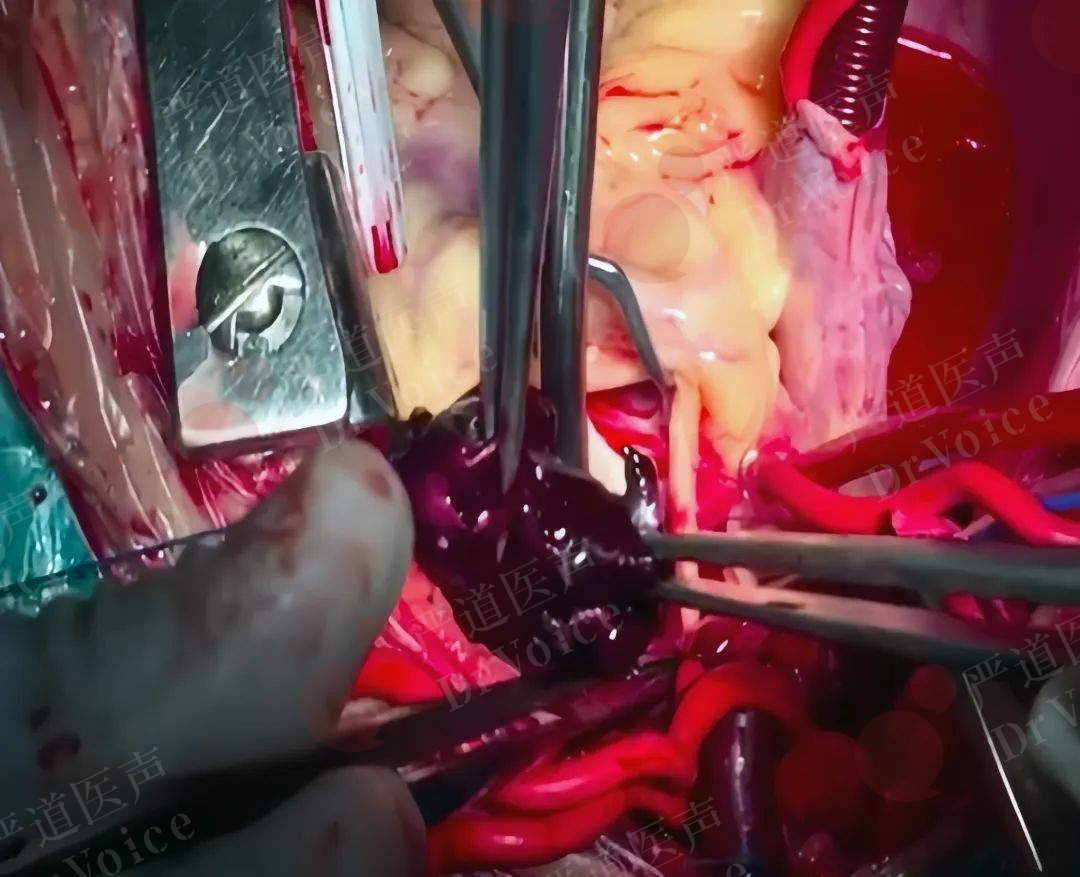
图10-1-6 PE溶栓失败(图A,箭头),外科取栓提示机化血栓(图B)
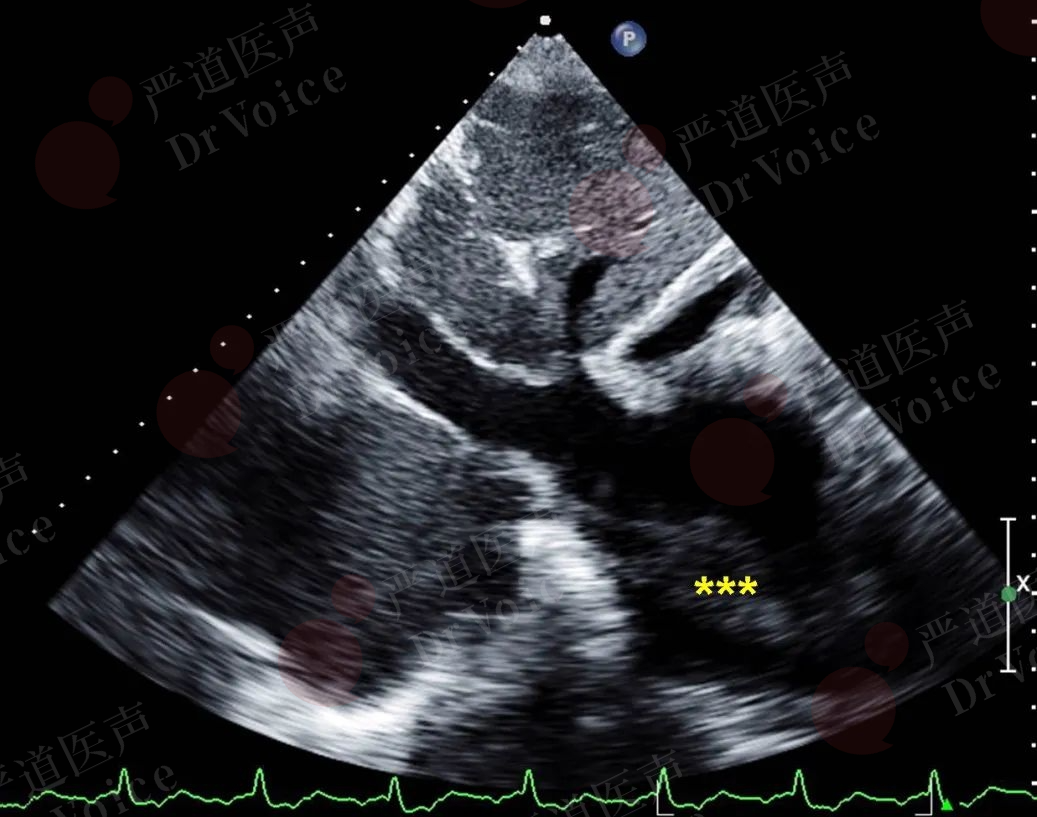
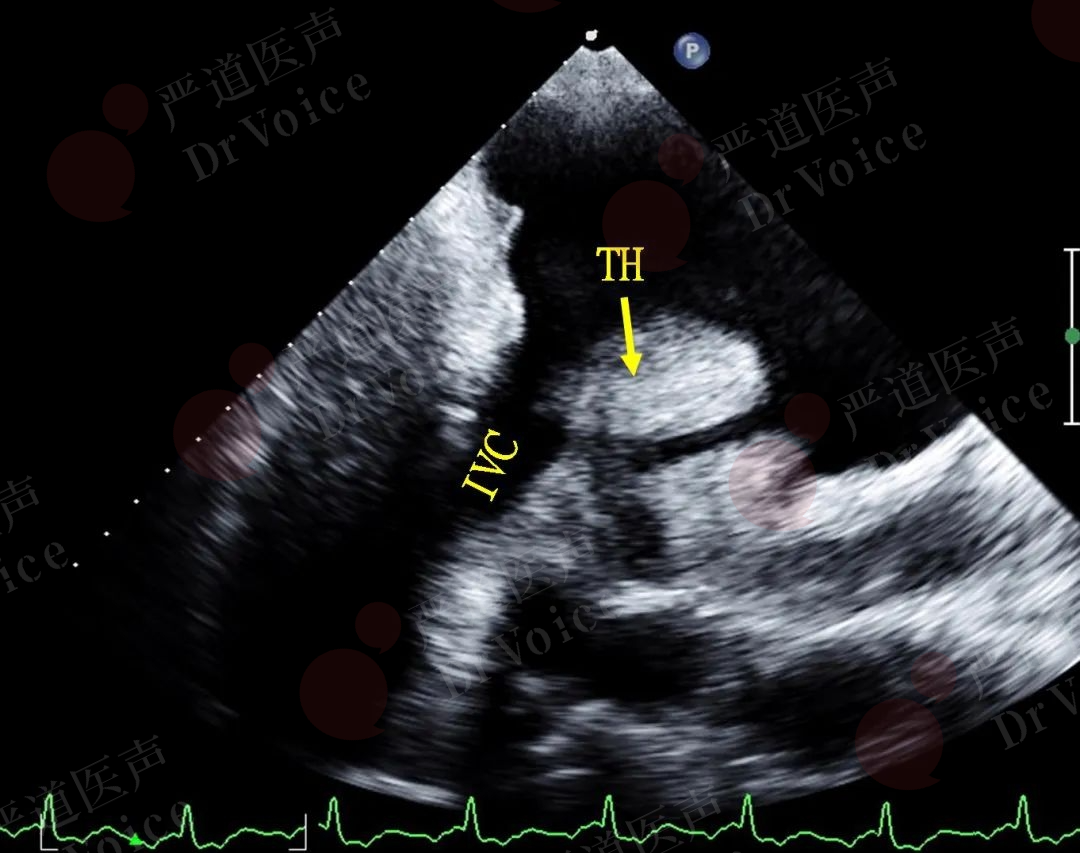
图10-1-7 右心房内血栓:二维超声示右心房内血栓(图A,星号);右心房内血栓(TH)紧邻下腔静脉口(IVC)。
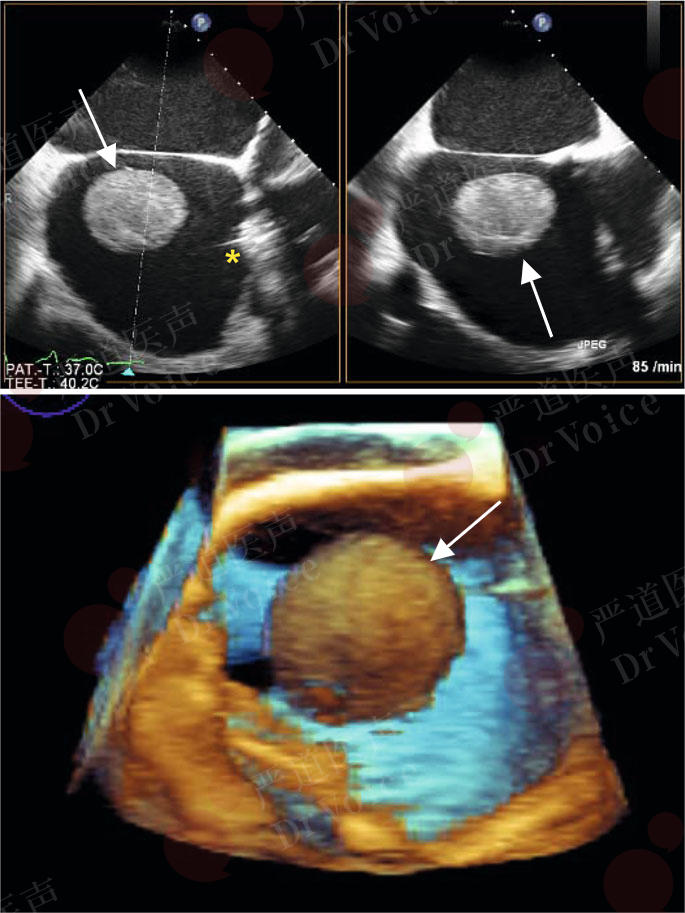
图10-1-8 PE患者右心房内活动性球形血栓(箭头)
PE可造成右心压力负荷过重,导致右心变形、重构。其间接征象可作为PE诊断的有力佐证,从而提示进一步行其它影像学及实验室检查,尤其是下肢深静脉超声检查,排除有无深静脉血栓存在;PE主要间接超声征象见表10-1-1。
表10-1-1 PE主要间接超声表现
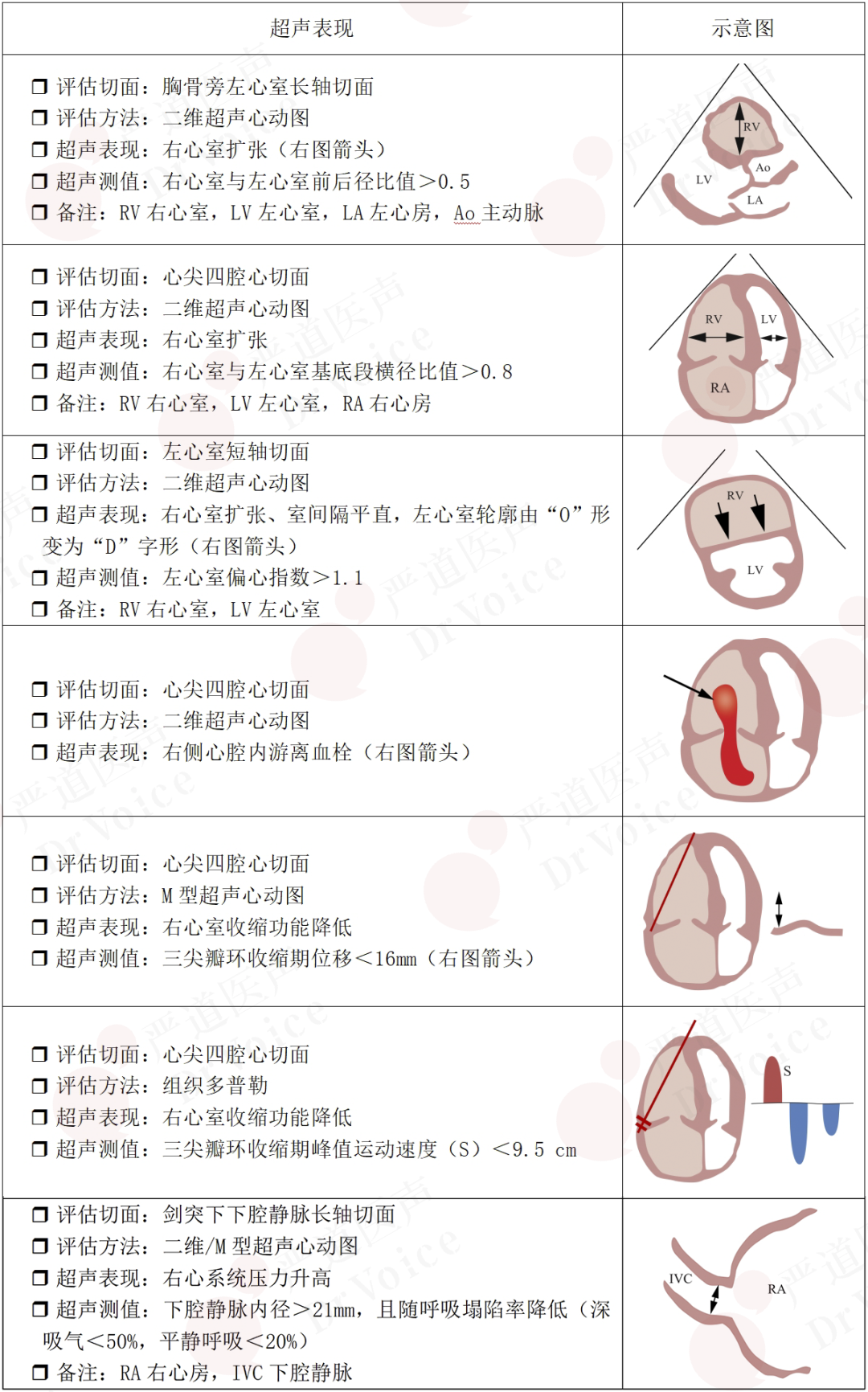
1. 右心房/室扩大
收缩末期右心房面积>18cm²;胸骨旁左心室长轴切面右心室与左心室前后径比值>0.5;心尖四腔心切面,右心室与左心室横径比值>0.8;左心室短轴切面左心室轮廓由“O”形变为“D”字形,左心室偏心指数>1.1(图10-1-9)。
由于右心系统压力升高,患者可能出现卵圆孔重新开放。早期发现的右心室功能障碍或扩大,有助于区分低、中风险人群;该表现与急性PE患者死亡率增加显著相关,但并不足以证明需要常规升级治疗。右心室对压力、容量负荷过重的反应性不同,短轴切面中观察室间隔运动形态,有助于确定病因。
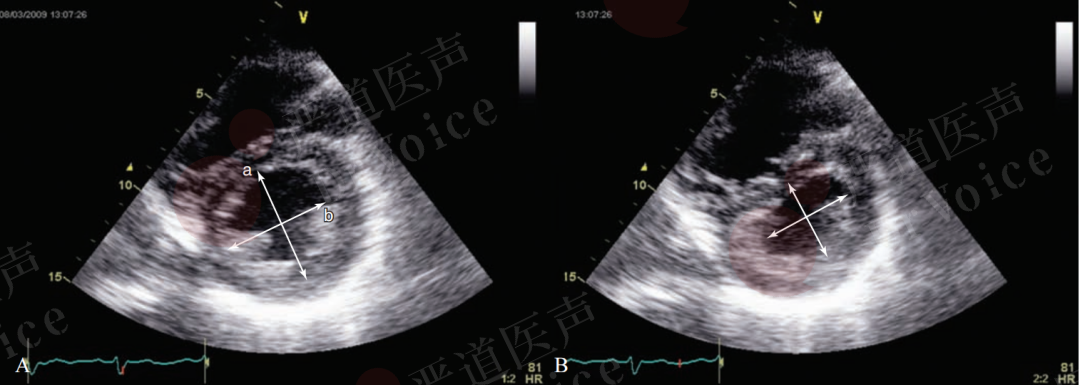
图10-1-9 正常人及PE患者心室形态学变化:图A为正常人左心室短轴切面,收缩期左心室长短径比值(b/a)≈1;图B为PE患者,右心室扩大后,左心室受压,左心室长短径比值(b/a)>1.1。
2. 右室壁运动搏幅明显减低
由于右心室负荷急剧增加和心肌氧耗加重,可以出现右室游离壁运动幅度普遍降低,通常搏幅<2 mm。大面积的PE,右室壁运动甚至可以完全消失,而心尖段运动正常或增强;上述超声表现被称为McConnell’s征(图10-1-10、图10-1-11)。
McConnell’s征产生机制并不是很明确,推测可能包括:①心肌供血差异:右心室游离壁主要由右冠状动脉供血,PE时右心室压力骤升,心肌氧耗增加,而冠状动脉灌注压下降,导致游离壁缺血;右心室心尖部主要由左冠状动脉前降支远端分支供血,受右心室压力升高的影响较小,因此收缩功能得以保留。②心肌收缩特性:右心室游离壁较薄,对急性压力负荷的代偿能力差,而心尖部肌纤维排列和收缩方向可能更有利于代偿性收缩。
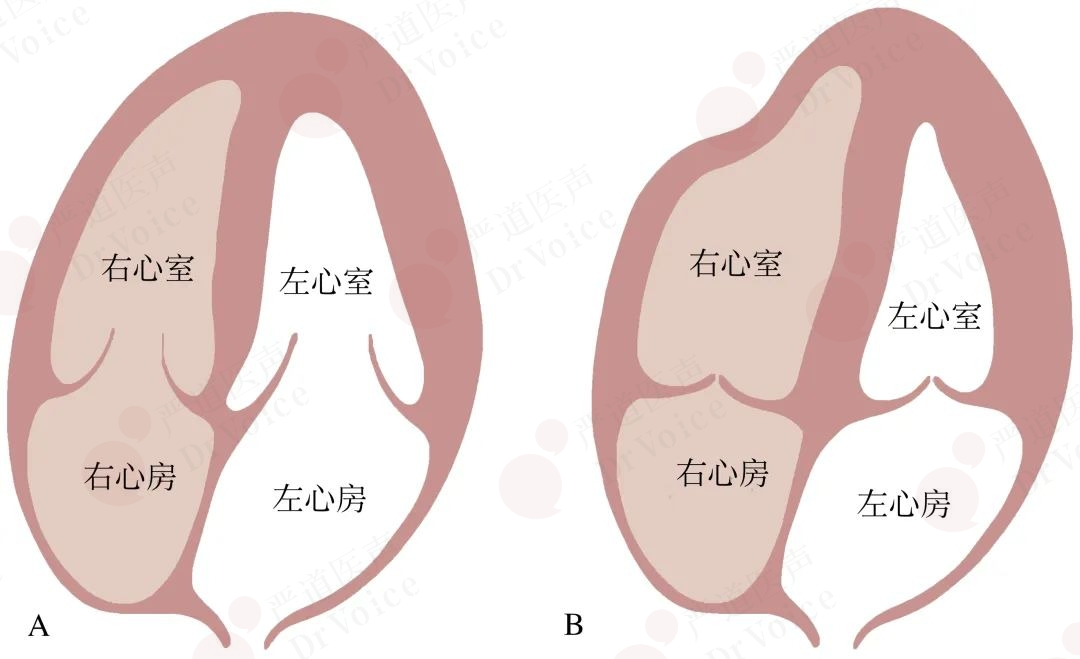
图10-1-10 McConell’s征:舒张期右心室整体扩张(图A);收缩期由于缺血及负荷过重,右心室侧壁运动消失,而心尖处则呈现过度收缩(图B)。
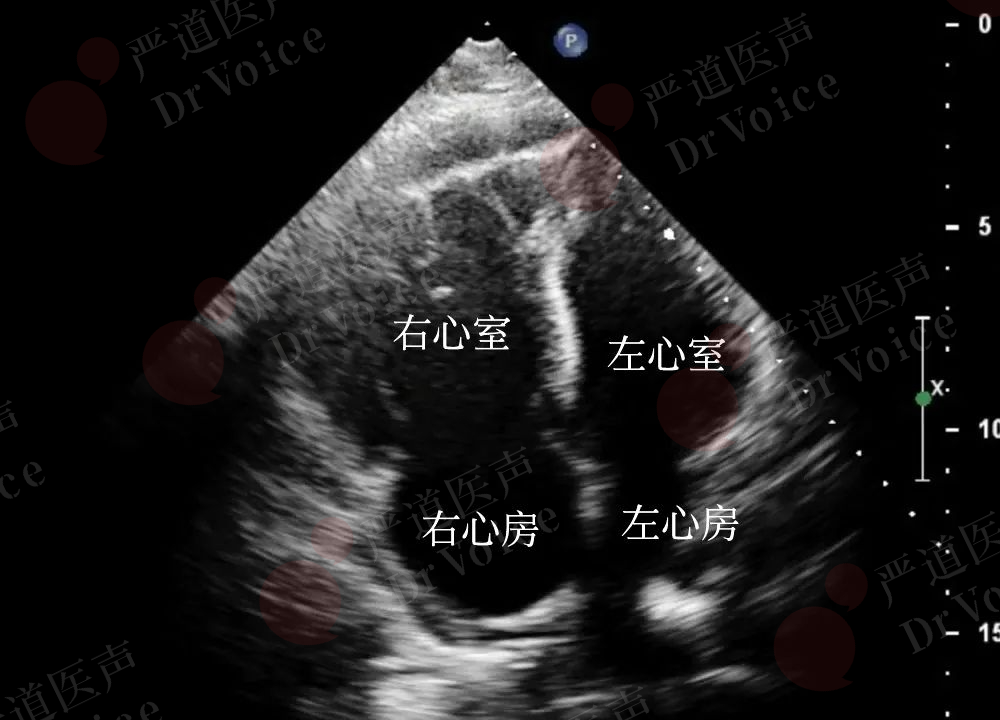
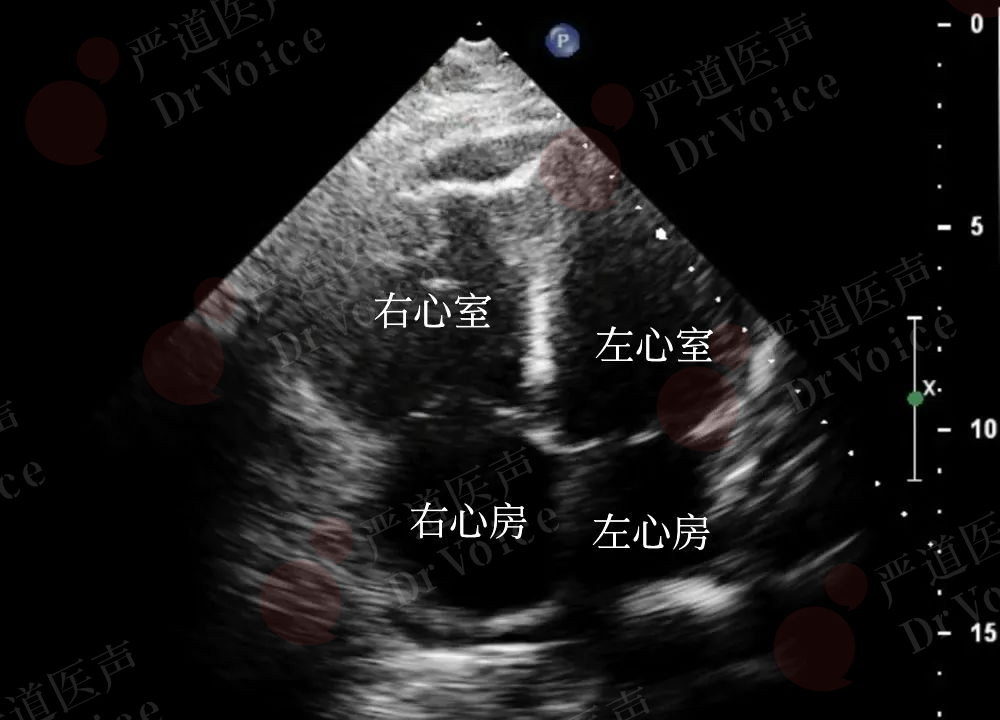
图10-1-11 McConell’s征超声表现:舒张期右心室扩张(图A),收缩期右心室游离壁运动减弱,心尖运动保留(图B)。
3. 室间隔形态、运动异常
急性PE为右心室压力负荷过重,室间隔在舒张末期和收缩末期呈平直状或弯向左心室侧。而右心室容量负荷过重的患者,舒张期室间隔移向左侧,收缩期则朝右移动(图10-1-12、图10-1-13)。
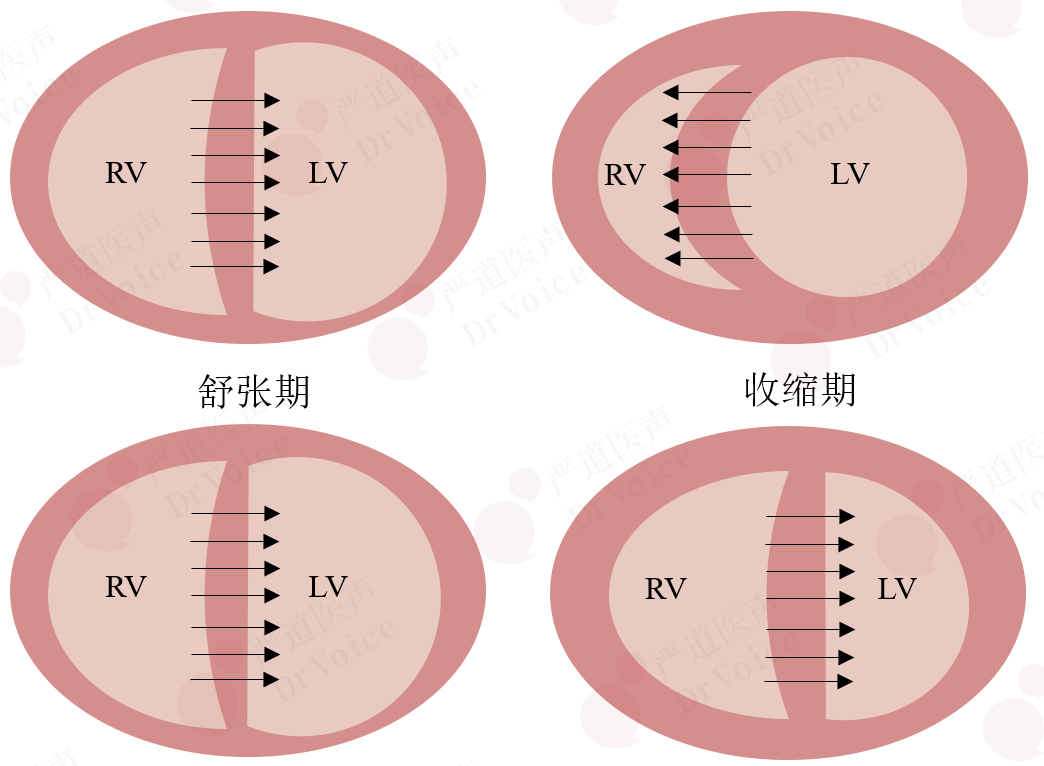
图10-1-12 容量(上图)及压力负荷(下图)过重时室间隔形态特点:容量负荷过重的患者,舒张期室间隔平直,左心室(左心室)被推挤成马蹄形/D字形,收缩期室间隔会再次凸向右心室(RV)侧,而压力负荷过重的患者,室间隔始终凸向左侧
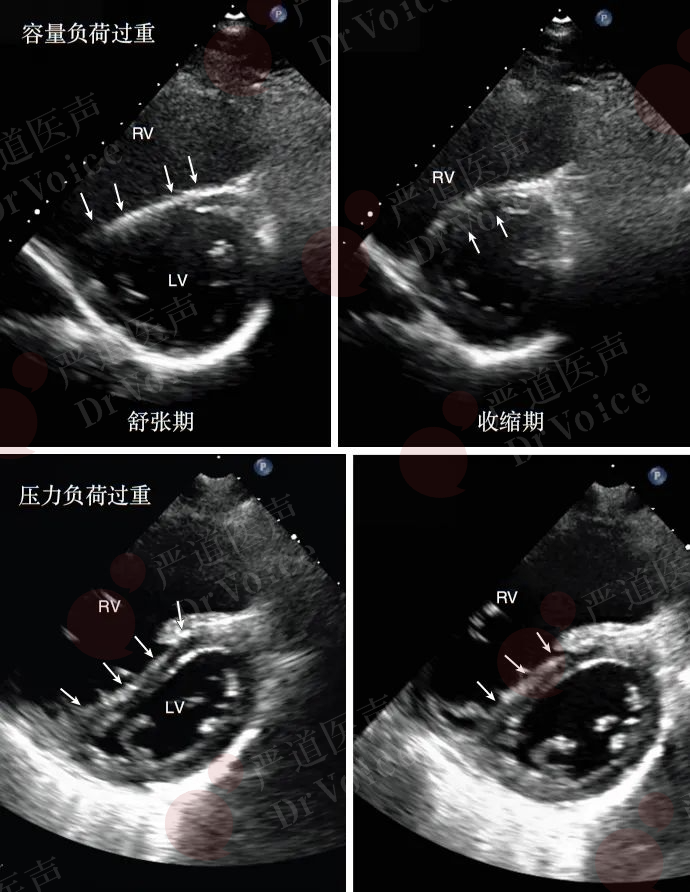
图10-1-13 不同负荷类型对室间隔运动的影响
4. 肺动脉内径
在急性PE时肺动脉主干多数扩张不明显,在亚急性或慢性患者,肺动脉主干内径可出现扩张(肺动脉内径>25mm)。
5. IVC变化率
右心房压力升高时,IVC吸气性塌陷减弱,表现为深吸气-呼气时IVC内径变化率降低,这种异常改变在亚急性和慢性PE患者更为明显。在使用多普勒超声估测肺动脉压力时常需要了解患者右心房压力变化,此时可借助IVC内径变化率进行间接评估(图10-1-14~图10-1-16,表10-1-2)。
表10-1-2 右房压评估的超声参考指标
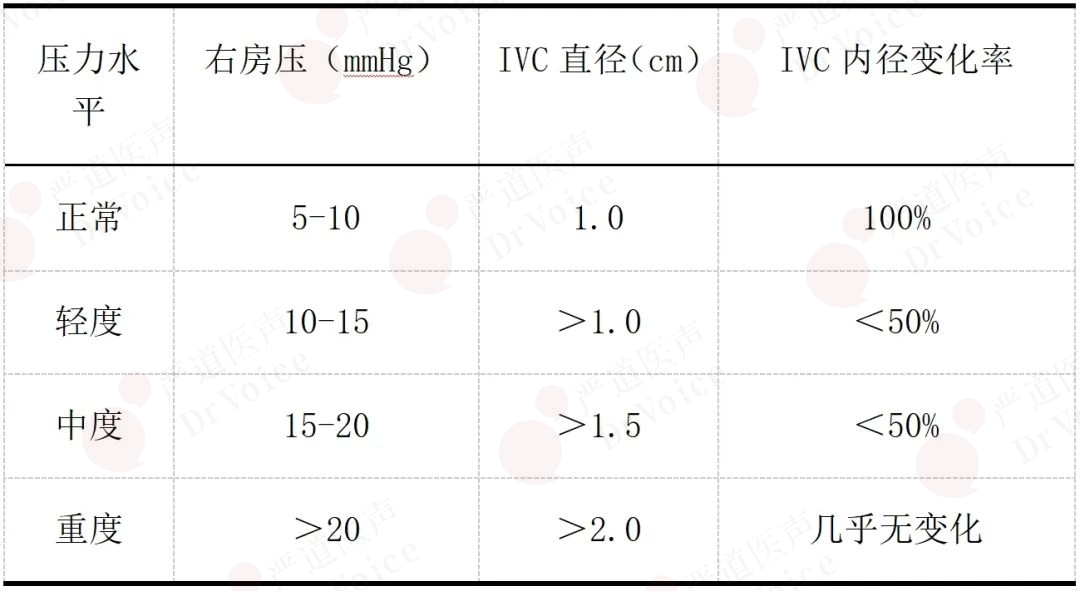
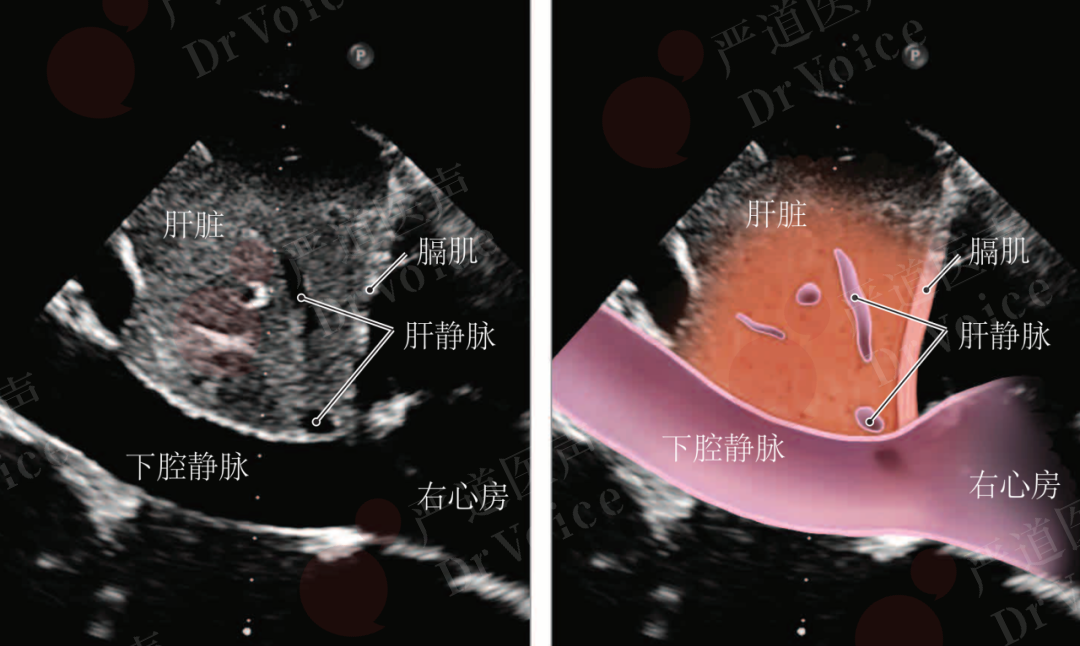

图10-1-14 下腔静脉内径(图A)及其随呼吸塌陷率测量(图B)有助于估测右心房压
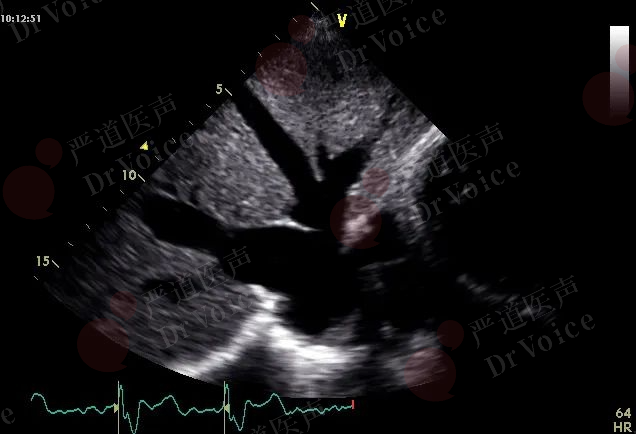
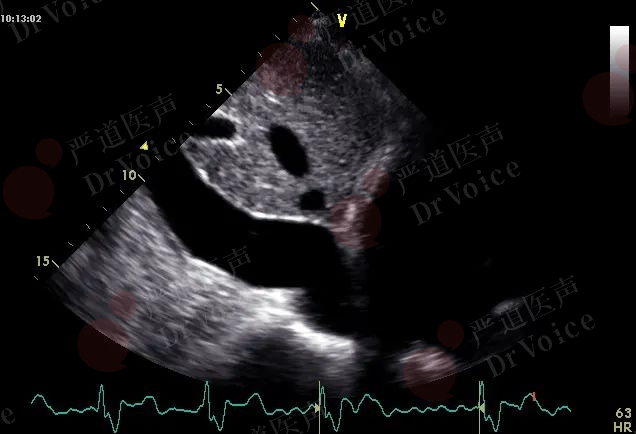
图10-1-15 剑突下切面示肝静脉(图A)及下腔静脉(图B)明显增粗,通过测量下腔静脉内径及其随呼吸变化率可间接评估右心房压力。
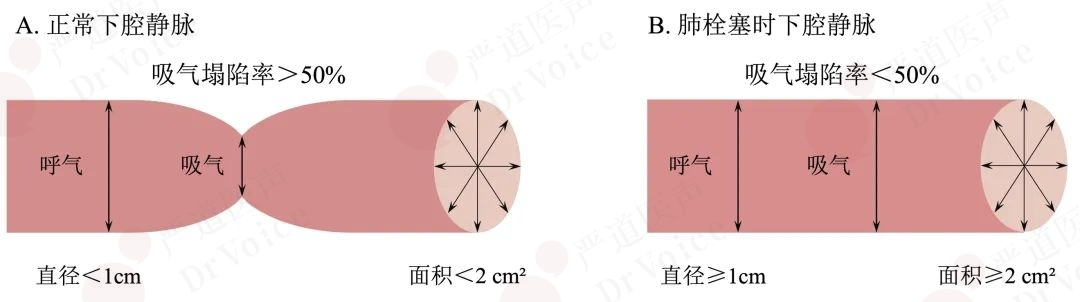
图 10-1-16 PE患者由于右心系统压力升高,致下腔静脉扩张且随呼吸塌陷率较正常人明显减低。
(三)多普勒超声心动图
彩色多普勒有助于鉴别伪像和血栓,如为血栓栓塞,当血流通过时流速加快,血流色彩亮度增加,在栓塞的近端则血流黯淡。当血栓较大时,肺动脉管腔内可无明显血流信号。
当彩色多普勒观察到三尖瓣反流信号时,可运用连续波多普勒测量反流峰值速度,并根据反流压差估测肺动脉收缩压(图10-1-17)。PE患者舒张早期肺动脉反流速度>2.2m/s;肺动脉及主动脉前向血流减少,容易出现前负荷降低所致低血压。
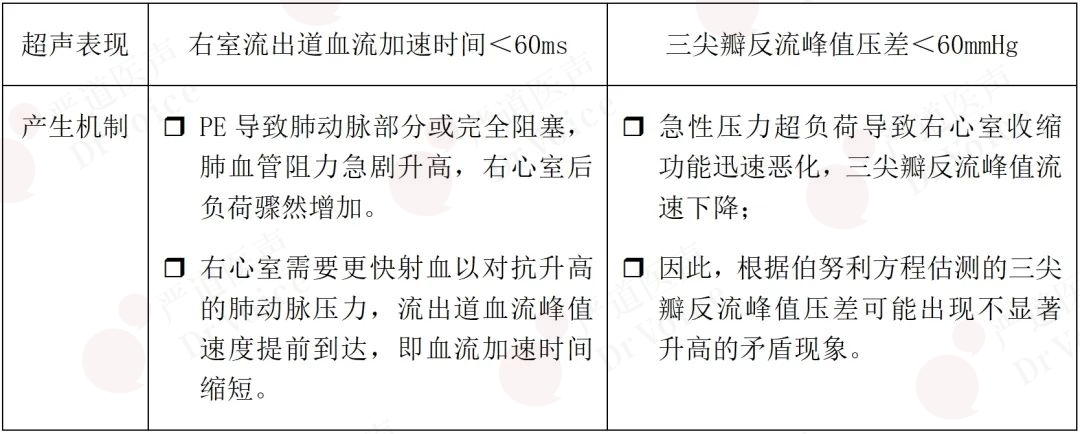
超声检查则表现为主、肺动脉血流速度时间积分降低以及“60-60征”。其中,“60-60征”指的是右室流出道血流加速时间缩短(≤60ms)以及根据伯努利方程估测的三尖瓣反流峰值压差<60mmHg(图10-1-18、图10-1-19);其产生机制见表10-1-3;该表现诊断PE的敏感性较低,但特异性高达94%。
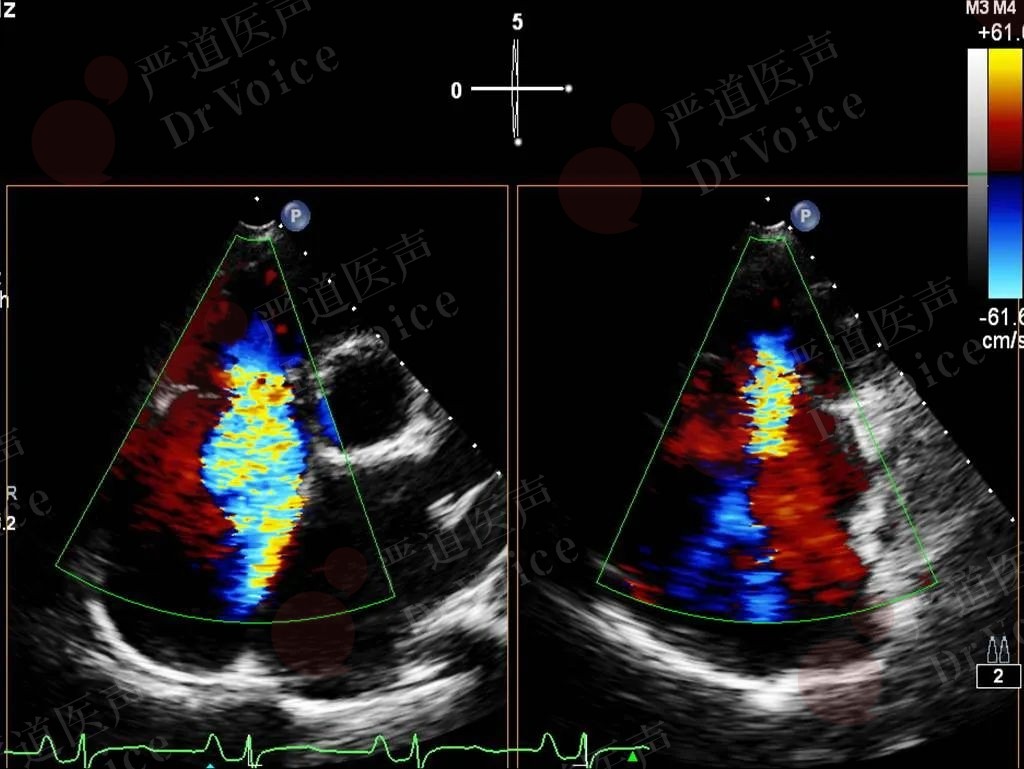
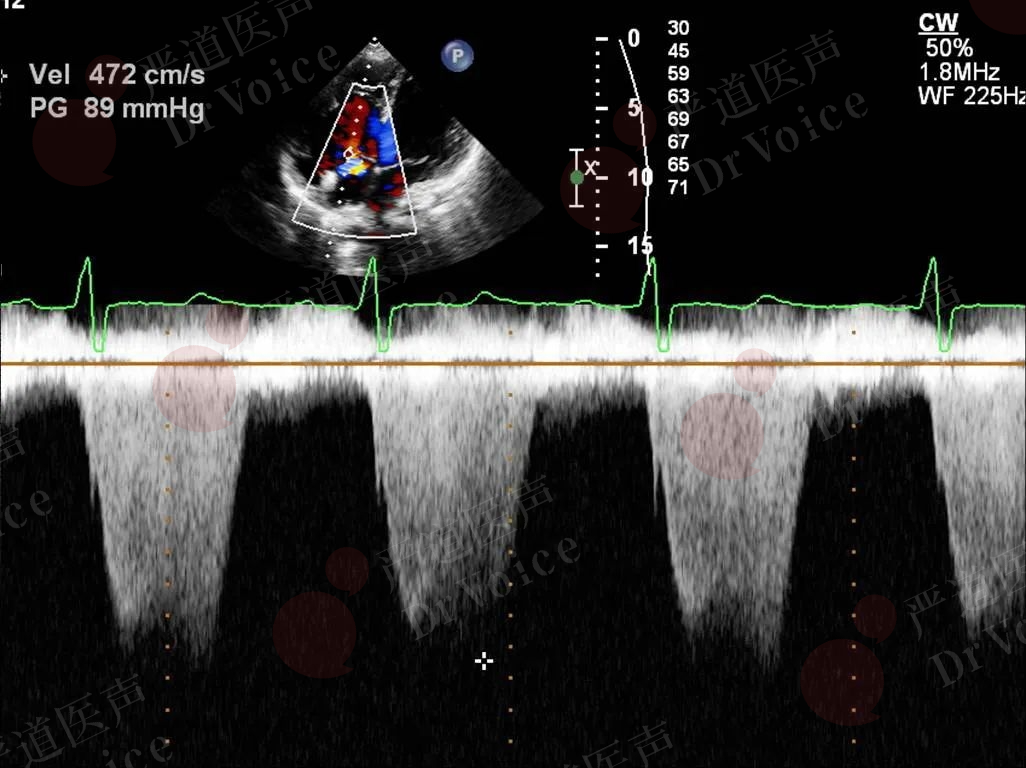
图10-1-17 彩色多普勒示三尖瓣大量反流(图A),连续多普勒测量三尖瓣反流峰值流速及跨瓣压差可间接评估肺动脉收缩压(图B)。
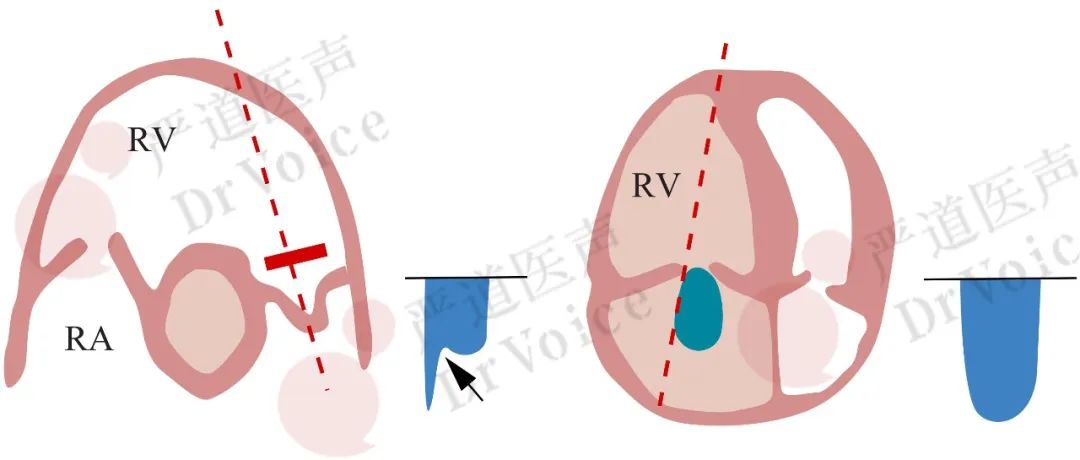
图10-1-18 “60-60”征示意图:右室流出道前向血流加速时间<60ms和/或收缩中期出现切迹;(左图,箭头),三尖瓣反流峰值压差<60mmHg(右图);上述两种多普勒超声表现同时存在,即“60-60”征;RA右心房,RV右心室。
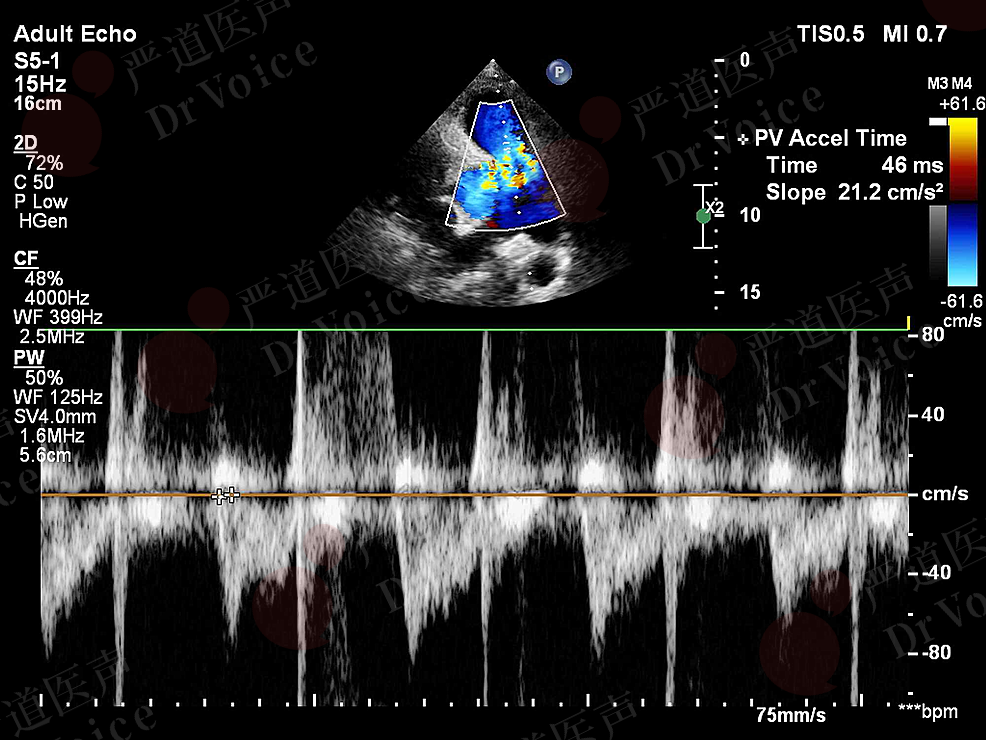
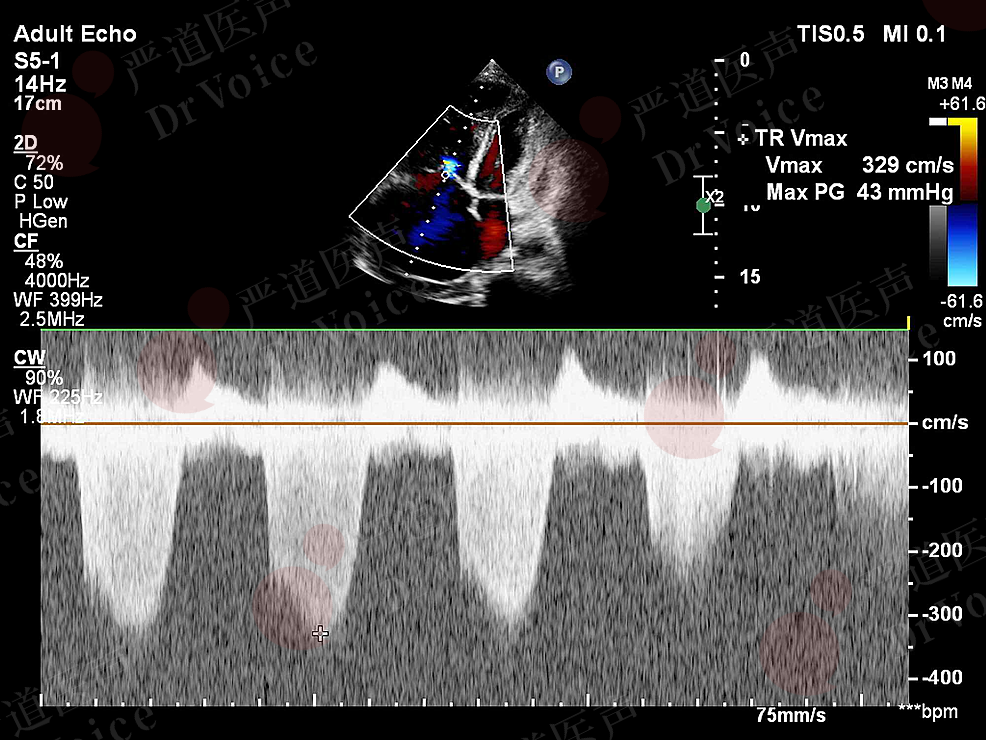
图10-1-19 “60-60”征超声表现:右室流出道前向血流加速时间46 ms伴收缩中期顿挫(图A),通过伯努利方程估测的三尖瓣反流峰值压差<60mmHg(图B)。
表10-1-3 “60-60”征产生机制
(四)经食管超声心动图
经食管超声较经胸超声更能清晰显示肺动脉特别是左、右肺动脉,可提高主肺动脉及其分支内的血栓检出率(图10-1-20、图10-1-21),特别是对左肺动脉远端血栓的检出率更具价值。其主要作用包括:①检出或排除与PE有关的病因,如心腔内肿物、血栓、瓣膜赘生物以及是否合并卵圆孔未闭和房间隔缺损;②经胸超声无法确诊,同时并存循环障碍需即刻明确诊断者;③确认血栓的位置、大小、机化程度及其与肺血管的关系。但此项检查不适用于可疑PE的急性重症患者。
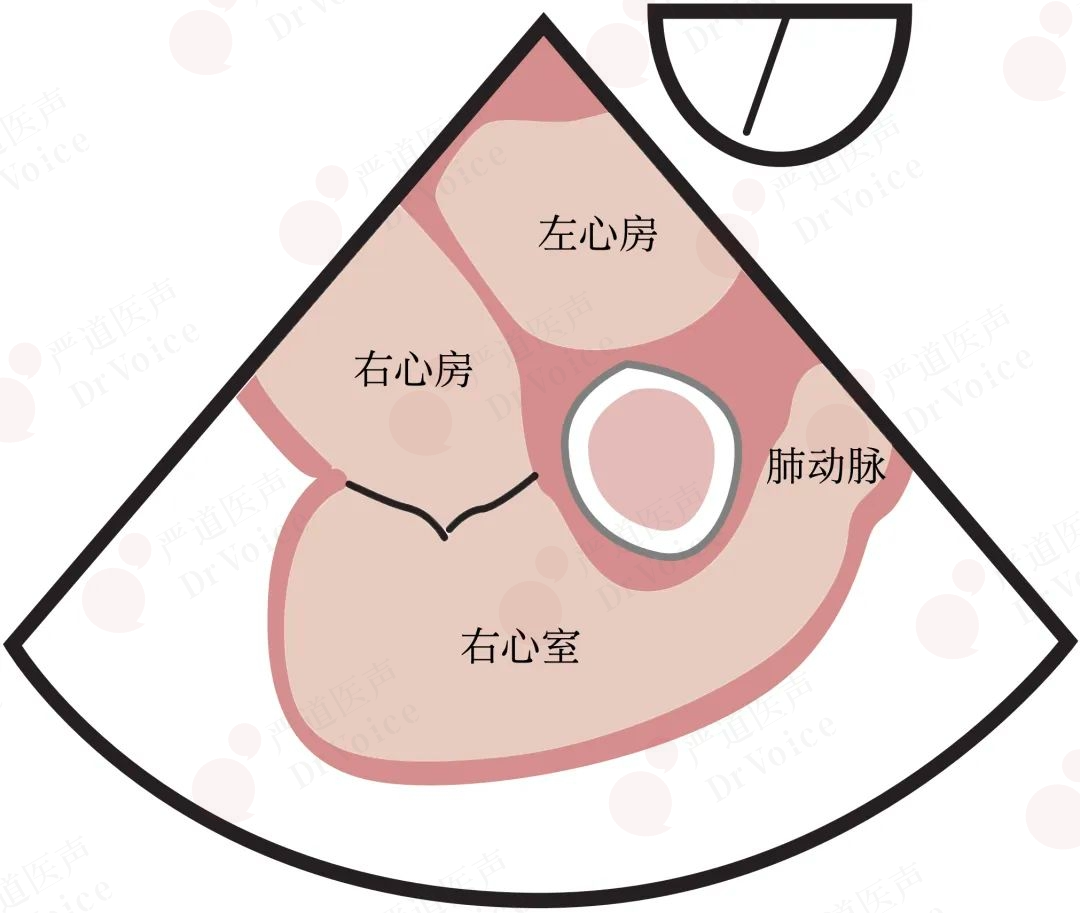
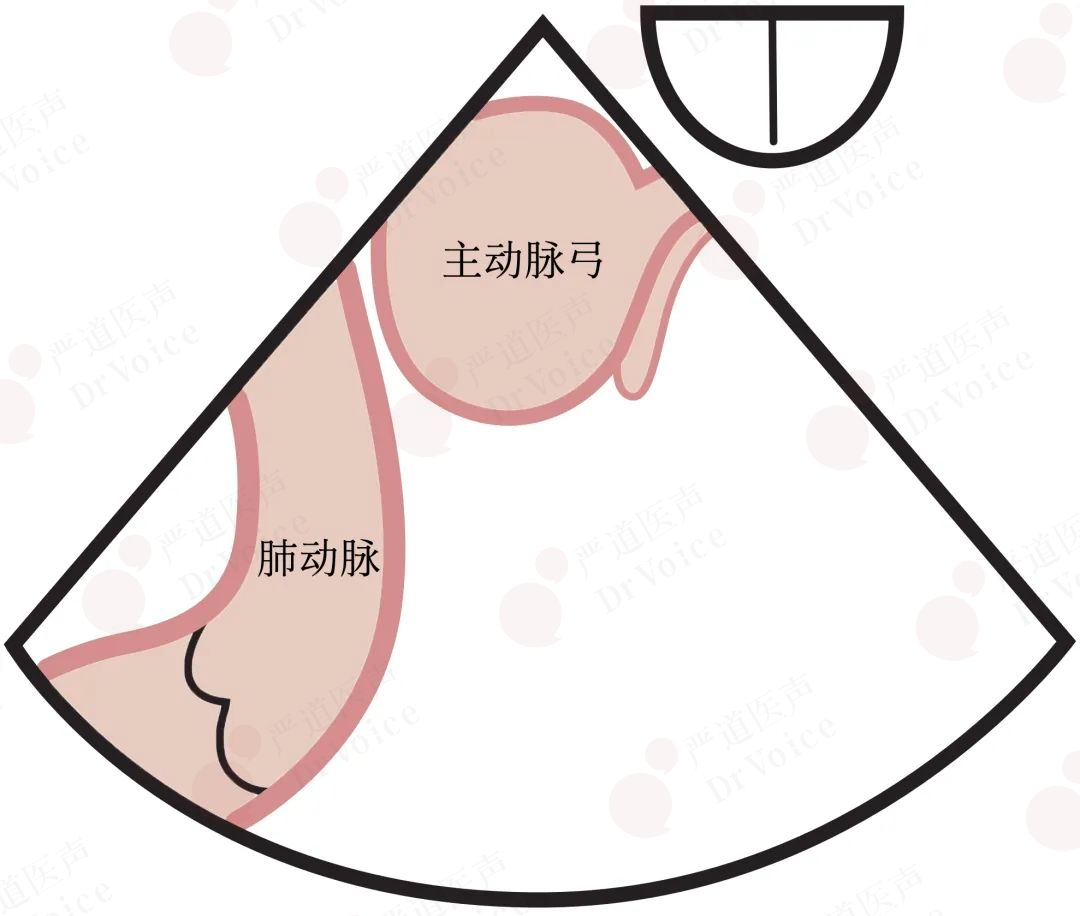
图10-1-20 经食管超声心动图评估肺动脉切面:食管中段右室流入-流出道切面显示肺动脉近端(图A),食管上段主动脉短轴切面显示肺动脉中、远端(图B)。
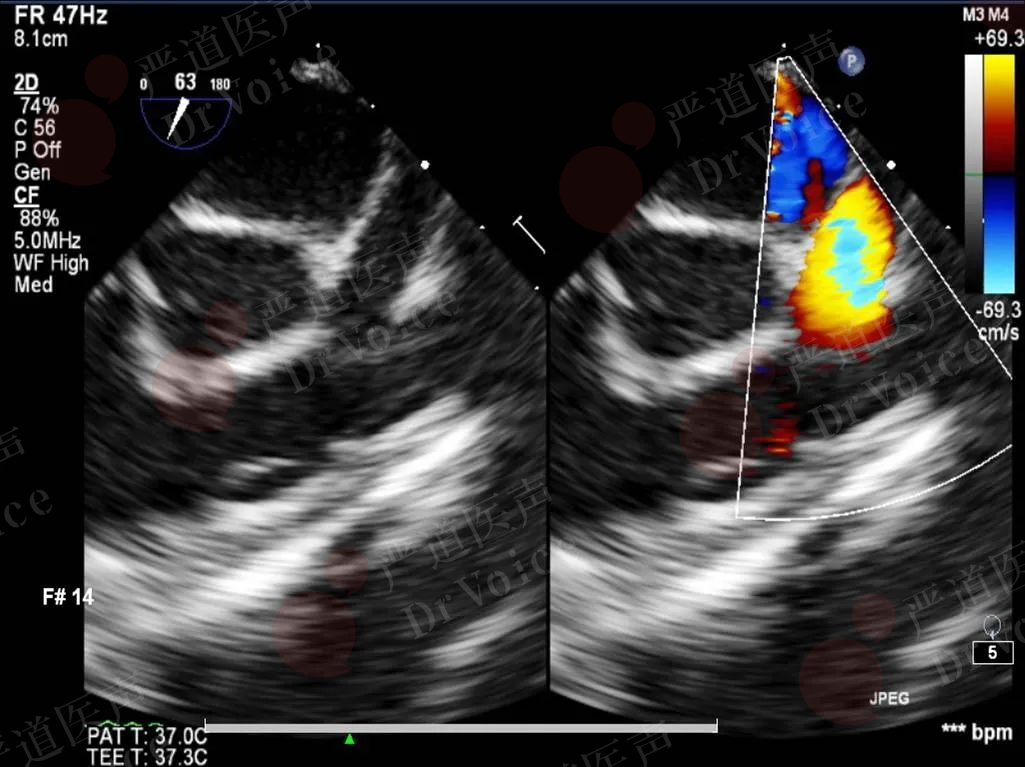
图10-1-21 经食管超声心动图显示肺动脉主干及分支
(五)实时三维超声心动图
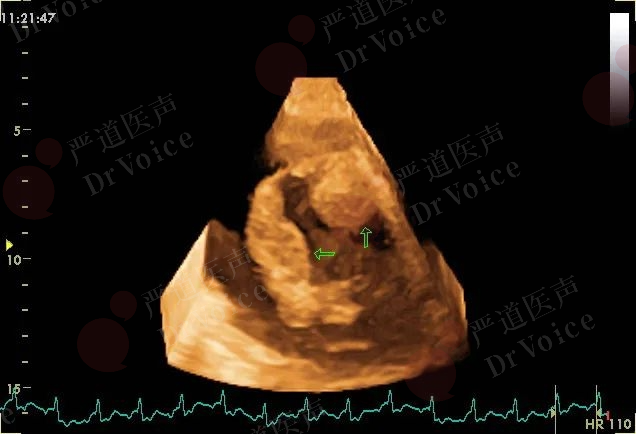
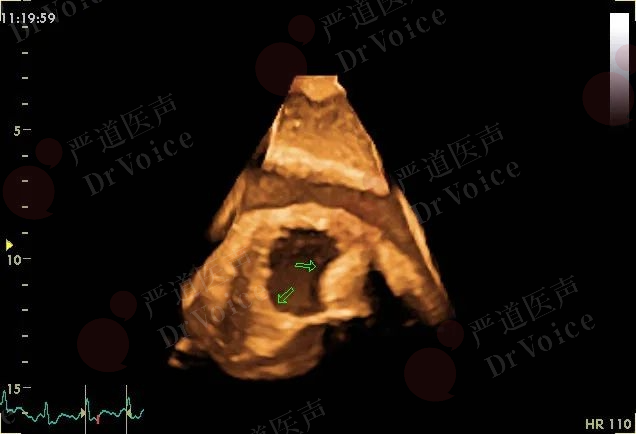
图10-1-22 经胸实时三维超声示右心房内转移瘤,质地坚硬,与心房壁附着牢固(箭头),此类患者脱落致PE的风险相对较小。
三、治疗方式
PE的治疗包括外科血栓剥离和内科介入治疗。介入治疗又包括对于PE的治疗性介入和预防性介入两种方式。前者指的是经导管给予溶栓药物、导管碎栓和除栓,肺动脉球囊血管成形术、肺动脉支架植入术。后者即下腔静脉滤器植入术,主要为防止下肢深静脉血栓脱落致PE形成,危重患者可在床旁超声引导下进行。
(一)术中超声引导与检测
目前有多种成像技术用于引导下腔静脉滤器施放, 在X线透视下、彩色多普勒超声和血管内超声引导下放置滤器均有报道。超声检查组织分辨率较高,但受腹腔内气体干扰较明显。术前6~8 h禁食以及灌肠等都是减少肠胀气的有效方法。
超声用于引导滤器释放需要注意:(1)要确定下腔静脉和施放滤器的静脉通路无血栓形成,以避免术中造成血栓脱落;(2)准确测量下腔静脉的内径, 避免将直径较小的滤器放置于过宽的下腔静脉,导致滤器的脱落或移位;(3)明确肾静脉与下腔静脉的开口位置,以确定滤器释放点。因肥胖或胃肠气体干扰无法清晰显示时,可考虑血管内超声或X线透视引导;(4)超声引导下静脉穿刺,可有效减少穿刺并发症(图10-1-23、图10-1-24)。术后即刻超声可用于检查滤器位置是否准确,张开的形态是否完全,并观察血流通过情况。
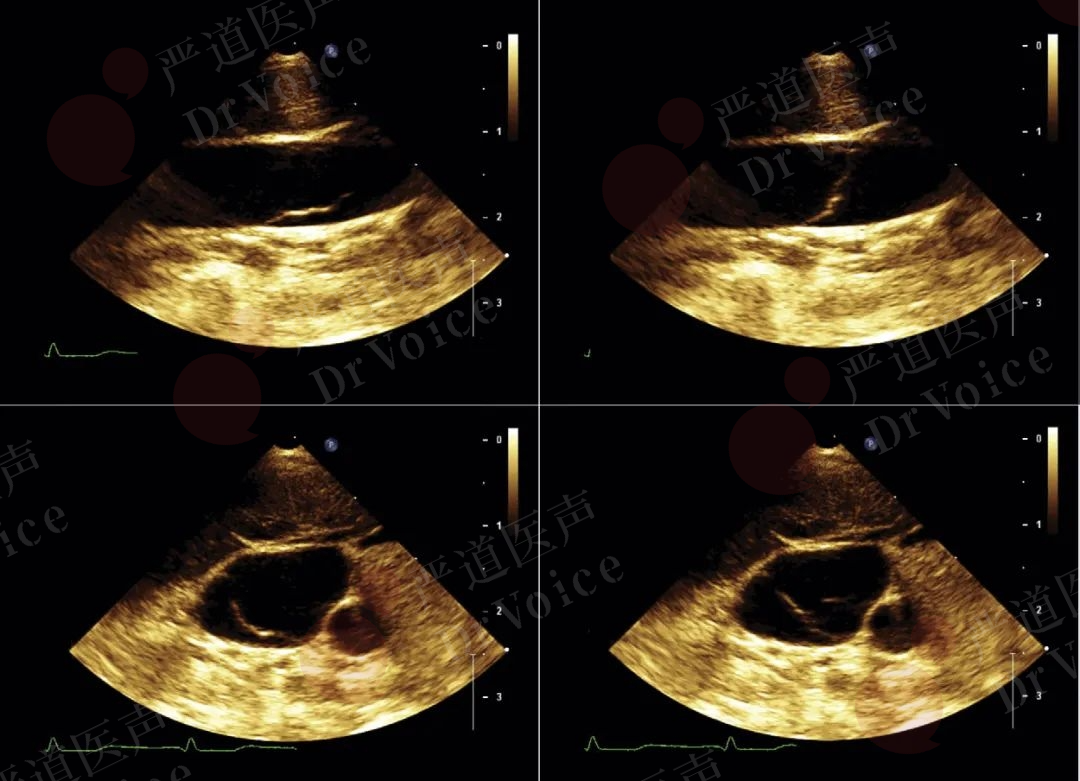
图10-1-23 术前超声检查提示颈内静脉管腔通畅,可见静脉瓣
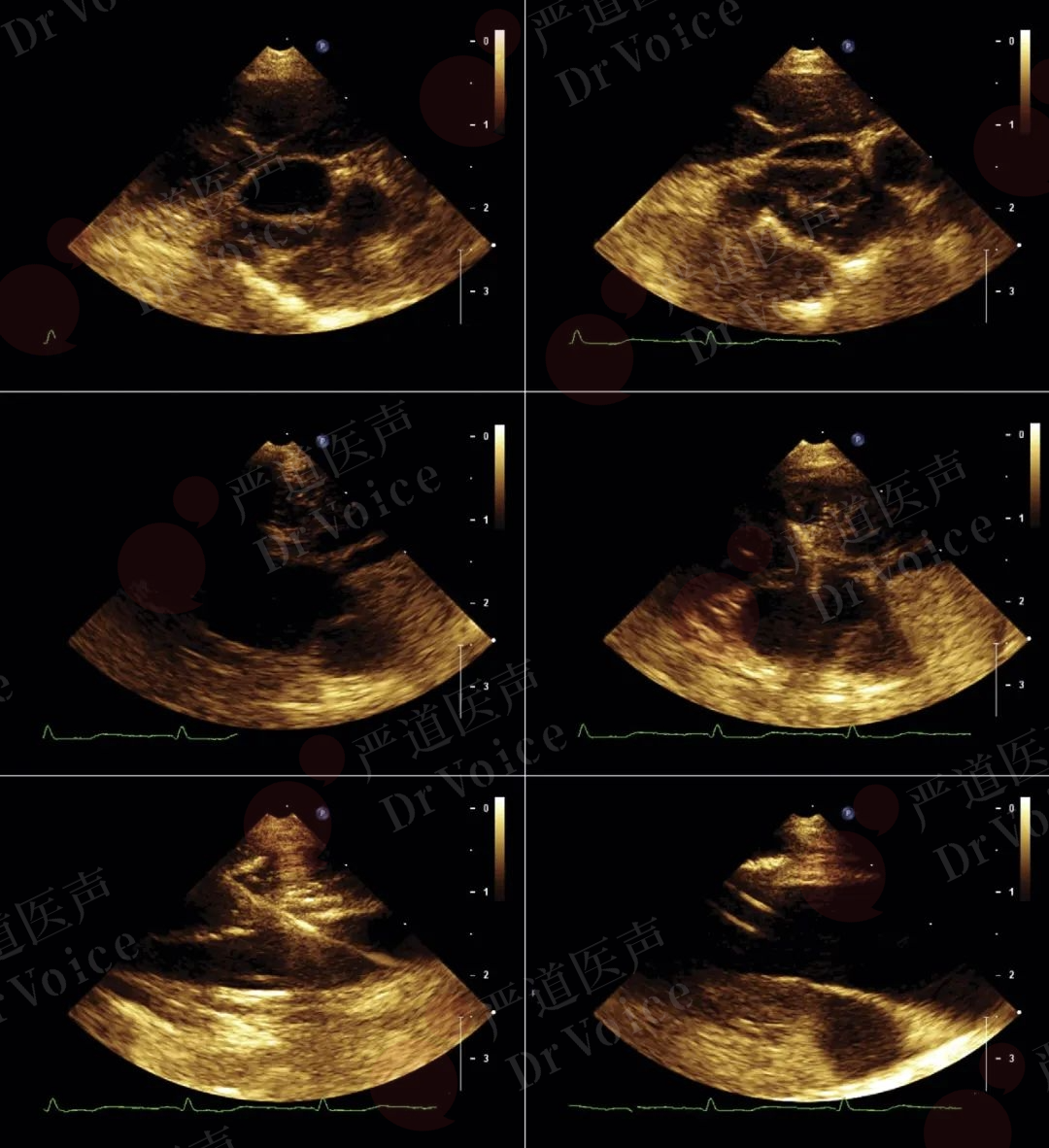
图10-1-24 超声引导颈内静脉穿刺的形态
等等
别急着离开
↓↓

【活动规则】
(1)活动时间:3月29日起至4月29日
(2)抽取5位优秀笔记作者,赠送《手把手教你学超声心动图》1本。
【参与方式】
(1)读书笔记投稿给学习助手-道道,并同时发布在小红书/抖音平台
(2)笔记末尾附上:@严道医声网 写读书笔记,送《手把手教你学超声心动图》,一起来参与吧!

添加道道
加入读者交流群!
谨分享此文给更多医生同仁,我们期待能为读者带来更多感悟与心得。我们将与孔教授共同投身于促进超声心动图这一领域的建设发展中,为学科进步与人才培养贡献更多力量。
这不是普通的工具书,而是一位超声发烧友与时间赛跑的医学手札,更是打开心脏超声奥秘的密钥。