
翻译作者:朱君,副主任医师,江南大学附属医院心血管内科
【致谢】严道医声衷心感谢各位医生同仁无偿提供专业的医学内容。谨以本文向所有推动医学科普的践行者致敬,期待与更多医者携手,传递医者声音,共建学术生态。
往期回顾

扫码添加道道,领取中文完整版pdf

4.ST 段抬高型心肌梗死(STEMI)和非 ST 段抬高型急性冠状动脉综合征(NSTE - ACS)的标准化治疗
4.1氧疗
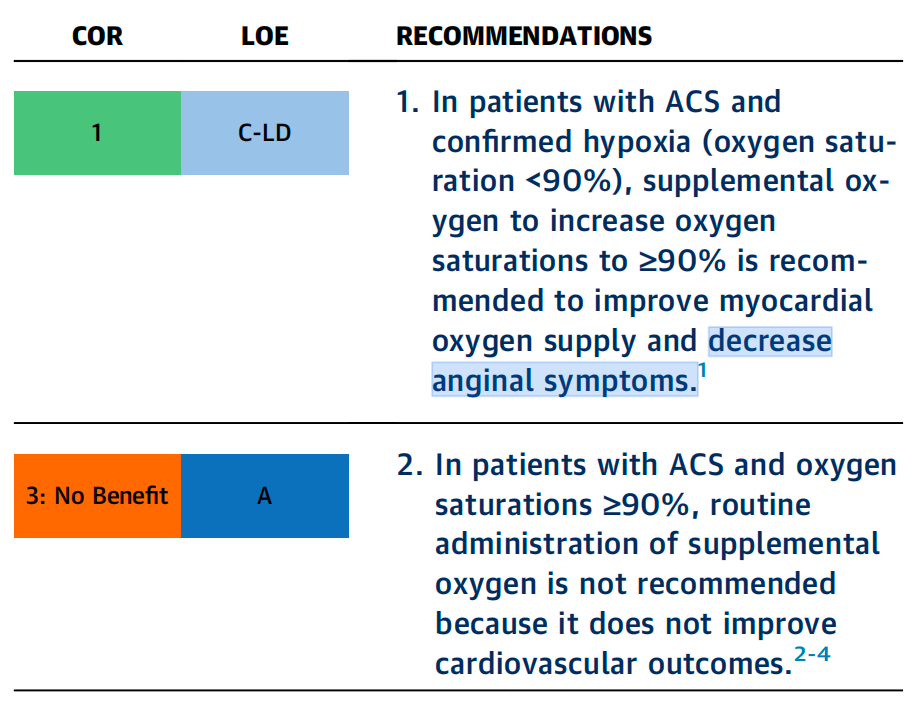
氧疗建议
支持这些建议的参考文献研究总结于证据表中。
内容概要
一直以来,在疑似急性冠状动脉综合征(ACS)患者的常规治疗中,都会给予补充吸氧。然而,目前缺乏证据表明,在无缺氧情况时吸氧会带来临床获益 [5]。针对无缺氧症状的心肌梗死(MI)患者开展的随机试验显示,常规补充吸氧(氧流量≥6 升 / 分钟)并无任何临床获益 [2 - 4,6]。而且,有研究提出担忧,吸氧可能会通过加剧血管收缩和增加氧化应激反应,进而加重心肌损伤 [3]。
指南推荐意见的相关支持性文本
补充吸氧可能对存在缺氧情况(外周毛细血管血氧饱和度 < 90%)的患者有益,其中包括那些因急性或慢性疾病,需要通过补充吸氧才能使血氧饱和度达到 ≥ 90% 的患者。一项针对各类急性病成年患者的随机对照试验(RCT)的系统评价和荟萃分析显示对于各类无缺氧情况的急性病成年患者开展的研究表明,与保守给氧相比,过度给氧会导致患者短期和长期死亡率升高 [7]。这些研究未能明确既能将潜在危害降至最低,又能使临床获益最大化的最佳血氧饱和度目标范围。观察发现,氧合情况与患者预后之间呈 U 型关系,初诊时外周血氧饱和度(SpO₂)在 94% - 96% 的患者死亡率最低 [8]。
3.目前,多项随机试验表明,对于已知或疑似患有急性心肌梗死(AMI)且血氧饱和度 ≥ 90% 的患者,常规使用补充吸氧并不能带来心血管方面的益处。尽管各研究的排除标准有所不同,但通常会排除那些在家需要长期吸氧、因支气管痉挛发作而需要补充吸氧,或就诊时发生心脏骤停的患者 [2 - 4,6]。“ST 段抬高型心肌梗死中空气与氧气对比研究(AVOID)” 探讨了在血氧饱和度 ≥ 94% 的 ST 段抬高型心肌梗死(STEMI)患者中使用补充吸氧(8 升 / 分钟)的效果。结果显示,常规补充吸氧并无益处,甚至可能会加重心肌损伤,增大梗死面积 [3]。“疑似心肌梗死患者补充氧疗的疗效和结局研究(DETO2X - AMI)” 对 6629 例疑似心肌梗死且血氧饱和度 ≥ 90% 的患者使用常规补充吸氧(6 升 / 分钟)的情况进行了评估。结果发现,补充吸氧并不能降低患者 1 年的全因死亡率,也无法减少因心肌梗死导致的再次住院率 [2,9]。研究发现,对于基线血氧饱和度处于较低水平(90% - 94%)的患者,补充吸氧也未显示出临床获益 [10]。
4.2止痛药
概述
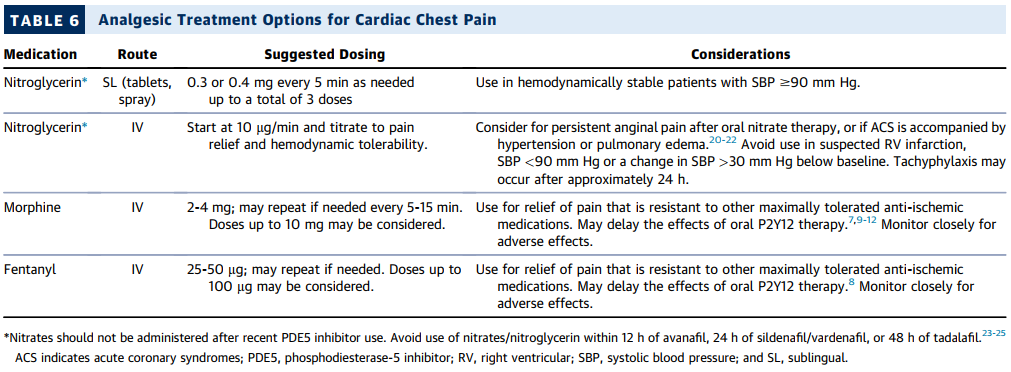
已知或疑似急性冠状动脉综合征(ACS)的患者常常会经历胸痛或其他不适症状。迅速且有效地缓解疼痛仍然是一项重要的治疗目标,以防止交感神经激活和不良临床后果(见表 6)。镇痛疗法或许能缓解症状,但尚无证据表明其能改善 ACS 患者的临床结局 [1,2]。硝酸酯类药物和阿片类药物仍然是治疗 ACS 疼痛的有效选择,但应谨慎使用,以防止潜在危害 [3 - 6]。特别是对于使用硝酸酯类药物后缺血症状仍持续不缓解的患者,应尽快进行冠状动脉血运重建,而不应仅使用阿片类药物来掩盖这些症状。此外,人们还担忧使用阿片类药物可能会延缓口服 P2Y₁₂抑制剂在胃肠道的吸收,从而延迟其在接受经皮冠状动脉介入治疗(PCI)患者中的药效学作用 [7 - 10]。然而,这些药效学发现的临床相关性仍存在争议 [11 - 14]。只要有可能,应避免使用非阿司匹林类非甾体抗炎药来治疗疑似或已知的缺血性疼痛 [15 - 17]。使用非甾体抗炎药会增加有或无心脏病史患者发生主要不良心血管事件(MACE)的风险,且并无确凿证据支持在 ACS 患者中常规使用该类药物 [15 - 19]。
4.3抗血小板治疗
4.3.1 阿司匹林

概要
长期以来,阿司匹林一直被视为急性冠状动脉综合征(ACS)患者抗血小板治疗中不可或缺的一部分,用于预防动脉粥样硬化血栓形成事件的复发 [1 - 3,6]。阿司匹林可降低急性心肌梗死(AMI)后血管性死亡的发生率 [3],在包括心肌梗死(MI)后患者的二级预防试验中,它能减少血管和冠状动脉事件(包括心肌梗死和中风)的发生 [2]。虽然传统上认为 ACS 患者应终身服用阿司匹林,但现在对于部分患者,在发病 1 - 3 个月后的维持阶段,可以考虑停用阿司匹林,而非停用 P2Y12抑制剂,以降低出血风险(见第 11.1 节 “出院后前 12 个月的双重抗血小板治疗策略”)。对于正在接受全剂量抗凝治疗并持续使用 P2Y12抑制剂的患者,在经皮冠状动脉介入治疗(PCI)后 1 - 4 周停用阿司匹林也是合适的(见第 11.1.1 节 “出院后接受抗凝治疗患者的抗血小板治疗”)。对于有阿司匹林过敏史的患者,若条件允许,首选进行阿司匹林脱敏治疗,以便能够开始使用双重抗血小板治疗 [7 - 9]。无论患者是否有阿司匹林过敏史,均建议所有 ACS 患者使用 P2Y12抑制剂。但是,对于就诊时无法服用阿司匹林的患者,应尽早给予 P2Y12抑制剂负荷剂量。
指南推荐意见的相关支持性文本
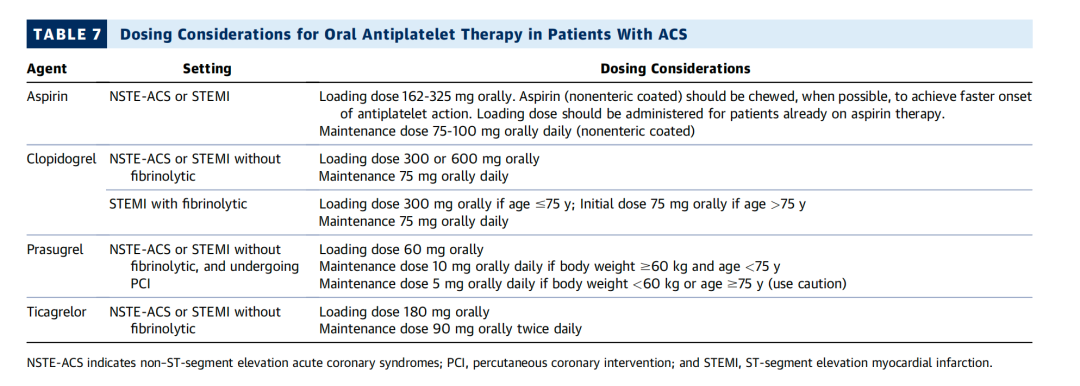
1.对于无绝对禁忌证的急性冠状动脉综合征(ACS)患者,一经确诊,无论最终采取何种治疗策略(侵入性或非侵入性),都应尽快给予阿司匹林负荷剂量(162 - 325 毫克),随后进行每日维持剂量治疗(具体见第 4.3.2 节 “住院期间口服 P2Y12抑制剂” 中的表 7)。对于无法口服药物的患者,可选择直肠给药或静脉给药(若有相应剂型)。现有证据支持使用非包衣低剂量阿司匹林(75 - 100 毫克)进行每日维持治疗。每日 75 - 100 毫克的阿司匹林剂量超过了抑制血小板血栓素 A₂所需的最低有效剂量,可应对不同个体对药物反应的差异 [10]。在采取侵入性治疗策略的 ACS 患者中,在初始负荷剂量后连续 30 天使用全剂量阿司匹林(每日 300 - 325 毫克),在降低主要不良心血管事件(MACE)方面并不优于低剂量阿司匹林(每日 75 - 100 毫克),反而会增加轻微出血和胃肠道出血的风险 [4]。
在一项针对已确诊动脉粥样硬化性心血管疾病(ASCVD)患者的开放性随机对照试验(RCT)中,其中 35% 的患者有心肌梗死病史,每日服用 81 毫克阿司匹林的患者与每日服用 325 毫克阿司匹林的患者在 MACE 或严重出血方面未观察到显著差异,不过观察到研究组间存在较高的交叉换药率 [5]。综合这些数据,支持使用低剂量阿司匹林(每日 75 - 100 毫克)进行维持治疗。根据对 PLATO(血小板抑制与患者预后)试验的事后分析中阿司匹林剂量与预后的关联,接受替格瑞洛治疗的患者应始终使用每日剂量≤100 毫克的阿司匹林 [11]。
4.3.2住院期间口服 P2Y12抑制剂

概要
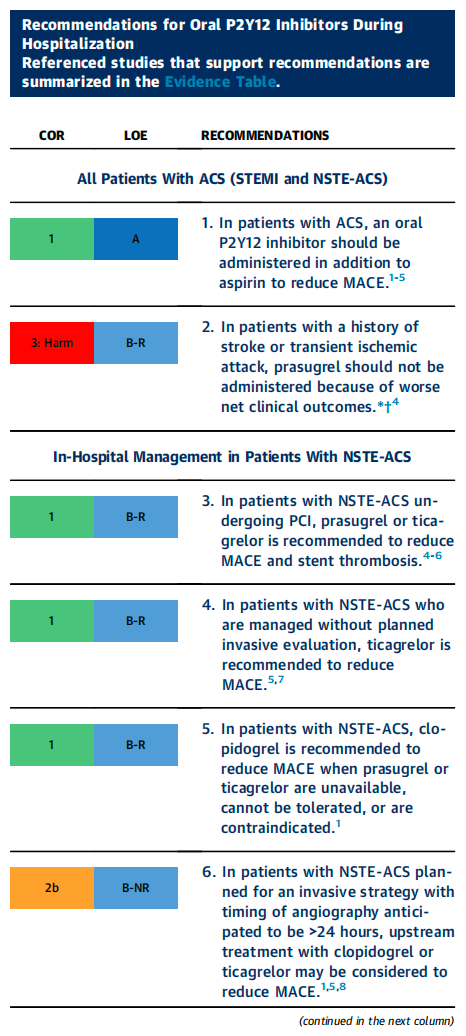
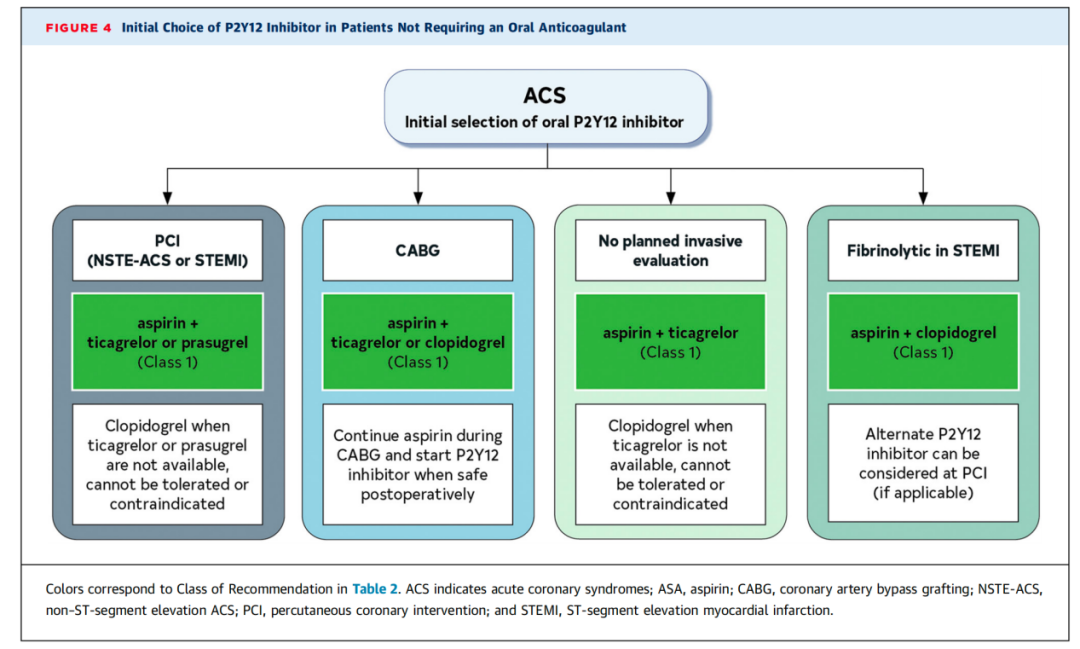
血小板 P2Y12受体的口服抑制剂能够拮抗二磷酸腺苷(ADP)介导的血小板活化。在整个急性冠状动脉综合征(ACS)范围内,在阿司匹林治疗的基础上加用 P2Y12抑制剂可显著降低血小板聚集,并且已证实能降低复发性主要不良心血管事件(MACE)的发生率,但同时会增加出血风险 [1 - 5,9,10]。因此,除了服用阿司匹林外,ACS 患者还应先给予口服 P2Y12抑制剂的负荷剂量,随后进行每日维持剂量治疗(见表 7)。选择具体类型的口服 P2Y12抑制剂时需要考虑多个因素,包括患者预期的治疗策略以及出血风险(见图 4)[1 - 5,9,10]。临床上可用的口服 P2Y12抑制剂包括氯吡格雷、普拉格雷和替格瑞洛。氯吡格雷是效力最弱的口服 P2Y12抑制剂,在给予负荷剂量后,需要更长时间才能达到最大程度的血小板抑制效果,因为它需要在肝脏中进行生物转化以形成其活性代谢产物。已有充分研究描述了氯吡格雷药效反应的变异性 [14,15],在经皮冠状动脉介入治疗(PCI)后使用氯吡格雷治疗时,反应低下者发生 MACE 和支架内血栓形成的风险可能会增加 [16,17]。替格瑞洛和普拉格雷的药效比氯吡格雷更强,能更快地抑制血小板活化,但与氯吡格雷相比,它们会增加出血风险。值得注意的是,约 10% - 15% 的急性冠状动脉综合征(ACS)患者在使用替格瑞洛后可能会出现自觉的短暂性呼吸困难 [5]。双重抗血小板治疗的疗程问题将在第 11.1 节 “出院后前 12 个月的双重抗血小板治疗策略” 中讨论。
指南推荐意见的相关支持性文本
1.多项试验已证实,口服 P2Y12抑制剂在急性冠状动脉综合征(ACS)治疗中可降低主要不良心血管事件(MACE)的发生风险,但会增加出血风险。在非 ST 段抬高型急性冠状动脉综合征(NSTE - ACS)和 ST 段抬高型心肌梗死(STEMI)的随机安慰剂对照试验中,无论采取何种治疗策略,在阿司匹林治疗基础上加用氯吡格雷均可降低 MACE 风险 [1 - 3]。对于接受溶栓治疗的 STEMI 患者,在阿司匹林基础上加用氯吡格雷可降低 30 天内 MACE 的发生风险(包括复发性心肌梗死),并提高生存率 [2, 3]。此外,在随机试验中,与氯吡格雷相比,对于未同时接受溶栓治疗的 STEMI 患者或 NSTE - ACS 患者,使用普拉格雷和替格瑞洛可进一步降低 MACE 以及支架内血栓形成的风险 [4, 5]。口服 P2Y12抑制剂的益处在冠状动脉旁路移植术(CABG)后的患者中也得到了证实 [18 - 21]。关于准备接受 CABG 手术的患者中断用药剂量的指导信息详见表 8。CABG 手术后的用药时长在第 11.1 节 “出院后前 12 个月的双重抗血小板治疗策略” 中有详细说明。

2.在一项针对急性冠状动脉综合征(ACS)患者的随机、双盲 TRITON - TIMI 38 试验(通过优化普拉格雷血小板抑制作用评估治疗结果改善情况的试验 - 心肌梗死溶栓 38 试验)的二次分析中,比较了在阿司匹林基础上加用普拉格雷和氯吡格雷的效果。亚组分析以净临床获益(主要不良心血管事件加上出血情况)为结局指标,结果显示,对于有既往短暂性脑缺血发作或中风病史的患者,使用普拉格雷相较于氯吡格雷会带来净危害 [4]。对于年龄≥75 岁以及体重<60 千克的患者,应考虑降低普拉格雷的剂量(见表 7)。
3.随机、双盲的 TRITON - TIMI 38 试验和 PLATO 试验表明,与氯吡格雷相比,普拉格雷(TRITON - TIMI 38 试验)或替格瑞洛(PLATO 试验)可使心血管死亡、心肌梗死或中风复合终点事件的发生率降低 16% - 20%,同时也降低了支架内血栓形成的风险 [4,5]。在 PLATO 试验中,还观察到与氯吡格雷相比,替格瑞洛可使全因死亡率有一定程度的降低 [5]。在 TRITON - TIMI 38 试验中,仅对经评估认为解剖结构适合进行经皮冠状动脉介入治疗(PCI)的非 ST 段抬高型急性冠状动脉综合征(NSTE - ACS)患者使用 P2Y12抑制剂(普拉格雷或氯吡格雷)。在 PLATO 试验中,72% 的患者采用了计划内的侵入性治疗策略,并且侵入性治疗人群在降低主要不良心血管事件(MACE)以及心血管死亡和全因死亡方面的结果与整个试验高度一致 [6]。
与氯吡格雷相比,普拉格雷和替格瑞洛都会增加非冠状动脉搭桥术(CABG)相关的严重出血风险 [4,5]。已有研究表明,普拉格雷会增加危及生命的出血风险 [4]。目前关于直接比较普拉格雷和替格瑞洛疗效和安全性的数据有限。一项开放性随机试验报告称,与在接受侵入性评估的急性冠状动脉综合征(ACS)患者中作为上游治疗使用的替格瑞洛相比,在经皮冠状动脉介入治疗(PCI)时使用普拉格雷,前者主要不良心血管事件(MACE)发生率更低,且出血情况相似 [22]。
4.随机双盲的 PLATO 试验比较了替格瑞洛与氯吡格雷在急性冠状动脉综合征(ACS)患者中的疗效,该试验纳入了采用或不采用计划内侵入性治疗策略的患者。在未采用计划内侵入性治疗策略的 28% 的患者(n = 5216)中,与使用氯吡格雷相比,使用替格瑞洛使血管性死亡、心肌梗死或中风这一主要终点事件的发生率降低了 15%,这与整个试验中主要不良心血管事件(MACE)发生率降低 16% 的结果高度一致。同样,出血情况的研究结果也与整个试验的结果相符 [5,7]。
5.在随机、双盲、安慰剂对照的 CURE(氯吡格雷用于不稳定型心绞痛以预防复发事件)试验中,对于正在接受阿司匹林治疗、采用药物保守治疗或接受血运重建治疗的非 ST 段抬高型急性冠状动脉综合征(NSTE - ACS)患者,加用氯吡格雷显著降低了心血管死亡、心肌梗死或中风的复合终点事件发生率 [1]。尽管在接受经皮冠状动脉介入治疗(PCI)的急性冠状动脉综合征(ACS)患者中,与氯吡格雷相比,普拉格雷和替格瑞洛能进一步降低主要心血管事件的发生风险,但这两种强效药物也会进一步增加出血风险 [4,5]。对于出血风险高,或存在使用普拉格雷或替格瑞洛禁忌证的患者,氯吡格雷是一种有效的替代 P2Y12抑制剂。在一项开放性试验中,接受 PCI 的老年 ACS 患者交叉换药率较高,与使用替格瑞洛的患者相比,使用氯吡格雷的患者缺血事件发生率相似,但出血情况更少 [23]。已有研究描述了患者对氯吡格雷药效反应存在显著的个体差异 [15]。
6.在 CURE 试验中一项针对接受经皮冠状动脉介入治疗(PCI)患者(n = 2658)的前瞻性亚组研究中,那些在 PCI 术前接受氯吡格雷预处理(中位时间 6 天)的患者,在 PCI 术前以及术后 30 天内主要不良心血管事件(MACE)的发生率均显著降低 [8]。氯吡格雷是一种前体药物,需要通过细胞色素 P450 酶系统进行代谢才能形成其活性代谢产物。因此,在给予负荷剂量后,可能需要数小时才能观察到显著的抗血小板效果。一项针对接受 PCI 的急性冠状动脉综合征(ACS)患者使用氯吡格雷的试验的荟萃分析发现,氯吡格雷预处理可显著降低患者 30 天内心血管死亡或心肌梗死的风险 [11]。然而,对于起效更快、作用更强的 P2Y12抑制剂时代,是否需要进行预处理,目前了解较少。在一项比较普拉格雷预处理与在经皮冠状动脉介入治疗(PCI)时给药的随机试验中,预处理(中位时间仅 4.4 小时)并未改善缺血性结局,但但显著增加了出血风险 [24]。在 PLATO 试验中,开始使用研究药物前并不要求知晓冠状动脉解剖结构;然而,该试验并未专门比较替格瑞洛早期使用与在 PCI 时给药这两种策略。因此,对于非 ST 段抬高型急性冠状动脉综合征(NSTE - ACS)患者,在 PCI 前使用替格瑞洛是否有益仍不清楚。基于此,临床试验数据并不支持对采用早期侵入性治疗策略(<24 小时)的患者常规进行预处理。不过,对于预计在给予负荷剂量后 24 小时或更久才进行血管造影及后续侵入性治疗的患者,考虑使用氯吡格雷或替格瑞洛进行预处理可能是合理的。
7.在 TRITON - TIMI 38 试验和 PLATO 试验中,对于接受直接经皮冠状动脉介入治疗(PPCI)或在 ST 段抬高型心肌梗死(STEMI)初始治疗后进行延迟(再次)PCI 的患者,与氯吡格雷相比,普拉格雷和替格瑞洛的临床疗效表现一致 [4,5]。在 TRITON - TIMI 38 试验的 STEMI 亚组患者(n = 3534)中,普拉格雷在 15 个月时使主要不良心血管事件(MACE)显著降低了 21%,支架内血栓形成降低了 42%,且未明显增加出血风险 [9]。在 PLATO 试验中,对于接受 PPCI 的 STEMI 患者(n = 7544),与氯吡格雷相比,使用替格瑞洛治疗在降低心血管死亡、复发性心肌梗死或中风方面呈现出一致的趋势,同时显著降低了支架内血栓形成的风险,全因死亡风险降低了 18%[10]。RITON - TIMI 38 试验和 PLATO 试验均允许对接受直接 PCI 的 STEMI 患者在首次血管造影前使用研究药物。在另一项针对 STEMI 患者 PPCI 的随机试验中,院前给予替格瑞洛或入院后给予替格瑞洛,均未改善 PCI 前冠状动脉再灌注这一主要终点 [25]。然而,早期给予替格瑞洛与降低支架内血栓形成相关,且各治疗组间出血情况相似。登记数据也未显示 STEMI 患者预先负荷使用 P2Y12抑制剂有明确的临床益处 [26],但一项纳入 STEMI 患者的荟萃分析显示,氯吡格雷预处理与降低 MACE 风险相关,且不增加出血风险 [27]。
8.氯吡格雷在预防接受经皮冠状动脉介入治疗(PCI)的 ST 段抬高型心肌梗死(STEMI)患者发生支架内血栓和早期复发性缺血事件方面是有效的 [11]。和非 ST 段抬高型急性冠状动脉综合征(NSTE - ACS)患者的情况一样,对于接受直接经皮冠状动脉介入治疗(PPCI)的 STEMI 患者,与氯吡格雷相比,普拉格雷和替格瑞洛可降低复发性主要不良心血管事件(MACE)的风险 [9,10]。对于出血风险高或存在使用普拉格雷或替格瑞洛禁忌证的 STEMI 患者,使用氯吡格雷是这两种药物的替代方案。
9.在 CLARITY(氯吡格雷作为辅助再灌注治疗) - TIMI 28 试验中,对于年龄小于 75 岁、接受溶栓治疗的 ST 段抬高型心肌梗死(STEMI)患者,在阿司匹林基础上加用氯吡格雷,降低了血管造影显示梗死相关动脉闭塞的几率,同时也降低了 30 天内心血管死亡、复发性心肌梗死或因复发性缺血而需紧急血运重建等复合终点事件的发生几率 [2]。在随机、安慰剂对照的 COMMIT(心肌梗死患者氯吡格雷与美托洛尔试验)研究中,针对服用阿司匹林、疑似心肌梗死(93% 为 STEMI,54% 接受了溶栓治疗)的患者,每日服用 75mg 氯吡格雷(未用负荷剂量)显著降低了死亡、再梗死或中风的复合终点风险,以及单纯死亡终点的风险,在接受溶栓治疗的亚组中结果一致 [3]。与安慰剂相比,使用氯吡格雷未观察到显著的出血增加。基于这两项试验的设计,当采用溶栓作为再灌注策略时,建议年龄小于 75 岁的患者服用氯吡格雷时给予负荷剂量(300mg,然后每日 75mg),而年龄大于等于 75 岁的患者则不用负荷剂量,直接每日服用 75mg。对于接受溶栓治疗后需进行经皮冠状动脉介入治疗(PCI)的患者,氯吡格雷、替格瑞洛(年龄小于 75 岁,在溶栓药物使用后 24 小时内)或普拉格雷(溶栓药物使用后超过 24 小时)均可作为支持 PCI 治疗的替代方案 [9 - 12,28]。在一项涉及 3799 例接受溶栓治疗的 STEMI 患者的试验中,其中 89% 的患者在使用溶栓药物时也同时使用了氯吡格雷。随机分组后,在溶栓治疗后中位时间 11.4 小时(四分位间距 5.8 - 18.2 小时)给予替格瑞洛,在严重出血方面不劣于氯吡格雷组 [28]。
4.3.3 静脉注射 P2Y12抑制剂治疗

概要
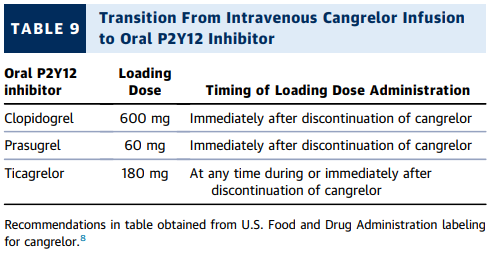
坎格瑞洛是一种直接作用的 P2Y12受体静脉拮抗剂,其特点是具有快速且强效的血小板抑制作用,在停药后 1 小时内血小板功能即可恢复 [6]。这些药理学特性在以下临床中应用可能有益:口服 P2Y12抑制剂的吸收障碍或无法口服的情况;以及在经皮冠状动脉介入治疗(PCI)后不久就需要进行冠状动脉搭桥术(CABG)或其他手术,因长时间停用 P2Y12抑制剂可能不安全的患者 [7]。在 3 项随机对照试验(RCT)中,比较了坎格瑞洛与氯吡格雷或安慰剂在从未使用过 P2Y12抑制剂而因慢性或急性适应证接受 PCI 患者中的安全性和有效性 [1 - 3]。在对这些研究进行的患者水平汇总分析中,PCI 期间使用坎格瑞洛显著降低了围手术期缺血事件的发生,尽管代价是更为频繁的轻微出血 [4]。与替格瑞洛或普拉格雷相比,坎格瑞洛在缺血事件方面的安全性和有效性尚未确定。从静脉注射 P2Y12抑制剂过渡到口服 P2Y12抑制剂是一个重要的考虑因素,以确保在坎格雷洛输注结束后仍有足够的血小板抑制作用(见表 9)[8]。
指南推荐意见的相关支持性文本
1.CHAMPION PHOENIX 研究(一项比较坎格瑞洛与氯吡格雷标准治疗在需要接受经皮冠状动脉介入治疗 [PCI] 患者中的疗效的临床试验)评估了在因急性或稳定性冠状动脉综合征而接受 PCI 的患者中,坎格瑞洛与氯吡格雷的治疗效果差异 [2]。在该研究中,坎格瑞洛组患者在 PCI 术前先静脉推注坎格瑞洛,随后持续静脉滴注至少 2 小时,或持续至手术结束(以时间较长者为准)。而对照组患者在 PCI 术前或术后立即给予 600mg 或 300mg 的氯吡格雷负荷剂量。研究结果显示,在 48 小时时,坎格瑞洛组的主要终点事件(全因死亡、心肌梗死、因缺血导致的血运重建或支架内血栓形成)发生率显著降低。并且,在非 ST 段抬高型急性冠状动脉综合征(NSTE - ACS,n = 2810)和 ST 段抬高型心肌梗死(STEMI,n = 1991)亚组患者中,也观察到了相似的效果。这一结果与早期的 CHAMPION PLATFORM 研究(坎格瑞洛与标准治疗以实现最佳血小板抑制管理)和 CHAMPION PCI 研究(一项验证坎格雷洛疗效的临床试验)的中性结果形成了对比。这两项早期研究分别将坎格瑞洛与安慰剂和氯吡格雷进行了比较。不同试验中氯吡格雷的给药时机以及对心肌梗死(MI)和支架内血栓形成的定义存在差异,这可能在一定程度上解释了缺血事件发生率和所观察到的治疗效果的不同。在对这些试验的汇总分析中,与对照组相比,坎格瑞洛可显著降低围手术期缺血事件的发生率,且在不同类型的急性冠状动脉综合征(ACS)表现中,均未发现异质性的证据 [4]。
4.3.4静脉应用糖蛋白Ⅱb/Ⅲa抑制剂

概要
糖蛋白 Ⅱb/Ⅲa 受体抑制剂是通过胃肠外途径给药的药物,它能阻止纤维蛋白原或血管性血友病因子与糖蛋白 Ⅱb/Ⅲa 受体结合,进而阻断血小板交联,以此来抑制血小板聚集。在现代抗血小板治疗和介入治疗策略出现之前,就已经开始对这些药物进行评估了,而且当时从发病到进行冠状动脉血运重建的时间要比现在长得多。因此,关于糖蛋白 Ⅱb/Ⅲa 受体抑制剂在接受强效 P2Y12抑制剂治疗的患者,以及在使用当代药物洗脱支架(与前代支架相比,其发生支架内血栓的风险更低)且更早接受经皮冠状动脉介入治疗(PCI)的患者中的应用数据有限。在当前的临床实践中,糖蛋白 Ⅱb/Ⅲa 受体抑制剂的应用主要局限于以下两种情况:一是用于血栓负荷较大的患者在 PCI 时的辅助治疗;二是作为 PCI 并发症(如无复流现象,或病变部位持续存在血栓、血栓复发等)的 “补救” 或 “挽救” 治疗 [1]。
指南推荐意见的相关支持性文本
1.在一项针对 452 例经过筛选的、大面积前壁 ST 段抬高型心肌梗死(STEMI)且血栓负荷较大的高危患者的研究中,冠状动脉内使用阿昔单抗作为辅助治疗,可降低血栓负荷并减小梗死面积 [1]。其他试验也表明,糖蛋白 Ⅱb/Ⅲa 受体抑制剂能够降低 STEMI 和非 ST 段抬高型急性冠状动脉综合征(NSTE - ACS)患者的冠状动脉内血栓负荷 [7,8]。因此,对于冠状动脉血栓负荷较大,或者出现无复流或慢血流(认为是由血栓远端栓塞所致)的患者,在进行经皮冠状动脉介入治疗(PCI)时可考虑使用糖蛋白 Ⅱb/Ⅲa 受体抑制剂。在比较糖蛋白 Ⅱb/Ⅲa 受体抑制剂静脉注射和冠状动脉内注射的临床试验中,临床结局、出血情况、血栓溶解情况以及梗死面积等方面总体上相似 [2,9,10]。
2.对于急性冠状动脉综合征(ACS)患者使用糖蛋白 Ⅱb/Ⅲa 受体抑制剂,已经评估了多种策略。这些药物的 “上游” 给药定义为:在确诊 ACS 后,在计划进行血管造影和经皮冠状动脉介入治疗(PCI)之前,早期给予小分子药物(依替巴肽或替罗非班)以稳定病情。在 EARLY - ACS(非 ST 段抬高型急性冠状动脉综合征患者早期糖蛋白 Ⅱb/Ⅲa 抑制)试验中,9406 例非 ST 段抬高型急性冠状动脉综合征(NSTE - ACS)患者被随机分组,一组在入院后 8 小时内常规进行依替巴肽的 “上游” 给药,另一组则是在 PCI 时按需进行依替巴肽的辅助给药。结果显示,缺血性结局并未得到改善反而出血风险增加。另一种方法是,对于 ST 段抬高型心肌梗死(STEMI)或非 ST 段抬高型急性冠状动脉综合征(NSTE - ACS)患者,在进行经皮冠状动脉介入治疗(PCI)时常规辅助使用糖蛋白 Ⅱb/Ⅲa 受体抑制剂。尽管在强效 P2Y12抑制剂应用之前开展的早期试验表明,这种方法能改善手术预后并减少围手术期心肌坏死,但在接受氯吡格雷预处理的患者中开展的此研究并未证实常规辅助使用糖蛋白 Ⅱb/Ⅲa 受体抑制剂能减少缺血性事件,反而增加了出血并发症 [5,11]。
4.4胃肠外抗凝治疗


概述
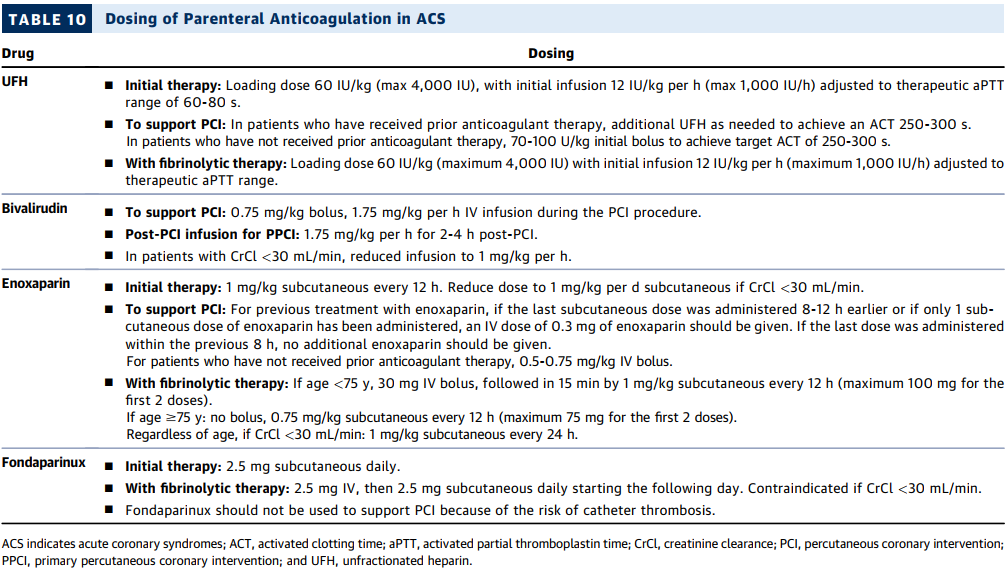
建议对所有急性冠状动脉综合征(ACS)患者进行胃肠外抗凝治疗,无论其初始治疗策略如何,目的是针对潜在的病理生理过程(冠状动脉粥样硬化血栓形成)进行治疗,并减少主要不良心血管事件(MACE)的风险再发(见表 10)。尽管可能最终会诊断重新分类(例如,诊断为其他非动脉粥样硬化血栓形成性的 ACS,如冠状动脉痉挛,或其他类似 ACS 的病症,如应激性心肌病或心肌炎),但初始胃肠外抗凝治疗旨在治疗疑似 1 型心肌梗死患者因动脉粥样硬化斑块破裂或糜烂所导致的血栓 [32]。抗凝策略应早期上游启动(在诊断时且在冠状动脉造影之前),以支持经皮冠状动脉介入治疗(PCI)或其他再灌注治疗。对于接受 PCI 的 ACS 患者,术中可能会发生凝血酶生成和血小板聚集,因此建议进行胃肠外抗凝治疗以降低血栓性并发症的风险 [33]。胃肠外抗凝药物的选择可能较为复杂,因为它会受到多种因素的影响,包括血管穿刺部位、肾功能以及是否同时使用其他抗血小板或抗凝药物。普通肝素(UFH)和低分子肝素都可能引发肝素诱导的血小板减少症(HIT);在这种情况下,阿加曲班和比伐卢定作为直接凝血酶抑制剂,是已知患有 HIT 患者可接受的替代抗凝药物 [34,35]。
指南推荐意见的相关支持性文本
1.传统上,普通肝素(UFH)一直是治疗非 ST 段抬高型急性冠状动脉综合征(NSTE - ACS)患者的首选抗凝药物 [1 - 4]。然而,其使用存在一些局限性,包括剂量反应不可预测,以及有诱发肝素诱导的血小板减少症(HIT)的风险 [33]。在不稳定型心绞痛方面,一项纳入了来自 6 项随机研究的 1353 例患者的荟萃分析显示,与仅使用阿司匹林治疗的患者相比,使用阿司匹林联合肝素治疗的患者在随机治疗期间发生心肌梗死(MI)或死亡的风险较低,尽管这种差异无统计学意义(相对风险为 0.67 [95% 置信区间为 0.44 - 1.02])[3]。在当前双联抗血小板治疗(DAPT)和早期血运重建的时代,尚未评估其与安慰剂相比的疗效 [33]。
2.磺达肝癸钠是一种合成的五糖,它能选择性地与抗凝血酶结合,从而快速且可预测地抑制凝血因子 Ⅹa 的活性,针对该药物开展了相关评估研究。在 OASIS - 5(急性缺血综合征治疗策略评估第五次组织研究)试验中 [5],磺达肝癸钠在 9 天时的缺血事件风险方面与依诺肝素相似,但它能减少严重出血。约 40% 的患者接受了经皮冠状动脉介入治疗(PCI),与依诺肝素相比,使用磺达肝癸钠时引导导管血栓形成率有所增加(0.9% 对 0.3%)。在非 ST 段抬高型急性冠状动脉综合征(NSTE - ACS)中,尽管有一些数据支持依诺肝素优于普通肝素(UFH)[11],但多项荟萃分析并未显示出其在疗效上明显优于 UFH [7,26,36]。一项对 5 项随机试验中 12171 例非 ST 段抬高型 ACS 患者进行的比较低分子肝素和 UFH 的荟萃分析显示,在死亡或心肌梗死发生率(2.2% 对 2.3%)以及严重出血风险方面,两者均无显著差异 [36]。
3.对于接受冠状动脉血运重建术(冠状动脉搭桥术 [CABG] 或经皮冠状动脉介入治疗 [PCI])的急性冠状动脉综合征(ACS)患者,在血运重建完成前均需进行胃肠外抗凝治疗。过早停用抗凝药物会导致凝血酶活性和活化蛋白 C 水平短暂反跳性升高,进而使缺血事件复发 [12,13],其中在停用抗凝药物后的最初 4 至 8 小时内,再梗死风险最高。
4.传统上,普通肝素(UFH)一直是支持非 ST 段抬高型急性冠状动脉综合征(NSTE - ACS)患者进行经皮冠状动脉介入治疗(PCI)时的首选抗凝药物。在经皮冠状动脉介入治疗(PCI)中,会使用活化凝血时间(ACT)来指导用药剂量 [37]。尽管普通肝素(UFH)的药代动力学效应并非总是可预测的,但其抗凝作用可通过给予鱼精蛋白来逆转。
5.比伐卢定是一种直接凝血酶抑制剂,已在非 ST 段抬高型急性冠状动脉综合征(NSTE - ACS)和 ST 段抬高型心肌梗死(STEMI)患者中进行了评估,可用于支持经皮冠状动脉介入治疗(PCI)。在 BRIGHT - 4(急诊经皮冠状动脉介入治疗 [PPCI] 期间比伐卢定延长全剂量输注与肝素对比)试验中 [15],该试验纳入了采用桡动脉途径(占 93%)进行 PPCI 的 STEMI 患者,以开放标签设计对比了比伐卢定与单用肝素的疗效。比伐卢定治疗方案包括标准的静脉推注和持续给药(先推注 0.75mg/kg,然后以每小时 1.75mg/kg 的速度持续输注),并在 PCI 术后以全剂量(每小时 1.75mg/kg)继续输注 2 至 4 小时。结果显示,术后采用全剂量比伐卢定持续输注在降低 30 天全因死亡或 BARC(学术研究联合会出血标准)3 - 5 型出血复合终点事件方面优于普通肝素(UFH)(4.39% 对 3.06%;P = 0.007)[15]。比伐卢定还降低了全因死亡风险(3.92% 对 2.96%;P = 0.04),以及 30 天支架内血栓形成风险(0.37% 对 1.1%;P = 0.0015)。基于这些研究结果,当使用比伐卢定支持 STEMI 患者的 PPCI 时,建议在术后以全剂量持续输注 2 至 4 小时 [15,38,39]。
6.对急性冠状动脉综合征(ACS)患者使用比伐卢定与普通肝素(UFH)(联合或不联合糖蛋白 Ⅱb/Ⅲa 受体抑制剂)进行比较的荟萃分析显示,使用比伐卢定可降低严重出血的风险 [16,17,40]。在非 ST 段抬高型急性冠状动脉综合征(NSTE - ACS)中,比伐卢定在 ACUITY(急性冠状动脉综合征中阿加曲班与肝素的比较)试验中进行了评估。在该试验中,就主要不良心血管事件(MACE)风险而言,比伐卢定不劣于普通肝素(UFH)联合糖蛋白 Ⅱb/Ⅲa 受体抑制剂,并且在降低 30 天严重出血风险方面更具优势 [41]。该研究中使用的出血定义是专门针对 ACUITY 试验设定的。比伐卢定还在 MATRIX(通过桡动脉入路和系统性应用阿加曲班减少不良出血事件)试验中进行了评估,该试验将比伐卢定与单用 UFH(即不联合使用糖蛋白 Ⅱb/Ⅲa 受体抑制剂)进行了对比 [42]。在 30 天的缺血或出血事件方面,两组之间未观察到显著差异。
7.在急诊经皮冠状动脉介入治疗(PPCI)的场景下,与普通肝素(UFH)相比,静脉注射依诺肝素能降低缺血性结局的风险,且在出血风险方面无显著差异。在 ATOLL(随访急性心肌梗死行急诊血管成形术治疗,术中静脉注射依诺肝素或普通肝素的短期和长期的缺血及出血事件)试验中 [24],该试验纳入了 ST 段抬高型心肌梗死(STEMI)患者。主要终点为 30 天时死亡、心肌梗死并发症、手术失败或严重出血的发生率。依诺肝素组该发生率为 28%,而 UFH 组为 34%(P = 0.06)。虽然依诺肝素组和 UFH 组在主要终点发生率上无显著差异,但依诺肝素组 30 天时死亡、急性冠状动脉综合征(ACS)复发或紧急血运重建这一次要终点的发生率显著更低(7% 对 11%;P = 0.015)。此外,与 UFH 相比,依诺肝素具有显著的净临床获益(死亡、心肌梗死并发症或严重出血)(10% 对 15%;P = 0.03)。在一项针对 10451 例患者的荟萃分析中,静脉注射依诺肝素可显著降低死亡和严重出血的发生率 [26]。
8.由于存在导管血栓形成的风险,磺达肝癸钠不应作为支持经皮冠状动脉介入治疗(PCI)的唯一抗凝药物 [5,27,31]。在 OASIS - 5 试验中,与依诺肝素相比,使用磺达肝癸钠时导管相关血栓形成率有所增加(0.9% 对 0.4%)[5]。在 OASIS - 6(ST 段抬高型心肌梗死患者中磺达肝癸钠与对照治疗的安全性和有效性比较)试验中也观察到了类似结果,即在 PCI 过程中使用磺达肝癸钠时,引导导管血栓形成率更高,且冠状动脉并发症更多 [27]。
9.在接受溶栓治疗的 ST 段抬高型心肌梗死(STEMI)患者中,建议在溶栓治疗前后进行胃肠外抗凝治疗,以减少缺血性事件的发生。在诸如 GUSTO(全球应用链激酶和组织型纤溶酶原激活剂治疗冠状动脉闭塞)试验、ASSENT - 3(评估新溶栓方案的安全性和有效性)试验或 ExTRACT - TIMI 25(依诺肝素与溶栓再灌注治疗急性心肌梗死 - 心肌梗死溶栓试验 25)研究等溶栓治疗的研究中,静脉注射肝素的疗程至少为 48 小时 [10,29,43]。在 ExTRACT - TIMI 25 研究中,普通肝素(UFH)至少静脉滴注 48 小时,也可由主治医生根据情况决定延长使用时间;而皮下注射依诺肝素则持续至患者出院或最长使用 8 天(出院时间或最长使用时间为准)[10]。与 UFH 组相比,随机分配至依诺肝素组的患者在 30 天内死亡或非致命性复发性心肌梗死(MI)的风险更低(9.9% 对 12.0%);然而,使用依诺肝素治疗会增加严重出血的风险(2.1% 对 1.4%)[10]。
10.对于接受溶栓治疗且不打算进行有创治疗的 ST 段抬高型心肌梗死(STEMI)患者,相较于普通肝素(UFH),依诺肝素是更优选的抗凝药物 [9,10,28,29,44]。在 ExTRACT - TIMI 25 研究中,对 20506 例接受溶栓治疗的 STEMI 患者进行了研究。其中一组患者使用依诺肝素,持续至出院或最长使用 8 天(以先到者为准);另一组患者使用 UFH,至少静脉滴注 48 小时,也可由主治医生根据情况决定延长使用时间 [10]。研究的主要终点为 30 天内死亡或非致命性复发性心肌梗死(MI)的发生率。UFH 组的发生率为 12%,而依诺肝素组为 9.9%。在一项包含 14 项随机试验的荟萃分析中,对于接受溶栓治疗的患者,UFH 并不能降低再梗死率或死亡率。相反,与安慰剂相比,低分子肝素能降低再梗死和死亡风险,同时也能降低再梗死的风险 [45]。
11.对于不太可能接受有创治疗的 ST 段抬高型心肌梗死(STEMI)患者,磺达肝癸钠是一种可供选择的替代抗凝药物。在 OASIS - 6 试验中,研究对象为接受溶栓药物(主要是链激酶)治疗的 STEMI 患者。与安慰剂或普通肝素(UFH)相比,磺达肝癸钠显著降低了 30 天内死亡或再梗死这一主要终点事件的发生风险,其中包括显著降低死亡率、再梗死率以及严重出血发生率 [27,30]。
4.5血脂管理
概要
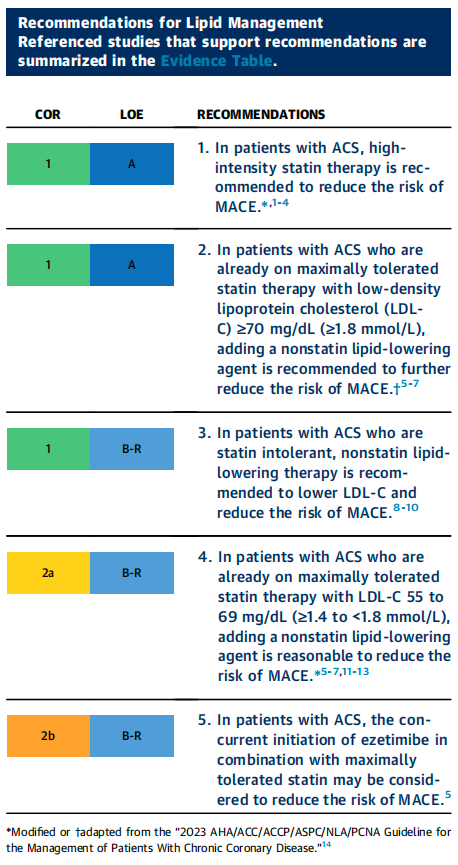
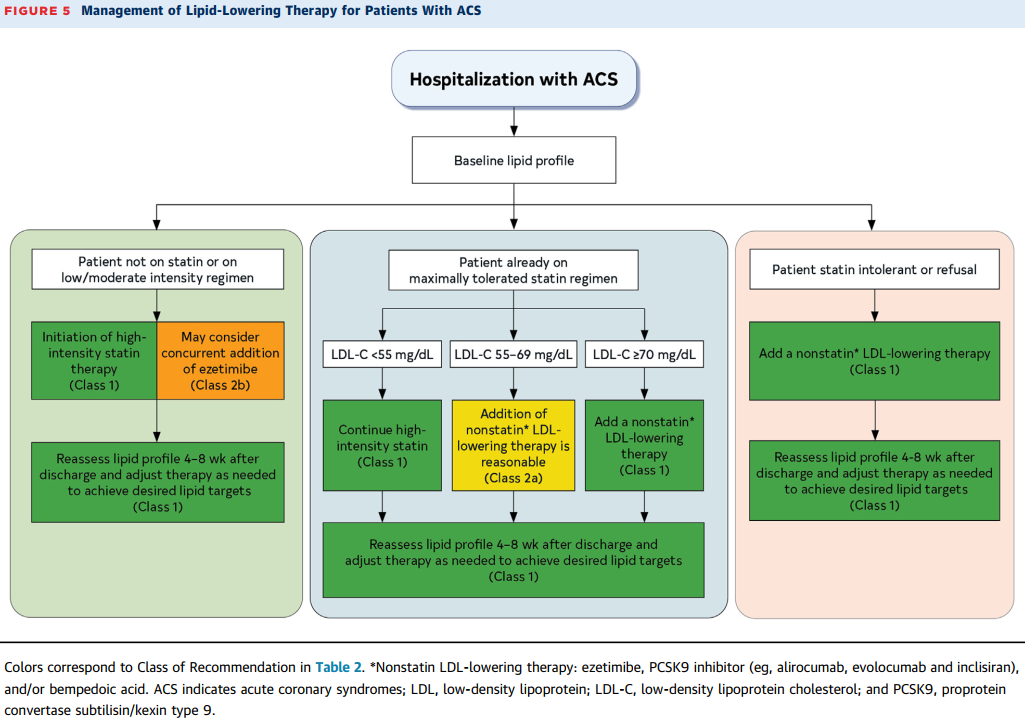
当前的建议主要聚焦于近期(即 12 个月内)发生急性冠状动脉综合征(ACS)的患者。2023 年美国心脏协会(AHA)/ 美国心脏病学会(ACC)/ 美国胸科医师学会(ACCP)/ 预防心血管疾病专业协会(ASPC)/ 美国国家脂质协会(NLA)/ 预防心血管病护士协会(PCNA)发布的心血管疾病(CCD)指南,针对既往有 ACS 病史患者的血脂长期管理给出了更为详细的建议 [14]。近期发生 ACS 的患者,其动脉粥样硬化性心血管疾病(ASCVD)事件发生率显著高于患有 CCD 的患者,据估计,其 1 年内发生心血管死亡、心肌梗死(MI)和缺血性中风的概率在 10% 至 15%。急性冠状动脉综合征(ACS)患者住院后,其动脉粥样硬化性心血管疾病(ASCVD)事件发生率显著高于患有心血管疾病(CCD)的患者。据估计,ACS 患者在住院后的 1 年内发生心血管死亡、心肌梗死(MI)和缺血性中风的概率在 10% - 15%[15,16]。与 CCD 患者相比,ACS 患者更高的风险支持为近期发生 ACS 的患者设定更积极的低密度脂蛋白胆固醇(LDL - C)目标(图 5)[14 - 16]。随机对照试验(RCTs)已经证明,通过多种不同的药物治疗方法降低 LDL - C 水平可减少 ASCVD 事件,且获益程度与 LDL - C 水平降低的程度成正比 [17]。在 ACS 患者中,RCTs 显示,与中等强度他汀类药物治疗相比,高强度他汀类药物治疗在降低主要不良心血管事件(MACE)方面有额外的获益 [1 - 4]。对于采用最大耐受剂量他汀类药物治疗仍未达到 LDL - C 治疗目标,或对他汀类药物不耐受的患者,有几种非他汀类疗法可供选择,包括依折麦布、前蛋白转化酶枯草溶菌素 /(PCSK9)单克隆抗体和苯扎贝特酸。这些疗法在不同人群中既能降低 LDL - C 水平,又能改善 ASCVD 结局 [5 - 10]。英克司兰也可通过阻止 PCSK9 信使核糖核酸(mRNA)的翻译来降低 LDL - C 水平,但目前尚无相关临床结局研究(表 12)。尽管如此,降低 LDL - C 治疗的相对获益预计与观察到的 LDL - C 水平降低程度成正比(表 11 和表 12)[5 - 11]。建议在 ACS 发作后尽快进行血脂检测(图 5),因为从症状发作 24 小时后 LDL - C 水平会略有下降 [18]。出院后的血脂管理将在第 11.2 节 “出院后血脂水平的重新评估” 中讨论。
指南推荐意见的相关支持性文本
1.高强度他汀类药物治疗方案平均可使低密度脂蛋白胆固醇(LDL - C)浓度降低 50%(表 11)。胆固醇治疗试验协作组(CTT)对 5 项随机对照试验(RCTs)进行的荟萃分析显示,在冠状动脉疾病(CAD)患者中,与中等强度他汀类药物相比,高强度他汀类药物降低 LDL - C 浓度可使主要血管事件减少约 15%[4]。对 A to Z(Aggrastat to Zocor)试验和 PROVE IT(普伐他汀或阿托伐他汀评估和感染治疗) - TIMI 22 试验(这两项试验均针对急性冠状动脉综合征(ACS)后早期病情稳定的患者开展)的个体参与者荟萃分析表明,与低强度他汀类药物治疗方案相比,高强度他汀类药物治疗方案可显著降低心血管死亡和全因死亡风险 [19]。高强度他汀类药物治疗方案在 ACS 发生后不久即可显现益处,且这种益处会持续存在 [3]。ACS 后使用高强度他汀类药物的益处似乎与似乎与基线低密度脂蛋白胆固醇(LDL - C)浓度无关。在使用他汀类药物或其他降脂疗法使 LDL - C 浓度降至非常低的水平时,并未观察到任何安全方面的担忧。因此,对于能够耐受治疗的患者,在随访期间不应降低高强度他汀类药物的治疗强度 [13]。
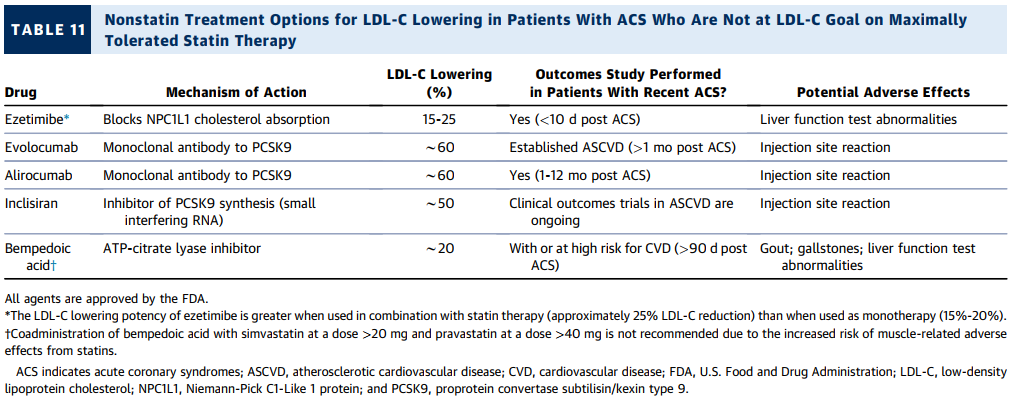
2.当前有多种治疗选择可与最大耐受剂量的他汀类药物联合使用,以帮助急性冠状动脉综合征(ACS)患者达到理想的低密度脂蛋白胆固醇(LDL - C)目标(表 12)。在 IMPROVE IT(改善预后;维妥立国际疗效试验)研究中,对于 ACS 发作后 10 天内的患者,在每日服用 40mg 辛伐他汀的基础上加用依折麦布,经过中位时间为 6 年的随访,主要不良心血管事件(MACE)有小幅但显著的降低 [5]。在包括急性冠状动脉综合征(ACS)发作 1 个月以上患者在内的研究中,随访中位时间 2 - 3 年,PCSK9 抑制剂可使主要不良心血管事件(MACE)的相对风险降低 15%[6,7,20]。研究表明,在更接近 ACS 发作时开始使用 PCSK9 抑制剂的患者能获得更大的绝对获益 [20,21]。依洛尤单抗能在 ACS 发生后早期有效降低低密度脂蛋白胆固醇(LDL - C)水平,并且在非 ST 段抬高型心肌梗死(NSTEMI)患者中,通过冠状动脉内成像技术可观察到斑块成分出现了有益的改变 [22 - 24]。对于接受阿利西尤单抗治疗的急性心肌梗死(AMI)患者,冠状动脉内成像也显示斑块有更明显的消退 [25]。英克司兰是一种靶向 PCSK9 蛋白合成的小干扰 RNA 药物,初始剂量给药后,每 6 个月给药一次。英克司兰可使 LDL - C 水平降低约 50%,且耐受性良好 [26],但目前尚无临床结局研究。苯扎贝特酸作用于肝脏中他汀类药物作用位点的上游,可使 LDL - C 水平降低约 20%。对于他汀类药物不耐受的患者,在 ACS 发作 90 天后开始使用苯扎贝特酸,可使 MACE 降低 13%[10]。
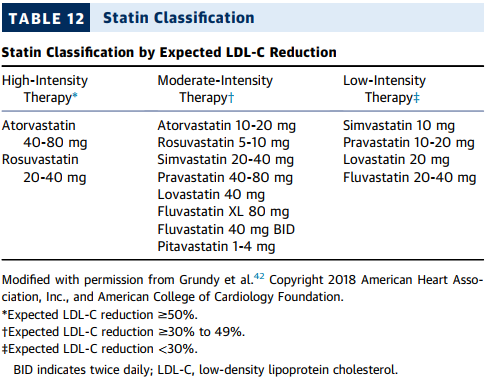
3.在临床实践中,他汀类药物不耐受的情况较为常见,最常报告的原因是他汀相关的肌肉症状 [27]。要认定患者存在他汀类药物不耐受,至少应尝试使用两种他汀类药物,其中至少一种要采用获批的最低日剂量 [28]。目前,对于完全或部分不耐受他汀类药物治疗的患者,可供选择的药物包括依折麦布、PCSK9 抑制剂单克隆抗体、英克司兰和贝派地酸。研究已证实,依折麦布和 PCSK9 抑制剂在他汀不耐受患者中使用安全且耐受性良好,还能改善血脂参数 [8,9]。然而,目前尚无关于这些药物在他汀不耐受患者中单独使用或联合使用的结局研究。苯扎贝特酸是一种 ATP 柠檬酸裂解酶抑制剂,可使低密度脂蛋白胆固醇(LDL - C)水平降低 15% - 25%,且肌肉相关不良反应的发生率较低 [29,30]。一种将贝派地酸与依折麦布制成的复方制剂可使 LDL - C 水平降低约 35%[31]。在 CLEAR Outcomes(通过贝派地酸,一种 ACL 抑制方案降低胆固醇)试验中,将贝派地酸与安慰剂在不耐受他汀类药物且患有或有高风险发生动脉粥样硬化性心血管疾病(ASCVD)的患者中进行了对比。随机分组前 90 天内发生过急性冠状动脉综合征(ACS)的患者被排除在该试验之外。入组时患者的平均 LDL - C 水平为 139mg/dL,与安慰剂组相比,贝派地酸组的 LDL - C 水平降低了 29mg/dL。贝派地酸组的主要不良心血管事件(MACE)降低了 13%。不过,在试验中,一小部分患者使用贝派地酸后尿酸水平升高,同时肝功能检查异常、痛风和胆结石的发生率也有所增加 [10]。
4.在 IMPROVE IT 试验中,研究人员将急性冠状动脉综合征(ACS)后低密度脂蛋白胆固醇(LDL - C)水平在 50mg/dL 至 125mg/dL(若正在接受降脂治疗则为≤100mg/dL)的患者随机分组,一组接受辛伐他汀(40mg)与依折麦布(10mg)联合治疗,另一组接受辛伐他汀(40mg)与安慰剂治疗(即辛伐他汀单药治疗),入组时患者的中位 LDL - C 水平为 69.5mg/dL。与安慰剂组相比,加用依折麦布使主要不良心血管事件(MACE)的相对风险降低了 6.4%[5]。基线 LDL - C 水平在 50 至 70mg/dL 的患者与 LDL - C 水平≥70mg/dL 的患者所获得的益处相似 [32]。FOURIER(高危受试者 PCSK9 抑制进一步心血管结局研究)和 ODYSSEY OUTCOMES(急性冠状动脉综合征后阿利西尤单抗治疗期间心血管结局评估)试验纳入了 LDL - C 水平≥70mg/dL 的患者,因此并未专门评估在 LDL - C 水平为 55 至 70mg/dL 的患者中加用 PCSK9 抑制剂治疗的结局 [6,7]。然而,这两项试验的二次分析均显示,LDL - C 降至 < 50mg/dL 的患者比 LDL - C 水平≥50mg/dL 的患者结局更好,且呈单调关系,这表明即使 LDL - C 水平远低于 50mg/dL,随着 LDL - C 水平的逐步降低,患者的结局也会更好 [11,12]。在使用 PCSK9 抑制剂使 LDL - C 降至极低水平的患者中,神经认知事件和肌肉事件(包括出血性中风)的发生率并未增加 [11,12]。长期随访研究支持在二级预防中使用 PCSK9 抑制剂使 LDL - C 达到并维持在极低水平数年后仍具有持续的获益和安全性 [33]。依折麦布和 PCSK9 抑制剂在既往有 ACS 且合并糖尿病、患有更严重的冠状动脉疾病或多血管疾病,或生物标志物升高的高危患者中似乎能带来更大的益处 [20,34 - 41]。
5.依折麦布通过阻断胆固醇经尼曼匹克C1样1蛋白(NPC1L1)从胃肠道的吸收,可使低密度脂蛋白胆固醇(LDL - C)水平降低 15% 至 25%。“改善预后(IMPROVE IT)” 试验对过去 10 天内因急性冠状动脉综合征(ACS)住院的患者开展研究,对比了辛伐他汀(40 毫克)与依折麦布(10 毫克)联合治疗(辛伐他汀 - 依折麦布组)和辛伐他汀(40 毫克)加安慰剂治疗(辛伐他汀单药治疗组)的效果。从 ACS 发生到随机分组的中位时间为 5 天,34% 的患者在 ACS 发作时已经在服用他汀类药物。经过中位时长 6 年的随访,与安慰剂组相比,加用依折麦布使主要不良心血管事件(MACE)的相对风险降低了 6.4%(风险比为 0.936,95% 置信区间为 0.89 - 0.99)。依折麦布耐受性良好,与安慰剂组相比,不良事件的发生情况无明显差异 [5]。
4.6β - 受体阻滞剂治疗

β 受体阻滞剂通过降低心率、血压和心肌收缩力来减少心肌氧需求 [1,3]。对于左心室射血分数(LVEF)<40% 且病情稳定的心力衰竭患者,包括心肌梗死后患者,β 受体阻滞剂的临床益处已得到充分证实 [3 - 5]。大多数关于在 ST 段抬高型心肌梗死(STEMI)中早期使用 β 受体阻滞剂治疗的随机对照试验(RCT)数据是在再灌注治疗时代之前开展的 [3]。目前尚未有足够样本量的 RCT 研究专门探讨非 ST 段抬高型急性冠状动脉综合征(NSTE - ACS)患者住院期间使用 β 受体阻滞剂的临床益处。虽然大多数研究是在 STEMI 患者中进行的,但对于大多数无禁忌证(例如急性心力衰竭 [Killip 分级 II - IV 级]、有低心输出量状态的证据或有发生心源性休克的风险、PR 间期 > 0.24 毫秒、无心脏起搏器的二度或三度心脏传导阻滞、严重心动过缓、活动性支气管痉挛)的 ACS 患者,建议在住院早期(24 小时内)开始使用 β 受体阻滞剂治疗 [1,2,6]。初诊时存在 β 受体阻滞剂治疗禁忌证的患者,在 24 小时后可重新评估,如果初始禁忌证已消除,则可开始口服 β 受体阻滞剂治疗。有必要进一步研究 β 受体阻滞剂在 NSTE - ACS 患者中的益处。尽管一项开放标签的随机试验对接受冠状动脉血运重建且左心室(LV)功能保留的 ACS 患者出院后长期使用 β 受体阻滞剂治疗的益处提出了质疑 [7],但这一领域仍在研究之中。
指南推荐意见的相关支持性文本
1.来自再灌注治疗前时代和早期再灌注治疗时代的随机对照试验(RCTs)均显示,ST 段抬高型心肌梗死(STEMI)患者早期启动 β 受体阻滞剂治疗可降低再梗死和室性心律失常的风险 [1 - 3]。“心肌梗死氯吡格雷和美托洛尔试验(COMMIT)” 纳入了 45852 例患者(约 50% 接受了溶栓治疗,7% 为非 ST 段抬高型急性冠状动脉综合征 [NSTE - ACS] 患者),结果表明,与安慰剂组相比,早期大剂量使用美托洛尔(即静脉注射高达 15 毫克,随后每日口服 200 毫克)可降低再梗死和心室颤动的风险,但会增加心源性休克的风险,且心源性休克主要发生在最初的 24 小时内 [1]。在一项针对 801 例接受经皮冠状动脉介入治疗(PPCI)的 STEMI 患者的小型开放标签试验中,卡维地洛在 3 年内并未降低主要不良心血管事件(MACE)的发生率,但该试验样本量不足,可能无法检测出差异 [8]。总体而言,现有证据倾向于建议,对于无禁忌证的急性冠状动脉综合征(ACS)患者,确诊后应尽早(<24 小时)开始使用低剂量口服 β 受体阻滞剂,并根据血压和心率情况缓慢增加剂量。若患者出现新发或加重的心力衰竭症状,或有心源性休克的体征,则应停用 β 受体阻滞剂。对于血流动力学稳定且无急性心力衰竭的 STEMI 患者,若仍有症状或有临床用药指征,可在再灌注治疗前静脉使用 β 受体阻滞剂。但由于在经皮冠状动脉介入治疗(PPCI)前静脉使用 β 受体阻滞剂对梗死面积或临床结局是否有有利影响尚无一致结果,因此现有证据不支持在 PPCI 前常规使用静脉 β 受体阻滞剂 [9,10]。对于左心室射血分数(LVEF)保留的患者,β 受体阻滞剂的最佳使用时长仍不明确。尽管一项随机试验未证实,对于接受冠状动脉血运重建且左心室功能保留的低风险患者,出院后继续使用 β 受体阻滞剂有长期获益 [7],但该领域仍有更多研究正在进行中。
4.7 肾素血管紧张素醛固酮系统
概述
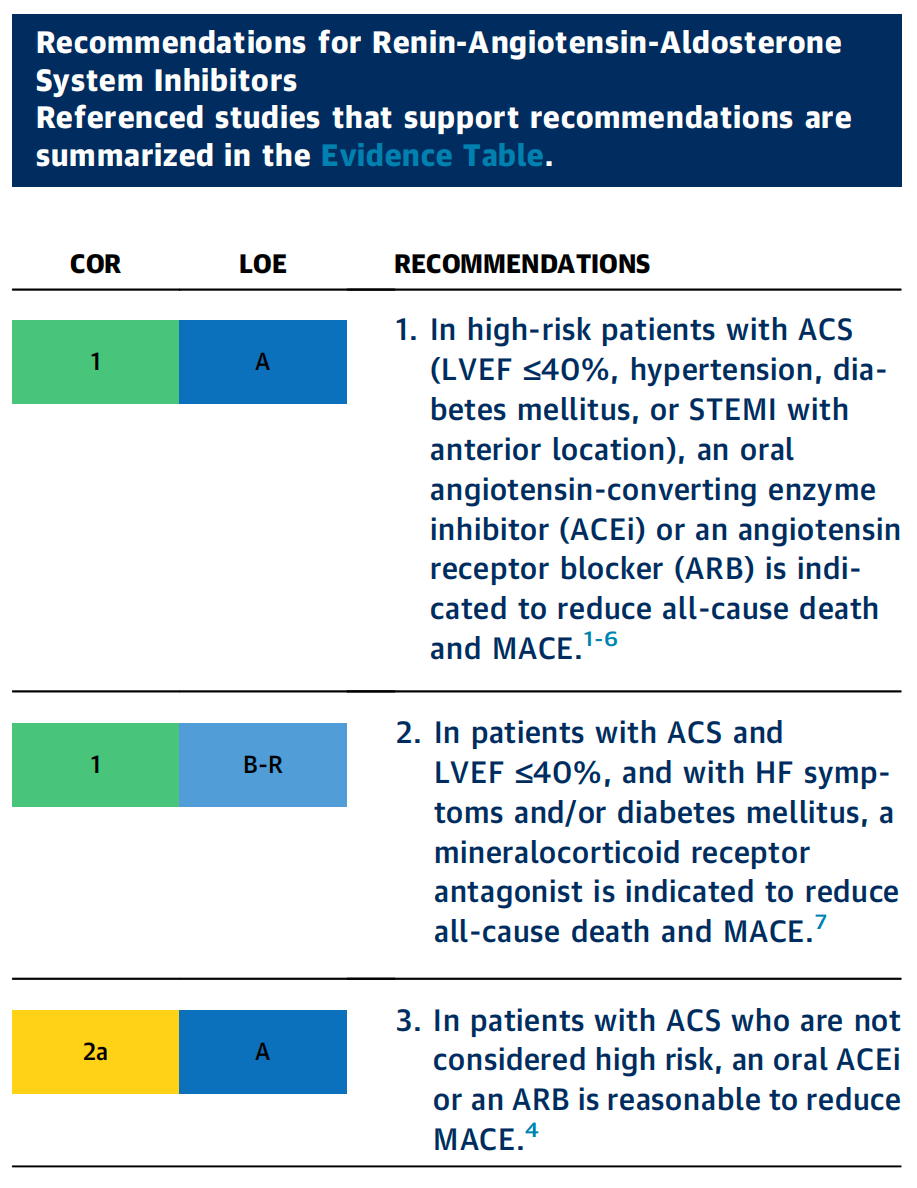
口服血管紧张素转换酶抑制剂(ACEI)可降低 ST 段抬高型心肌梗死(STEMI)或非 ST 段抬高型心肌梗死(NSTEMI)患者的全因死亡率和主要不良心血管事件(MACE)发生率,尤其当患者伴有高危特征(左心室射血分数 [LVEF]≤40%、高血压、糖尿病或前壁 STEMI)时 [1 - 4,6]。即使是无高危特征的急性心肌梗死(AMI)患者,使用口服 ACEI 也能带来一定的生存获益 [4]。与 ACEI 相比,血管紧张素 Ⅱ 受体拮抗剂(ARB)在伴有心力衰竭(HF)或左心室收缩功能障碍的 AMI 患者中的获益相似 [5]。因此,若无禁忌证,应在合适的 AMI 患者中启动口服 ACEI 或 ARB 治疗 [5,8]。对于 LVEF≤40%、伴有 HF 症状和 / 或糖尿病的 AMI 患者,加用盐皮质激素受体拮抗剂(MRA)可降低全因死亡率和 MACE 发生率。若患者无晚期慢性肾脏病、高钾血症或其他禁忌证,则应给予 MRA 治疗。对于有症状的心力衰竭(HF)且左心室射血分数(LVEF)降低的患者,研究已证实,沙库巴曲缬沙坦在降低心血管死亡或因心力衰竭住院风险方面优于血管紧张素转换酶抑制剂(ACEI);然而,该试验排除了急性冠状动脉综合征(ACS)发生后 3 个月内的患者 [9]。在一项针对心肌梗死(MI)早期、LVEF ≤ 40% 和 / 或存在肺淤血患者的试验中,与 ACEI 相比,沙库巴曲缬沙坦并未显著降低心血管死亡或新发心力衰竭的风险。使用沙库巴曲缬沙坦时低血压事件更为常见,但未观察到其他安全问题。因此,如果计划使用沙库巴曲缬沙坦治疗射血分数降低的心力衰竭,在心肌梗死后早期用这种复方制剂替代 ACEI 或血管紧张素 Ⅱ 受体拮抗剂(ARB)似乎是安全的 [10]。
指南推荐意见的相关支持性文本
1.随机对照试验已证实,对于左心室射血分数(LVEF)≤40% 的急性心肌梗死(AMI)患者以及前壁 ST 段抬高型心肌梗死(STEMI)患者,加用口服血管紧张素转换酶抑制剂(ACEI)可降低全因死亡率和主要不良心血管事件(MACE)的发生率 [1,3]。一项针对 98496 例 AMI 患者的个体患者荟萃分析也显示,使用 ACEI 可带来生存获益,其中高血压、糖尿病和前壁 STEMI 患者的绝对获益最大 [4]。在 “缬沙坦治疗急性心肌梗死试验(VALIANT)” 中,针对伴有左心室收缩功能障碍和 / 或心力衰竭(HF)症状的 AMI 患者,使用血管紧张素 Ⅱ 受体拮抗剂(ARB)在统计学上不劣于 ACEI,且两组的全因死亡率相似 [5]。由于与单独使用任一种药物相比,同时启动 ACEI 和 ARB 治疗会增加不良事件的发生风险,却没有额外获益,因此应避免在 AMI 患者中同时使用这两种药物 [5,8]。
2.在 “依普利酮治疗急性心肌梗死后心力衰竭疗效与生存研究(EPHESUS)” 试验中,对于左心室射血分数(LVEF)≤40%、同时伴有心力衰竭(HF)症状和或糖尿病的急性心肌梗死(AMI)患者,在平均 16 个月的随访期间,盐皮质激素受体拮抗剂依普利酮降低了全因死亡率和主要不良心血管事件(MACE)的发生率。该人群中基于循证医学的治疗方法应用比例相对较高,入组时 86% 的患者使用了血管紧张素转换酶抑制剂(ACEI)或血管紧张素 Ⅱ 受体拮抗剂(ARB),75% 的患者使用了 β 受体阻滞剂 [7]。患有晚期慢性肾脏病(血清肌酐 > 2.5mg/dL)或高钾血症(血清钾 > 5.0mmol/L)的患者被排除在入组之外 [7]。在一项针对 1012 例无 HF 病史的急性 ST 段抬高型心肌梗死(STEMI)患者的试验中,与安慰剂组相比,使用依普利酮降低了主要终点事件的发生率,但这种获益在很大程度上是由于利钠肽水平的降低所致的 [11]。
3.收集血管紧张素转换酶抑制剂(ACEI)应用心肌梗死组,对 98496 例急性心肌梗死(AMI)患者进行的荟萃分析显示,接受 ACEI 治疗的 AMI 患者 30 天死亡率为 7.1%,而接受安慰剂治疗的AMI患者 30 天死亡率为 7.6%(死亡比例降低 7%,95% 置信区间为 2% - 11%;P = 0.004),并且这种获益似乎与基线风险无关 [4]。与安慰剂相比,使用 ACEI 还降低了非致命性心力衰竭的发生风险 [4]。
5.STEMI管理 再灌注策略
5.1 STEMI区域性救治

概述
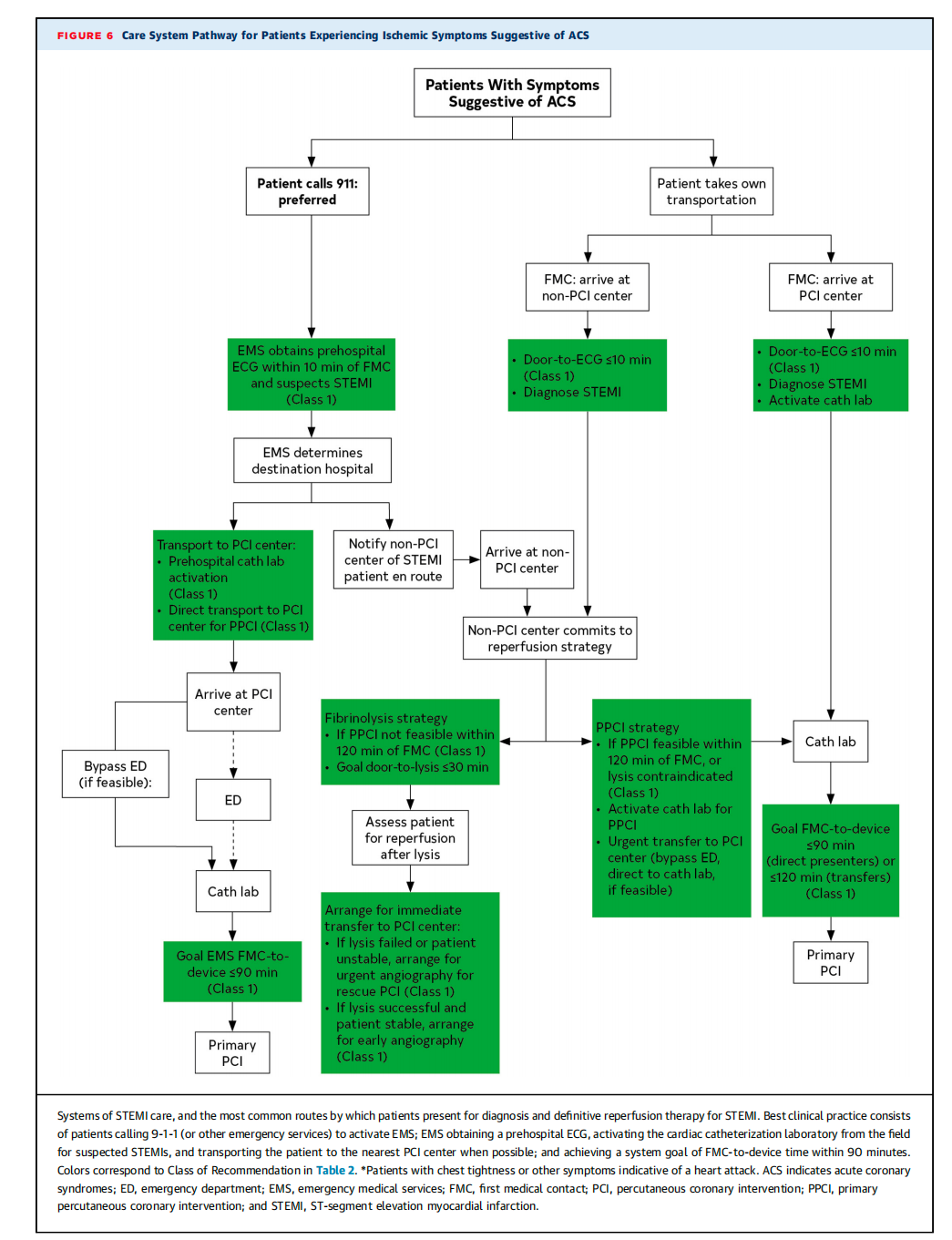
优化 ST 段抬高型心肌梗死(STEMI)患者预后的目标,不仅依赖于高效执行 STEMI 的救治流程,还依赖于各照护团队之间无缝的沟通与协作。因此,每个社区的目标是确保对每一位 STEMI 患者做出协调一致的响应,无论患者发病时身处何处,以尽量缩短总缺血时间。要建立并维持一个成功的 STEMI 救治体系,需要详细规划 STEMI 患者可能的所有就诊途径,确保无论是在具备经皮冠状动脉介入治疗(PCI)能力的机构还是不具备 PCI 能力的机构,患者都能得到诊断和确切的再灌注治疗,同时还能获得心脏外科治疗及其他高级治疗方式(如图 6 所示)。STEMI 区域救治体系的众多利益相关方(包括医院、急救医疗服务(EMS)公司、区域公共卫生部门和地方政府)必须确保 STEMI 救治体系的各个组成部分协调运作,避免救治流程出现漏洞,以帮助改善社区内 STEMI 患者的预后。
指南推荐意见的相关支持性文本
全球多项实施前后对比研究表明,建立协调的 ST 段抬高型心肌梗死(STEMI)区域救治体系可缩短再灌注时间,并提高 STEMI 患者的生存率 [1 - 6]。在过去 15 年里,STEMI 患者从首次医疗接触(FMC)到再灌注的时间显著缩短,且再灌注时间的改善与患者预后的改善相关 [5,7]。遗憾的是,近期有报道称,达到既定 STEMI 绩效指标的比例有所下降 [8],部分原因是新冠疫情以及在确保急救医疗服务(EMS)机构和医院有足够资源和人员配置方面面临的相关挑战。因此,所有社区都应继续建立、重振和维护 STEMI 区域救治体系,以改善全球 STEMI 患者的预后。在救治的每个阶段收集高质量数据是 STEMI 救治体系不可或缺的一部分。成功的 STEMI 救治体系具备强大的机制,用于:1)向公众宣传,出现缺血症状时应立即拨打 9 - 1 - 1(或当地其他合适的紧急救援电话),而不要自行前往最近的医院;2)数据收集应在确保充分捕获数据的同时,避免造成数据负担过重;3)在医院各科室(如急诊科和心内科)之间或医院与 EMS 机构之间进行数据共享;4)召开会议,在本地和系统层面审查和讨论共享数据,以推动流程改进。
5.2 具备经皮冠状动脉介入治疗(PCI)能力的医院进行再灌注治疗
5.2.1. STEMI患者直接经皮冠状动脉支架介入术
概述
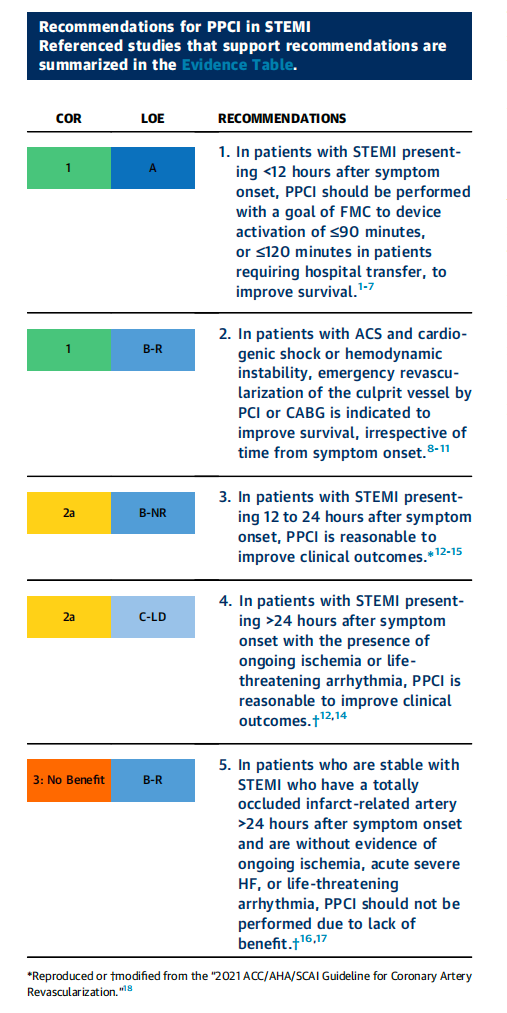
对于 ST 段抬高型心肌梗死(STEMI)患者而言,与将溶栓治疗作为主要的再灌注治疗手段相比,及时进行直接经皮冠状动脉介入治疗(PPCI)可提高患者生存率 [6,7]。旨在缩短 STEMI 患者接受 PPCI 治疗时间的医疗救治体系,对于降低患者早期死亡风险具有重要意义 [19,20]。目标是在确诊 STEMI 后尽快实施 PPCI,对于自行来院就诊以及由急救医疗服务(EMS)转运的患者,从首次医疗接触(FMC)到首次器械操作启动应在 90 分钟内完成;对于从不具备 PCI 能力的医疗机构转诊的患者,这一时间应在 120 分钟内完成 [1 - 7]。对于症状发作超过 12 小时的患者,PPCI 的获益开始减少,但在症状发作后约 24 小时内进行 PPCI 似乎仍有持续的益处 [12,13]。对于症状发作超过 48 小时且冠状动脉已闭塞的病情稳定、无症状的患者,在不存在持续心肌缺血的情况下,常规 PCI 尚未显示出益处;对于症状发作后 24 至 48 小时之间的无症状 STEMI 患者,常规 PCI 的相对有效性尚未得到严格验证 [14,15]。然而,对于延迟就诊且仍有持续心肌缺血的体征和症状(包括心源性休克、急性严重心力衰竭、持续性心绞痛和危及生命的心律失常)的患者,应考虑进行冠状动脉血运重建。
指南推荐意见的相关支持性文本
1. 对于伴有缺血症状的 ST 段抬高型心肌梗死(STEMI)患者,若能在首次医疗接触(FMC)至首次器械启动时间在 90 分钟内完成直接经皮冠状动脉介入治疗(PPCI),或者对于转诊患者在 120 分钟内完成,PPCI 是推荐的再灌注治疗方法,这样可提高患者生存率 [1-7]。2006 年美国心脏协会(AHA)推出了 “使命:生命线” 项目,该项目涉及急救医疗服务(EMS)人员以及临床医生(如急诊医学科医生、心内科医生、护士等),通过实施针对性的细化项目和区域化医疗服务 [21],促进了 PPCI 在实现这些目标方面的成功。这不仅改善了心肌挽救情况,还降低了死亡风险和不良结局的发生几率 [4,22,23]。当患者所在医院不具备 PCI 能力,且预计转送至具备 PCI 能力的医院的时间超过 120 分钟时,才会使用溶栓治疗,但 PPCI 优于溶栓治疗。与存在类似治疗延迟的溶栓治疗相比,PPCI 能使梗死相关动脉更易开通,恢复心肌梗死溶栓治疗(TIMI)3 级心外膜血流分级,并且复发性心肌缺血、再梗死、紧急重复血运重建手术、颅内出血和死亡的发生率更低 [6,7]。与经股动脉途径相比,经桡动脉途径进行 PPCI 进一步降低了死亡率,减少了穿刺部位出血,降低了输血需求,并减少了急性肾损伤的发生(详见第 7.1 节 “PCI 的血管入路选择”)[24,25]。
2. 1999 年报道的 “心源性休克时是否应紧急对阻塞冠状动脉进行血运重建(SHOCK)” 试验中,患有急性心肌梗死(AMI)和心源性休克的患者被随机分配接受药物治疗或紧急血运重建治疗。在被随机分配接受血运重建治疗的患者中,64% 的患者接受经皮冠状动脉介入治疗(PCI),36% 的患者接受冠状动脉旁路移植术(CABG)。从随机分组到接受血运重建治疗的中位时间,PCI 为 0.9 小时,CABG 手术为 2.7 小时。尽管在 30 天的主要终点死亡率方面没有显著差异,但无论是采用 PCI 还是 CABG 手术进行紧急血运重建,都降低了 6 个月时的死亡率 [9],并且这种降低死亡率的益处一直持续到 1 年和 6 年 [26,27]。在 “ST 段抬高型心肌梗死的反馈干预和治疗时间(FITT - STEMI)” 试验的一项观察性分析中,对于心源性休克患者,从首次医疗接触(FMC)后 60 分钟起,每延迟 10 分钟进行直接 PCI(PPCI),每 100 名患者中就会额外增加3至4例死亡,且若从 FMC 起延迟超过 6 小时,死亡率将超过 80%[8]。因此,建议对于患有 ST 段抬高型心肌梗死(STEMI)和心源性休克的患者,应尽快进行直接冠脉内介入术,理想情况下在 90 分钟内完成,以降低死亡率。观察性研究表明,对于不适合进行 PCI 初始再灌注治疗 [10,11] 或 PCI 治疗未成功的心源性休克患者,紧急 CABG 手术仍是一种治疗选择 [11,28]。
3. 对于症状发作后12至24小时出现的无症状患者,PCI 的获益尚未得到充分研究。针对 STEMI症状发作后12至48小时患者的小型随机试验表明,PPCI可减小梗死面积并改善左心室射血分数(LVEF)。这些发现得到了观察性数据的进一步支持。
4. 目前尚未有专门的试验来研究对于症状发作超过 24 小时后才就诊、有持续缺血临床证据、急性严重心力衰竭或危及生命的心律失常的 ST 段抬高型心肌梗死(STEMI)患者,直接经皮冠状动脉介入治疗(PPCI)的获益。观察性数据和小型试验表明,对于延迟就诊的 STEMI 患者进行 PCI 是合理的,且与改善预后相关。
5. 如果患者无症状且已发生完全梗死,不建议对闭塞的梗死相关动脉进行经皮冠状动脉介入治疗(PCI)。在心肌梗死(MI)后 3 至 28 天,闭塞梗死相关动脉的患者与接受 PCI 的患者的主要不良心血管事件(MACE)结局相似(闭塞动脉试验 [OAT])[16],并且在7年的随访中结果也没有差异 [29]。在 “心肌梗死后冠状动脉再通(DECOPI)” 试验中也有类似的发现,该试验纳入了症状发作后2至15天出现动脉闭塞且心电图有 Q 波的患者 [17]。
5.2.2急诊冠脉搭桥术

概述
评估冠状动脉旁路移植术(CABG)在ST段抬高型心肌梗死(STEMI)中疗效与安全性的试验有限 [4]。当由于解剖学原因无法进行经皮冠状动脉介入治疗(PCI),或者存在复杂病变时,CABG手术可作为主要的再灌注策略来实施。在梗死相关动脉成功实现再灌注后,对于处理存在更广泛的非梗死相关动脉病变的患者,CABG手术也至关重要(第 7.4.1节,“ST段抬高型心肌梗死中多支冠状动脉疾病的管理”)。
STEMI患者进行CABG手术的合适时机应根据个体情况来确定,需考虑患者的血流动力学稳定性、是否存在持续缺血以及处心肌坏死的范围。在直接 PCI(PPCI)失败后,如果不存在大面积处于危险中的心肌,或者如果手术预期效果不佳,并且与非手术治疗相比,手术可能会增加死亡风险和不良心血管事件的发生几率,那么不建议进行紧急CABG手术[5]。关于出现心源性休克或机械性并发症的患者进行 CABG手术的建议,请参考第8.1节 “伴有心源性休克的急性冠状动脉综合征的血运重建” 和第9.1节 “机械性并发症”。
指南推荐意见的相关支持性文本
1.目前尚无随机对照试验(RCT)对ST段抬高型心肌梗死(STEMI)情况下直接经皮冠状动脉介入治疗(PPCI)与外科血运重建术进行比较。对于血流动力学稳定的STEMI 患者,如果其梗死相关动脉的解剖结构不适合进行PPCI,或者PPCI未获成功,若存在大面积处于危险中的心肌,冠状动脉旁路移植术(CABG)可能会有用。在这类患者中,特别是存在持续缺血的情况或者有大面积心肌处于危险中时,CABG手术可作为主要的再灌注策略,或者在PPCI之后有效地实施。尽管患者的发病严重程度有所增加且合并症负担加重,但STEM 患者接受CABG手术后的院内死亡率仍在持续下降。
5.3不具备经皮冠状动脉介入治疗(PCI)能力的医院进行再灌注治疗
概述
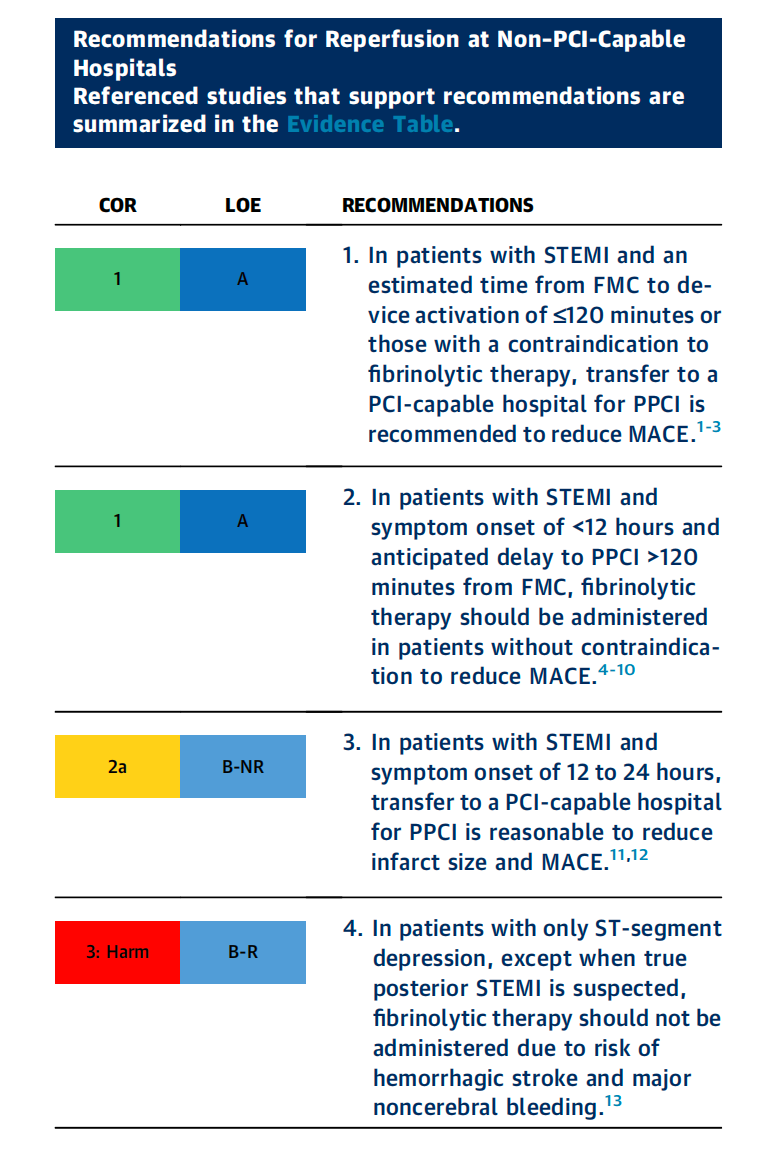
全球有很大一部分患者居住距离具备经皮冠状动脉介入治疗(PCI)能力的医院超过1小时车程。在不具备PCI能力的医院,如果可以合理预测从首次医疗接触(FMC)到具备PPCI能力医院的设备启动的时间小于2小时,建议转运患者进行直接经皮冠状动脉介入治疗(PPCI)。如果无法做到这一点,且患者症状出现时间小于12小时,建议进行溶栓治疗以降低复发性主要不良心血管事件(MACE)的风险。症状发作12小时后到不具备PCI能力的医疗机构就诊的ST段抬高型心肌梗死(STEMI)患者,应尽可能转运至具备PCI能力的机构。然而,如果患者伴有血流动力学不稳定或有大面积梗死区域处于危险中,其发病和死亡风险非常高,在无法及时进行PPCI的情况下,给予溶栓治疗的益处可能超过长时间转运为进行 PPCI 的益处。
指南推荐意见的相关支持性文本
1. 当从首次医疗接触(FMC)到进行直接经皮冠状动脉介入治疗(PPCI)能在120分钟内完成时,推荐采用PPCI以降低主要不良心血管事件(MACE)的风险。一名患有 ST 段抬高型心肌梗死(STEMI)且就诊于不具备PCI能力医院的患者,当这种(PPCI)干预措施能在120分钟内完成时,应被转送至具备 PCI 能力的医院。[1,2,18]。与转运相关的系统延误常常被低估,并且在将每位 STEMI 患者转运去接受 PPCI之前,都应该根据具体情况进行个案评估。[19 - 21]
2. 在美国,对于ST段抬高型心肌梗死(STEMI)患者使用溶栓治疗,主要是因为这些患者无法及时接受直接经皮冠状动脉介入治疗(PPCI)(即从首次医疗接触到器械启动的时间小于120分钟)。大量的随机对照试验(RCT)和荟萃分析已经表明,PPCI优于溶栓治疗。然而,随着与PCI相关的时间延迟增加,PPCI相对溶栓治疗的益处会逐渐减少。以至于在120分钟之后,与及时给予的溶栓治疗相比,PPCI的益处就不再那么明显了。[19]对于这些无法及时进行PPCI的患者,对随机对照试验和观察性研究的荟萃分析显示,当患者无法及时接受PPCI时,采用药物侵入性治疗方法(例如,先进行溶栓治疗,然后在2至24小时内进行PCI),在发病率和死亡率方面在统计学上与其他方法相似。[4,5]“心肌梗死后早期策略性再灌注(STREAM)” 试验对189名早期就诊(症状出现时间小于3小时)且在首次医疗接触后1小时内无法接受PCI治疗的STEMI患者进行了随机分组。该试验发现,院前溶栓治疗组与转运进行 PPCI 组在30天的复合终点事件(如死亡、休克、充血性心力衰竭或再梗死)发生率以及 1 年死亡率方面相似。[10,22]。
3. 小型研究表明,对于症状发作后12至24小时的患者,直接经皮冠状动脉介入治疗(PPCI)仍能带来临床益处;因此,将患者转运至具备经皮冠状动脉介入治疗(PCI)能力的医院是合理的。[11,12] 就诊较晚的ST段抬高型心肌梗死(STEMI)患者,若伴有血流动力学不稳定或梗死面积较大,其急性病情恶化的风险非常高,并且长期存在发病的风险。在这种情况下,当无法及时进行直接经皮冠状动脉介入治疗(PPCI)时,给予溶栓治疗可能利大于潜在风险。在这种情形下进行溶栓治疗后,应尽快将患者转运至具备经皮冠状动脉介入治疗(PCI)能力的中心。
4. 对于出现疑似急性冠脉综合征(ACS)症状但无 ST 段抬高或疑似真正后侧壁 ST 段抬高型心肌梗死(STEMI)的患者,给予溶栓治疗没有益处,且存在潜在危害(如出血性卒中及严重的非脑性出血)。[13]
5.3.1溶栓治疗的时机和药物选择
概要
当 ST 段抬高型心肌梗死(STEMI)患者能够快速接受直接经皮冠状动脉介入治疗(PPCI)时,PPCI仍是首选的再灌注方式。在无法进行PPCI或无法及时进行PPCI的情况下,STEMI患者采用溶栓治疗实现冠状动脉再灌注的益处是明确的。在症状发作后的最初12小时内,溶栓治疗可降低死亡率和发病率,且这种获益具有时间依赖性,尤其对于那些症状发作后早期就诊、出血风险低且大面积前壁梗死的患者。[1-7] 虽然对于症状发作12小时后就诊的STEMI患者,溶栓治疗的益处尚未明确,[8-10] 但如果无法进行PCI,对于有大面积心肌处于危险状态或存在血流动力学不稳定的症状性患者,应考虑给予溶栓药物。
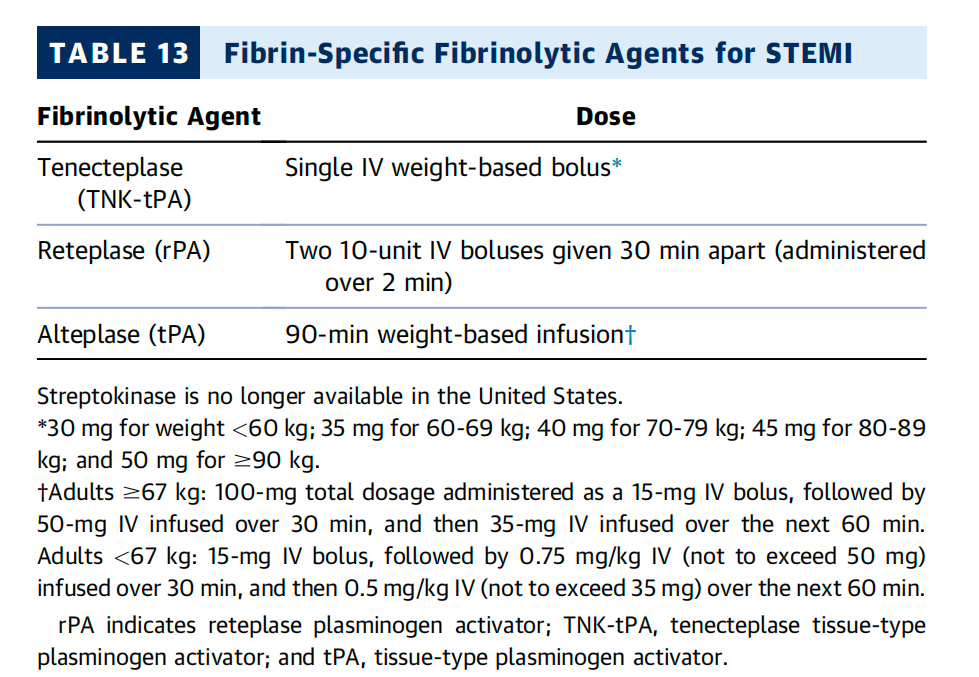
由于纤维蛋白特异性溶栓疗法具有更高的血管通畅率和更低的免疫原性,因此优于非纤维蛋白特异性药物(见表 13)。[11-16] 替奈普酶是阿替普酶的基因工程改良版,对纤维蛋白具有更高的特异性。在一项针对急性心肌梗死(AMI)患者的大型随机试验中,替奈普酶和阿替普酶在 30 天死亡率方面相当,但替奈普酶可减少非脑出血的发生。[17]
在心肌梗死(MI)患者中,与阿替普酶相比,瑞替普酶(重组纤溶酶原激活剂)并未显示出能提高生存率,但它的推注给药方式方便,使用起来更便捷。[18] 无论选择何种溶栓药物,都需要联合抗血小板和 / 或抗凝治疗(见 4.3.2 节 “住院期间口服P2Y12抑制剂” 和4.4节 “胃肠外抗凝”)。溶栓治疗的绝对和相对禁忌证见表14。
患者在开始溶栓治疗后,应转至具备经皮冠状动脉介入治疗(PCI)能力的医院进行常规冠状动脉造影(见 5.3.2 节 “溶栓治疗后的冠状动脉造影和 PCI”)。再灌注失败在 5.3.2 节中有讨论。

5.3.2溶栓治疗后冠状动脉造影和 PCI

概要
溶栓治疗后再灌注失败以及溶栓成功后再闭塞的风险是溶栓治疗的重要局限。因此,所有接受溶栓治疗的患者都应转至具备经皮冠状动脉介入治疗(PCI)能力的医院,以便根据临床情况进行即刻或早期的心导管检查。医院应制定转运方案,确保在安全的情况下能无缝转至具备PCI能力的机构。详细评估临床状况对于确定血管造影的时机至关重要。缺血症状无改善、ST段持续抬高(前壁导联ST段抬高未降低 50%,下壁导联未降低70%[从基线ST段抬高最大的导联测量,或测量各导联ST段偏移总和]),[13]或存在血流动力学或电不稳定,都可能表明溶栓治疗未实现完全再灌注。[14]当出现再灌注失败的迹象时,患者应立即进行冠状动脉造影和补救性PCI。对于其他患者,建议在溶栓治疗后2至24小时内进行常规冠状动脉造影,并根据需要进行冠状动脉血运重建。
指南推荐意见的相关支持性文本
1. 许多临床试验已经对溶栓治疗后早期进行冠状动脉造影并可能实施经皮冠状动脉介入治疗(PCI)的策略进行了评估。与常规治疗相比,这种立即转运并进行造影的策略与复发性缺血事件发生率降低相关。[1-5]无论血管造影的时机如何,立即转运能让患者更早地到达专科中心,专科中心可提供重症监护服务,并且现场的心导管室团队能够协助进行临床评估,以判断再灌注的可能性,还能让病情不稳定的患者更早地接受血管造影检查。
2. 对于溶栓治疗后出现再灌注失败临床迹象的患者,补救性 PCI可改善其预后。多项试验表明,当对溶栓失败的患者进行补救性PCI时,存在死亡率降低的趋势,且心肌梗死复发和心力衰竭的发生率显著降低。[6,7]“冠状动脉治疗的快速早期行动(REACT)” 试验[6]纳入了427名在溶栓后90分钟出现再灌注失败的患者,将他们分入三个治疗组中的一组,包括补救性 PCI 组、保守治疗组或重复溶栓治疗组。与保守治疗或重复溶栓治疗相比,补救性PCI在6个月时显著降低了死亡、再梗死、卒中或严重心力衰竭的复合主要终点事件发生率。荟萃分析也支持在这种情况下进行补救性PCI可降低死亡或再梗死的发生率。[8,9]然而,补救性PCI的轻微和严重出血以及卒中发生率明显更高。[6-8]这些研究是在股动脉入路的时代进行的,当时抗血小板和抗凝治疗的选择较少。如今使用桡动脉入路[15]以及不再常规使用糖蛋白IIb/IIIa抑制剂,已降低了出血风险。因此,对于大多数溶栓后有再灌注失败证据的患者来说,补救性 PCI 的获益大于风险。
3. 溶栓后常规早期进行造影,必要时实施PCI的治疗与常规治疗(延迟冠状动脉造影和 / 或缺血指导的血运重建策略)相比,可降低主要不良心血管事件(MACE)的发生。[1- 5, 11, 16]在这些研究中,超过80%被转运的患者接受了PCI,以治疗梗死相关动脉的严重残余狭窄或血流不佳。随机对照试验的荟萃分析显示溶栓治疗后采用早期有创治疗策略,可降低死亡或再梗死的复合终点事件发生率。[10,17,18]在一项评估ST段抬高型心肌梗死(STEMI)不同再灌注方式临床结局的网状荟萃分析中,药物 - 有创策略(定义为溶栓与PCI 之间的间隔时间≤2小时)与单纯溶栓策略相比,死亡率降低了 21%。[18]此外,当代的注册研究表明,当转运时间较长时,与直接经皮冠状动脉介入治疗(PPCI)相比,药物 - 有创策略与更好的结局相关。[19]溶栓治疗后进行血管造影和 PCI 的最佳时机尚未明确界定,但在临床试验所涵盖的各个时间范围内,对缺血终点的类似获益是明显的。[17,20]尽管早期研究担心极早期心导管检查(平均时间为2.2小时)会增加出血风险,[21]但更多的当代数据表明,即使在溶栓治疗后极早期进行心导管检查,出血发生率也相似。[17,20]
未完待续,连载中……