
运动通过增加心输出量、心率、心肌收缩力、儿茶酚胺、核心体温、电解质变化和酸碱紊乱,显著增加心脏负荷,可能在病理性心脏触发致命性心律失常和心脏性猝死(SCD)。既往观点认为,所有肥厚型心肌病(HCM)患者都应该限制运动,导致许多患者在确诊后减少体力活动(PA)。然而,久坐的生活方式会导致肥胖和动脉粥样硬化性心血管风险增加,从而恶化预后。肥胖在HCM患者中很常见,并与更严重的表型表达相关,包括更大的左心室(LV)质量、更明显的梗阻、更严重的症状和更多的心力衰竭及心房颤动。
最近的证据表明,在大多数HCM患者中,运动的益处大于风险。当前指南对运动限制采取了更为宽松的态度,并建议进行低至中强度的PA,不再普遍禁止HCM患者进行高强度PA。
然而,欧洲和美国指南中关于高强度PA(包括竞技运动)的建议存在差异,尽管最近的研究表明它不会恶化预后,但HCM患者进行高强度PA的安全性仍不确定。此外,尚缺乏证据来证明是否应根据传统SCD风险分层或形态学表现来确定能否进行高强度PA。
近期《Heart》发表的研究调查了HCM伴SCD事件患者在SCD事件发生时的PA水平,及其与临床和形态学特征、SCD风险特征和遗传学之间的关联,旨在确定与高强度PA相关SCD相关的因素。

肥厚型心肌病患者高强度体力活动与心脏性猝死的相关因素分析
Factors associated with high-intensity physical activity and sudden cardiac death in hypertrophic cardiomyopathy

方法
研究人群
这项回顾性研究分析了2005年1月至2023年4月期间在韩国延世大学附属医院连续评估的HCM患者。纳入记录了PA水平的SCD事件患者。对于有多次SCD事件的患者中,主要分析首次记录的事件。
数据收集和SCD风险分层
从医疗记录中收集直至2023年9月的合并症和结局数据,并从韩国国家死亡登记记录中确认死亡原因。根据主治医生的判断进行动态心电图监测、心血管磁共振(CMR),包括晚期钆增强(LGE)成像、心肺运动试验(CPET)和基因检测。
基因检测确定了与HCM明确相关的肌节蛋白基因变异,并根据当前标准将其分类为致病性、可能致病性、意义未明的变异或无/良性/可能良性。粗肌丝变异包括肌球蛋白和肌球蛋白结合蛋白基因,细肌丝变异包括肌动蛋白、肌钙蛋白和原肌球蛋白基因。
猝死风险分层
根据2024年AHA/ACC和2014年ESC HCM指南进行SCD风险分层,该分层也在亚洲患者中得到了验证。具有一个或多个主要AHA/ACC危险因素或ESC 5年SCD风险评分≥6的患者被建议进行植入式心律转复除颤器(ICD)进行一级SCD预防(IIa类推荐),并被视为高风险。
SCD事件定义
SCD事件包括SCD、SCD未遂和适当的ICD电击。SCD定义为在症状出现后1小时内或最后被发现存活后24小时内发生的疑似心脏原因导致的突然死亡。有ICD的患者定期进行随访,适当的ICD电击定义为用于治疗持续性室性心动过速或心室颤动的电击,不包括抗心动过速起搏。
PA水平的定义
从病历中收集了SCD事件时PA的描述,这些记录由医护人员在SCD事件后的急诊室或医院就诊期间通过对患者或其家属的访谈记录。根据患者SCD事件时的PA水平进行分组:
第1组包括在休息时或进行轻度或中度PA时发生的SCD事件。第2组包括与高强度PA相关的SCD事件,定义为在高强度PA或PA期间或之后立即发生。
SCD事件时的PA水平被分类为低强度(<3个代谢当量(METs))、中度强度(≥3至<6 METs)和高强度(≥6 METs)活动。
结果
研究人群
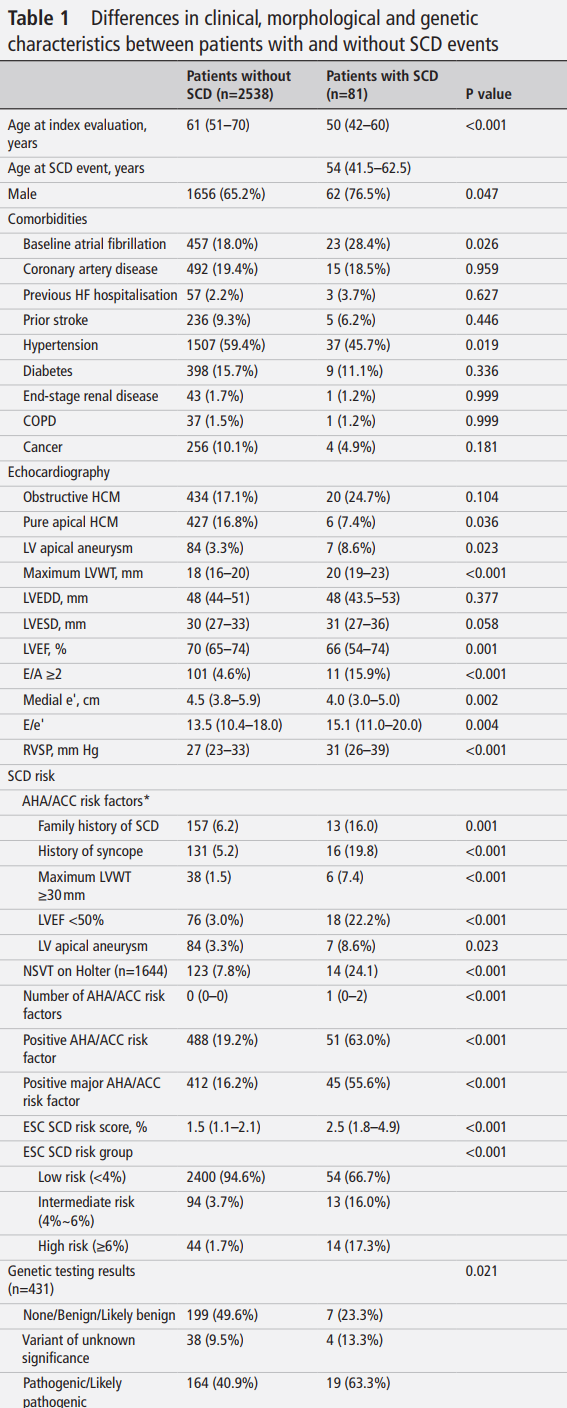
在2619例连续入组的HCM患者中,有81例(3.1%)发生了SCD事件。表1展示了发生与未发生SCD事件患者之间的临床、形态学和遗传学特征差异。总体而言,发生SCD事件的患者具有更高的SCD风险特征、更年轻、有更多的心房颤动、心尖部HCM更少、左室心尖部室壁瘤更多、LV壁更厚、LVEF更低、LV舒张功能障碍更严重,且致病性基因变异的患病率更高。
表1 有和没有猝死事件的患者之间在临床、形态学和遗传特征方面的差异
SCD事件时的PA水平
75例患者的SCD事件时PA水平有记录,并被纳入本研究。75例SCD事件包括11例SCD、43例SCD未遂和21例适当的ICD电击。SCD事件时的中位年龄为54岁(IQR 41.5–62.5),其中60例(80.0%)为男性(表2)。大约四分之一(25.3%)的患者患有梗阻性HCM(LVOT最大压力梯度≥30 mmHg),4例(5.3%)患有单纯心尖部HCM。7例患者(9.3%)存在左室心尖部室壁瘤。33例患者接受了CMR检查,其中14例(42.4%)存在广泛的LGE。一半的患者存在AHA主要危险因素(n=44,58.7%)(表3)。中位ESC SCD风险评分为2.6(IQR 1.9–5.0),其中仅14例(18.7%)患者属于高风险类别。29例患者接受了基因检测,其中18例(62.1%)被发现存在致病性/可能致病性基因变异(表4)。
表2:根据SCD事件时PA水平划分的临床和形态学特征

表3:根据SCD事件时PA水平划分的SCD风险概况
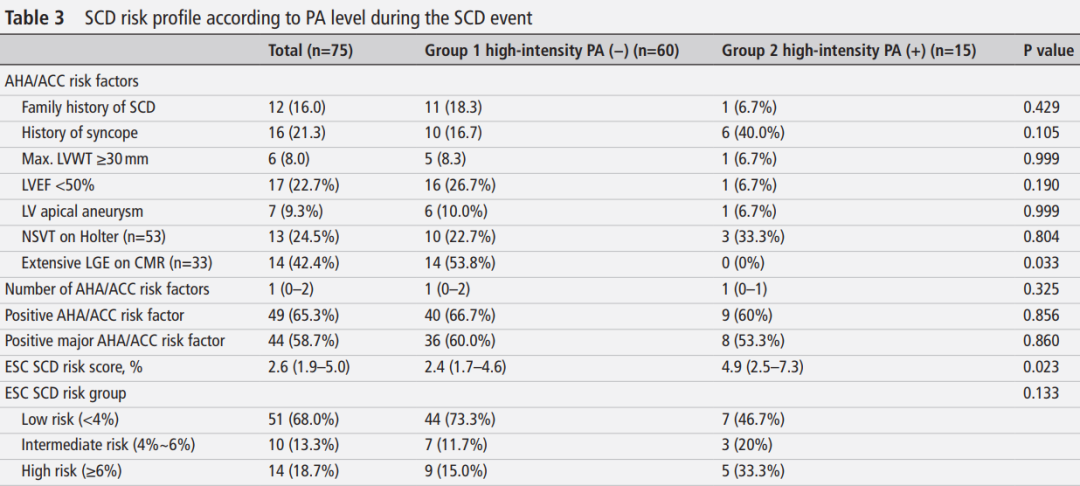
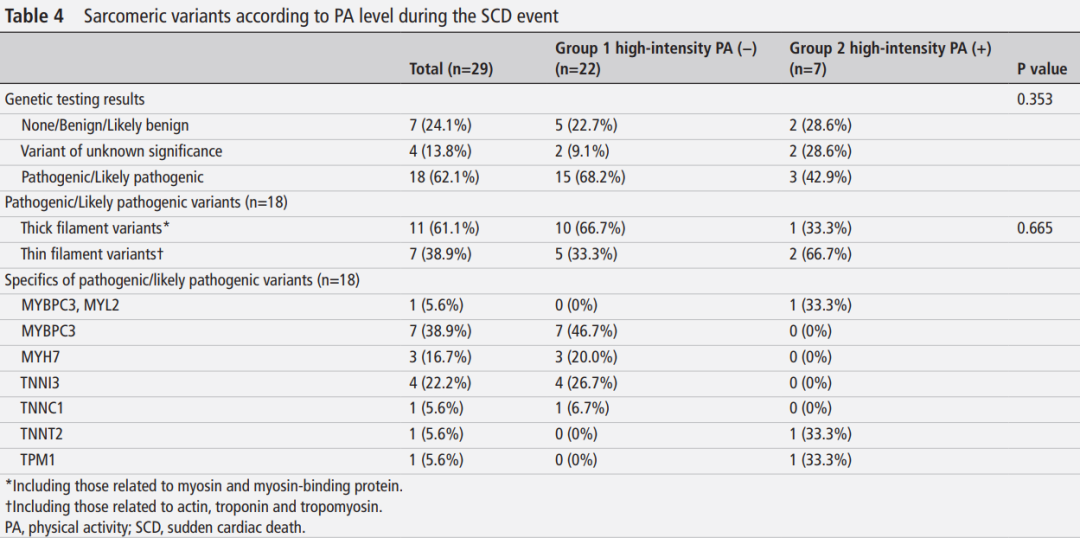
表4:根据SCD事件时PA水平划分的肌节变异
临床和形态学特征的比较:
第1组(低强度/中强度PA)有60例患者(80%),第2组(高强度PA)有15例患者(20%)。第1组的中位PA水平为1.3(IQR 1.0–2.5)METs,第2组为7.5(6.4–10.5)METs。第2组患者年龄明显小于第1组患者(56岁(47–65岁)vs 25岁(16.5–42.5岁),p<0.001)(表2)。第2组所有患者年龄均<60岁,而第1组有40%的患者年龄≥60岁。高强度PA相关的SCD事件比例随年龄增长而显著降低(p趋势<0.001)(图1)。第2组所有患者均表现为SCD未遂。两组间合并症情况无显著差异。第2组患者的LV较小,但按体表面积校正后无显著差异。两组间在梗阻性、单纯心尖HCM、心尖室壁瘤、最大LV壁厚度以及LV收缩和舒张功能参数方面均未观察到显著差异。

图1:根据年龄划分的高强度PA相关SCD事件比例。
条形图上方的数字表示高强度PA相关SCD事件的比例。
SCD风险概况的比较:
两组间AHA/ACC SCD危险因素的数量无显著差异(表3)。拥有≥1个主要SCD危险因素的患者比例也无显著差异(60.0% vs 53.3%,p=0.860)。除广泛晚期钆增强(LGE)外,两组间SCD危险因素的流行率无显著差异。第1组26例患者(43.3%)和第2组7例患者(46.7%)接受了心脏磁共振成像(CMR)检查;第1组患者中有一半(53.8%)存在广泛LGE,而第2组患者均无。第2组的ESC SCD风险评分高于第1组(2.4(IQR 1.7–4.6)vs 4.9(2.5–7.3),p=0.023),但高风险类别的比例无显著差异(15.0% vs 33.3%,p=0.133)。
致病性基因变异的比较:
第1组和第2组间存在致病性/可能致病性基因变异的患者比例无差异(68.2% vs 42.9%,p=0.353)(表4)。粗丝或细丝变异在两组间也无显著差异。
CPET的比较:
35例患者接受了CPET(第1组26例;第2组9例),两组间大多数参数均无显著差异,包括峰值耗氧量、通气效率、最大工作量或ST段压低(>2 mm)的发生。值得注意的是,第2组在CPET期间室性早搏或心动过速的发生率较低(表5)。
表5:根据SCD事件时PA水平划分的CPET结果

复发性SCD事件与PA水平:
23例患者(30.7%)发生复发性SCD事件,组间无显著差异(16/60(26.7%)vs 7/15(46.7%),p=0.234)。然而,与第1组相比,第2组中更多复发性SCD事件与高强度PA相关(p<0.001):第2组所有7例患者(100%)至少发生一次与高强度PA相关的复发性SCD事件,而第1组的16名患者中只有2名(12.5%)。
高强度PA相关SCD事件的危险因素
单变量回归分析显示,在高强度PA期间的SCD事件中,仅较年轻的年龄和较高的ESC SCD风险评分与高强度PA显著相关(表6)。最大LV壁厚度、梗阻性生理特征或AHA/ACC危险因素的数量或存在与否,与高强度PA相关的SCD事件之间无显著相关性。在多变量回归模型中,较年轻的年龄仍与高强度PA相关的SCD事件显著相关,而调整年龄后,ESC SCD风险评分变得不再显著。
表6 高强度PA相关SCD事件的危险因素:logistic回归
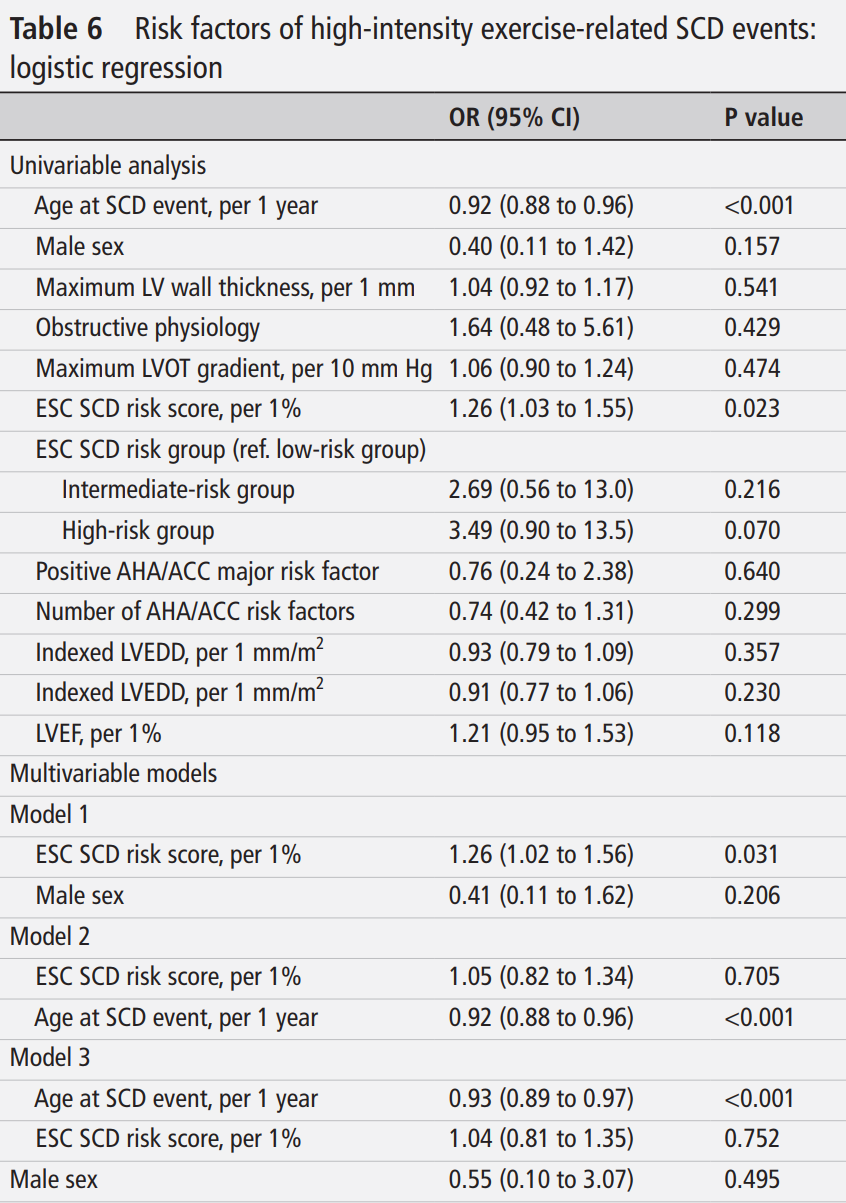
样条回归曲线显示,高强度PA相关SCD事件的优势比(OR)随年龄增长而降低,在大约50岁后趋于平稳(图2A–C)。调整ESC SCD风险评分和性别后,这种与年龄相关的趋势依然存在。高强度PA相关SCD事件的OR随ESC SCD风险评分的增加而呈上升趋势(图2D–F),但调整年龄后,这种相关性消失。

图2 年龄和ESC SCD风险评分与高强度PA相关SCD事件的关系。
样条回归曲线描述了年龄(A–C)或ESC SCD风险评分(D–F)与高强度PA相关SCD事件风险之间的关系。
按低强度、中强度和高强度PA分组进行分层分析
将研究人群按PA分为低强度、中强度和高强度三组的分析结果显示出一致性:高强度PA组年龄较轻,CMR检查显示LGE范围较小,并有ESC SCD风险评分较高的趋势。同时,低强度PA组和中强度PA组在临床、形态学或遗传学特征上无显著差异。
讨论
本研究发现年轻年龄是PA相关SCD唯一显著预测因素,而与传统危险因素无关联。SCD事件中,仅20%发生在高强度PA期间。高强度PA相关的SCD事件与较年轻年龄相关,且所有事件均发生在60岁以下。值得注意的是,LV肥厚程度、LVOT梗阻、致病性肌节蛋白变异、CPET中的室性心律失常以及AHA/ACC危险因素的数量与高强度PA期间SCD风险增加无关联。尽管ESC风险评分与高强度PA相关的SCD事件相关,但调整年龄后,这种相关性变得不再显著。在高强度PA相关SCD的幸存者中,高强度PA相关的复发性SCD事件更为频繁。研究结果表明,高风险形态学特征或传统SCD风险分层不能作为运动资格的评估标准。
仅十年前,HCM患者还被普遍建议不要进行高强度PA。之前的观察性研究确定HCM是年轻竞技运动员SCD的常见原因,但运动作为触发因素的作用尚不清楚。小型回顾性尸检研究表明,HCM中SCD很少与运动相关。小型随机对照试验显示,中强度和高强度PA训练可提高体能,且无不良事件。近期研究报道,诊断为HCM的竞技运动员继续运动后,死亡率或心律失常事件并未增加。大型HCM队列的观察性研究表明,剧烈运动与死亡率或SCD事件增加无关,甚至可能降低全因死亡率和心血管死亡率。然而,这不排除HCM患者中可能存在对运动触发SCD更易感的亚群,这也是我们此次研究的重点。
在高强度PA期间经历SCD事件的患者明显比在低强度或中等强度PA期间发生SCD事件的患者更年轻。年轻与高强度PA相关SCD事件之间的显著关联可能受到随年龄增长PA水平自然下降或幸存者偏差的影响。年轻人通常比老年人更活跃。然而,从机制上讲,心肌细胞处于动态生长和发育阶段的年轻患者可能更易受到剧烈运动引发的电生理不稳定的影响。
先前对SCD患者进行的尸检研究也表明,与老年人相比,SCD在儿童或青少年运动期间更为常见。此外,在66例年龄≤30岁、有SCD病史和潜在HCM的年轻患者中,SCD在运动期间更为常见,尤其是在10~15岁时。本研究表明,运动相关SCD的比例随年龄增长而下降,60岁以后未发生高强度PA相关的SCD事件。即60岁后存活或确诊的HCM患者病情较轻,SCD相关和HCM相关死亡率较低。尽管研究队列中LGE的总体发现率较高(42.4%),但高强度PA组中未发现广泛LGE。这可以用高强度PA组的年轻年龄来解释,因为LGE随时间显著增加,在年轻HCM患者中发现率较低。这些观察结果表明,HCM的形态学特征不能可靠地预测患者是否容易发生高强度PA触发的SCD事件。此外,按照AHA/ACC或ESC指南进行的传统SCD风险分层未能区分在高强度活动期间出现不良结局风险较高的患者。ESC SCD风险评分与高强度PA相关的SCD事件相关,但这是由于年龄因素所致。基因检测和CPET也无法区分高强度PA相关SCD风险较高的患者。在高强度PA相关SCD事件的患者中,CPET检测到的室性心律失常的发生率反而较低。同时,此类事件幸存者中高强度PA相关SCD事件的高比例强调了这一亚组患者的持续风险。尽管各组之间SCD复发事件的比例没有显著差异,但第2组中的复发事件与高强度PA相关,这提示在易感患者中存在潜在的触发机制。
临床意义
ESC指南建议,在形态学轻度的HCM的无症状低风险个体中可考虑进行高强度PA和竞技运动,但不建议在高SCD风险、梗阻性生理改变或运动诱发室性心律失常的个体中进行。与此同时,AHA/ACC指南未根据形态学标准或SCD风险提出具体的运动建议,指出高强度娱乐性PA在HCM患者中是合理的,竞技运动可在患者经过年度全面评估和共同决策后考虑。本研究结果证实了识别高强度PA相关猝死事件高风险患者的困难,并质疑了基于“高风险形态学特征”或传统SCD风险分层制定运动限制的合理性。指南中提到的LV肥厚程度、LVOT梗阻或运动诱发室性心律失常与高强度PA相关SCD事件无关。年轻是唯一的独立危险因素,这表明高强度PA相关SCD事件的风险会随年龄变化。这些观察结果表明,对于老年HCM患者,运动限制可能不必要,或需要制定特定年龄段的运动建议,尽管需要进一步研究来支持这些假设。此外,临床医生应建议有高强度PA相关SCD病史的患者避免剧烈运动。
结论
在这个小样本的HCM猝死事件患者中,年轻是高强度PA相关SCD的唯一显著危险因素。LV肥厚程度或LVOT梗阻程度、SCD风险分层、CPET和遗传学检查无法识别在高强度PA期间SCD风险增加的患者。有高强度PA相关SCD病史的患者应避免剧烈运动。