
据报道,30% ~ 60%的脓毒性休克患者有脓毒性心肌病,但弥漫性心肌钙化却是罕见并发症,自2000年以来文献中报道的病例不到20例。心肌钙化可能在脓毒性休克发作后的最初几天至1年内发生。这种心肌钙化被认为是“营养不良性”(发生在受损组织中)或“转移性”(继发于钙稳态异常,如血液透析的慢性肾衰竭患者、甲状旁腺功能亢进或草酸尿症患者),导致收缩和/或舒张功能障碍。近期《Eur Heart J Case Rep.》报告了一名孕妇在脓毒性休克后迅速出现营养不良性心肌钙化的病例。

脓毒性休克后迅速出现心肌钙化
病例报告
一名42岁的孕妇(G2P1),孕24周,既往除因子宫内膜异位症接受过腹腔镜手术外,无其他病史,因急性呼吸窘迫入院。入院前1周出现咳嗽、发热和呼吸困难。她曾接受对乙酰氨基酚对症治疗。入院时的生命体征如下:心率125次/分,血压80/45 mmHg,SpO2 80%,呼吸频率40次/分,体温38°C。入院后24小时内的心电图正常。听诊显示规则性心动过速,但无异常心音。双肺均可闻及弥漫性湿啰音。
经胸超声心动图显示LVEF:45%,LVOT VTI:17 cm;LV-GLS:-13.6%(图1),二尖瓣多普勒血流频谱(E 峰:80 cm/s;A 峰:118 cm/s;E/A 比值:0.7;侧壁 e' 峰:7.1 cm/s;E/e' 比值:11.3)提示舒张功能异常,并存在少量非压迫性心包积液。
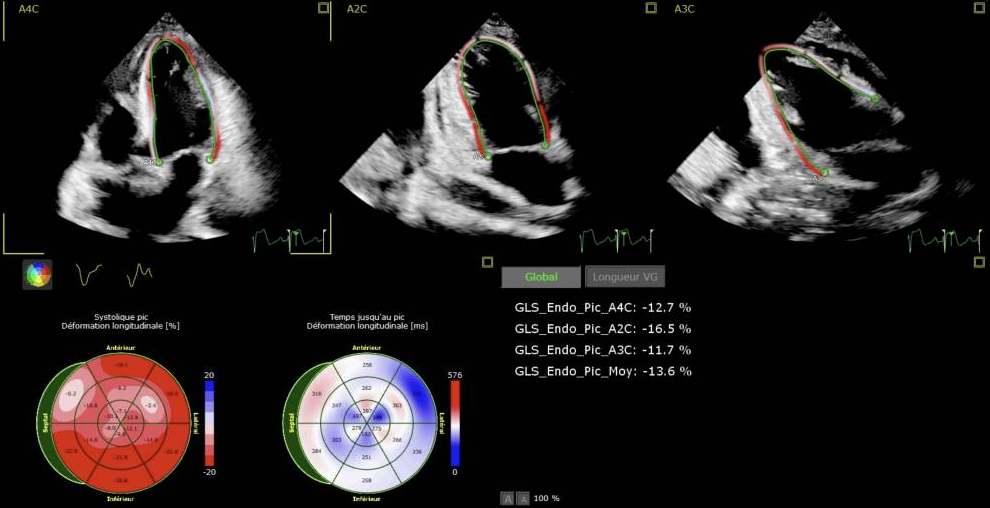
图1.第1天左心室功能的整体纵向应变LV-GLS。
胸部X光片显示双侧肺泡浸润,胸部CT证实双肺下叶实变。尿检肺炎链球菌抗原阳性,呼吸道聚合酶链反应检测流感病毒A阳性。此外,血培养结果示铜绿假单胞菌阳性。患者被诊断为流感合并细菌感染。开始给予静脉抗感染治疗,用药包括哌拉西林-他唑巴坦(4 g负荷剂量,随后持续输注16 g/24 h,持续7天)、螺旋霉素(每次300万单位,每日3次,持续3天,尿抗原阴性排除嗜肺军团菌后停药)、阿米卡星(单次剂量2 g)和奥司他韦(每次75 mg,每日2次,持续5天)。
尽管给予高流量氧疗和间歇性无创正压通气,但患者持续低氧血症,予以经口气管插管、深度镇静、肌松和保护性机械通气。气体交换持续恶化,引入静脉-静脉体外膜肺氧合(VV-ECMO)支持,并进行了三次俯卧位通气。
脓毒性休克导致宫内胎儿死亡和多器官衰竭,入重症监护室时SOFA评分为19分[范围(0–24),预测死亡率>90%]。急性肾衰竭采用连续静脉-静脉血液透析(CVVHD)和枸橼酸盐抗凝治疗。此外,患者还出现急性肝衰竭[胆红素:249 µmol/L(正常值<21µmol/L);凝血酶原时间:22%(正常值>65%)],严重血管麻痹,需要大剂量血管升压药(去甲肾上腺素4µg/kg/min和血管加压素0.03 UI/min),以及流感心肌炎导致的轻度左心室功能障碍(LVEF:45%)[高敏肌钙蛋白I:43000 ng/L(正常值<11.6 ng/L)]。
第16天,肺部CT显示左心室游离壁存在广泛心外膜下钙化。回顾性观察发现,虽然第8天的CT中钙化不太明显,但已可检测到。定期重复CT以评估肺实质和心肌钙化进展(图2)。此外,患者左侧咬肌和右肩关节囊也出现钙质沉积。
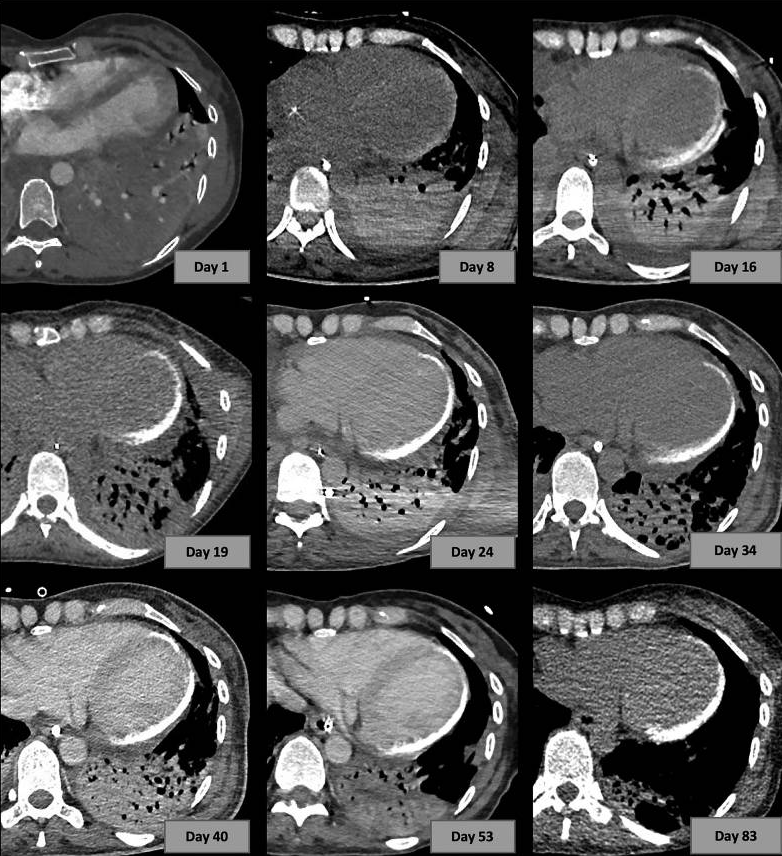
图2.急性呼吸窘迫综合征病程中连续胸部CT复查显示的心肌钙化演变。
考虑到甲状旁腺素[8 pg/mL(正常值11–57 pg/mL)]和维生素D[12.8 pg/mL(正常值19.9–79.3 pg/mL)]的水平较低,以及血钙 [2.23 mmol/L(正常值2.20–2.65 mmol/L)] 水平正常,排除了甲状旁腺功能亢进症。
在入院后的第29天和第31天,患者发生了两次窦房结功能障碍,需要心肺复苏。随后植入了无导线起搏器。
从入院开始,每天进行超声心动图评估(包括LV-GLS),以监测左心室收缩功能。第8天时观察到左心室功能完全恢复[LVEF:55%;LVOT VTI:22 cm;LV-GLS:-18.9%(图3);E:52.3 cm/s;A:59.6 cm/s;E/A:0.9;侧壁e':10.1 cm/s;E/e':5.2]。
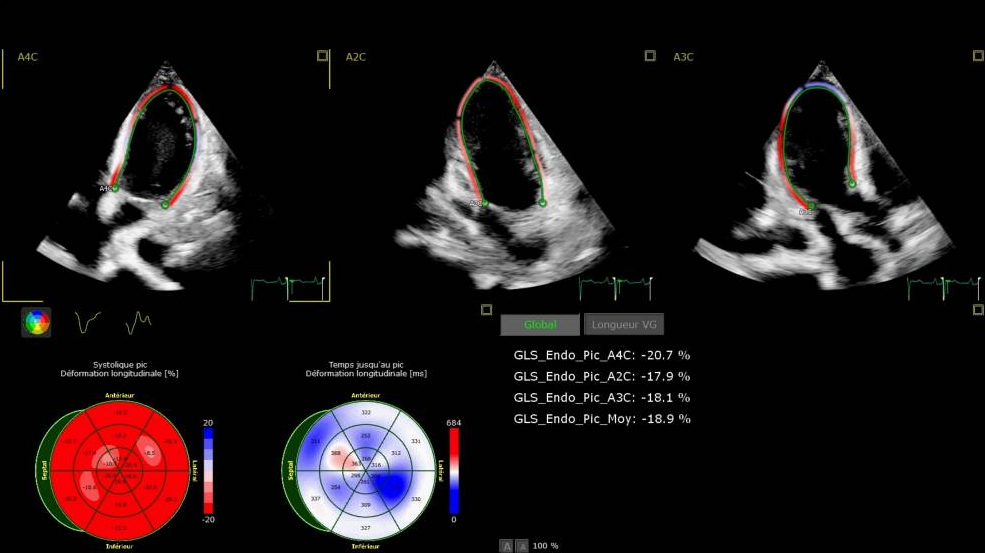
图3.第8天左心室功能的整体纵向应变LV-GLS。
尽管心肌钙化加重,所有器官功能改善后,患者于第44天转入康复病房。
出院后两个月复查心脏CTA,发现心肌钙化稳定,且未发现冠状动脉病变。
出院后一年,心电图显示窦性心律,并且在多次随访中,无导线起搏器的刺激率低于1%。随访超声心动图检查完全正常,排除了心肌缩窄(LVEF:60%;LV-GLS:-19%;E:92 cm/s;A:35 cm/s;E/A:2.6;中间e':10.7 cm/s;侧壁e':11.4 cm/s;E/e':8),且无心包积液。还进行了心脏MRI检查,显示左心室侧壁心外膜下晚期强化,与近期心肌炎一致,但心腔容积和心室功能正常。
讨论
在这例严重脓毒性休克患者中,观察到在CVVHD采用枸橼酸盐抗凝的背景下,患者早期就出现了广泛的心肌钙化,且未检测到任何代谢紊乱。入院时患者的高肌钙蛋白水平符合急性心肌炎的诊断。因此,我们将这种钙化称为“营养不良性”钙化。
在采用VV-ECMO或VA-ECMO治疗心肌炎的情况下,仅有极少数心肌钙化病例报道。其病理生理机制尚不完全清楚,但长时间的血流动力学紊乱、严重酸中毒、大剂量升压药以及急性呼吸窘迫综合征(ARDS)似乎与脓毒症相关钙化相关。心肌钙化在第8天就变得可见,这是非常不寻常的。
以往研究表明,心肌钙化与收缩、舒张功能改变有关,从而导致收缩、舒张功能障碍。患者在入院时LV-GLS异常(-13.6%),但每日测量结果显示,尽管心外膜钙化在进展,但该参数在10天内完全恢复。由于很难在所需的三个切面上获得完美的内膜检测,因此对于机械通气患者获得的LV-GL值应谨慎看待。在本例中,LV-GLS的变化反映了LVEF的变化,支持了左心室功能的矛盾性改善。LV-GLS与心肌钙化进展之间缺乏相关性,可能部分归因于该指标源自心内膜的缩短,而钙化发生在心外膜下。然而,心外膜大量钙化与内膜纵向缩短同时改善之间的分离现象非常显著,且尚未有过报道。
钙化还可能影响传导通路,一些作者报道了慢性肾衰竭患者的猝死与传导系统内的钙沉积相关。患者在接受27天的肾脏替代治疗后从急性肾损伤中恢复,随后出现了两次导致心脏骤停的窦房结功能障碍。初步假设是,传导系统中的钙沉积可能是这种危及生命的传导障碍的原因,因为找不出触发迷走神经事件的诱因。考虑到心肌钙化的不可逆性,临时起搏等临时方法可能不足以解决问题,因此决定紧急植入永久性起搏器。回顾来看,由于患者恢复了自主窦性心律,这一假设可能是错误的,迷走神经机制可能是原因所在。同时,右肩和左咬肌的钙化在这种背景下也非常不寻常。
尽管患者的血钙水平始终正常,但CVVHD的枸橼酸盐抗凝(需要持续输注钙)可能在心肌钙化的发展中发挥了作用。假设在这种特定情况下有潜在危害,我们决定从枸橼酸盐抗凝转换为普通肝素。
结论
心外膜下钙化是严重脓毒性休克后的一种罕见并发症。本例患者的特点在于钙化发生早且进展迅速,以及钙化程度与左心室收缩和舒张功能保留之间的鲜明对比。局部枸橼酸钙抗凝在此并发症发展中的作用仅为假设,需要更多观察才能提出可能的发病机制。