
在心血管疾病的现代治疗中,植入式心脏复律除颤器(ICD)、心脏再同步化治疗(CRT)以及无导线起搏器等技术扮演着至关重要的角色。随着临床研究的深入,我们对这些技术的适应症和应用有了更明确的认识。然而,在实际临床应用中,医生往往需要面对复杂多变的患者情况,而传统的临床指南可能并不能涵盖所有具体的临床场景,因此适宜性使用标准应运而生。
AUC的分类与评分系统
适应症标准通过一系列临床情境的评分,帮助医生在临床决策中作出更合理的判断。每个情境都由多学科专家小组制定,并通过德尔菲法独立评级小组评定。评分分为"适宜"(7-9分)、"可能适宜"(4-6分)和"很少适宜"(1-3分)三个等级:
适宜 (Appropriate)
对于那些具有充足的临床试验证据或临床经验支持的设备植入情境,给予“适宜”评定,表明此治疗对该患者群体具有明显益处,获益明显大于风险。

可能适宜(May Be Appropriate)
这些情境基于实践经验或证据,可能适合该患者群体,但应由临床医生根据其他临床因素和患者意愿来判断,因此被归类为“可能适宜”。

很少适宜(Rarely Appropriate)
不适宜的治疗选项(通常不可接受且不合理)。由于缺乏明确的益处,作为治疗选项的适宜性较低,若选择此类方案,应有充分的临床理由进行说明。

心脏性猝死(SCD)二级预防的ICD适宜性标准和具体临床应用情景
在讨论植入式心脏复律除颤器(ICD)用于心脏性猝死的二级预防时,我们关注的是那些已经经历过严重心律失常事件的患者。这些事件包括心脏骤停、室颤(VF)或持续性室性心动过速(VT)等。ICD在这些情况下的应用,旨在防止这些患者再次发生致命性心律失常,从而挽救生命。
根据2025年的AUC方案,ICD在二级预防中的适应症主要包括以下几个方面:
经历过心脏骤停:如果患者曾经因为心脏骤停被成功复苏,这表明他们有发生致命性心律失常的高风险,此时ICD的植入是适宜的。
持续性室性心动过速(VT):如果患者曾经出现持续的室性心动过速(VT),尤其是那些导致血流动力学不稳定的情况,ICD可以有效地预防未来的复发。
无明显可逆原因的室颤(VF):对于那些经历过室颤(VF),且未发现明确可逆原因(如急性心肌梗死、严重电解质紊乱)的患者,ICD的植入同样是重要的预防措施。
简而言之,ICD的二级预防适用于那些已经经历过严重心律失常事件的患者,其目的是为了防止这些事件再次发生,从而挽救生命。这些指导原则为非专科医生提供了重要的参考,帮助他们在临床实践中做出更为准确的判断。
2017年AHA/ACC/HRS室性心律失常患者管理及心脏性猝死预防指南和欧洲指南中均指出无论缺血性或非缺血性心脏病患者,尤其是那些因室性心动过速(VT)/室颤(VF)生还或经历血流动力学不稳定的室性心动过速(VT)或稳定的持续性室性心动过速(非可逆原因),且预期生存期超过1年,推荐植入ICD预防心脏性猝死为Class I级别。而通过2025AUC的细化评估,临床医生能够更好地理解ICD在不同临床情境下的应用,从而优化患者的治疗方案,提高治疗效果。
以下是2025AUC对于相关情景的推荐:
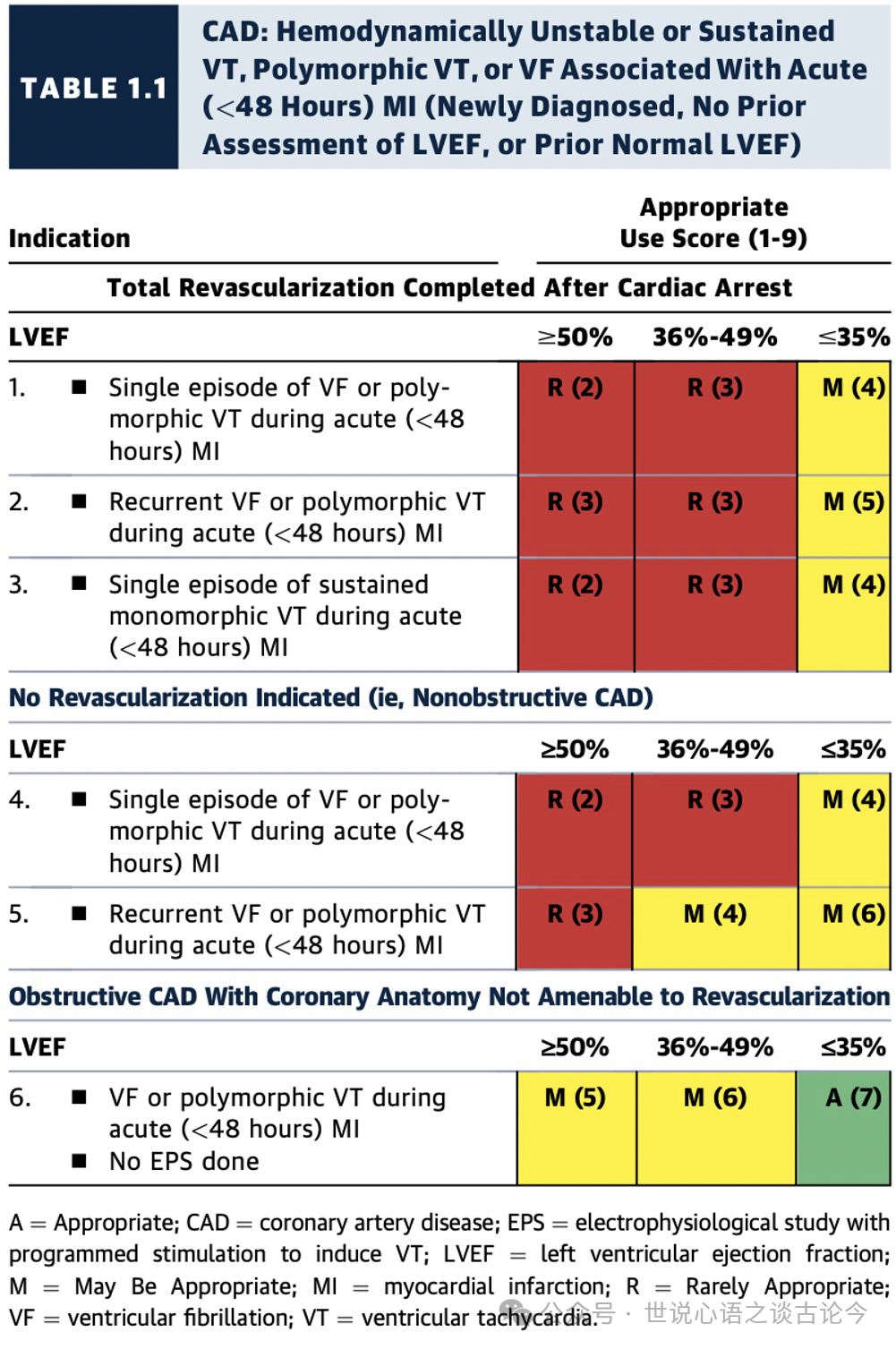
1.1 冠状动脉疾病(CAD): 急性(<48小时)心肌梗死(新诊断,未评估LVEF或先前LVEF正常)合并血流动力学不稳定或持续性室性心动过速、多形性室速、或室颤
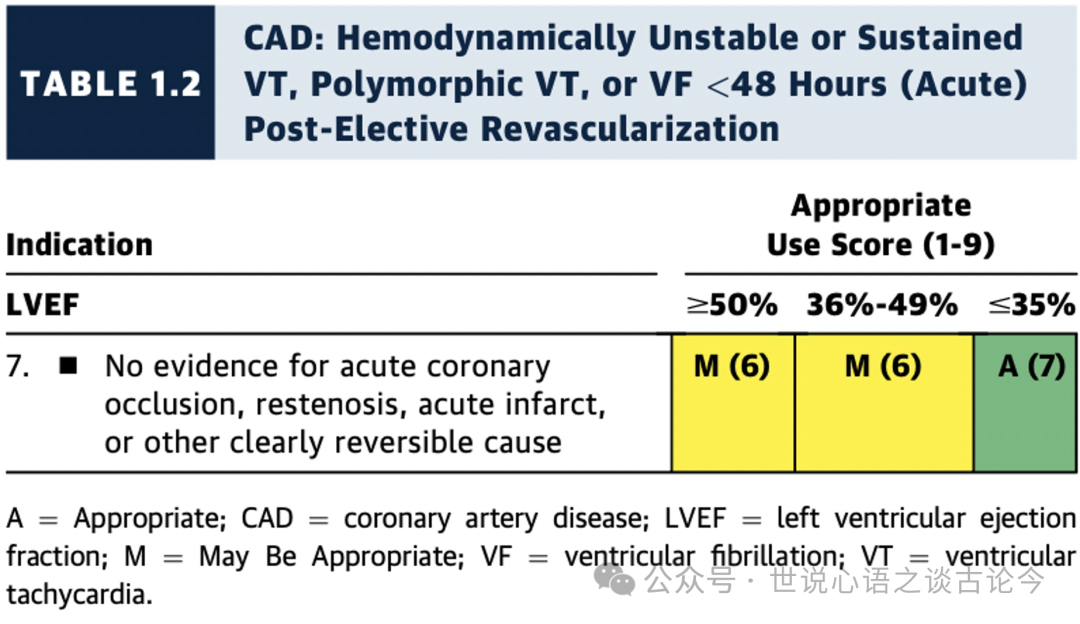
1.2 冠状动脉疾病(CAD):择期血运重建后48小时内发生(急性)的血流动力学不稳定或持续性室性心动过速、多形性室速、或室颤
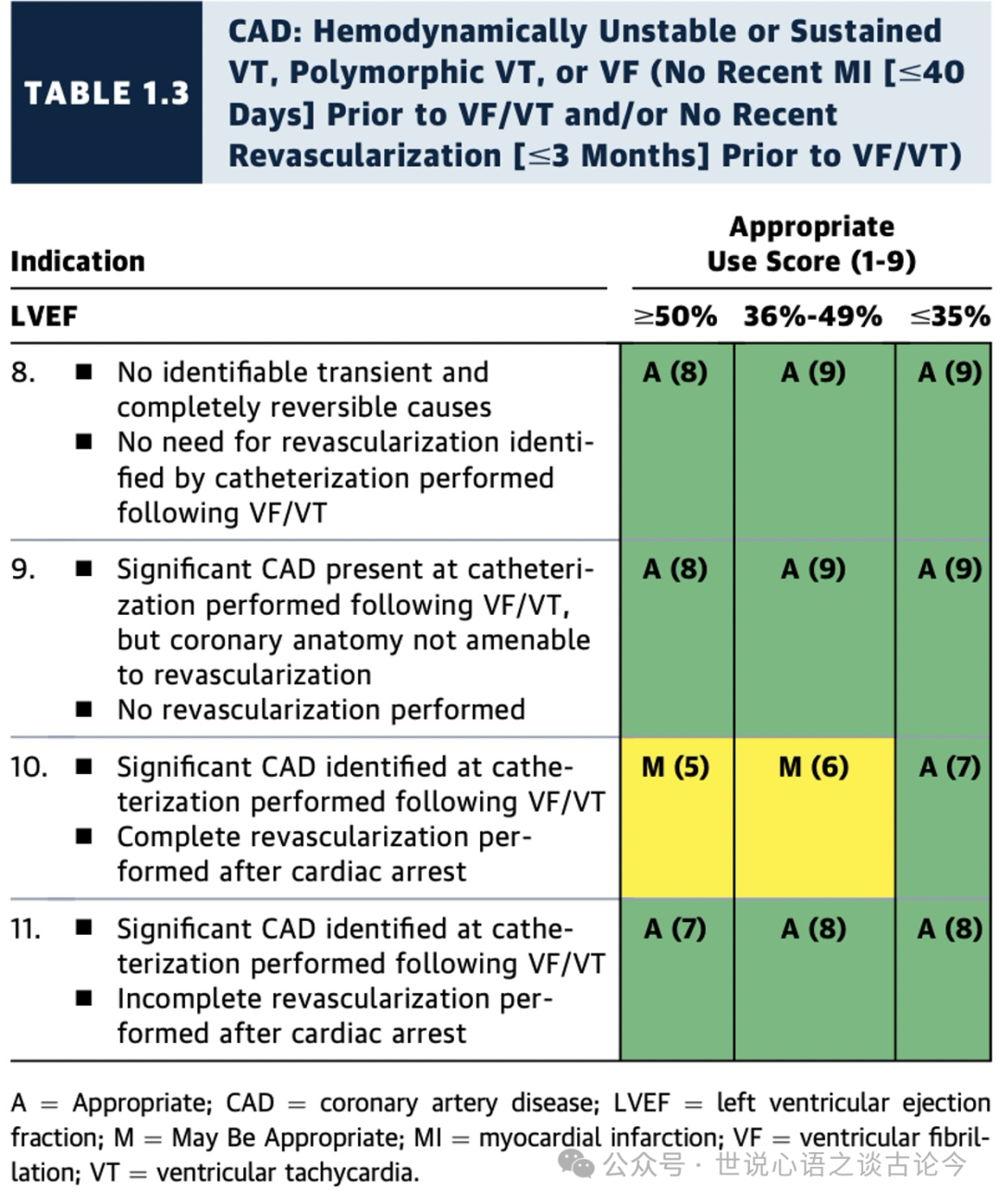
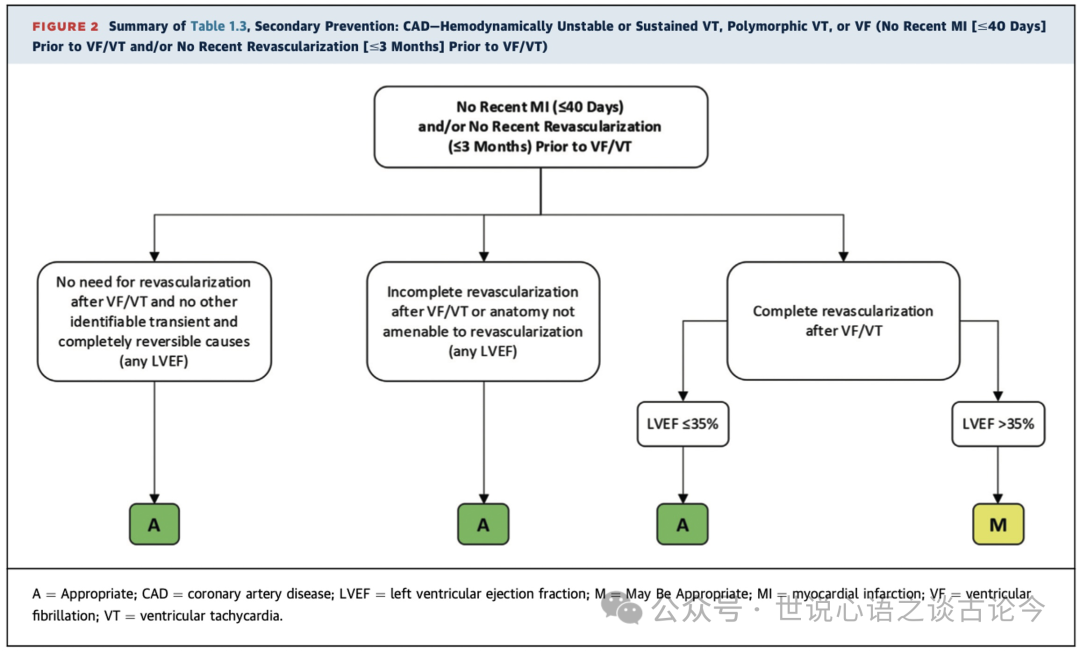
1.3 冠状动脉疾病(CAD):血流动力学不稳定或持续性室性心动过速、多形性室速、或室颤(无近期心肌梗死[<=40天]或无近期血运重建[<=3个月])
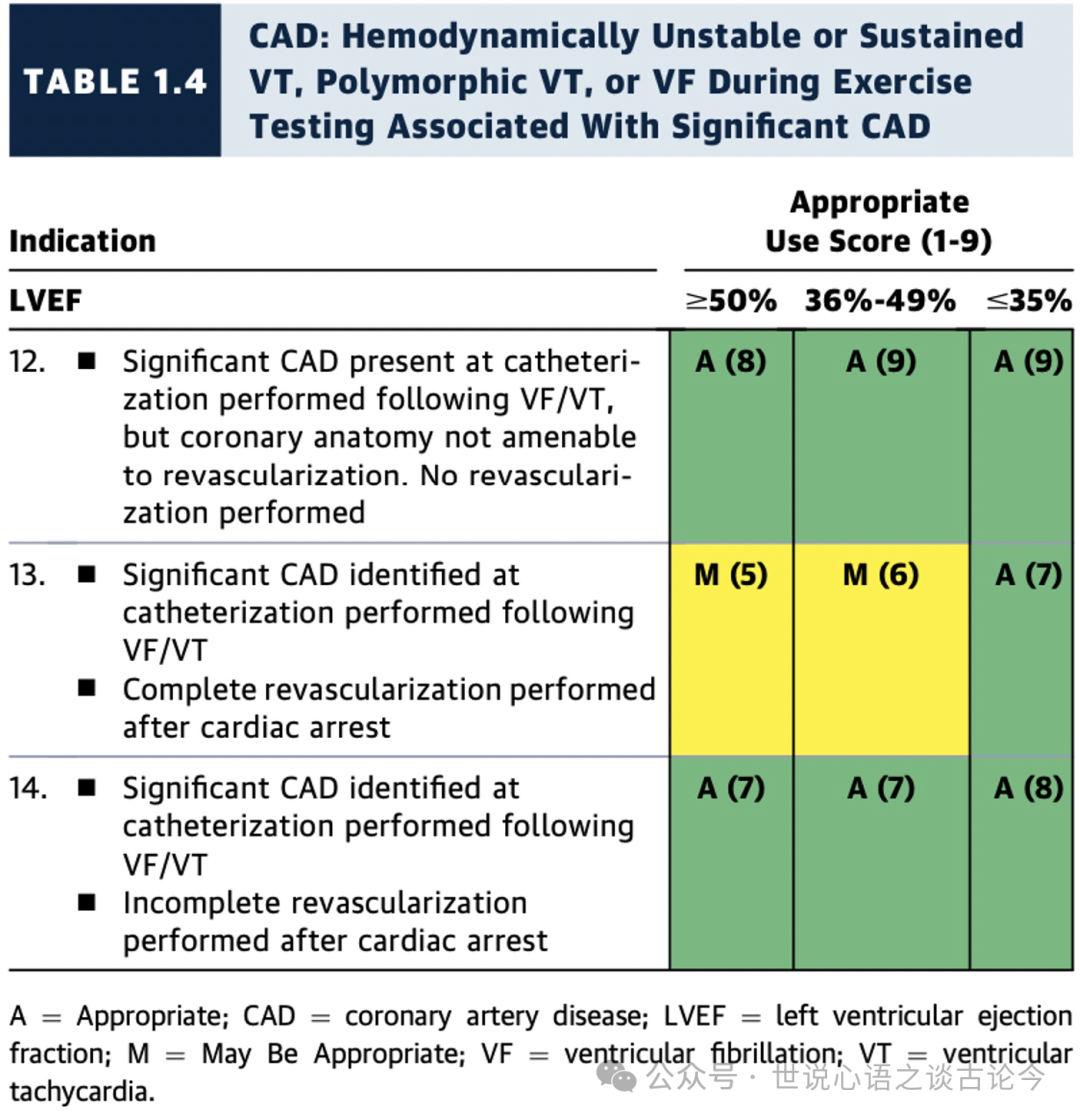
1.4 冠状动脉疾病(CAD):与明显冠状动脉疾病相关的,且在运动试验中发生的血流动力学不稳定或持续性室性心动过速、多形性室速、或室颤
重点提示:
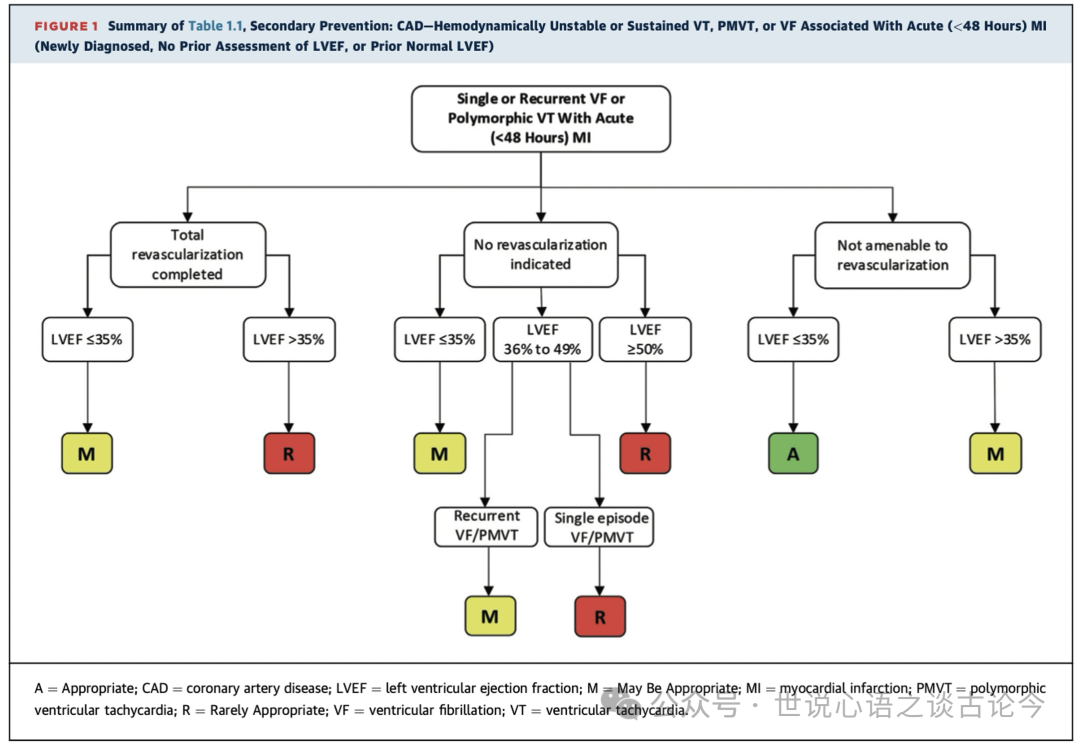
在合并冠状动脉疾病(CAD)背景下,患者出现室颤(VF)或持续性多形性室性心动过速(PMVT)时,其发生情况受心肌梗死(MI)后的时间、血运重建时间或运动负荷试验的影响(见表1.1至1.4,图1和图2)。
对于急性MI(<48小时)中的室颤或PMVT,尤其是左心室收缩功能(LVEF)保留或仅轻度至中度减低时,ICD植入被认为“很少适宜”。这与指南一致,指南指出,对于“完全可逆”的室性心律失常不应推荐ICD植入。然而,当LVEF <=35%时,ICD植入被评定为“可能适宜”,尤其对于那些存在左心室收缩功能障碍的患者,尽管这些障碍可能是既往存在的。
如果LVEF <=35%,且室颤或PMVT发生在不能进行血运重建的冠状动脉病变背景下,ICD植入则被评定为“适宜”。因为血运重建无法进行的阻塞性冠状动脉疾病可能使患者面临持续的室性心律失常复发风险,因此不属于“完全可逆”的情况。
1.5 无冠状动脉疾病(无CAD):血流动力学不稳定或持续性室性心动过速、多形性室速、或室颤


1.6 遗传性疾病伴持续性室性心动过速/室颤


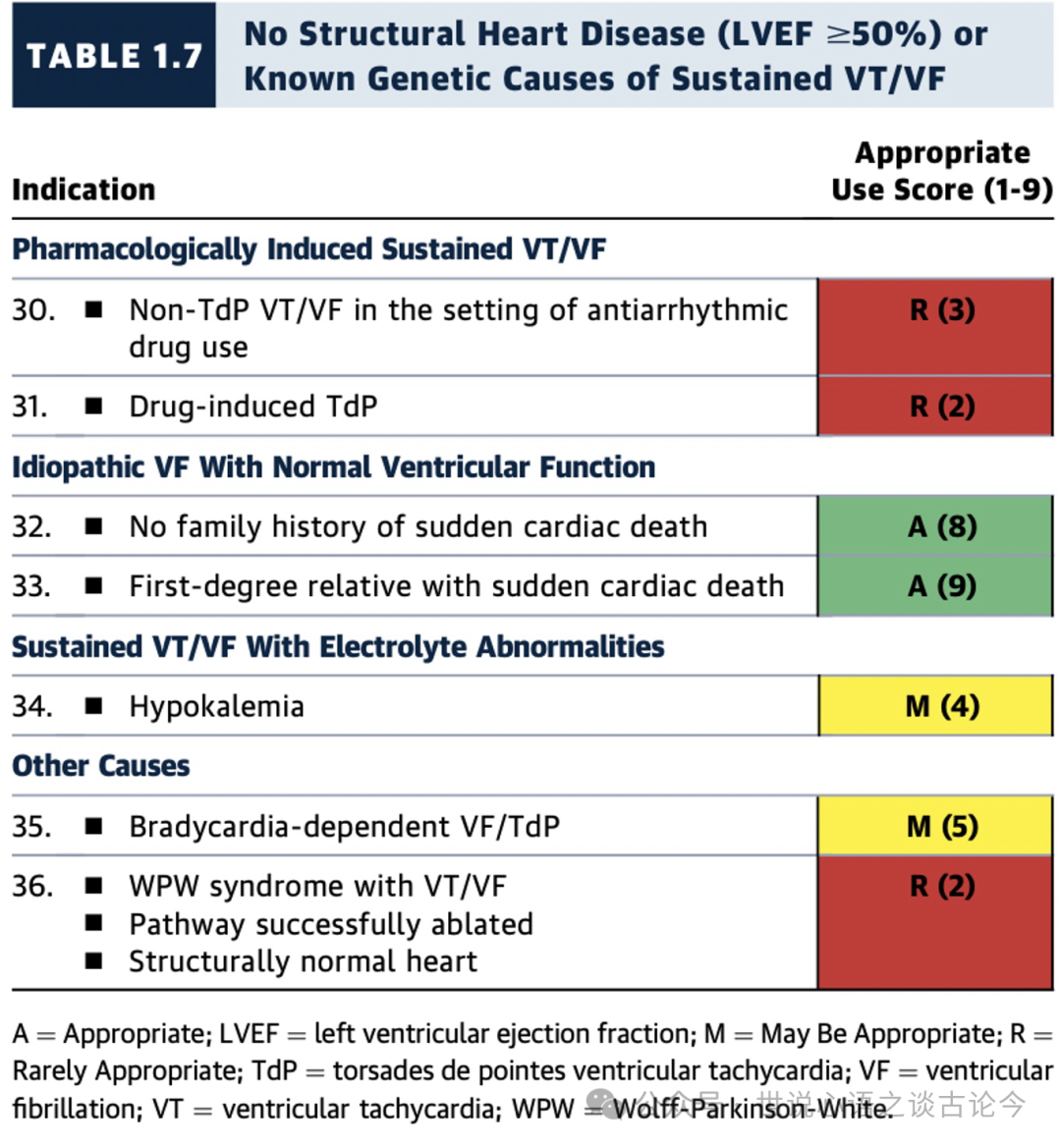
1.7 无结构性心脏病(LVEF>=50%)或已知遗传性病因的持续性室性心动过速/室颤

重点提示:
在非缺血性心脏病背景下发生的持续性室性心动过速或室颤,包括遗传性疾病、浸润性心肌病、心肌炎等情况,以及没有可检测到结构性心脏病的情形(见表1.5至1.7,图3和图4)。这些临床情境中,部分并未在指南或临床试验中明确提及,因此在这些情况下,ICD植入的决策通常需要根据有限的证据来进行临床判断。
1.8 晕厥患者的临床场景:3类情景
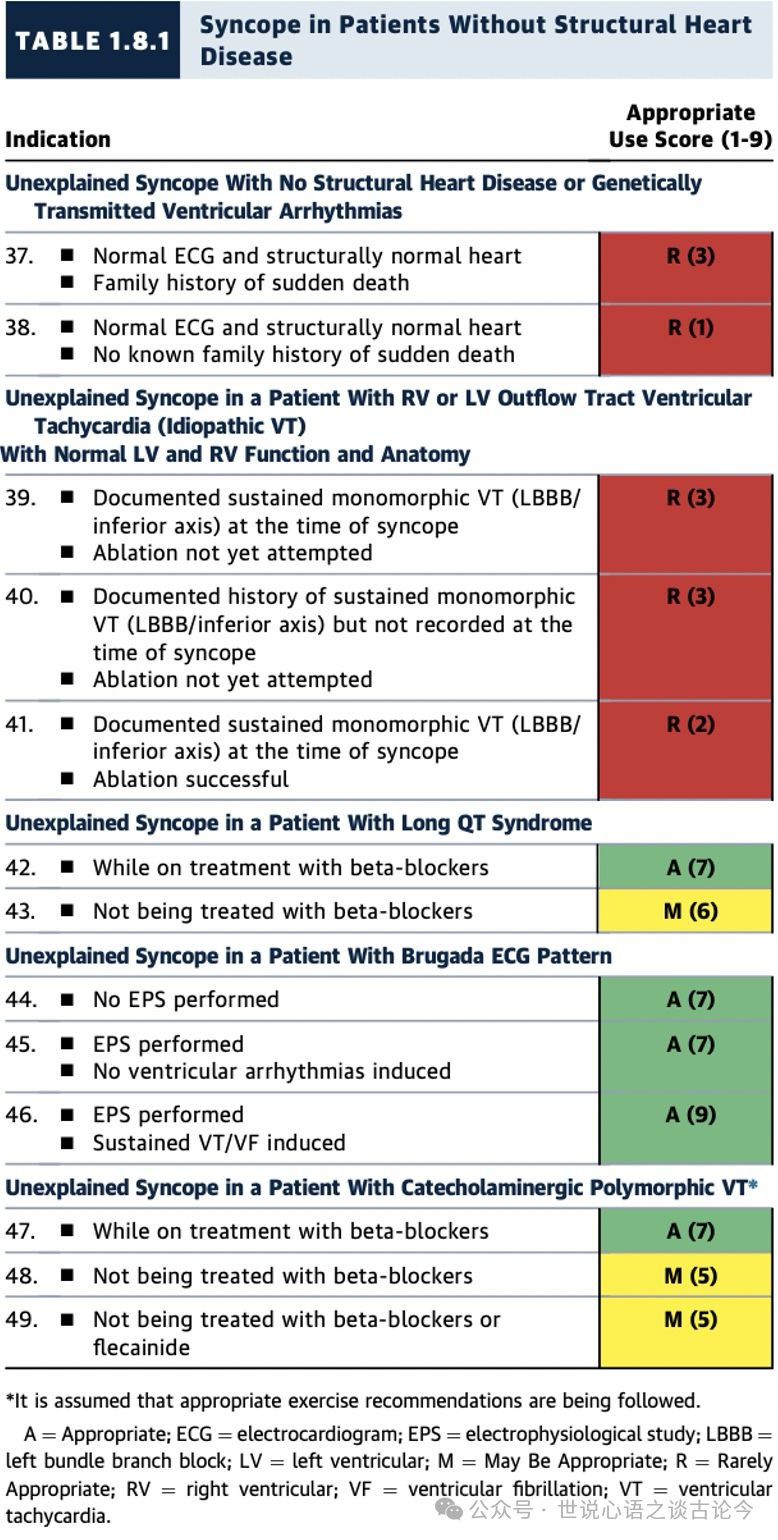
1.8.1无结构性心脏病患者的晕厥
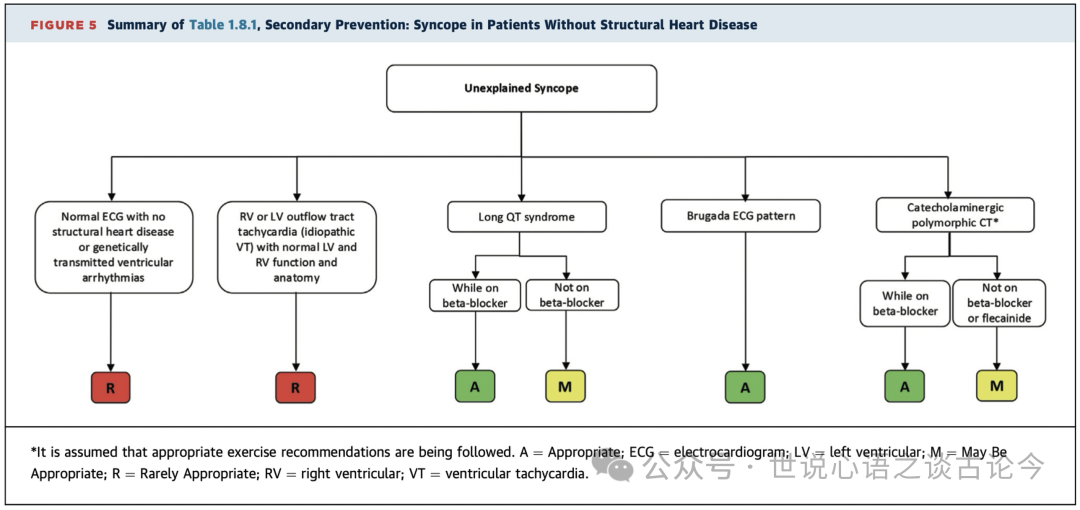
1.8.2冠状动脉疾病(CAD)患者的晕厥
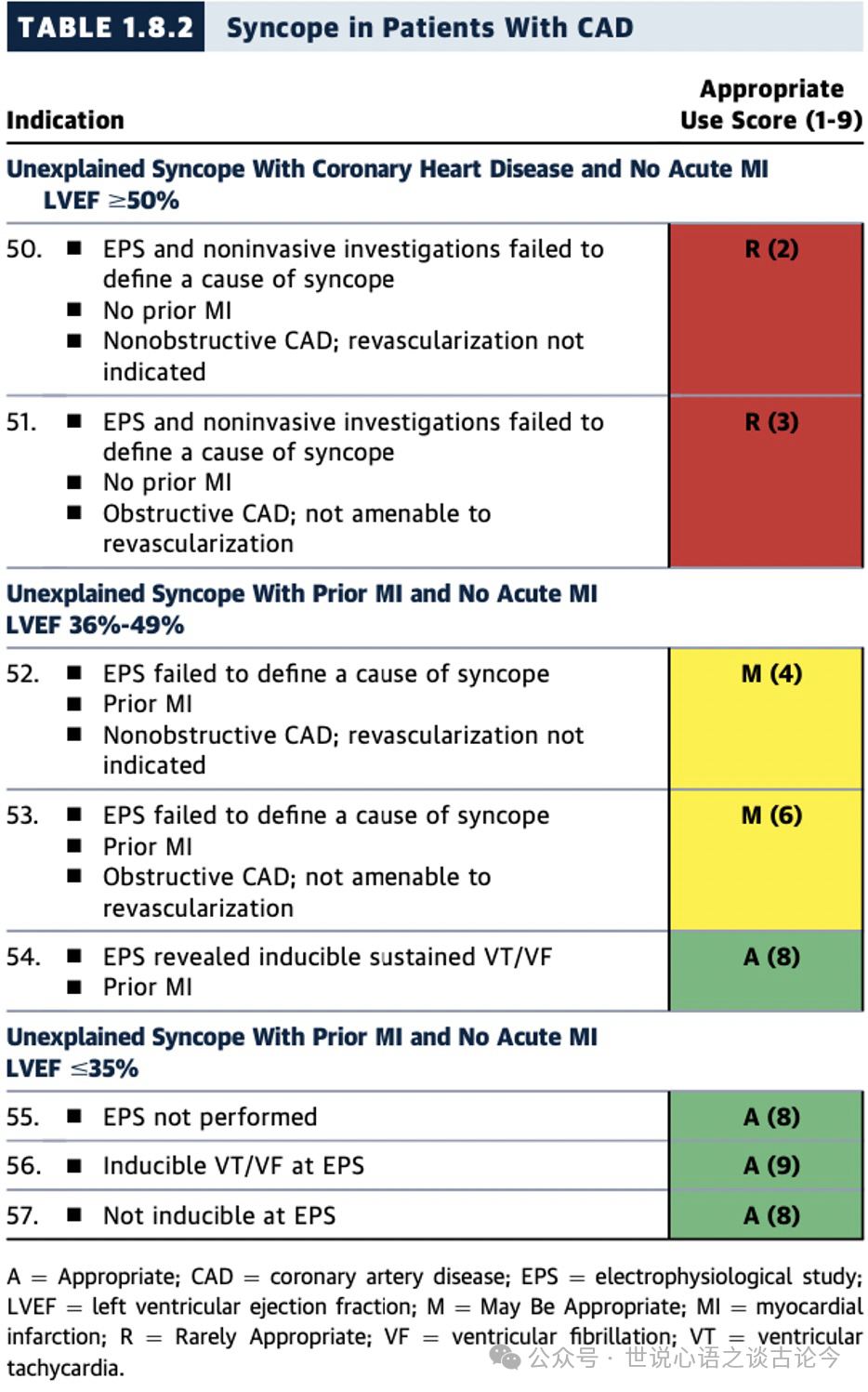
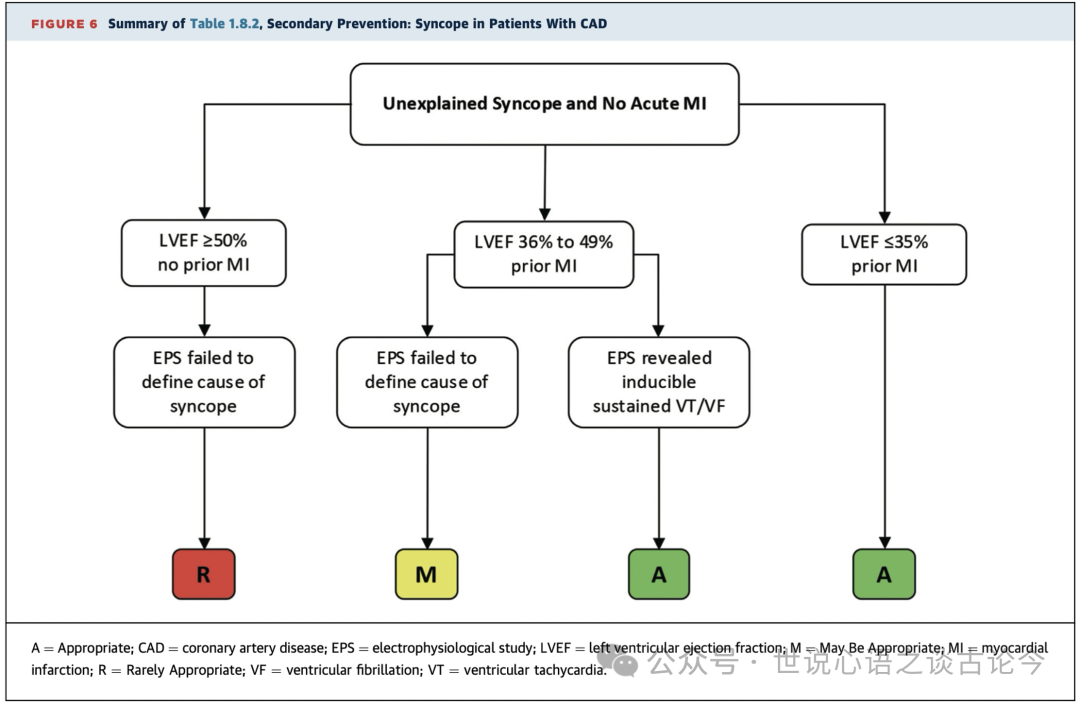
重点提示:
在伴有CAD的晕厥患者中,临床情境会根据LVEF进行调整(见表1.8.2,图6)。对于既往心肌梗死且LVEF <=35%的不明原因晕厥患者,无论EPS检查结果如何,ICD植入被认为“适宜”。在LVEF为36%-49%且既往有心肌梗死病史的情况下,只有当EP检查诱发持续性室性心动过速或室颤时,ICD植入才被评定为“适宜”,否则为“可能适宜”。
1.8.3非缺血性的结构性心脏病患者的晕厥


重点提示:
在非缺血性结构性心脏病的晕厥患者中,ICD植入的适宜性取决于心脏病类型、LVEF和/或EP检查结果(见表1.8.3,图7)。例如,具有致心律失常性右心室心肌病(ARVC)的患者,无论EPS检查或消融治疗情况如何(无论是否消融或消融是否有效),ICD植入均被认为“适宜”。对于非缺血性扩张型心肌病合并晕厥的患者,若LVEF <=35%,ICD植入被认为“适宜”;当LVEF >35%时,则评定为“可能适宜”。
有关晕厥的临床情境包括有或没有基础性结构性心脏病及伴随冠状动脉疾病(CAD)的情况(见表1.8.1至1.8.3,图5)。在没有结构性心脏病的患者中,发生长QT综合征、Brugada样ECG(不论EPS检查结果如何)和儿茶酚胺性PMVT的患者,且正在接受β-受体阻滞剂治疗时,ICD植入被评定为“适宜”。对于晕厥原因不明、心脏和ECG正常且没有与突发死亡相关的遗传性疾病的患者,或当晕厥发生在左心室功能正常、且是特发性室性心动过速(包括右室流出道[RVOT]起源或左室流出道[LVOT]起源)的患者,无论是否进行消融治疗,ICD植入则被评定为“很少适宜”。
1.9 伴结构性心脏病的血流动力学稳定的持续性单形性室性心动过速


重点提示:
在有结构性心脏病背景下,血流动力学稳定的持续性单形室性心动过速(MMVT)与血流动力学不稳定的室性心动过速或室颤应分开考虑,主要因为它们可能存在不同的心律失常基质,以及对导管消融的反应差异。对于LVEF <=35%的患者,无论是否为缺血性或非缺血性心脏病背景,或是否有室速的导管消融病史(即无论室速的导管消融是否成功),ICD植入被认为是“适宜”的治疗选择(见表1.9,图8)。
转自:世说心语之谈古论今

