
前言
1949年,Madden教授在JAMA杂志上首次报道了切除左心耳可以预防房颤血栓的形成[1],自此左心耳干预的话题开始逐渐进入公众的视野。随后有大量的研究揭示左心耳血栓与房颤栓塞事件的直接关系,其中最重磅的当属1990至1996年间,发表在JAAC、Circulation、Stroke等知名杂志上的基于经食道超声(TEE)及尸检报告的Meta分析[2-3],结果表明:非瓣膜性房颤(NVAF)患者中有90%左右的心源性栓子来源于左心耳(这一比例在瓣膜性房颤患者中为57%),结合同一时期Framingham研究得出的结论:房颤会增加5.6 ~ 7.1倍的卒中风险[4],干预左心耳以达到预防房颤卒中的相关课题受到越来越多的关注,由此多项干预技术也相继出现并取得了长足的发展。
本文对左心耳干预的由来、术式演进和器械发展进行系统性地梳理和介绍,并籍此对左心耳干预的未来发展进行了总结。
01
左心耳干预的病理生理学基础
左心耳是胚胎左心房的残留物,为狭长、弯曲的管状盲腔结构,长度2 ~ 4cm,内部有丰富的梳状肌,与左心房有一相对狭窄的连接部,毗邻左上肺静脉,下缘邻近回旋支。左心耳具有特定的生理功能。第一,收缩功能;参与心房收缩期排血,增加左心室充盈;第二,容量器官功能;在左心房压力升高、容量负荷增加时,通过左心房扩张可起到缓冲压力作用;第三,神经内分泌功能;在牵拉等机械刺激下可以分泌心房利钠钛(ANP),起到利钠利水作用;第四,有研究显示左心耳是多种干细胞的储存库,对心脏的损伤修复可能起到一定作用。
左心耳虽然具备多种生理功能,但是因为对房颤患者有潜在危害而又被称为“最致命的”人类附属结构,其危害主要包括以下两个方面。
第一,左心耳是房颤血栓的重要来源。缺血性卒中是房颤致残率最高的并发症,对于非风湿性瓣膜病房颤患者卒中的年发病率约为5%[5],而临床所有的缺血性卒中15% ~ 20%由房颤引起[4]。房颤时心房有效收缩消失,心耳内血流瘀滞,心耳局部凝血因子聚集;加上心房涡流、内皮损伤等激活了内外源性凝血途径,导致血栓的形成,进一步则可引起动脉栓塞事件。
第二,左心耳是房颤异位激动的重要来源。Di Biase 等通过研究发现在987例再次房颤导管消融的患者中,266例(27%)患者的房性心律失常(房性早博、房颤、房速)起源于左心耳 ,其中86例(8.7%)患者的左心耳是唯一的房颤触发灶[6]。
因此,左心耳干预的主要目的为降低房颤患者血栓风险以及减少房颤异位激动。
02
左心耳干预的主要方法
在降低房颤患者血栓栓塞风险方面对左心耳的干预方式主要是封闭左心耳,而其管状盲腔的形态结构决定了其干预方式主要是以外科干预为代表的“截”与内科干预为代表的“堵”为主;而减少房颤异位激动方面则主要是左心耳电隔离(LAAI)。
2.1 外科干预
外科手术是左心耳干预的经典方法,常规的外科方法分为两大类(1)左心耳切除,主要包括直接切除缝合和切割缝合器切除(Stapler切除);(2)左心耳隔离,包括经心外膜结扎、经心内膜缝合及心外膜夹闭器夹闭;按手术入路分类又可分为常规切口手术和微创手术(胸腔镜辅助或全胸腔镜)两种(图1)。

图1 左:外科干预左心耳的常规方式,右:A. 完整左心耳形态;B. 左心耳切除后;C. 切除后缝合;D. 经心外膜左心耳接扎;E. 心外膜夹闭器夹闭左心耳
2.1.1 常规外科方法
直接切除缝合、经心外膜结扎和经心内膜缝合是去除左心耳早期和最常用的方法。1949年Madden的首次报道即是通过外科切除的方法[1],到1952年Leonard和Cogan通过结扎/切除的方法切除了8例房颤患者的左心耳,但因术后并发症较多,遂放弃左心耳切除手术[7],直至1991年Cox开创了迷宫手术[8],同时配合TEE的广泛应用,左心耳才再次成为关注的热点(图2)。

图2 Cox迷宫手术
常规外科方法干预左心耳除了并发症较多之外成功率低是另一大难题。LAAOS Ⅰ 研究是第一个外科左心耳闭合领域的探索性、前瞻性随机对照研究,其目的是对比经心外科左心耳闭合手术与未行手术的房颤患者之间栓塞事件发生率。该研究发现,以左心耳与左心房间无残余分流、心耳残端 < 1 cm为手术成功标准,LAAOS Ⅰ研究中左心耳缝线结扎(suture ligation)的成功率仅为43%[9]。也因此,后续的LAAOS Ⅱ,LAAOS Ⅲ 的研究在设计上摒弃了单纯结扎,转而采用左心耳基底外科切除加固缝合、左房内双层缝线缝闭等方式。除此之外,Kanderian等通过对1993 年到 2004 年中接受外科左心耳手术的2,546 名患者进行 TEE随访来探究其手术成功率,结果表明心外膜直接切除左心耳的成功率约为73%,而经心内膜缝合左心耳的成功率则仅为23%[10]。
为了提高左心耳去除的成功率,心外科领域也开展了很多探索,多种经心外膜左心耳闭合系统如外科缝合器、圈套/缝合环以及左心耳夹闭系统等应运而生,这些新技术不仅提高了成功率,而且操作更加简便,更适合微创手术。
2.1.2 缝合器切除(Stapler切除)
Stapler 技术最早于 1988 年由Disesa 等[11]报道用于动物实验,2005 年 Blackshear等[12]将其首次用于心外科手术。多项研究报道 Stapler去除左心耳的成功率最高约为73%[10]。
在众多缝合器系统中,Tiger Paw 系统(Maquet Medical Systems,Wayne,NJ)是第一款专为左心耳手术研发设计的植入式的缝合钉(图3)。该系统最早于 2013 年就获得美国食品药品监督管理局(FDA) 510(K) 许可,但是后续有报道称该设备导致左心耳撕裂,造成死亡等严重不良事件,FDA 于 2015 年发布了该设备的 I 类召回。由此,采用Stapler切除来干预左心耳方法逐渐退出主流。

图3 Tiger Paw系统
2.1.3 圈套/缝合环(snares/suture loops)
区别于缝合器可能会对左心耳造成直接创伤,圈套/缝合环结扎系统则巧妙的避免了这一问题,目前应用于左心耳闭合的主要有Sierra和LARIAT(需经心腔内和TEE指导,后续介绍)两款系统。
Sierra 结扎系统(Aegis Medical Innovations,Vancouver, Canada) 是一种经心外膜左心耳隔离器械(图4)。该系统由左心耳抓取器和结扎器(缝合圈套)两部分组成,抓取器具有铰接钳口,并装有电极,可识别左心耳的电活动,将其与其他心脏组织区分开来;抓取器固定左心耳后,将空心缝合环推进到抓取器上,并绕着左心耳进行最终夹合。目前正在美国和加拿大进行早期可行性研究(NCT02583178)。

图4 Sierra 结扎系统
2.1.4 左心耳夹闭系统
左心耳夹闭系统充分结合了缝合器和结扎系统优点是目前应用最多的外科左心耳闭合装置,相较于传统方法其优势在于包括可以重新定位、快速植入、对左心耳造成创伤最小以及不会损伤回旋支等周边组织。
▹AtriClip
AtriClip(Atricure,Dayton,OH)早在2010年获得到了FDA 510(K)批准上市,是目前发展最为成熟、临床应用最多的左心耳闭合系统(图5)。自上市以来全球应用已超过 35万例,手术成功率高、疗效确切。第一代AtriClip(图5 A)临床试验将 73 例 CHADS2 > 2分,需正中开胸的心脏手术患者纳入研究,术后随访3 个月,结果表明左心耳闭合率高达98.4%,无围手术期死亡,无AtriClip相关的并发症[13]。随后AtriClip的迭代加速,迅速推出了第二代产品AtriClip Flex V将第一代 AtriClip闭合结构变成开放的U形结构,更方便微创手术使用(图5B)。目前 AtriClip 已进入第七代(图5C),其最新一代产品在2023年入组了首例LeAAPS临床试验患者(NCT05478304)。

图5 AtriClip系列产品
▹Penditure左心耳闭合系统
美敦力公司在2023年8月从Syntheon收购Penditure™左心耳闭合系统并于11月27日宣布获得其FDA的510(K)许可,由此正式官宣入局左心耳领域。该夹子被设计成弯曲的形状,以更好地匹配心房的解剖结构;同时,夹子表面也没有织物,能够实现无创伤闭合,减少患者的炎症。Penditure是目前是唯一一款可以在手术过程中重新取回、重新释放的左心耳夹闭系统,术者可以更好地适应手术过程中的变化(图6)。该系统的相关临床试验(PendITure™ Post-Market Study)已与2024年年初启动,计划在全美25个地方招募约150名患者,旨在进一步评估Penditure™左心耳封堵系统在临床上的效果(NCT06203054)。
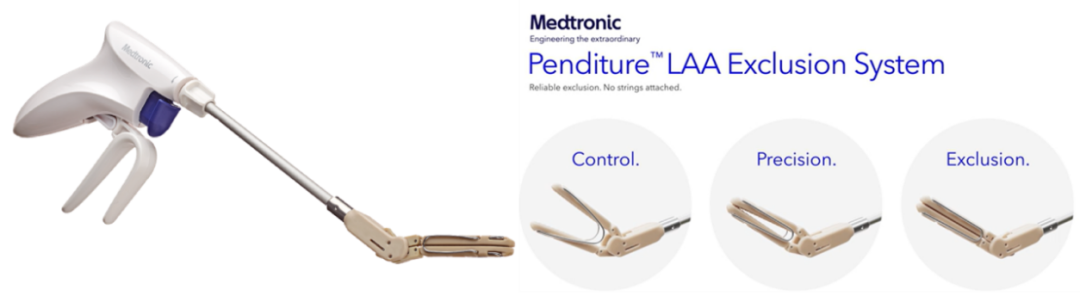
图6 Penditure左心耳闭合系统
▹PerClip左心耳夹闭系统
PerClip系统由北京普惠生物设计研发,在2022年9月9日获得了中国国家药品监督管理局(NMPA)批准上市,该系统适用于心脏外科开胸手术或微创手术同期进行左心耳夹闭的房颤患者。PerClip系统在设计上进行了诸多创新,其输送系统可以进行全景角度调节,纵向、横向、周向均可实现方向调整以适应不同形态的左心耳解剖结构;同时加持双重剪线窗口使操作范围更大,操作更加轻松,更便于术者操作;一键自锁重复定位的功能也使其释放过程更加稳定精准。
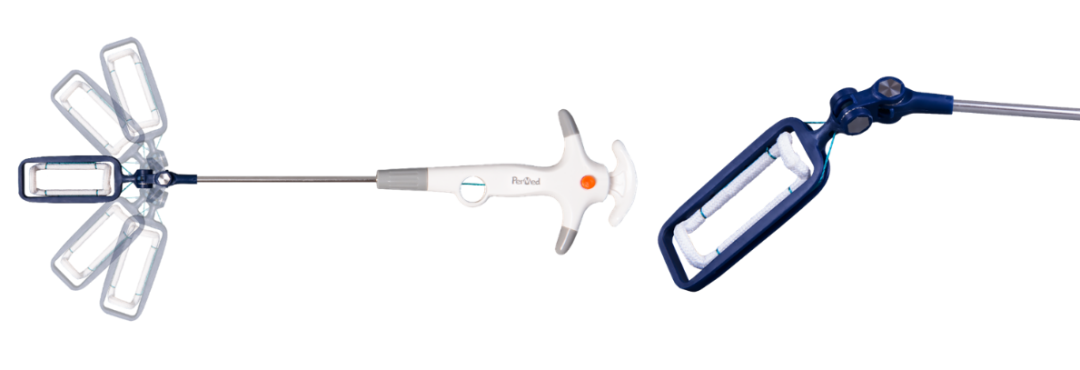
图7 PerClip左心耳夹闭系统
E-Clip左心耳夹闭系统
北京迈迪顶峰公司研发的E-Clip®左心耳闭合系统在2019取得NMPA的产品注册许可证 。该系统操作简单,通过心外膜夹闭,心内无异物,闭合位可调节,避免损伤冠脉回旋支和肺动脉等周围组织,左心耳根部夹闭,减少残端。适合不同形状、不同大小左心耳;适用于微创或开胸手术;也适用于心脏停跳或不停跳手术。

图8 E-Clip左心耳闭合系统
相较于直接切除缝合、接扎等传统左心耳闭合外科方法,左心耳闭合系统操作简单,手术安全性与成功率高,并且更适合微创手术,是未来外科处理左心耳的主要发展方向。
2.2 内科干预
以常规的外科干预左心耳的方式为代表的“截”的思路存在诸多的局限性,例如:经心内膜缝合方法因为避免损伤回旋支,所以缝合深度往往较浅,导致左心耳闭合不全,而同时左心耳开口又是一个复杂的三维螺旋结构,这也增加了缝合的难度[14];直接切除缝合及Stapler 切割缝合器技术主要缺点在于左心耳残端过长以及出血风险;而结扎技术则往往因为回旋支及其分支的经过,以及左心耳根部宽大而不能彻底地结扎左心耳,而心脏复搏后心房的充盈也会增加缝线撕脱和滑脱的概率[15]。
所以,以经导管的方式从心腔内将左心耳“堵”住的内科干预术式应运而生,这就是经皮左心耳封堵术(LAAC)。LAAC凭借创伤小、手术简便,并发症低以及预后良好等优势,在近10年高速发展并迅速成为当前的主流左心耳干预术式。LAAC的器械目前种类繁多,根据形态结构可大致分为“塞式”与“盖式”封堵器。
2.2.1塞式封堵器
▹PLAATO——LAAC开山鼻祖
PLAATO(Appriva Medical, Inc., California, USA)是首款塞式左心耳封堵器也是首个商用经皮左心耳封堵器,该封堵器由覆盖有聚合物膜的自膨胀镍钛合金笼制成,直径为15 ~ 32 mm,通过12 F鞘管输送(图9)。早期15例患者的植入经验表明,器械封堵成功率100%,随访1个月影像学显示植入器械保持稳定,心房表明光滑,无血栓迹象;随访6个月时,封堵情况依旧良好,对左心耳和上肺静脉的结构或功能无明显影响[16]。2005年发表的一项前瞻性、多中心研究,纳入111例植入PLAATO封堵器的患者,平均随访9.8个月。结果显示,手术成功率为97.3%,随访1个月和6个月未发现器械表面血栓且随访期间仅2位(1.8%)患者发生卒中事件。该研究首次证实,PLAATO经皮封堵器有望为长期华法林禁忌的房颤患者提供了一种替代治疗方案[17]。虽然后续因为商业原因退市,但是PLAATO封堵器的临床成功如同打开了潘多拉的魔盒,自此左心耳封堵器百花齐放进入了高速发展阶段。

图9 PLAATO左心耳封堵器
▹Watchman系列——LAAC集大成者
Watchman(Boston Scientific, Inc., Minnesota, USA)系列封堵器是目前临床应用最广泛、临床循证最充分、也是第一款获得FDA批准上市的左心耳封堵器。左心耳封堵领域首项RCT研究——PROTECT AF 试验,以及目前最大真实世界研究——NCDR LAAO均是植入的Watchman系列封堵器[18.19]。其首款封堵器Watchman 2.5于2015年获FDA批准上市,波科公司加速研发与产品迭代在随后的几年里推出第二代封堵器Watchman FLX以及Watchman FLX pro并分别于2020年和2023年获批上市(图10)。Watchman FLX封堵器在外形结构、骨架技术、锚定钩设计、材料工艺等诸多细节进行了改进,提高封堵成功率和手术的安全性。据最新的真实世界研究SURPASS研究数据显示,Watchman FLX手术相关不良事件的发生率为0.37%,手术成功率高达98%;Watchman FLX Pro则主要是增加表面覆膜涂层以加速器械表面内皮化进程,优化术后抗凝[20]。

图10 Watchman系列封堵器。Watchman 2.5(左);Watchman FLX(中);Watchman FLX Pro(右)
▹WaveCrest——半球形封堵器
Coherex WaveCrest(Biosense Webster, Irvine, CA)左心耳封堵器是以镍钛丝弹簧圈构成的伞形半球形结构,表面覆有聚四氟乙烯多孔膜, 镍钛丝上有20个锚定倒钩,可回收和定位。Coherex WaveCrest 封堵器于 2013 年获得欧盟(CE)认证(图11)。首个关于安全性和有效性注册研究(WAVEREST)入选 73 例患者,手术成功率及急性闭塞率为93%, 随访45d完全封堵率为92%,2例发生严重心包积液,无围术期死亡、严重的器械栓塞及致残性脑卒中并发症[21]。

图11 WaveCrest封堵器
▹MemoLefort系列——首倡可降解
MemoLefort 左心耳封堵器系统是由乐普心泰医疗科技研发的国内第一款塞式封堵器,已于2020年6月正式获得了NMPA三类医疗器械注册证(图12)。该款产品形状类似Watchman封堵器,采用内塞式设计,由形状记忆合金镍钛骨架作为支撑,具备良好的径向支撑力。该公司最新研发的生物可降解左心耳封堵器Bio-Lefort也已于2023年初启动了上市前临床试验(图12)。
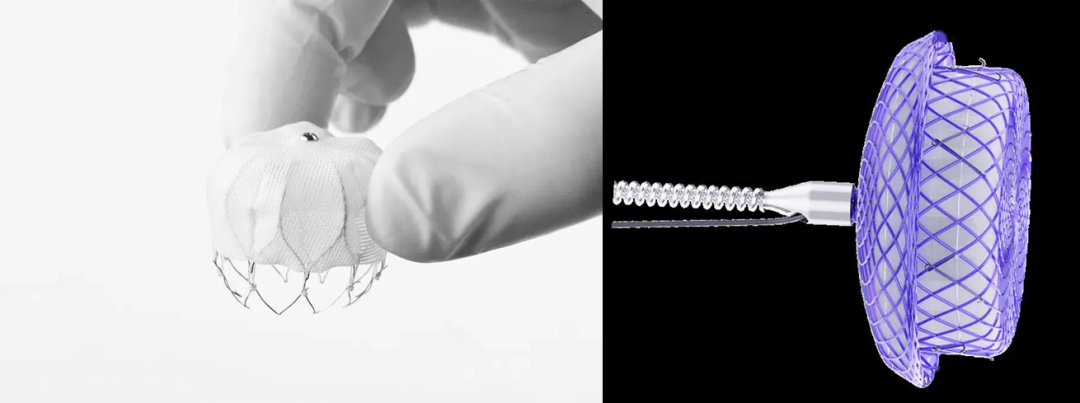
图12 MemoLefort(左)Bio-Lefort(右)左心耳封堵器
▹AnchorMan——半封闭封堵器
2024年1月5日,微创心通医疗科技公司的AnchorMan左心耳封堵器系统获NMPA批准上市,成为中国唯一获批的半封闭型左心耳封堵器(图13)。AnchorMan的设计特点在于其尾部的12个“3D”折叠单元与网架结构相互配合形成了独有的半封闭结构,兼顾了开放式和封闭式封堵器的优点。AnchorMan左心耳封堵器系统已于2021年9月完成临床入组,注册临床结果在2023年5月在欧洲心血管介入大会(Euro-PCR 2023)最新突破性临床试验(Late Breaking)主板块发布[22]。研究显示,AnchorMan左心耳封堵器系统 12个月临床结果达到其对比对照组产品非劣效性的主次要终点;在封堵有效性方面,其术后12个月的完全封堵和微小残余漏(残余分流 < 3mm)情况优于对照组产品。
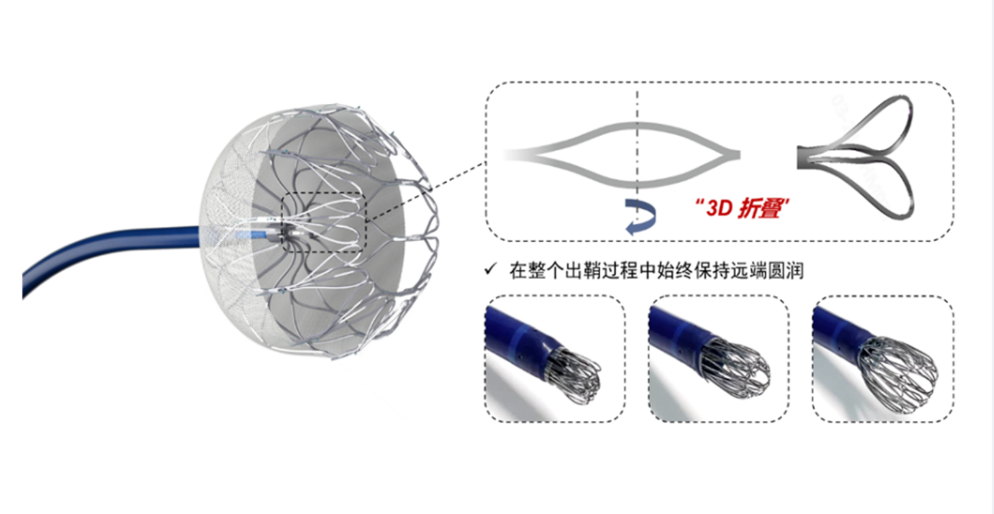
图13 AnchorMan®左心耳封堵器系统
▹CLAAS——开辟蹊径泡沫基质
CLAAS左心耳封堵系统是由Conformal Medical公司研发的一款完全不同于已上市器械的左心耳封堵器,它摒弃了传统封堵器的“金属骨架覆膜”的设计,使用一种独特基于泡沫的架构。这种泡沫的架构采用聚四氟乙烯(ePTFE)泡沫基质,具有多孔开孔结构,孔大小为400 ~ 600 μm,利用泡沫材料的弹性和可塑性,使封堵器能够充分贴合LAA的内壁,形成一个均匀的封闭层并减少血栓形成事件。仅有两种型号(27 mm和35 mm),却可以广泛治疗患者[23](图14)。CLAAS 左心耳封堵的正在进行临床研究是一项多中心、单臂、前瞻性研究,纳入了美国 10 中心、59例患者,并在植入后45天和1年内进行TEE随访,以评估手术的安全性和有效性。TCT 2023上发布了其一年TEE随访,结果显示97.7%的患者残余分流 ≤ 3mm,证实其密封性。

图14 CLAAS左心耳封堵系统
▹Occlutech——无倒钩设计
Occlutech 左心耳封堵器(Occlutech International AB, Helsingborg, Sweden)具有圆锥形自膨式镍钛合金网状结构,通过远端边缘的回折环固定,聚氨酯覆膜提高密封性和加快内皮化(图15)。该封堵器已于 2016 年获得 CE 批准。

图15 Occlutech 左心耳封堵器
2.2.2盘式封堵器
▹Amplatzer Cardiac Plug (ACP)系列——经典双盘设计
AMPLATZER Cardiac Plug (ACP; Abbott Vascular, Chicago, Illinois, US) 系列封堵器在世界享有盛名,旗下有多款经典针对先天性心脏病封堵器如,房间隔缺损、室间隔缺损、动脉导管未闭、卵圆孔未闭等,同时AMPLATZER也在早期也对LAAC进行诸多探索。2003年发表了第一项使用Amplatzer房间隔封堵器封堵左心耳的研究,共纳入16名58~83岁的NVAF患者在四个中心接受治疗,其中14人在局部麻醉下进行,其中1例发生急性器械栓塞[24]。
随后AMPLATZER研发出了首款盘式左心耳封堵器ACP I,该系统秉承了AMPLATZER经典的设计,采用全编织的双盘结构,其内盘置于左心耳内部用以固定,外盘封住左心耳口部(图16)。在一项纳入1047名患者,平均随访时间13个月的临床研究中,植入ACP I封堵器的手术成功率达97.3%,手术相关并发症为5%;平均随访12个月后,卒中或短暂性脑缺血发作(TIA)的年发病率为2.3%[25]。
Amulet(ACP II)是第二代Amplatzer 左心耳封堵器。相比ACP I,Amulet在锚定倒钩、内盘厚度、双盘连接长度等方面进行了改进(图16)。Amulet IDE作为一项前瞻性、多中心、随机对照研究,通过与Watchman封堵器的头对头比较,评价Amulet封堵器在预防房颤卒中方面的安全性和有效性,研究纳入了来自全球150家中心的1878名患者。结果提示,Amulet封堵器在主要安全性终点(14.5%对vs. 14.7%)和主要有效性终点(2.8% vs. 2.8%)方面均不劣于 Watchman封堵器[26]。Amulet在2021年8月获得了FDA批准上市。

图16 Amplatzer Cardiac Plug (ACP )系列封堵器
▹LAmbre系列封堵器——首款“中欧双认证”国产封堵器
LAmbre™左心耳封堵器系统由深圳先健科技有限公司研发设计,封堵器采用独立伞盘结构设计,是首款自主研发且拥有发明专利的国产左心耳封堵器系统,该系统于2016年获CE认证、2017年获中国NMPA注册批准(图17)。
2021年9月8日,先健科技公司宣布,其自主研发的新一代左心耳封堵器LAxible™获得NMPA注册批准。LAxible™左心耳封堵器最大的改进就是对初代的末端倒刺进行了钝化处理,球头末端增加了与心耳接触的表面积,有效降低对心耳壁压力,大大减少心包积液的发生率(图17B)。此外,LAxible™还扩充了规格型号至22种,针对患者心耳情况的多样性提供了更丰富的选择方案,这都使得其安全性和有效性得到了很大提升。
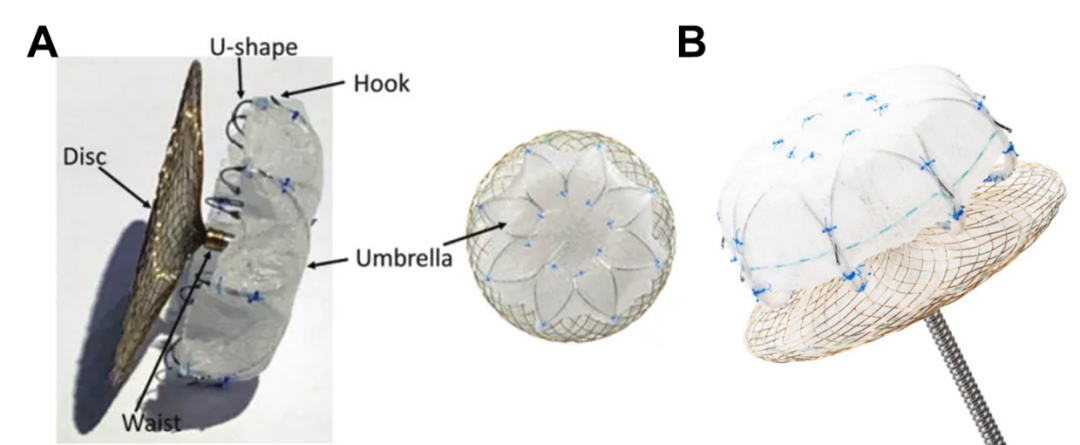
图17 LAmbre系列封堵器
▹LACbes系列封堵器——他山之石、可以攻玉
LACbes是由上海普实医疗器械股份有限公司自行设计研究开发的双盘式结构左心耳封堵器,于2017年获批NMPA“创新医疗器械特别审批”,2019年获准上市。该封堵器的主要创新点在于与固定柱一体化编织并使用激光雕刻技术完成、具有形状记忆性能的10 ~ 14个微倒钩,该设计的倒刺不仅可以固定牢固.而且经过反复回收和释放,倒刺形状和角度均无改变。在2023年,普实医疗研发出分体式LACbes,可根据心耳情况,自由组装内外盘,做到定制化封堵效果,已启动全国中心上市前临床试验。

图18 LACbes系列封堵器
▹LeftEAR——塞盖双封堵理念
LeftEAR®左心耳封堵器系统是广东脉搏医疗科技有限公司设计制造的全球首款“双盘内塞”式左心耳封堵器系统,已于2022年9月,获得NMPA的注册批准(图19)。据悉LeftEAR®左心耳封堵器系统不仅集结了内塞式与外盖式封堵器的众多优点,同时考虑到中国患者左心耳形态特点及中国术者的手术操作习惯,具有双重固定、双重封堵、低残余分流、型号齐全、操作简单等优势。LeftEAR®左心耳封堵器系统安全性及有效性俱佳,其一年随访研究结果显示器械相关血栓(DRT)发生率0%;器械周围残余分流(PDL)≤ 3 mm 98.3%;主要复合终点事件发生率1.6%[27]。

图19 LeftEAR®左心耳封堵器
▹Ultraseal——“三叶帆”外盘设计
Ultraseal(Cardia Inc,Eagan,MN)左心耳封堵器是一种自膨胀封堵器,包括锚定的球形框架和3 叶帆的封堵盘,两部分通过双铆钉连接,已于2016年获CE批准(图20)。Ultraseal Ⅱ在Ultraseal基础上的远端固定盘去除了中心固定铆,使得封堵器的径向张力减小,安全性增加;封堵器的总长度从15 ~ 21 mm减小至10 ~ 18 mm,且心房侧的覆盖盘边缘增加了聚合物裙边,避免了器械对周围组织结构的磨损。

图20 Ultraseal系列封堵器
▹Laager——“3+2”
Laager左心耳封堵器是由上海心玮医疗科技设计研发,已于2022年4月25日正式获得NMPA批准上市。Laager封堵器的设计可简化总结为“3+2”。“3”意指“三个圆设计”:圆润钝头倒刺设计、一体式圆结构固定盘以及编织圆形封堵盘及内嵌铆头;“2”则表示“两个点优势”:固定盘和封堵盘之间为活连接点,可自适应多样左心耳结构;规格型号更多点,多样选择满足不同临床需求(图21)。Laager左心耳封堵器安全性和有效性注册临床研究由全国12家中心共同参与完成,共计入组212例患者,王祖禄教授在CICI 2022大会上首次分享了研究结果:手术成功率为96.2%,3年随访结果显示4例患者在随访期间死亡,仅2例出现缺血性卒中(3.30%)。

图21 Laager左心耳封堵器
▹LAMax
LAMax左心耳封堵器是由深圳信立泰自主研发,已于2022年6月13日获NMPA批准上市,该系统据称具有MRI兼容、高耐腐蚀性能、收放自如且锚定稳固,以及器械血栓概率低等多项优点;此外,该产品规格覆盖全面,可适配不同的左心耳尺寸形态,适用于更广泛的患者群体(图22)。

图 22 LAMax左心耳封堵器
▹SeaLA系列封堵器——消融&封堵
SeaLA左心耳封堵器是由德诺电生理医疗科技有限公司自主研发的新一代左心耳封堵器系统,已于2022年11月获得NMPA批准注册(图23)。据悉,该产品的密封盘和锚定盘的设计均采用了创新的专利设计,保证了其可靠的锚定和密封性。该公司旗下最新的E-SeaLA封堵器是一款带有消融功能的左心耳封堵器,利用脉冲能量消融技术,集高效左心耳电隔离与左心耳封堵于一体,且临床中不需借助三维标测设备,仅靠DSA、超声的引导即可完成左心耳的消融与封堵,快速高效地实现左心耳完全电隔离。

图23 SeaLA系列封堵器
▹SimuLock
SimuLock左心耳封堵器宁波迪创医疗设计研发,据称是全球首款仿生型且可组装式左心耳封堵器(图24)。该封堵器有以下特点:1)全球首款可根据需求模块化组装设计的个性化定制产品,尺寸规格覆盖范围广,精准匹配广大房颤患者差异性巨大的左心耳解剖结构;2)全球首创的仿生鱼骨微刺+仿八爪鱼结合的仿生学设计,实现在左心耳腔内吸式填塞效应,助力锚定稳定性,并有望显著降低心包积液及填塞事件;3)内外双塞连体式层层封堵有效性更佳,是全球原创可控差异内皮化覆膜技术的产品,其中全氟化3D外包覆微孔阻流膜兼具防血栓、促内皮且可控内皮化,内塞阻流膜兼具促凝血、加速内皮化,有望彻底解决同类产品表面血栓形成率高发问题。该封堵器的前瞻性、多中心、随机对照确证性临床试验已于2023年正式启动,并于2023年11月8日由复旦大学附属中山医院完成了首例入组。

图24 SimuLock左心耳封堵器
2.2.3 其他类型封堵器
传统的“塞、盘”式封堵器在全世界已经植入了超过50万例,其安全性和有效性得到了充分的验证,但是仍存在两个较为棘手的问题,一是多数左心耳的开口并不平整,并且口部也往往存在发达的梳状肌,传统的封堵器无法完全贴合导致残余分流(Peri-device leak,PDL)的形成;二是封堵器作为既存在心腔内异物容易形成器械相关血栓(Device related thrombus, DRT),这也是为什么LAAC术后患者仍需抗栓治疗一短时间。鉴于此,许多的研发公司另辟蹊径提出了众多解决方案。
▹LaMinaR——旋转封闭 LAA
LaMinaR是继WaveCrest之后强生收购的第二款左心耳封堵系统。区别于常规的左心耳封堵器,LaMinaR系统是一个球锁结合的新器械,在系统进入左心房,并从输送系统中推出“Ball”,自膨胀镍钛合金“Ball”被推入左心耳,其中小结与组织接合,通过旋转至左心耳完全关闭;然后用一朵小雪花“Lock”从外部将“Ball”锁定到位,将左心耳完全关闭。该系统具备外科方式封闭左心耳的优势,可以最大限度地降低PDL 和DRT 形成的风险(图25)。在临床研究中成功植入到 15 名人体受试者,植入后 12 个月内没有发生安全事件,在 45 天时,通过TEE和 CT 扫描评估,所有受试者均达到了左心耳闭合的要求,没有器械相关血栓形成,在 12 个月的随访中保持稳定[28]。
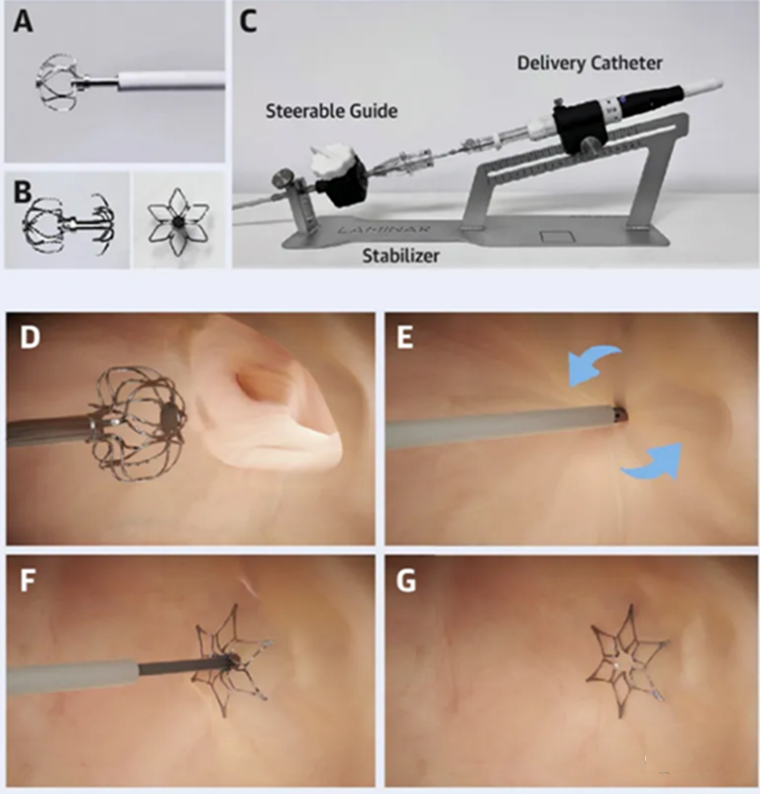
图25 LaMinaR左心耳关闭系统
▹Appligator—— “内科结扎”
Appligator(Append Medical,Inc. OR YEHUDA, ISRAEL)是一款从心腔内对左心耳进行结扎系统,其手术过程是利用输送系统将一个网篮装置固定在左心耳上,在通过将左心耳向左心房拉,使左心耳向左心房凹陷,最后通过缝线扎紧根部,实现左心耳完全关闭(图26)。Appligator优点类似于AtriClip,但是Appligator经股静脉进入,具有更小创伤。与传统的左心耳封堵器相比,具有两大新颖之处。首先:手术过程简化,无需进行测量和定位;其次,Appligator在术后只在心腔内留下一条缝合线,从而降低DRT的风险。

图26 Appligator左心耳封闭系统
▹Lariat——内外双管齐下
Lariat系统(Sentre HEART Inc, Palo Alto, Calif)是一种管腔外的软组织套索设备,它是在心包层面对左心耳进行封闭。不同于传统的外科介入器械,Lariat系统还需要在心腔内置入一个气囊导管与心包外导管上的磁铁相配合,以使接近左心耳基底部的心外膜结扎带置于最理想的位置,从而实现左心耳的彻底闭合(图27)。因此Lariat系统在使用上还需要透视或者TEE的引导。该系统获得FDA批准用于软组织封堵。
一项多中心的研究纳入了712名使用LARIAT装置行左心耳封闭的患者,结果显示手术成功率为95.5%,急性并发症包括1例死亡和10例经外科手术修复的心脏穿孔。TEE随访的显示,2-5 mm残余漏发生率为 6.5%,血栓发生率为 2.5%[29]。目前,没有关于 LARIAT 系统的RCT,其具体安全性和有效性还需进一步验证。

图27 Lariat系统
除此之外,还有多种尚在临床试验阶段的新兴设计器械,如采用独特的杯盘和圆盘设计的OMEGA(Eclipse Medical, Inc. Dublin,Ireland)左心耳封堵器(图28)、“内科stapler”的Sepiola Endomatic系统(图29)、带有消融功能的塞式Aurigen封堵器(图30)以及酷似Amulet内盘的塞式IrisSealTM封堵器(图31)。
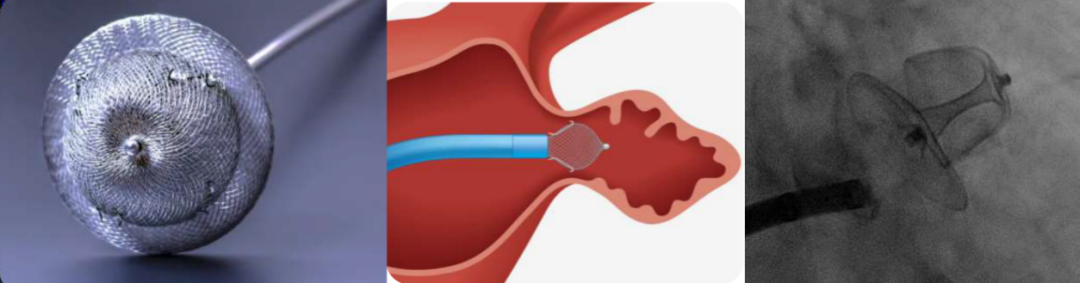
图 28 OMEGA Eclipse左心耳封堵器
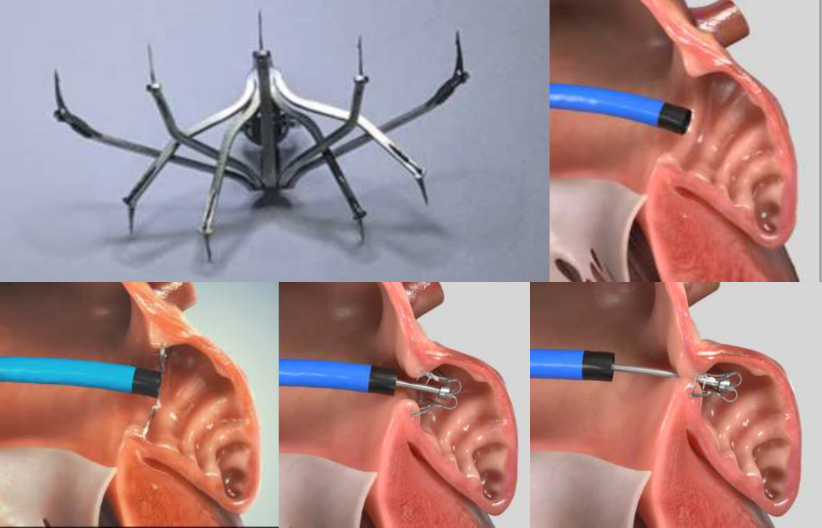
图29 Sepiola Endomatic系统
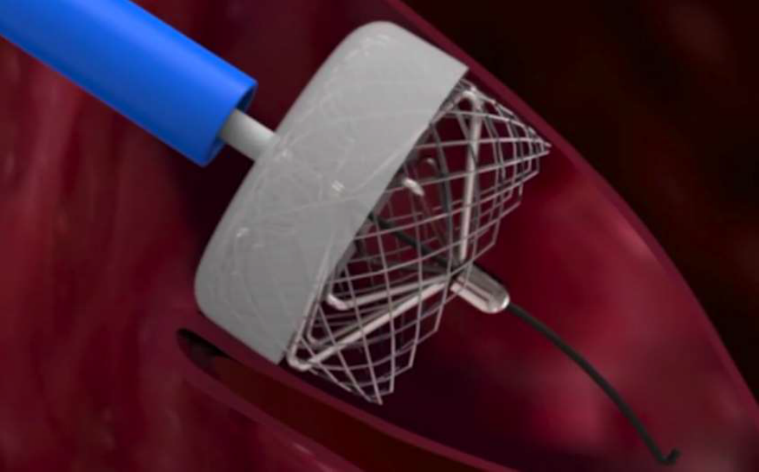
图30 Aurigen可以消融的左心耳封堵器

图31 IrisSealTM左心耳封堵器
03
左心耳干预的前景未来发展
左心耳干预方式从最开始的外科直接切除缝合发展到现在的微创经皮封堵,其中各类器械层出不穷,各项新兴技术如雨后春笋般蓬勃发展(图32),正逐步趋于追求更加安全有效以及更好的手术预后。得益于微创手术以及超高的安全性和有效性,内科干预左心耳的方式是目前的主流选择,但是术后仍存在PDL以及心腔内存在异物导致DRT仍是两个亟待解决的问题。从最新的器械设计来看,解决残余分流主要是优化封堵器骨架结构,使得封堵器贴合性更好;而解决DRT则是通过改进封堵器表面覆膜材料来实现。而最新的从心房侧完全关闭左心耳的方式(LaMinaR、Appligator、Sepiola Endomatic等系统)似乎有希望解决以上两大难题,只是目前的临床数据太少,尚无法明确器械的安全性与有效性。此外,针对不同人群的定制化左心耳封堵器也是解决问题的主要思路,如现在器械采用的分体式设计以及越来越多的型号选择都可以解决一些实际问题;同时随着材料的技术的不断发展,亲心肌细胞的水凝胶填充左心耳[30]以及3D打印技术“量身定制”左心耳封堵器[31]也让未来的LAAC事业充满想象。
在治疗理念上,未来左心耳干预的发展可能会更多地与房颤管理联合从而形成一套房颤管理体系,随着最新脉冲消融的逐渐成熟以及传统电生理企业在收购和商业合作上持续加码LAAC,未来房颤管理与左心耳干预的联动将更加频繁。
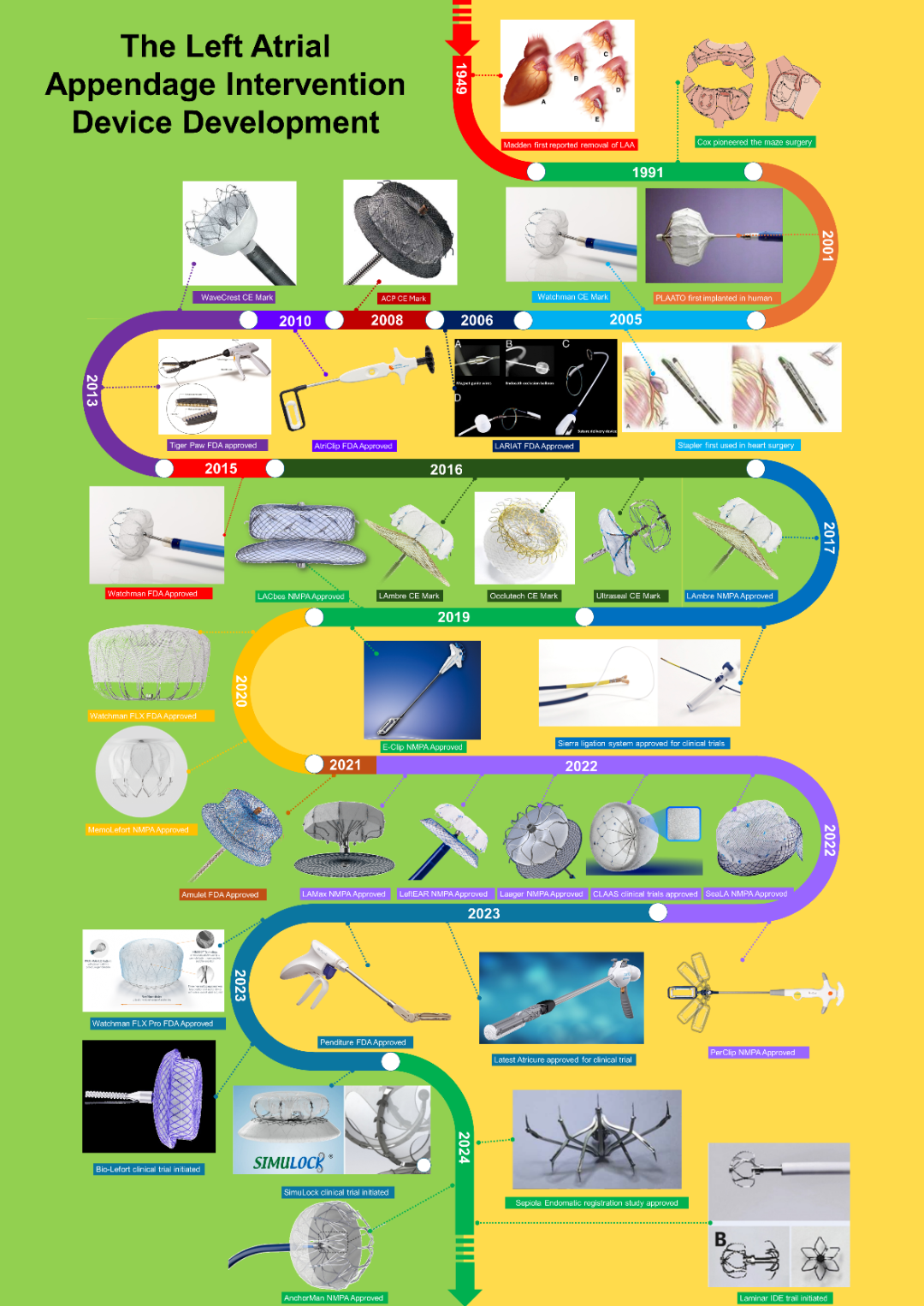
图32 左心耳干预的器械发展
参考文献:

