
近年来,关于血管内超声(IVUS)或光学相干断层成像(OCT)等腔内影像技术的临床数据大量涌现。这些研究数据的激增推动了腔内影像指导下的经皮冠状动脉介入治疗(PCI)在日常临床实践中的应用。当前随机临床研究的结果为腔内影像指导下PCI的益处提供了有力支持,特别是在复杂病变(如左主干病变、弥漫性长病变、慢性完全闭塞、严重钙化病变、分叉病变和支架内再狭窄)以及高危患者(如急性心肌梗死或慢性肾病患者)的诊断和治疗中。在腔内影像指导下的PCI术中,术者会努力实现支架植入优化,以最大限度地发挥腔内影像指导的优势。

近日,来自韩国的Yongcheol Kim等教授在本期《JACC: Asia》杂志发表了最新综述《Widespread Use of Imaging-Guided percutaneous coronary intervention in Asia: Time for Extended Application》,全面回顾了腔内影像指导下PCI的最新临床数据以及IVUS/OCT衍生的支架优化标准。严道医声网将全文翻译,供各位同道参考学习。

本文目录
一、要点
二、引言
三、腔内影像指导下的PCI的现状:指南与证据
腔内影像指导下的PCI的最新指南
IVUS指导下的PCI的关键临床数据
OCT指导下的PCI的关键临床数据
腔内影像指导下的PCI,以及IVUS指导与OCT指导下的PCI比较的关键临床数据
四、根据病变和患者亚组进行腔内影像指导的临床数据
左主干病变(Left main disease)
弥漫性长病变(Diffuse long lesion)
慢性完全闭塞病变(CTO lesion)
钙化病变(Calcified lesion)
分叉病变(Bifurcation lesion)
支架内再狭窄(ISR lesion)
血流储备分数阴性伴易损斑块的冠状动脉狭窄病变
急性心肌梗死(AMI)
五、腔内影像预测临床结局改善:PCI优化策略
支架植入前评估
支架植入后评估
➤ 支架膨胀情况(Stent expansion)
➤ 支架贴壁(Stent apposition)
➤ 支架边缘夹层(Stent edge dissection)
➤ 组织脱垂(Tissue prolapse)
腔内影像指导下的各种支架优化标准
六、支架植入后的随访评估
新生内膜增生和新生内膜覆盖(Neointimal hyperplasia and neointimal coverage)
新生动脉粥样硬化(Neoatherosclerosis)
晚期支架贴壁不良(Late SM)
七、结论
要点
腔内影像指导下的PCI可改善急性心肌梗死、复杂病变患者的临床预后。
OCT指导下的PCI的临床预后与IVUS指导下的PCI相当。
在腔内影像指导下的PCI中,支架优化是必需的,以最大限度地发挥腔内影像指导的优势。
引言
尽管冠状动脉造影仍然是评估病变严重程度、判断狭窄位置和管腔直径,进而指导治疗的重要手段,但其源自二维投影的局限性也显而易见。最近的研究强调了能够进行三维分析的血管内超声(Intravascular Ultrasound, IVUS)和光学相干断层成像(Optical Coherence Tomography, OCT)在临床结果上的优越性。因此,当前的指南建议,在进行支架优化时应考虑使用IVUS或OCT。本综述重点关注腔内影像指导下的经皮冠状动脉介入治疗(Percutaneous Coronary Intervention, PCI)的临床证据和实际应用,以及实现支架优化的策略,包括支架优化的具体标准。
01
腔内影像指导下的PCI的现状:指南与证据
腔内影像指导下的PCI的最新指南
关于腔内影像评估(包括IVUS或OCT的使用)的建议,最近的欧洲和美国指南给出了类似的立场,具体如下[推荐等级/证据水平]:
在接受冠状动脉支架植入术的患者中,应考虑使用IVUS或OCT以实现PCI的优化。[IIa/B]
在评估支架失败(如支架内血栓形成和支架内再狭窄)的机制时,应考虑使用IVUS和/或OCT。[IIa/C]
在无保护左主干病变患者中,应考虑使用IVUS以优化PCI。[IIa/B]
在最近的欧洲指南中,建议在急性冠状动脉综合征(Acute Coronary Syndrome, ACS)的情况下考虑使用腔内影像指导[IIa/A]。此外,对于ACS病因不明的患者,可以考虑使用OCT或IVUS(最好是OCT)进行冠状动脉内成像[IIb/C](表1)。

IVUS指导下的PCI的关键临床数据
许多随机临床研究研究了腔内影像指导的作用,特别是IVUS指导下的PCI。IVUS指导下的药物洗脱支架(Drug-Eluting Stent, DES)植入在慢性完全闭塞病变(Chronic Total Occlusion, CTO)患者中取得了显著改善,与冠脉造影指导相比,1年临床结果显著改善。
有两项关键的随机对照研究证明了,与冠脉造影指导相比,IVUS指导下的PCI对复杂病变的DES的短期和长期益处:IVUS-XPL(Impact of Intravascular Ultrasound Guidance on Outcomes of Xience Prime Stents in Long Lesions)研究和ULTIMATE(Intravascular Ultrasound Guided Drug Eluting Stents Implantation in “All-Comers” Coronary Lesions)研究。
最近,多中心随机研究——IVUS-ACS(Intravascular Ultrasound-Guided Versus Angiography-Guided Percutaneous Coronary Intervention in Acute Coronary Syndromes)表明,IVUS指导下的PCI改善了ACS患者的1年临床结果,改善主要由靶血管相关的心肌梗死和缺血驱动的靶血管血运重建所驱动。
最近的一些注册研究还表明,IVUS指导下的PCI在具有各种复杂病变特征或高缺血风险(如急性心肌梗死或慢性肾脏病)的患者中具有临床益处。IVUS指导下的PCI相关关键临床数据的总结可参见表2。

OCT指导下的PCI的关键临床数据
尽管OCT的分辨率(10微米)高于IVUS,但关于OCT指导下的PCI与传统冠脉造影指导下的PCI之间作用的数据却很少。在一项回顾性多中心注册研究CLI-OPCI(Centro per la Lotta contro l’Infarto–Optimization of Percutaneous Coronary Intervention)中,OCT指导下的PCI与改善临床结果显著相关。DOCTORS(Does Optical Coherence Tomography Optimize Results of Stenting)研究表明,与非ST段抬高型心肌梗死患者相比,OCT指导下的PCI在术后血流储备分数方面显著高于冠脉造影指导下的PCI。然而,在TOTAL(Thrombectomy Versus Percutaneous Coronary Intervention Alone)研究的一项前瞻性倾向匹配队列中,ST段抬高型心肌梗死患者在OCT指导与冠脉造影指导下的PCI之间的1年缺血风险没有显著差异。最近,两项大规模随机研究为OCT指导下的PCI的临床益处提供了有力证据;ILUMIEN IV: OPTIMAL PCI(Optimal Coherence Tomography Guided Coronary Stent Implantation Compared to Angiography: a Multicenter Randomized Trial in percutaneous coronary intervention)研究表明,OCT指导下的PCI在即刻最小支架面积(minimal stent area)方面取得了显著改善(OCT组为5.72 ± 2.04 mm²,冠脉造影组为5.36 ± 1.87 mm²;P < 0.001),但两组之间2年靶血管失败率没有显著差异。OCTOBER(Optical Coherence Tomography Optimized Bifurcation Event Reduction)研究表明,与冠脉造影指导下的PCI相比,OCT指导下的PCI在改善复杂分叉病变的2年靶病变失败率方面更优。正在进行的OCT随机研究(OCCUPI[Optical Coherence Tomography-Guided Coronary Intervention in Patients With Complex Lesions: a Randomized Controlled Trial; NCT03625908])有望进一步支持与冠脉造影指导下的PCI相比,OCT指导下的PCI在复杂病变中的有效性。OCT指导下的PCI相关关键临床数据的概述可参见表3。

腔内影像指导下的PCI,以及IVUS指导与OCT指导下的PCI比较的关键临床数据
针对复杂冠状动脉病变患者的RENOVATE-COMPLEX-PCI(Randomized Controlled Trial of Intravascular Imaging Guidance versus Angiography-Guidance on Clinical Outcomes after Complex Percutaneous Coronary Intervention)随机研究表明,与冠脉造影指导下的PCI相比,腔内影像指导下的PCI(包括IVUS74%和OCT26%)与心原性死亡、靶血管相关心肌梗死或靶血管血运重建的复合终点降低相关。
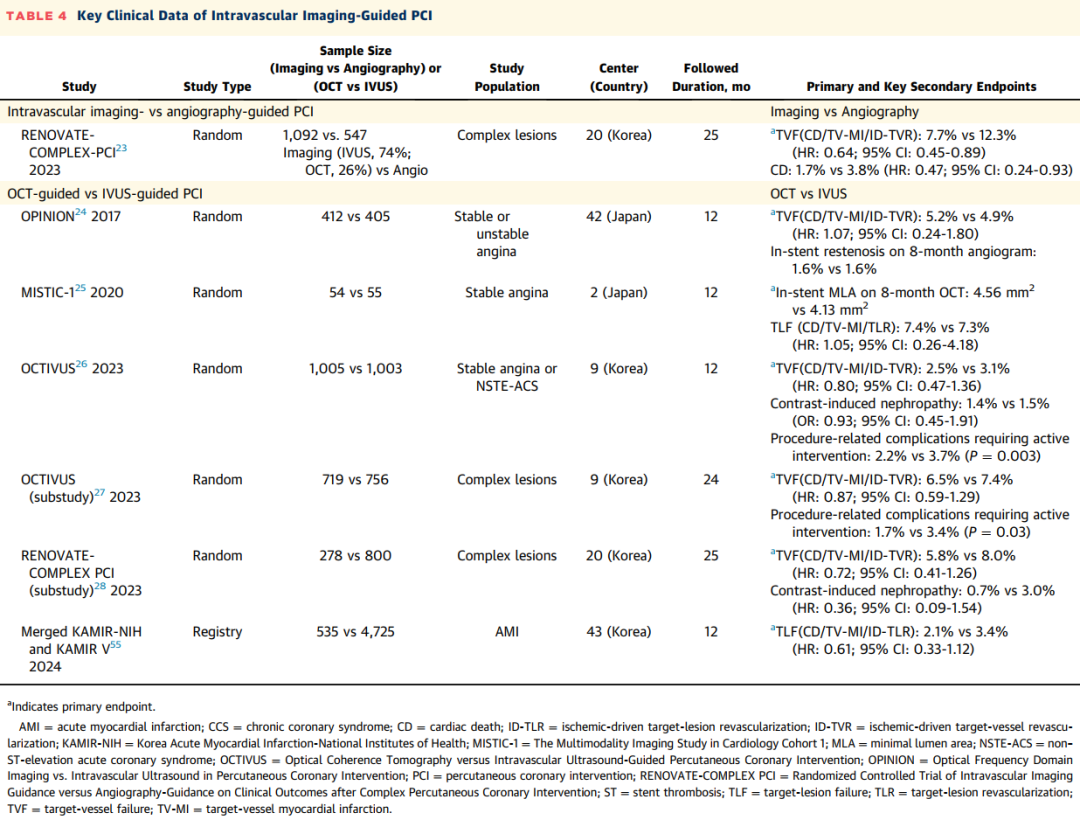
关于IVUS指导与OCT指导下的PCI之间的临床结果比较,两项随机非劣效性研究OPINION(Optical Frequency Domain Imaging vs. Intravascular Ultrasound in Percutaneous Coronary Intervention)和MISTIC-1(The Multimodality Imaging Study in Cardiology Cohort 1)研究表明,在中期和长期临床结果方面,OCT指导下的PCI并不劣于IVUS指导下的PCI。最近,OCTIVUS(Optical Coherence Tomography versus Intravascular Ultrasound-Guided Percutaneous Coronary Intervention)随机研究表明,在1年内心原性死亡、靶血管相关心肌梗死或靶血管血运重建的复合终点方面,OCT指导下的PCI并不劣于IVUS指导下的PCI。在RENOVATE和OCTIVUS研究的亚组分析中,对于复杂病变患者,OCT指导下的PCI与IVUS指导下的PCI在靶血管失败风险方面相似。这些研究的详细信息见表4。
02
根据病变和患者亚组进行腔内影像指导的临床数据
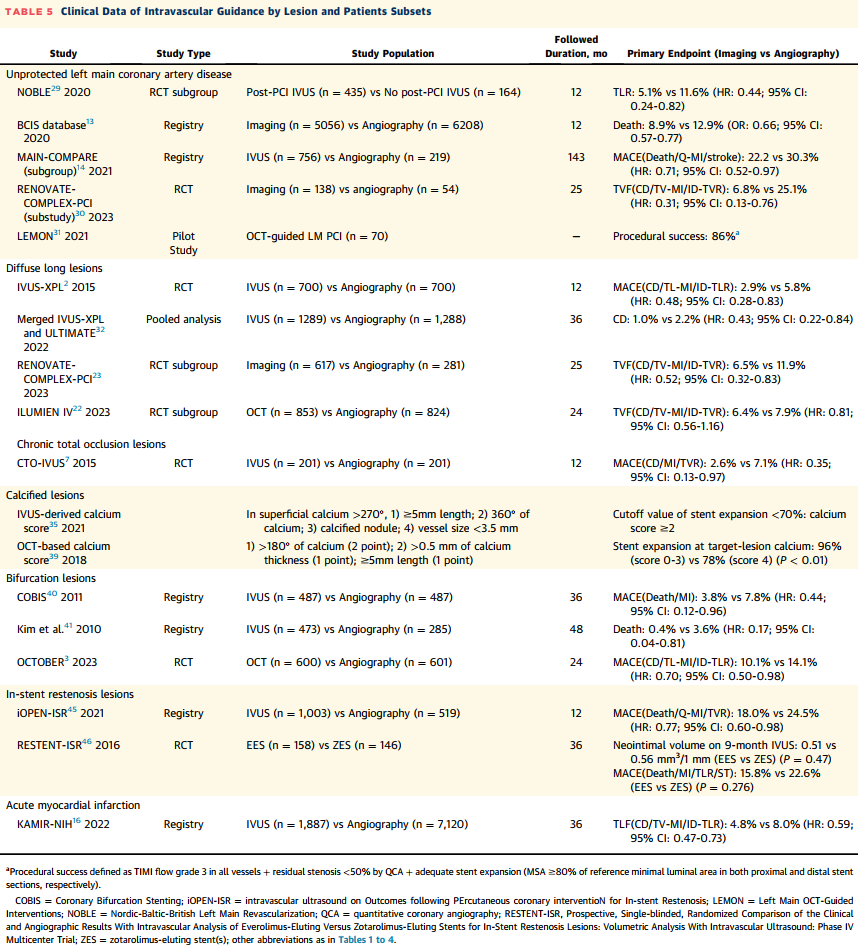
前瞻性队列和注册数据支持腔内影像模式(包括IVUS和/或OCT)指导的PCI对复杂冠状动脉病变的益处,这些病变包括无保护左主干病变、弥漫性长病变、CTO、严重钙化病变、分叉病变、支架内再狭窄,以及对高风险患者(如急性心肌梗死患者)的益处(表5)。
左主干病变(Left main disease)
对于左主干病变,IVUS指导可准确测量参考段的血管大小以及斑块向远端左主干分叉的延伸程度,从而通过选择合适的支架和支架后扩张来优化PCI。多项研究支持腔内影像对无保护左主干病变的益处,特别是IVUS指导。NOBLE(Nordic-Baltic-British Left Main Revascularization)研究的亚组分析显示,在无保护左主干病变的PCI中,使用IVUS预防支架膨胀不全可改善5年靶病变血运重建率(根据PCI术后LMS MSA将患者分为三组,最小支架面积≥13.4 mm²组为0%,而≤10.8 mm²组为12.2%,P = 0.002)。BCIS(British Cardiovascular Intervention Society)注册数据显示,与冠脉造影指导相比,腔内影像指导的无保护左主干病变PCI与较少的即时手术并发症以及1个月和12个月生存率改善相关。在MAIN-COMPARE(Revascularization for Unprotected Left Main Coronary Artery Stenosis: Comparison of Percutaneous Coronary Angioplasty Versus Surgical Revascularization)研究的亚组分析中,与冠脉造影指导的PCI相比,IVUS指导的无保护左主干病变PCI与较低的10年死亡风险相关。最近,RENOVATE-COMPLEX-PCI研究的亚组分析显示,与冠脉造影指导相比,腔内影像指导可显著降低无保护左主干病变的靶血管失败风险,且主要归因于心原性死亡的降低。
然而,因为难以获得最佳血液清除效果,OCT指导的无保护左主干病变PCI在评估左主干开口方面存在一些局限性。然而,一项初步研究证明了OCT指导的左主干中/远端PCI的可行性和安全性。未来需要随机研究来观察OCT指导的无保护左主干病变PCI是否可改善临床结局。
弥漫性长病变(Diffuse long lesion)
使用腔内影像技术进行精确的形态学评估有助于为弥漫性长病变选择合适的支架尺寸和长度。此外,与支架膨胀和贴壁情况、边缘有无夹层、病变覆盖是否完全以及残余病变相关的支架植入后评估,可以降低DES植入后支架内血栓形成的风险。在观察长支架(≥28 mm)的IVUS-XPL研究中,与常规冠脉造影指导相比,IVUS指导的PCI在1年时心原性死亡、心肌梗死或靶病变血运重建的复合终点发生率显著降低,且主要是由于靶病变血运重建的风险较低。在进一步随访中,与常规冠脉造影指导相比,IVUS指导的获益仍旧维持。从IVUS-XPL和ULTIMATE研究的患者水平分析来看,与冠脉造影指导的PCI相比,IVUS指导的长支架植入与3年时心原性死亡以及复合终点(心原性死亡、心肌梗死或支架内血栓形成)显著降低相关。
关于OCT指导弥漫性长病变的证据一直不足。RENOVATE-COMPLEX-PCI研究的亚组分析显示了IVUS和OCT对长病变(预期支架长度至少为38 mm)的益处。在ILUMIEN IV研究的亚组分析中,对于弥漫性长病变(≥28 mm)的患者,OCT指导的PCI在2年时并未降低靶血管失败的风险。未来需要进一步的研究来证实OCT指导对弥漫性长病变是否获益。
慢性完全闭塞病变(CTO lesion)
在CTO的PCI期间,IVUS指导对于其成功至关重要;在无锥形残端的情况下,建议将导丝送入CTO近端紧邻的侧支中。在顺行或逆行CTO的PCI期间使用IVUS也被证明在识别导丝位置、追踪导丝以及提供真腔或内膜下空间的关键信息方面有所帮助。此外,IVUS有助于确定最佳支架尺寸和着陆点,并确保支架完全扩张,并在治疗复杂的长段钙化CTO时发挥作用。在CTO-IVUS(Chronic Total Occlusion Intervention With Drug-eluting Stents)随机研究中,与常规冠脉造影指导的慢性完全闭塞PCI相比,IVUS指导的慢性完全闭塞PCI改善了DES植入后12个月的主要不良心脏事件发生率。
由于成像采集过程中对比剂注射存在可能扩大假腔或导致冠状动脉破裂的风险,OCT在CTO中的指导作用在日常实践中仍然受限。
钙化病变(Calcified lesion)
在管理钙化病变时腔内影像技术指导至关重要,其能精确评估钙化的严重程度、治疗效果,并指导选择合适的斑块修饰策略。基于IVUS得出的钙化评分考虑了钙化弧和长度、钙化结节的存在以及血管直径,已被证实可预测支架膨胀不全并指导钙化斑块修饰。然而,由于IVUS难以穿透钙化组织,因此在评估钙化斑块部位的钙化厚度和血管直径方面存在局限性。
OCT由于其更高的分辨率(优于IVUS),能够更好地描绘钙化病变,并对钙化病变进行定量分析,包括钙化厚度、钙化病变角度和钙化斑块长度等参数。多项研究提出了OCT的临界值,包括钙化弧和厚度,可以采用不同斑块修饰策略实现钙化斑块的成功碎裂。最近,一种基于OCT的钙化评分系统被引入,该系统考虑了钙化弧、厚度和长度,以辅助在支架植入前进行钙化斑块修饰。图1展示了OCT指导的PCI重度钙化斑块的代表性病例。

图1 OCT指导的严重钙化病变DES植入
病例1。(A) 一名67岁女性非ST段抬高型心肌梗死患者的前降支中段严重狭窄的冠脉造影图像。(B) 和 (C) PCI前的OCT评估显示纵向环形钙化斑块,基于OCT的钙化评分为3分(最大钙化角度>180° [2分],钙化长度>5.0 mm [1分],最大钙化厚度[0分])。(D) 经切割球囊扩张后的OCT显示钙化碎裂(箭头所指)。(E) 支架植入后OCT显示存在裂纹(箭头所指)。(F) 三维支架图像和贴合指数显示支架完全扩张且未发生贴壁不良。(G) 支架植入后最终冠脉造影显示远端血流良好,无残余狭窄。
病例2。(H) 一名54岁男性稳定型心绞痛患者的前降支近端至中段弥漫性严重狭窄伴重度钙化的冠脉造影图像。(I) PCI前的OCT评估显示弥漫性环形斑块伴厚钙化,基于OCT的钙化评分为4分(最大钙化角度>180° [2分],钙化长度>5.0 mm [1分],最大钙化厚度[1分])。(J) 经旋磨和非顺应性球囊扩张后的OCT显示钙化斑块得到良好修饰。(K) 支架植入后的OCT显示多处钙化碎裂(箭头所指)。(L) 最终冠脉造影显示远端血流良好,无残余狭窄。
分叉病变(Bifurcation lesion)
腔内影像评估对于分叉病变中的斑块在主支内的范围以及侧支开口受累情况的判断具有不可替代的作用。以往登记数据显示,对于非左主干分叉病变患者,IVUS指导的DES植入术与改善临床预后相关。已有数项研究探讨了IVUS预测分叉病变主支支架植入后侧支闭塞的危险因素。值得注意的是,研究结果表明,侧支开口处斑块,尤其是弥漫性斑块,或在支架植入后远端主支支架过度扩张导致嵴部移位,是IVUS指导下PCI过程中侧支闭塞的预测因素。
OCTOBER是首个针对复杂分叉病变的OCT随机研究,结果显示,与冠脉造影指导下的PCI相比,OCT指导下的PCI在2年内主要不良心血管事件的发生率显著降低(10.1% vs 14.1%)。由于OCT的分辨率高于IVUS,因此可以提供清晰的纵向重建图像,明确识别嵴部、侧支开口以及嵴部角度。一项回顾性OCT研究表明,近端主支斑块的高脂质含量和侧支开口狭窄严重程度是主支支架植入后侧支闭塞的独立预测因素。图2和图3展示了分叉病变PCI期间侧支受累相关的冠脉造影、IVUS和OCT因素,以及OCT指导下分叉病变PCI的典型病例。

图2 侧支受累的危险因素
斑块移位和嵴部移位的预测因素总结在方框中(①和②)。
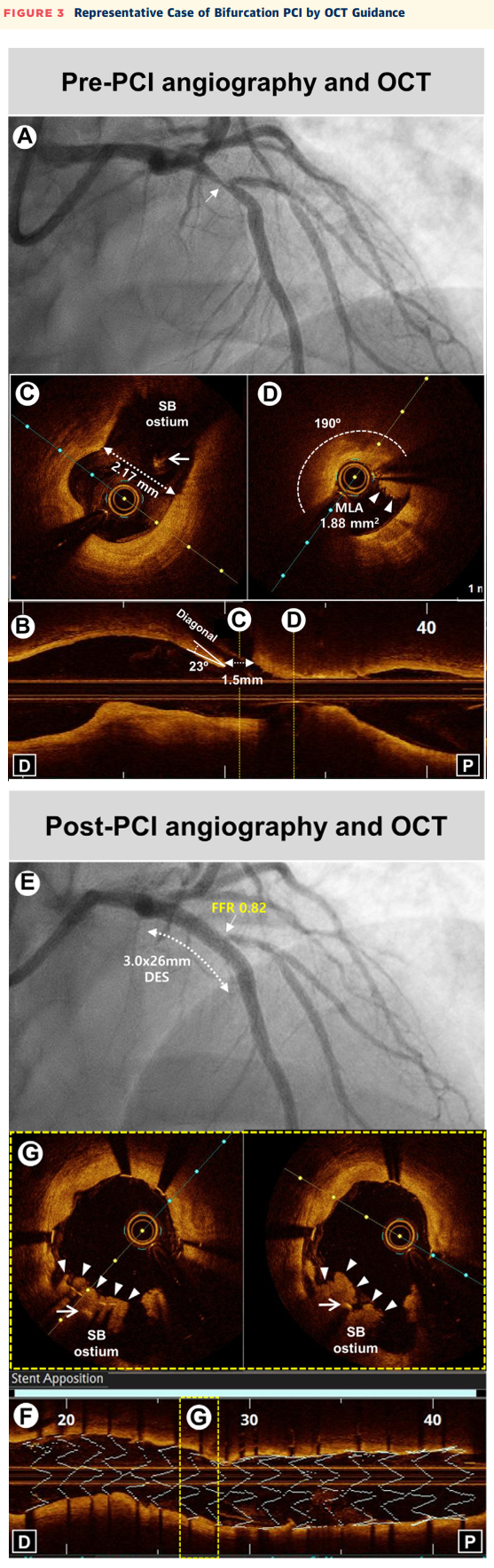
图3 OCT指导下分叉病变PCI的典型病例
(A)基线冠脉造影显示前降支近端分叉病变处严重狭窄(箭头)。(B)PCI前OCT显示嵴部角度狭窄(23°)且嵴部尖端至分支对侧距离短(1.5 mm)。(C和D)OCT图像显示最小管腔面积(MLA)为1.88 mm²,近端主支存在大范围富含脂质的斑块(190°)和管腔内血栓(箭头所指),侧支开口无狭窄(侧支开口直径:2.17 mm)(箭头:侧支导丝)。(E)PCI后冠脉造影显示,在前降支近端严重狭窄处采用侧支导丝保护技术成功实施了PCI,术后侧支开口处血流为TIMI 3级,证明血流储备功能无影响(FFR:0.82)。(F)三维支架图像和贴壁指数显示支架完美植入。(G)OCT图像显示斑块向侧支开口移位(箭头所指)(箭头:侧支导丝)。
支架内再狭窄(ISR lesion)
IVUS和OCT(OCT)在支架内再狭窄的管理中发挥着至关重要的作用,可以诊断和评估支架内再狭窄,辅助精确测量病变,确定再狭窄的原因(包括评估支架膨胀不全),并优化治疗策略。一项针对支架内再狭窄治疗患者的观察性研究表明,与冠脉造影指导的治疗相比,IVUS指导下的PCI在支架内再狭窄PCI后1年内的主要不良心血管事件(MACE)发生率更低。在针对DES内再狭窄患者的随机研究中,新一代DES的再次支架植入治疗在减少新生内膜体积和晚期管腔丢失方面安全有效,且MACE发生率较低。
高分辨率的OCT能够精确评估新生内膜组织。Gonzalo等人将OCT上的新生内膜特征分为三种不同的模式:均质型、异质型和分层型(图4)。回顾性OCT研究表明,药物涂层球囊(Drug-Coated Balloon,DCB)治疗后的再狭窄率在具有均质型新生内膜的支架内再狭窄病变中较低,而异质型新生内膜且OCT测得的最终最小管腔面积不足的情况与DES内再狭窄经DCB治疗后的再狭窄显著相关。此外,在DCB治疗支架内再狭窄病变中,OCT上新生内膜体积的大幅减少据报道可改善临床结局。应使用各种定性或定量OCT分析来研究使用DCB或DES治疗支架内再狭窄后的临床结局。

图4 新生内膜组织的代表性OCT图像
均质型(后向散射模式无局部变化的均匀光学特性)(A),异质型(局部变化的光学特性和各种不同后向散射模式)(B),分层型(具有不同光学特性的同心层)(C)。
血流储备分数阴性伴易损斑块的冠状动脉狭窄病变
指南不建议对血流储备分数(FFR)>0.80的非血流限制性中度狭窄病变进行血运重建,但易损斑块(也称为纤维粥样斑块、富含脂质或坏死核心的斑块)是未来发生不良心血管事件的潜在因素。一项前瞻性双盲研究表明,在FFR阴性的病变中,OCT检测到的薄帽纤维粥样斑块与糖尿病患者不良事件发生率高5倍相关。最近,PREVENT(Preventive Coronary Intervention on Stenosis with Functionally Insignificant Vulnerable Plaque)随机研究表明,与单独的最佳药物治疗相比,FFR阴性狭窄病变且经IVUS或OCT检测到的高风险易损斑块接受预防性PCI加最佳药物治疗在长期随访(长达7.9年)期间MACE的发生率显著降低。
急性心肌梗死(AMI)
尽管IVUS在急性心肌梗死救治中具有潜在的益处,但关于腔内影像指导下的PCI对急性心肌梗死-PCI后的临床结局影响的大规模随机研究仍然缺乏。几项注册数据支持在急性心肌梗死救治中使用腔内影像指导在短期和长期结局方面的优势。一项日本全国性的前瞻性注册研究J-MINUET(Japanese Registry of Acute Myocardial Infarction Diagnosed by Universal Definition)显示,与冠脉造影指导相比,IVUS指导下的PCI与较低的住院死亡率相关。在韩国KAMIR-NIH(Korea Acute Myocardial Infarction-National Institutes of Health)前瞻性注册研究中,对于接受PCI的急性心肌梗死患者,使用IVUS或OCT指导与1年临床结局的改善相关。关于IVUS指导的长期益处,与冠脉造影指导下的PCI相比,IVUS指导下的PCI在3年时的靶病变失败风险显著降低,这主要归因于包括心源性死亡或靶血管心肌梗死在内的硬性终点改善。
关于急性心肌梗死救治中OCT指导下的PCI,汇总数据显示,与IVUS指导相比,OCT指导下的PCI在1年靶病变失败方面的临床结局相当。需要进一步的随机研究来确定在急性心肌梗死中IVUS或OCT指导的益处。
03
腔内影像预测临床结局改善:PCI优化策略
据报道,基于腔内影像评估的支架优化策略与支架植入后的良好临床结局相关(表6)。IVUS-XPL研究显示,与未达到IVUS支架优化标准的患者相比,达到IVUS优化标准(IVUS指导下的PCI组中54%的患者)的患者在1年时的主要不良心血管事件发生率显著降低。同样,在ULTIMATE研究中,与未达到优化标准的患者相比,达到优化标准(IVUS指导下的PCI组中53%的患者)的患者在1年时的靶血管失败率显著降低。CLI-OPCI II OCT注册研究也显示,非优化支架植入是较差临床结局的独立预测因子。因此,在使用腔内影像指导下的PCI时,达到IVUS或OCT指导下的支架优化标准是改善临床结局的关键。在本节中,我们回顾了使用腔内影像指导下的支架优化标准的数据。

支架植入前评估
支架植入的腔内影像指导能够准确评估斑块特征以及病变段和参考段的横向和纵向测量,并对病变长度进行评估。基于病变段和参考段的测量为术者提供了支架着陆区信息,并允许精确选择支架的尺寸和长度以实现支架植入优化。
支架植入后评估
腔内影像能够在支架植入后评估支架膨胀、贴壁、边缘夹层和支架内情况。当腔内影像发现支架膨胀不全时,建议采用腔内影像指导下的高压球囊后扩张,并已知与较低的心脏事件风险相关。此外,腔内影像检测到的支架贴壁不良或边缘夹层可能需要进行进一步的支架优化手术。
支架膨胀情况(Stent expansion)
支架膨胀情况是支架优化标准中最重要的因素。最小支架面积作为绝对扩张(直接测量的横截面最小支架面积)和相对支架扩张(最小支架面积与平均参考管腔面积的比值)被认为是预测DES植入后不良事件的关键参数。在PCI前后进行腔内影像指导,可以通过使用非顺应性球囊进行后扩张,从而实现最佳的支架扩张,进而制定适当且安全的PCI策略。各种最小支架面积标准被引入;根据病变或临床特征,提出了绝对扩张(最小支架面积>4.5或5.0mm2),并根据平均参考管腔面积或远端参考管腔面积提出了相对扩张(最小支架面积≥平均参考管腔面积的80%或90%,或≥远端参考管腔面积的90%至100%)。关于支架膨胀不全的定义,日本IVUS专家共识将其定义为:支架扩张低于参考血管的80%或低于最小支架面积的临界值(例如,<5.0或5.5 mm2)。
由于OCT的回撤速度更快,无法在OCT图像中选择最大舒张期的帧,其测量值与IVUS不同。因此,OCT得出的临界值会小于IVUS标准:在非左主干病变中,OCT得出的最小支架面积<4.5 mm2与IVUS得出的最小支架面积<5.0 mm2或5.5 mm2相对应。OCT的相对扩张标准与IVUS相似:最小支架面积≥平均参考管腔面积的80%或90%,或≥远端参考管腔面积的100%。表7提供了最佳支架扩张的详细值。
支架贴壁(Stent apposition)
目前,腔内影像对支架贴壁情况影响的数据仍显示出相互矛盾的结果。支架贴壁不良被定义为在未涵盖侧支的血管节段中,至少一个支架小梁与血管壁之间缺乏接触,分为3种类型:
1)急性支架贴壁不良:DES植入后即刻检测到的贴壁不良;
2)晚期持续性支架贴壁不良:随访时依旧存在的原急性支架贴壁不良;
3)晚期获得性支架贴壁不良:尽管在支架植入后立即进行腔内影像时支架完全贴壁,但在随访期间新出现的支架贴壁不良。
尽管急性支架贴壁不良经常观察到,但据报道,在连续的OCT随访研究中,高达90%的病例都能得到很好的解决。然而,严重的急性支架贴壁不良可能会延至晚期持续性支架贴壁不良。关于急性支架贴壁不良的临床影响,据报道,它经常在支架内血栓形成的患者中观察到,但尚不清楚急性支架贴壁不良是否与支架内血栓形成的发生直接相关。详细的贴壁标准见表7。

支架边缘夹层(Stent edge dissection)
支架边缘夹层是与PCI后主要不良心脏事件(包括支架内血栓形成)相关的已知危险因素。由于OCT的分辨率高于IVUS,因此边缘夹层在OCT中更常被观察到。此外,IVUS得出的标准侧重于其角度和长度,而OCT得出的标准则侧重于其深度和长度。因此,通过腔内影像评估的夹层是否存在是与支架优化相关的主要因素。一般来说,非血流限制性支架边缘小夹层在临床随访中已知无影响;然而,在血流限制性或支架边缘大夹层的情况下,建议进行额外手术,包括补充支架。为了评估支架边缘大夹层的严重程度,强烈建议评估夹层沿横向或纵向的延伸情况以及中膜或外膜层的受累情况。表7详细列出了边缘夹层的各种优化标准。
组织脱垂(Tissue prolapse)
组织脱垂定义为通过支架小梁突入管腔内的组织(斑块和/或血栓),由于OCT的分辨率更高,因此在OCT中比IVUS更频繁地观察到组织脱垂。尽管在IVUS分析中,组织脱垂与围手术期心肌梗死、急性和亚急性支架内血栓形成相关,但有报道称,成功的PCI后的检出的组织脱垂对长期临床结果无显著影响。然而,一项多中心OCT注册研究显示,不规则组织脱垂(而非光滑或破裂纤维组织突出)是1年不良临床结果的独立OCT预测因子。下一步应研究和明确组织脱垂对腔内影像的短期和长期影响以及影响结果的组织脱垂特征。
腔内影像指导下的各种支架优化标准
腔内影像指导下的主要支架优化标准包括支架膨胀、支架贴壁以及边缘夹层存在与否的截止值或定义。支架膨胀作为支架优化的标准被描述为绝对扩张(最小支架面积)或相对扩张(最小支架面积与预定参考面积的比较)。支架贴壁标准经常使用血管壁与支架小梁之间的最大距离,通常小于200至400微米被认为是可接受的标准。边缘夹层是通过侧向和纵向评估受累主要夹层的存在来决定的,并且还会评估与支架边缘夹层相关的血流状态。各项腔内影像指导PCI随机研究中使用腔内影像指导的支架优化标准总结在核心图示和表7中。

04
支架植入后的随访评估
新生内膜增生和新生内膜覆盖(Neointimal hyperplasia and neointimal coverage)
支架植入后的随访腔内影像评估有助于对导致晚期管腔丢失、再狭窄或支架内血栓形成的新生内膜增生进行定性和定量评估。基于IVUS的研究主要评估了支架植入后和随访期间新生内膜增生的定量评估。然而,由于IVUS的分辨率较低,其在新生内膜类型定性评估方面存在局限性。相比之下,高分辨率的OCT在多项研究中实现了对支架植入后新生内膜的定性分析(图4)。由于从DES(DES)血栓形成的尸体解剖研究中已知,内皮化延迟是支架内血栓形成的最强组织学预测因子,因此OCT在评估各种DES小梁的新生内膜覆盖方面的作用备受关注。特别是,在OCT中,被定义为表面缺乏新生内膜的未被组织覆盖小梁,据报道在支架内血栓形成中较为常见,并且在与冠脉造影指导的随机对比中,通过OCT指导支架植入可以减少其出现。此外,在一项OCT注册研究中,随访时较高的未被组织覆盖小梁百分比(临界值为≥5.9%)与DES植入后不良缺血事件的发生相关,有些术者根据这一阈值在短期随访的OCT评估中个体化制定相应的抗血小板治疗方案。
新生动脉粥样硬化(Neoatherosclerosis)
病理学研究表明,在DES植入后,新生内膜中存在包含胆固醇结晶的大面积坏死核心,这与原生冠状动脉中遇到的易损斑块相似。OCT的分辨率高于IVUS,能够检测支架内新生动脉粥样硬化,测量纤维帽的厚度,并识别薄纤维帽粥样硬化斑块(TCFA),即支架内纤维帽厚度平均≤65微米,富含脂质的坏死核心,以及大量的巨噬细胞浸润的部分。就DES失败而言,新生动脉粥样硬化是导致晚期血栓形成和再狭窄的最重要机制,并且新生动脉粥样硬化斑块破裂被认为是导致支架内血栓形成的促成因素。有研究显示,新生动脉粥样硬化的决定因素为支架植入时长、当前吸烟状态和慢性肾病(CKD)。因此,在DES植入后的随访中,通过OCT检测新生动脉粥样硬化有助于预测患者的临床结果。
晚期支架贴壁不良(Late SM)
多项研究强调了晚期支架贴壁不良(包括晚期持续性和晚期获得性)的潜在重要性,这些情况在支架植入后的随访IVUS检查中观察到,可能与心血管事件发生率增加有关。在随访的IVUS研究中,晚期获得性支架贴壁不良已被报道与极晚期支架内血栓形成的风险增加相关,并被认为是预测DES失败的最重要因素。
关于晚期支架贴壁不良的OCT数据,尽管由于OCT的高分辨率能力,晚期支架贴壁不良的检出率较高,但其临床相关性仍然缺乏证据。由于大多数关于晚期支架贴壁不良的腔内影像研究都是基于回顾性或注册数据进行的,因此有必要进行大规模、前瞻性的长期腔内影像研究,以评估在当前DES时代晚期支架贴壁不良的临床影响。
05
结论
许多随机对照研究和注册研究表明,常规使用腔内影像指导的PCI可以显著改善冠状动脉疾病患者的临床结果,尤其是那些具有高缺血风险的患者,如急性心肌梗死、慢性肾病患者,以及复杂病变患者(包括无保护左主干病变、CTO、严重钙化病变、分叉病变和支架内再狭窄)。值得注意的是,最近的数据表明,OCT指导的PCI提供的临床结果与IVUS指导的PCI相当。
在腔内影像指导的PCI中,术者尝试实现支架优化植入,以使腔内影像指导的益处最大化。为了在日常临床实践中进一步改善患者的长期结果,需要制定专门的腔内影像指导支架优化植入标准。
JACC: Asia编委会
