
术中经食管超声心动图(TEE)在经导管三尖瓣修复及置换中起着关键性作用。但由于三尖瓣的解剖位置靠前易受伪影干扰且形态学变异度高,其经导管治疗的术中TEE成像较二尖瓣困难。近期德国Mainz心脏瓣膜中心及丹麦哥本哈根大学医院心脏中心分别对术中TEE在三尖瓣经导管缘对缘修复(TEER)和多模态成像在经导管三尖瓣置换(TTVR)中的应用进行了总结,现分享如下。

一

术中TEE在三尖瓣经导管
缘对缘修复(TEER)中的应用1
1.前言
德国Mainz心脏瓣膜中心每年有近100例经导管三尖瓣介入治疗患者,Jaqueline G及其团队根据在过去几年中积累的经验总结出了一套三尖瓣TEER术中TEE监测的规范化成像流程。该流程主要包括以下步骤:1)导管室TEE设备的合理放置,2)全面的声窗获取,3)三尖瓣形态学的详细评估,4)制定适当的介入治疗决策,5)术中操作引导,6)手术效果的评估。成像流程的关键部分是使用经胃声窗,以避免TEE成像中频繁遇到的阴影伪像。他们将这种使用经胃成像来引导瓣叶捕获的方法称为“Mainz法”。该成像流程适用于TriClip装置(Abbott,USA)和PASCAL修复装置(Edwards Lifesciences,USA)。
2.监测流程
2.1步骤1:导管室的设备放置
导管室中超声心动图设备的放置需要最大限度地减少超声医师的辐射暴露,并提供符合人体工程学的工作环境。为此强烈建议超声医师的位置尽量安排在操作台的头端,而C形臂则在左侧方。只有这样安排才能将两个移动的防护铅屏放置在C型臂和超声心动图设备之间,并为超声波设备、超声医师和食管探头放置台提供足够的空间(图1)。
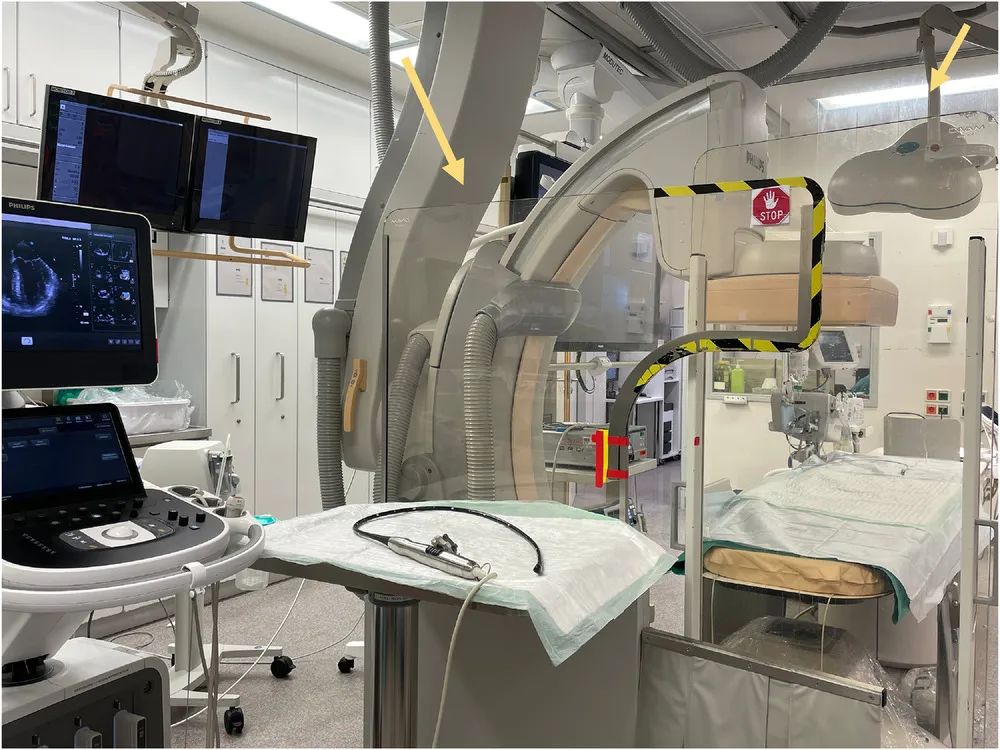
图1 杂交手术室。杂交手术室中超声心动图医生的位置位于导管室操作台的头端。两个移动的透明防护铅屏(黄色箭头)保证足够的辐射防护。注意C型臂的位置在工作台的侧面,为超声机、探头放置台和超声医生提供了足够的空间。
2.2步骤2:获取声窗及其相应的切面
由于三尖瓣解剖位置靠心脏前部,经食管超声成像会受到一定的影响,因此全面的声窗扫查至关重要。该规范流程主要依赖于两个经食管(即食管中段和食管下段)和一个经胃声窗。每个声窗应用于特定的切面/成像平面。

图2 用于三尖瓣的缘对缘修复的基本声窗、实时双平面切面以及TEE探头位置的相应透视图像。(A-C):食管中段RV流入-流出道切面;(D-F):食管下段RV流入-流出道切面;(G-I):三尖瓣的经胃短轴切面。
2.2.1食管中段右心室流入-流出道切面
经食管的成像旨在获得右心室(RV)的流入-流出道切面,该切面可用作双平面成像和3D渲染的主要成像平面。首先,食管中段声窗获得的RV流入-流出道切面(TEE探头的扫查角度通常为60-80度;图2A和B)的扫描平面平行于TV前后瓣与隔瓣的对合缘。如果成像平面正确,其对应的垂直平面(通过激活双平面成像获取)则显示为镜像的四腔心切面。如果隔瓣显示完整且没有阴影伪像(尤其是在前联合处),则说明该切面成像质量较好。
2.2.2 食管下段右心室流入-流出道切面
通常,从食管下段声窗可以更好的获得RV流入-流出道切面(图2D和E)。该切面是通过将TEE探头推进到右心房后壁正后方的远端食管中获得的(图2F)。探头在这个位置可以避开左心房、主动脉瓣以及房间隔,毫无遮挡的显示三尖瓣,而且避免了阴影伪像干扰。它是使用双平面进行三尖瓣功能评估并获取高帧频三尖瓣3D容积图像的理想切面。该切面TEE探头的扫查角度通常稍大于食管中段RV流入-流出道切面(80-100度)。
2.2.3 经胃短轴切面
评估三尖瓣瓣叶的一个基本切面是从经胃声窗获取的经胃短轴切面(图2G和H)。这是唯一能同时显示所有三尖瓣瓣叶的二维切面。它获取的是三尖瓣的短轴横切切面,在一个平面上显示所有瓣叶。通过实时双平面成像可以控制主成像平面的最佳扫查角度,并在其垂直方向的辅助成像平面上显示三尖瓣环(图2H)。获取该切面的方法是将TEE探头推进到胃中,并使探头前曲,同时将探头向患者右侧(顺时针方向)旋转(图2I)。扫查角度通常在20到60度之间,在RV增大和心轴偏离非常严重的情况下,可能需要更大的扫查角度。探头位置和角度的微调有助于优化成像平面。图2展示了所有三个不同声窗的15个切面示例图,同时显示了相应的透视下TEE探头位置。
2.2.4 3D成像的应用
3D成像在术中很有帮助,特别是在经胃成像不佳的患者中。除了完整瓣膜形态的三维显示之外,多平面重建(MPR)等专用工具还可以帮助测量瓣环内径、对合缘间隙大小或指导钳夹/瓣叶的相对位置调整。从所有声窗都可以获得三尖瓣的3D数据集。由于3D数据集的质量完全取决于2D图像的质量,因此应尽量在获取3D数据前将三尖瓣显示清晰。
为了对TV形态进行正确的3D MPR评估,所有三个成像平面都需要正确对齐。横向平面必须平行于三尖瓣环,另外两个平面的方向应生成RV流入-流出道切面和四腔心切面。横向平面的轻微平移可以更清晰的显示瓣叶边缘从而更准确的获得对合缘间隙的大小。将四腔心平面旋转到垂直于对合线的位置时,可以描记任何选定目标区域的瓣叶长度、环状直径和对合间隙大小(图4F-G)。
2.3 步骤3:三尖瓣形态学评价
三尖瓣是心脏里最复杂且解剖学变异度最大的瓣膜。尽管被称作三尖瓣,实际上却只有在大约50%的被检者中是真的三个瓣叶。在另一半的被检者中,多为四个瓣叶,且拥有两个后瓣叶的最为多见(图3A-F)。
因此,全面评估三尖瓣形态学并识别导致三尖瓣反流(TR)的潜在病理改变是制定合适的介入治疗策略的关键。TEER的原理是将RV游离壁(前瓣和/或后瓣附着处)向隔瓣牵引,因为所有修复装置均将隔瓣作为锚定点。所以,足够的隔瓣长度和活动度是保证TEER成功的关键,在手术前应该仔细评估。钳夹植入目标区域的隔瓣径向长度和栓系的存在与否是观察的重点,因为它们将直接影响手术结果。此外,通常位于前部的隔瓣切迹需要很好地显示识别,以避免抓握不足(图3)。
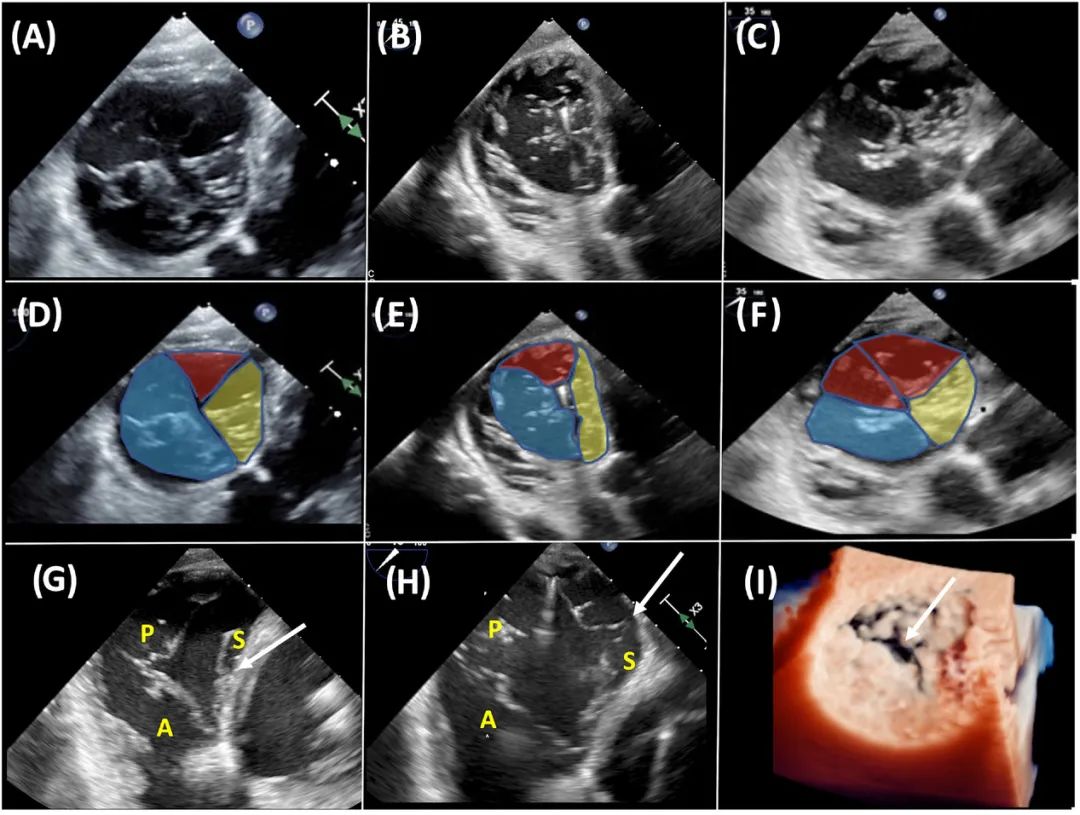
图3 具有不同瓣叶数目、大小、联合及切迹的三尖瓣形态。三尖瓣的经胃短轴切面显示三尖瓣瓣叶的解剖变异(A-C),后瓣P为红色,隔瓣S为黄色,前瓣A为蓝色(D-F)。根据深度和大小,可以鉴别较小的隔瓣切迹(G;白色箭头)和分隔两个隔瓣叶的联合缘(H;白色箭头)。图(I)显示TrueVue渲染的3D zoom容积图,从图中可获取有意义的三尖瓣形态学信息,包括中央对合间隙的大小。
2.3.1 对合间隙大小
(Coaptation gap size,CGS)
大多数进行性继发性TR患者存在的一个会影响缘对缘修复的成功的关键就是对合间隙的大小(CGS)。三尖瓣环的扩大或RV重构引起的瓣叶栓系,会导致三尖瓣对合间隙的产生,且最常位于前瓣(ATL)或后瓣(PTL)与隔瓣(STL)之间。不考虑栓系模式或瓣环径情况下,CGS决定了TEER治疗能否成功。数据表明CGS>7 mm可作为使用第二代MitraClip患者的技术性失败的预测指标。目前新一代装置使用的钳夹更长,稍大的三尖瓣对合间隙(≤10 mm)仍可以合理地使用TEER进行治疗。大的对合间隙,尤其是非中心或非前-隔位置的对合间隙已被证实会导致不良的手术结果,而孤立的前-隔对合间隙的治疗效果会比较好。钳夹植入的目标区域的对合间隙大小需要与瓣膜中心的最大间隙大小区分开来。虽然目标区域的间隙尺寸决定了成功植入钳夹的几率,但中心对合间隙尺寸也与钳夹植入成功的概率相关联(比如TR减小到≤2+)。
RV流入-流出道切面的实时双平面成像中对应的四腔心切面可进行对合间隙大小的测量。然而,对于2D超声心动图,只有经胃短轴切面才能显示对合间隙的全部范围和确切位置。这种情况下,正确选取成像平面并对真实的瓣叶边缘进行成像很重要,否则对合间隙大小会被高估。当不能获得经胃声窗时,3D MPR已被证明是测量对合间隙大小并定位钳夹植入的目标区域的一种很好的替代方法(见图4F-G)。3D容积图可以从所有声窗获取,但一般来说,从食管声窗获取的容积的时间和空间分辨率更高。
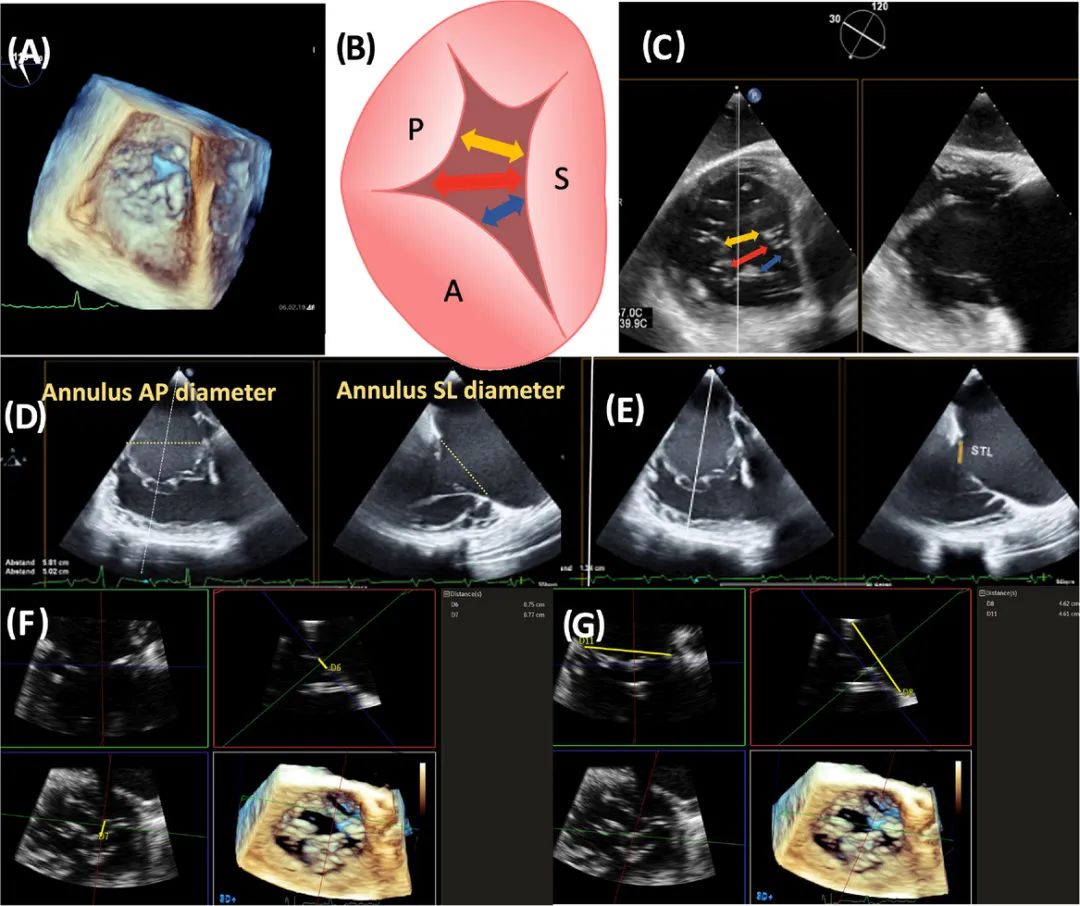
图4 TEER术前三尖瓣形态的关键测量。三尖瓣的3D-TEE显示一较大的中央对合间隙(A)。三尖瓣经胃短轴切面示意图显示对合间隙内径的测量:一个为横向的最大间隙内径(红色箭头);另两个位于放置钳夹的目标区域,分别在前瓣和隔瓣之间(蓝色箭头)以及后瓣和隔瓣之间(黄色箭头)(B)。三尖瓣的短轴切面显示的间隙测量值(C)。实时双平面瓣环前后径和横径的测量(D);在目标区域测量的隔瓣长度(E)。将两个正交切面的切割线调整到瓣环平面后的3D-TEE多平面重建图像显示:中央对合间隙(右上和左下图)(F)和瓣环前后径和横径的测量(左上和右上图)(G)。
2.4 步骤4:装置植入决策
差异化的装置植入决策是三尖瓣TEER成功的关键。在对瓣膜进行了详细的分析后,需要预先明确从哪里开始以及以何种模式植入装置。
一般来说,三尖瓣的TEER决策类似于二尖瓣。钳夹植入的目标位置是对合最差(或彩色多普勒信号最多)的部位。然而,在三尖瓣的TEER中,由于对合间隙尺寸常较大,该位置通常不能直接确定,并且需要多个钳夹的植入。而第一个钳夹的目标区域常临近最大间隙尺寸处。一般越靠近瓣叶联合,对合间隙越小。这主要发生在前联合处,因为在大多数患者中,对合间隙常向前延伸。第一个钳夹植入后不仅增加了对合面积,还将瓣叶对合保持在一个更中心的位置,方便后续钳夹的植入。该技术有助于处理较大的对合间隙。根据对合间隙向前联合和后联合的延伸,可以区分两种装置放置模式。仅对前-隔联合的治疗被称为“双孔化”;而对前-隔和后-隔两处联合的治疗被称为“三叶草策略”(图5E-F)。对于这两种技术,强烈建议从前面开始,因为更靠后放置的钳夹可能会导致经胃切面中大量的阴影伪像,影响随后的钳夹放置。在某些适应症中,比如后瓣脱垂时,有明确的钳夹植入位点可以直接解决病理问题,就不需要考虑这种阴影伪像影响。
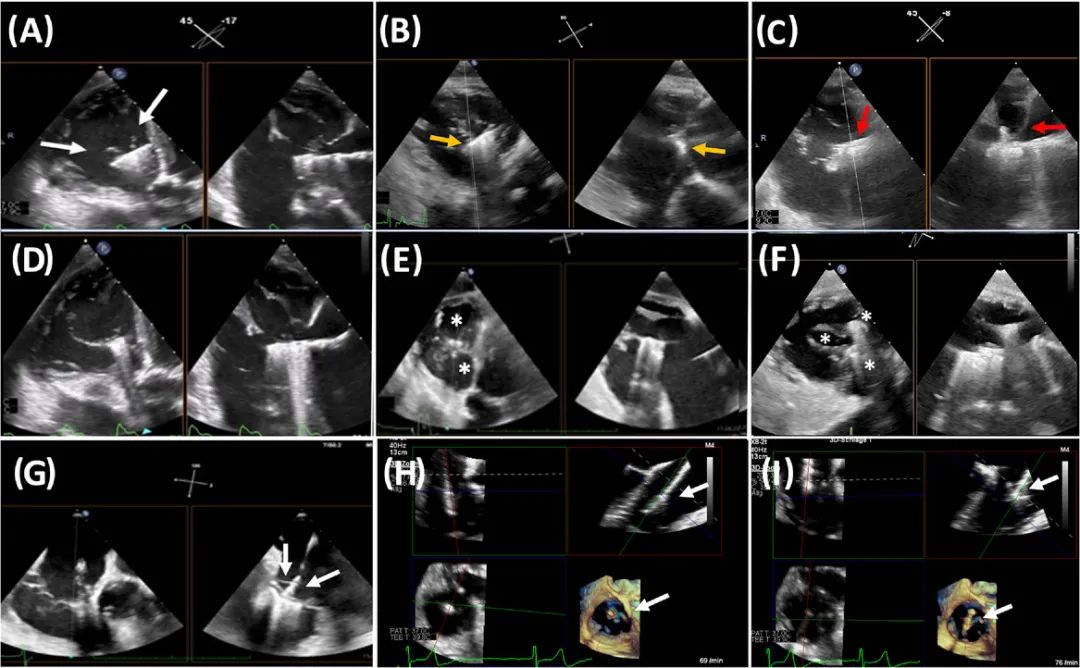
图5 双平面成像下三尖瓣的经胃短轴切面。(A-F):(A)显示一展开状态的TEER钳夹,两个瓣叶都已经进入钳夹内(白色箭头——注意瓣叶的明亮边缘);(B)和(C)记录整个钳夹的“扫查”式观察,确认前瓣在钳夹前臂上(黄色箭头)且隔瓣在钳夹间隔侧臂上(红色箭头);(D):钳夹闭合后前瓣和隔瓣的组织桥(注意瓣叶边缘如何直接延伸到钳夹的中心);(E)显示了在前-隔对合缘植入一个钳夹后形成的典型双孔结构(星号),而(F)中的三尖瓣在前-隔对合缘和后-隔对合缘分别植入一个钳夹后形成了三孔结构(星号)。没有经胃声窗的患者的替代切面:双平面成像的RV流入-流出道切面,显示瓣叶的捕获(箭头显示两个瓣叶都停留在打开的钳夹臂上)(G);三尖瓣的实时3D多平面重建图像显示三尖瓣瓣叶、钳夹与瓣环平面对齐(H),以及钳夹在前-隔方向的旋转(I)(白色箭头显示钳夹)。
2.5 步骤5:手术监测---瓣叶捕获
手术监测的步骤包括装置输送的成像、瓣叶-钳夹相互关系的显示和治疗效果的评估。右心房中的装置引入和转向可以通过双平面成像进行监测,首先从双腔切面,然后从RV流入-流出道切面进行观察。特别是在有多束起搏器导线的患者中,3D成像可以帮助指导临近瓣膜的操作,因为它能提供比双平面成像或透视成像更好的深度感知和空间定向。
与其它的监测流程不同,Jaqueline G及其团队开创性使用经胃切面作为主要成像平面来观察瓣叶捕获(图5)。首先,经胃切面获得的三尖瓣形态学相关信息比经食管切面多,这有助于识别瓣叶捕获时需要避开的瓣叶的联合或切迹。其次,钳夹本身,尤其是瓣叶插入钳夹的过程,可以在经胃切面中更精确地显示。这得益于横向成像平面能提供更多的信息,并且阴影伪像比经食管切面要少。后者甚至会导致经食管切面完全无法用于瓣叶捕获的引导。在这种情况下,能否熟练使用经胃切面将决定治疗的成败。
具体来讲,经胃短轴切面主要用来引导钳夹在目标区域的方向调整,并使用实时双平面成像来显示钳夹(图5A)。为了在经胃短轴中成功引导瓣叶捕获,需要非常小心地对相应瓣叶的明亮(高回声)边缘进行成像。只有这样,在瓣叶捕获时才能快速明确瓣叶是否夹合稳固。当然,从经食管声窗也能显示钳夹与瓣叶的关系(图5G)。Jaqueline G等指出,经胃短轴切面能完整显示瓣叶边缘(及其在进入钳夹臂后的状态),更好的确认正确的瓣叶位置,而经食管成像平面往往仅能显示瓣叶的矢状切面(且经常有阴影)(图5A)。此外,瓣叶与钳夹臂的贴合信息可以通过在经胃双平面成像中对两个钳夹臂进行取样线的 “扫查”操作来获取(图5B和C)。尽管通常不能在辅助成像切面中显示钳夹臂的完整长度(除非钳夹方向平行于超声束),但仍然很有帮助(图5B)。在绝大多数情况下,经胃成像也用来指导钳夹臂的夹合,因为在显示完整的瓣叶结构及其被夹入钳夹的过程方面经胃成像比经食管成像更具优势。
一般来说,成像扇区应该尽量缩小,以优化空间和时间分辨率。这一点在夹子降低、钳夹臂闭合时尤其重要。因为这是一个需要全神贯注的关键步骤,应该进行全面记录,方便对瓣叶捕获过程进行回顾分析,并对瓣叶插入的最终结果评估提供信心(图5D,动图1)。使用经胃切面引导瓣叶捕获过程的另一个优点是能即刻显示瓣叶捕获后形成的双孔或三孔结构,这是确保捕获成功的关键图像信息(图5E和F,图8)。
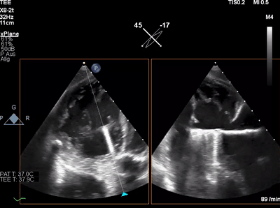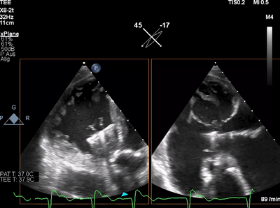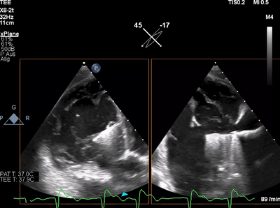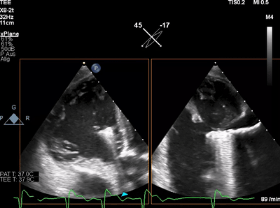
动图1 “Mainz方法”:TEE三尖瓣经胃短轴切面显示的瓣叶捕获过程,其中包括瓣叶在钳夹臂上的正确位置、钳夹夹合以及对形成的双孔结构的即刻评估
在少数无法获取经胃底TEE切面的患者中,介入手术的成功只能依赖于经食管TEE切面。如果图像较理想的话,可以通过单平面或双平面成像很好地显示瓣叶的捕获(图5G)。而调整钳夹方向有一个变通方法就是使用实时3D MPR(图5H和I),成像平面的切割类似于离线3D MPR分析(参见步骤2)。如果空间和时间分辨率足够的话,使用实时3D MPR来引导瓣叶捕获时,需要准确定位四腔心切面,尽量使其能显示输送装置的导管结构,以引导瓣叶-钳夹的相互位置调整。

图6 三尖瓣TEER装置植入后双平面成像的扫查角度调整。与二尖瓣的TEER一样,引导三尖瓣瓣叶插入的双平面成像也依赖于主成像平面的正确扫查角度(垂直于钳夹的打开角度)。如图所示,主平面的正确扫查角度将从显示前-隔钳夹装置的60度调整到显示后-隔钳夹装置的85度。

图7抓握不充分后出现前瓣的单瓣叶脱离(SLD)。一系列的双平面图像显示了此次钳夹放置因为前瓣的早期脱离而变得复杂。放置前(A)、放置中(B)和放置后(C)的钳夹图像。最初,两个瓣叶似乎都正确插入钳夹中(C),但仅几分钟后,就发现前瓣脱离(D)。使用双平面成像的三尖瓣短轴切面,显示钳夹在展开前出现完整的组织桥(E)和展开后脱离的前瓣(F)
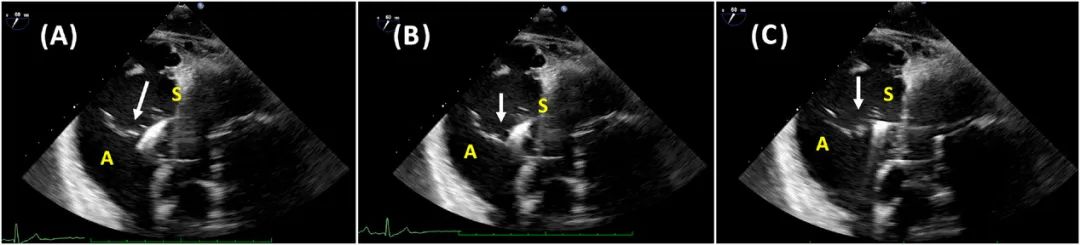
图8 三尖瓣的经胃短轴切面显示前瓣捕获不足所导致的早期SLD。钳夹成功捕获前瓣和隔瓣(A);在钳夹夹合(B)期间,前瓣部分脱离前钳夹臂(箭头);瓣叶部分捕获(C),注意瓣叶边缘没有进入钳夹的正中心。
2.6步骤6:手术监测——结果评估
在钳夹释放之前,需要确保瓣叶捕获充分,以防止单瓣叶脱离(single leaflet detachment,SLD)(图7和8)或钳夹脱落栓塞。Jaqueline G及其团队强烈建议在三尖瓣的经胃短轴切面下确认该操作,因为该切面可以显示瓣叶的捕获,并且可以非常准确地观察到插入的瓣叶(图5D,图8)。
此外,可以在经食管声窗使用实时双平面成像观察组织桥。主平面的扫查角度可以根据钳夹的位置和旋转角度进行微调。这种调整类似于二尖瓣TEER结果的双平面成像(图6)。如果在这个切面中能确保两个瓣叶均充分插入,则钳夹可安全释放。如果两个瓣叶都到达了钳夹的中心部位,则插入足够充分。如果某一个瓣叶的活动度较大则提示可能插入不充分,并可能会导致钳夹释放后瓣叶滑脱。
有时,经食管声窗成像较困难,无法确定瓣叶插入的情况。这种情形下,强烈建议使用经胃成像获得的信息来决定是否应该释放钳夹。在钳夹展开前确保足够的瓣叶插入是至关重要的,因为不均匀或不充分的捕获可能导致SLD。图8中展示的病例可以表明经胃成像对发现不充分的瓣叶捕获有多敏感。在一个早期三尖瓣前瓣滑脱的病例中,捕获过程的经胃图像显示前瓣存在滑动,捕获长度并不理想,在钳夹释放后出现了早期的瓣叶滑脱(图7)。虽然经胃成像也需要一个学习曲线,但它所提供的信息量和细节使其成为一个获取高质量的三尖瓣图像的强大工具。
此外,在钳夹释放前使用彩色血流多普勒(CFD)评估TR是否明显减轻,也是瓣叶捕获充分的标志。释放前,必须检测三尖瓣前向跨瓣压差,尤其是在放置多个钳夹时,以排除相关的瓣膜狭窄。释放后,CFD和跨瓣压差是评估TEER对TR的即刻影响以及决定是否植入第二或第三个钳夹的关键(动图2和3)。由于术后残余TR常呈多束分布,对其精确的分级存在困难。残余PISA区大小、CW多普勒信号密度和肝静脉收缩期血流是评估残余TR严重程度的间接标志。缩流面积的3D CFD平面测量能更准确地定量评估残余反流。
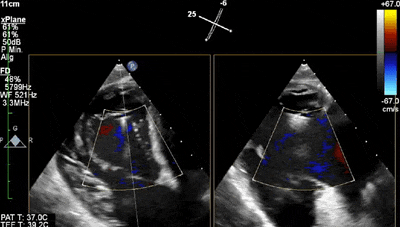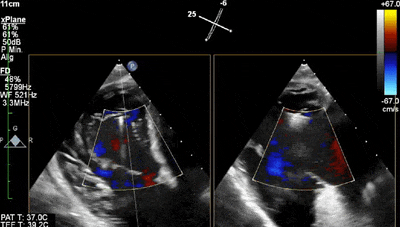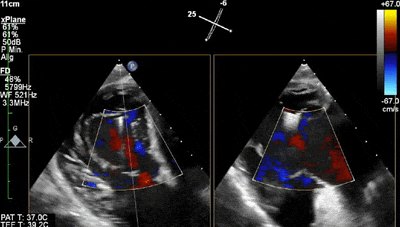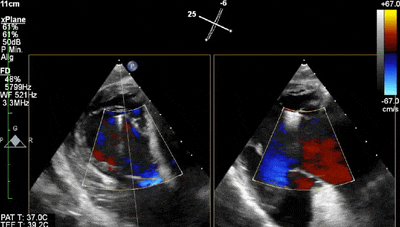
动图2 经胃TEE彩色血流多普勒显示三尖瓣中央反流和后-隔联合处起搏器导线。

动图3 三尖瓣经胃短轴切面彩色血流多普勒显示在中央位置前-隔间放置一钳夹后的效果。起搏器导线周围仅有微量残留反流。
3.结论
与其他介入手术相比,三尖瓣TEER的成像要求更高,且对手术的安全性和有效性起着重要作用。因此,标准化的围手术期监测方法对于确保最佳手术效果至关重要。通过经胃声窗扫查所获得的丰富形态学信息能充分指导所有相关的步骤。

二

术中TEE在经导管三尖瓣置换
(TTVR)中的应用2-3
1.前言
经导管三尖瓣置换术(TTVR)有望迅速成为治疗重度及以上症状性TR的标准治疗策略。目前已有数种原位瓣膜置换装置已应用于临床或正在进行临床研究。不管是手术过程还是最终的手术结果在很大程度上都取决于术中成像的引导和监测。TEE是TTVR术中三尖瓣成像的“金标准”,但由于三尖瓣的解剖位置会导致其TEE成像易受其他心脏结构的声影干扰,多模态成像包括CT-透视融合成像及心腔内超声心动图(ICE)可以协助TTVR顺利安全进行。国内研发的LuX-Valve/Plus系统(JensCare Scientific,中国)是一种非径向支撑力的原位三尖瓣置换装置,通过三尖瓣前瓣夹持键和室间隔锚定器进行固定,避免了对瓣环结构的损伤,目前处于临床试验阶段。舒先红、葛均波及其团队基于临床试验经验总结出术中TEE在TTVR(LuX-Valve/Plus系统)术中实时监测和引导的操作规范及流程2。丹麦哥本哈根大学医院心脏中心亦基于其临床试验经验对多模态成像在TTVR(LuX-Valve Plus系统)术中的应用进行了总结(图9)3。
本节内容主要分享术中TEE在TTVR(LuX-Valve/Plus系统)关键步骤中的应用。

图9显示在TTVR(LuX-Valve Plus系统)术中使用的标准TEE切面3。
A,前瓣;Ao,主动脉;CS,冠状窦;LA,左心房;LV,左心室;P,后瓣;RA,右心房;RV,右心室;RVOT,右心室流出道;S,隔瓣;TR,三尖瓣反流;TEE,经食管超声心动图;TTVR,经导管三尖瓣置换术。
2.术中TEE监测关键步骤
2.1 引导输送系统进入右室
在输送系统远端进入RV之后,需要到达一定深度,并且位于三尖瓣环的中心且垂直于三尖瓣环平面(同轴)。输送系统相对三尖瓣环的深度和同轴度的评估一般使用经食管中段及下段RV流入-流出道切面xPlane视图,同时显示RV流入-流出道切面及四腔心切面。输送系统的头端应位于三尖瓣环远端约4cm处(图10A)。在引导输送系统过程中应尽量显示头端避免触碰周围结构或缠绕腱索,导致室壁穿孔或腱索断裂。

图10显示在TTVR(LuX-Valve Plus系统)术中关键步骤的TEE成像3。
2.2 确认两个夹持键在RV面托住并抓握三尖瓣前瓣
在展开瓣膜之前,通过超声成像确认两个夹持键(也称为“兔耳”)的正确位置是瓣叶捕获步骤的关键。 夹持键抓握的目标为三尖瓣前瓣(位于外侧),一般使用食管中段RV流入-流出道切面和经胃xPlane视图确认两个夹持键均位于三尖瓣前瓣下方(图10C),且在前后瓣联合处的前乳头肌的上方。
2.3 引导锚定针攻入后间隔中上段
LuX-Valve展开后,至关重要的是确保锚定片与室间隔能在整个心动周期中保持贴合。可使用xPlane视图同时获取食管中段四腔心切面和右心室短轴切面,或使用TEE深部经胃xPlane视图显示三尖瓣短轴,评估锚定片与室间隔的同轴情况(图10E)。一般输送系统的进入角度已经使得锚定片位于室间隔位置,然后在TEE成像的引导下,通过调整输送系统的屈曲角度和旋转装置内轴使得锚定片贴合于后间隔中上段位置。在将锚定针推出持针器之前,确认锚定片与室间隔在整个心动周期均贴合良好非常关键。
3.病例分享
3.1 基本信息
患者,女,66岁;于2003年因“活动时心慌、气促10年”在武汉亚洲心脏病医院诊断为“风湿性心脏瓣膜病,二尖瓣重度狭窄,主动脉瓣及三尖瓣中度关闭不全,房颤”,并行DVR+TVP+左心耳缝闭术。2023年因“换瓣术后20年,腹胀、纳差半月”再次入院。患者入院前半月出现腹胀、纳差、尿少、伴夜间阵发性呼吸困难。入院查体:心界无扩大,心室率110bpm,律不齐,第一心音强弱不等,心尖区及主动脉瓣听诊区可闻及机械瓣开瓣音。经胸超声心动图提示“符合二尖瓣置换+主动脉瓣置换+三尖瓣成形术后改变:人工瓣机能正常 三尖瓣重度反流”。
3.2 TTVR术中TEE
经食管RV流入-流出道切面xPlane视图见三尖瓣稍厚、回声稍强并重度反流(动图4及5)。

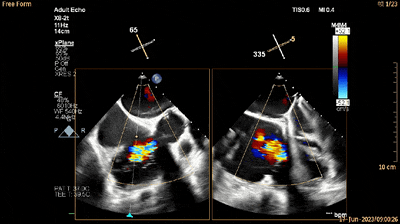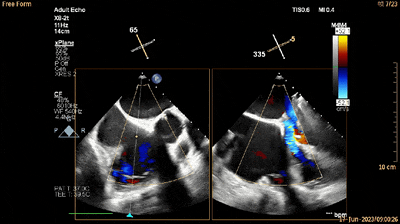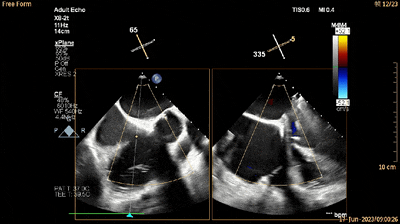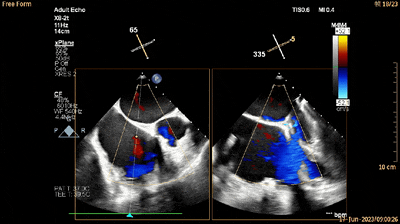
动图4
动图5
经食管四腔心切面引导输送系统进入RV(动图6)。
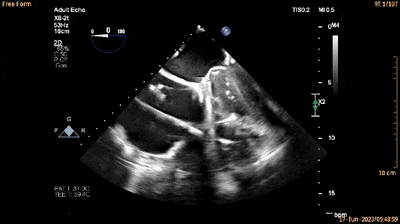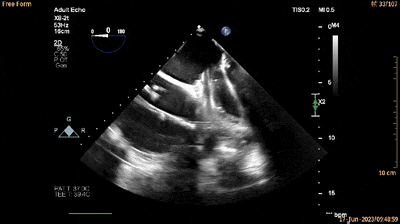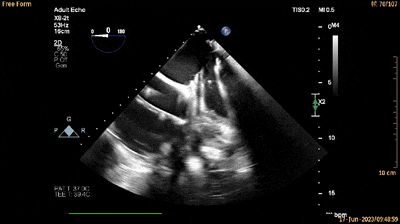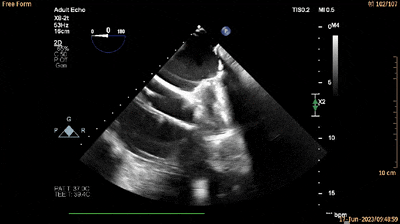
动图6
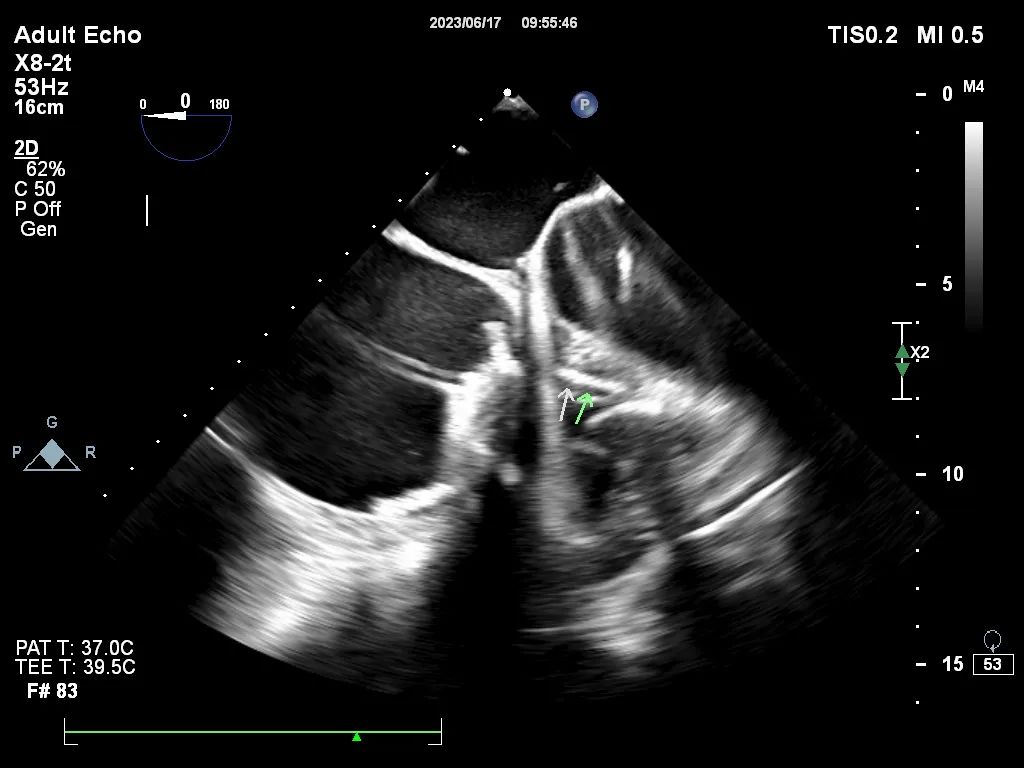
经食管RV流入-流出道切面xPlane视图可见夹持键位于三尖瓣前瓣下方(单箭头所示为夹持键,双箭头所示为三尖瓣前瓣)(动图7及图11)。
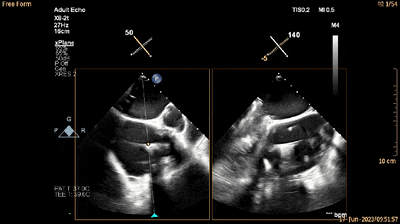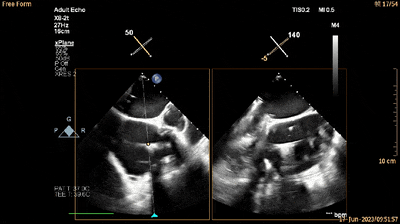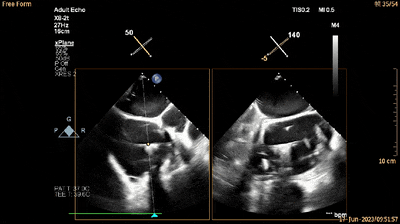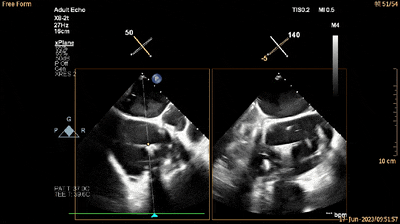
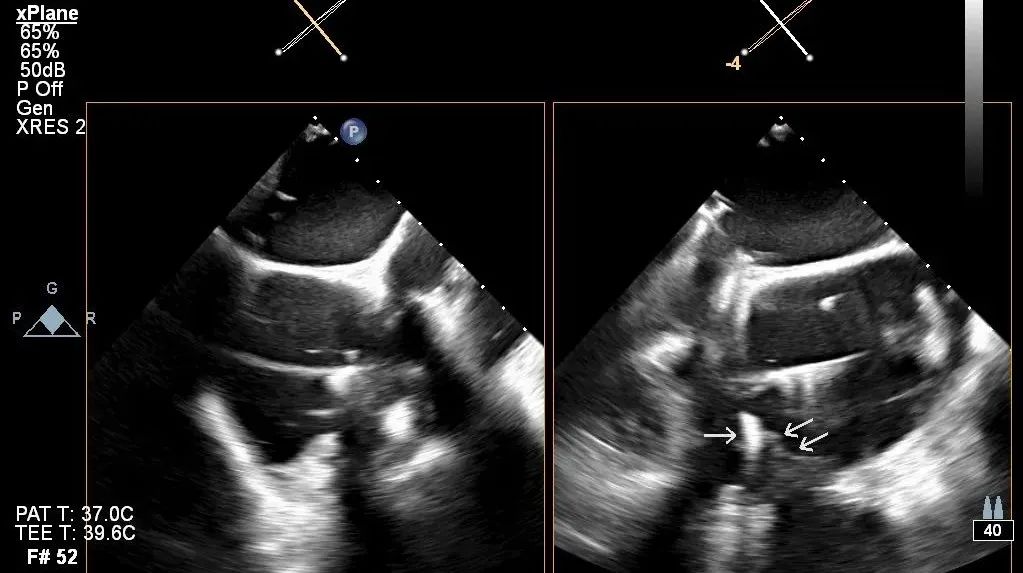
动图7
图11
经食管四腔心切面可见生物瓣展开后锚定片(双箭头所示)与室间隔在整个心动周期中保持贴合(动图8及图12)。
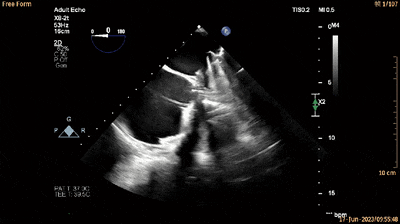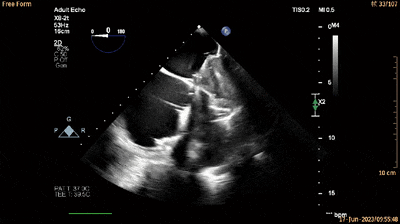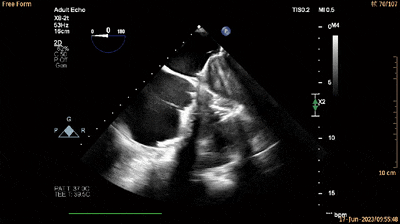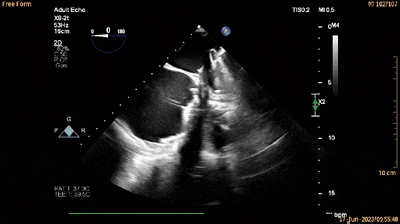
动图8
图12
经食管RV流入-流出道切面xPlane视图见三尖瓣生物瓣启闭活动正常,仅瓣周见微量反流(动图9)。

动图9
经食管TrueVue Glass视图显示瓣周微量反流(动图10及图13)。

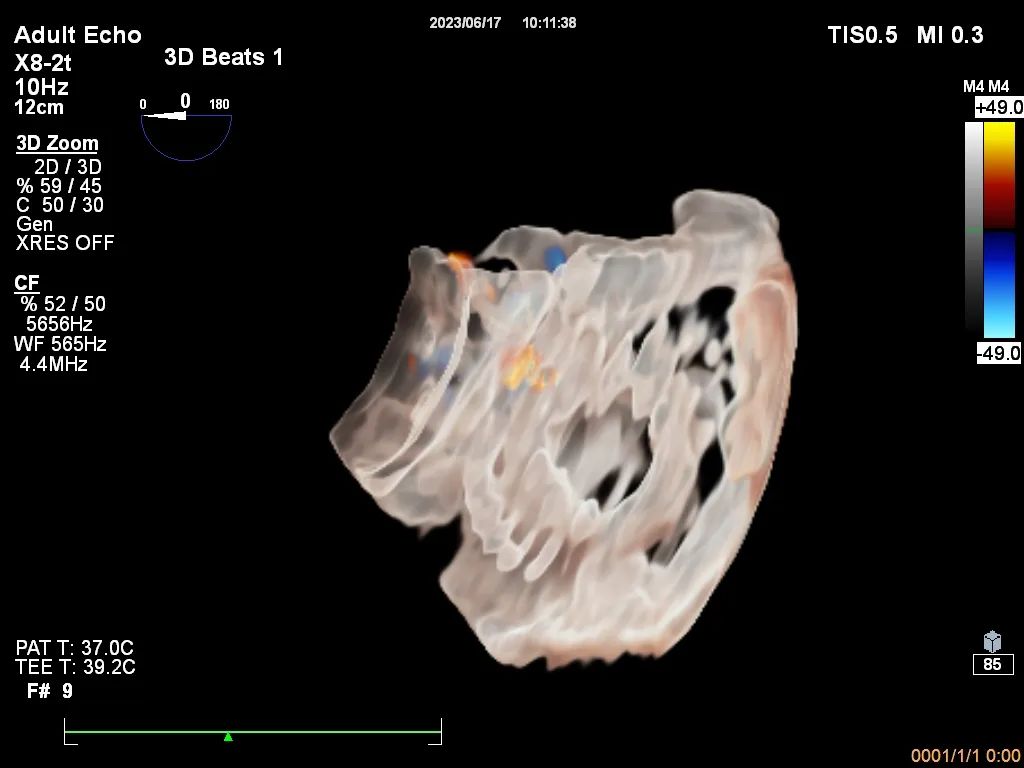
动图10
图13

小编的话
飞利浦心血管超声第二代矩阵三维经食管超声探头X8-2t具备卓越的图像分辨率和更高的容积帧频,结合xPlane及先进的心腔镜(TrueVue Plus)成像技术,能全面评估三尖瓣形态及血流动力学,并且在经导管三尖瓣修复及置换中,能有效辅助医生制定介入治疗方案,同时引导术中操作,并为评估手术效果提供准确信息。
作者介绍

王静静 副主任医师
武汉亚洲心脏病医院超声科
从事超声工作10余年,擅长各种先天性及后天性心脏病(瓣膜病、冠心病及心肌病 等)的超声诊断。
指导老师

马小静 主任医师 教授
武汉亚洲心脏病医院影像中心主任
武汉亚心总医院超声影像科主任
亚太卫生健康协会APHA超声专委会 执行主席
中国非公立医疗协会超声专业委员会 副主任委员
中华医学会超声分会超声心动图 学组委员
海峡两岸医药卫生协会超声专委会 常务委员
湖北省医学会超声医学分会 副主任委员
湖北省医师协会超声医师分会 常务委员
湖北省超声诊断与质量控制中心 副主任委员
武汉非公立医疗机构协会超声专委会 主任委员
武汉医学影像技术研究会 理事长
武汉医学会超声医学分会 副主任委员
从事临床医疗工作40年,荣获中宣部国家卫健委授予“中国好医生”称号,荣获中国第四届“白求恩式好医生”称号,荣获湖北省、武汉市科技进步三等奖1项
主译专业书籍2部,主编7本、参编10本;发表论文154 篇,其中SCI 30 篇;参与专家共识指南 8篇,发明专利 5项,参与国家科技部重点研发项目1项;主持湖北省科技局、卫健委和武汉市科技局、卫健委课题 8项
参考文献:
1.da Rocha e Silva, J. G., Ruf, T. F., Hell, M. M., Tamm, A., Geyer, M., Munzel, T., von Bardeleben, R. S., & Kreidel, F. (2021). Transgastric imaging—The key to successful periprocedural TEE guiding for edge-to-edge repair of the tricuspid valve. Echocardiography, 38(11), 1948–1958. https://doi.org/https://doi.org/10.1111/echo.15196.
2.潘翠珍,李伟,周达新,等.经食管二维、三维超声心动图在经导管三尖瓣置换术中监测及评价规范[J].中华超声影像学杂志, 2023, 32(5):449-454.DOI: 10.3760/cma.j.cn131148-20221214-00865.
3.Willemen, Y., Møller, J. E., Nejjari, M., Linde, J. J., Vejlstrup, N. G., von Bardeleben, R. S., Latib, A., Modine, T., & de Backer, O. (2024). Multimodality imaging for intraprocedural guidance of a transcatheter tricuspid valve replacement. European Heart Journal - Cardiovascular Imaging, jeae101. https://doi.org/10.1093/ehjci/jeae101.

扫码进入飞利浦学术专栏
了解更多精彩内容