
科技是国家强盛之基,创新是民族进步之魂。2023年作为疫情之后完全放开的第一年,全球各个国家和地区对医疗创新产业发展愈发重视,在新冠肺炎疫情的催化作用下,数字技术与医疗服务的深度融合推动医疗器械行业不断升级,产品创新迭代加快,同时,随着人们健康意识和环保意识的增强,医疗创新领域有望迎来新的变革。
尽管全球经济低迷,但是中国的创新市场已经开始逐步恢复活力。2023年,国产创新医疗器械质量和数量实现双丰收,创新医疗器械的“含金量”也在不断提升,各类新技术、新理念、新研究成果层出不穷。
现邀请中国心血管医生创新俱乐部(CCI)团队专家从结构性心脏病、冠脉领域、腔内影像、电生理、RDN、左心室辅助装置等领域开展年度盘点工作。
2023年冠心病介入治疗领域大量的临床研究仍然集中在腔内影像和功能生理学指导PCI,如复杂病变、左主干病变以及心梗非罪犯血管的介入治疗。此外,得益于腔内影像,尤其是OCT的快速用于临床,与易损斑块有关的临床研究也层出不穷。令人欣喜的是,仍然有关于冠脉支架方面的新的临床研究问世,特别是该支架是近年来不被看好的生物可吸收支架。无创影像方面,基于冠脉CTA的血流储备分数(FFRCT)开始用于临床识别高危稳定型冠心病患者。药物治疗方面,抗炎药物(秋水仙碱)正式获得美国FDA批准用于治疗ASCVD,预计国内指南很快也会更新,随后秋水仙碱就可以应用于临床。抗血小板药物吲哚布芬,以及近年来跨界到心血管领域的明星药物SGLT2i也有了全新的临床证据,为冠心病患者带来更好地临床预后。本文对2023年发表的有代表性的临床研究进行了整理和解读,从而更好地指导临床实践。
OCTIVUS研究:OCT指导PCI和IVUS指导PCI在疗效和安全性方面的比较
腔内影像指导的PCI较冠脉造影指导的PCI能够更好地改善高危患者的临床结果。作为两种目前主流的腔内影像工具,IVUS和OCT在指导PCI预后方面的优劣尚不清楚。本研究共纳入2008例患者,按1:1的比例随机分配到OCT指导PCI组(1005例)或IVUS指导PCI组(1003例)。主要终点为包括心原性死亡、靶血管心肌梗死、缺血驱动的靶血管血运重建等在内的复合终点。本研究对安全性也进行了评估。研究结果显示,术后12个月,OCT组有25例(2.5%)发生了主要终点事件,IVUS组有31例(3.1%)发生了主要终点事件(非劣效性P<0.001)(图1)。造影剂肾病的发生率相似(OCT组1.4% vs. IVUS组1.5%,P=0.85)。OCT组主要手术并发症的发生率低于IVUS组(2.2% vs. 3.7%,P=0.047)。在所有预设的亚组中,OCT和IVUS在改善患者预后方面未见显著差异(图2)。未观察到与成像操作相关的并发症。本研究显示,在因不同冠状动脉病变而接受PCI治疗的患者中,OCT指导PCI在心原性死亡、靶血管心肌梗死、缺血驱动的靶血管血运重建等主要终点方面不劣于IVUS指导PCI。造影剂肾病和成像操作相关安全事件的发生率两组间没有明显差异。
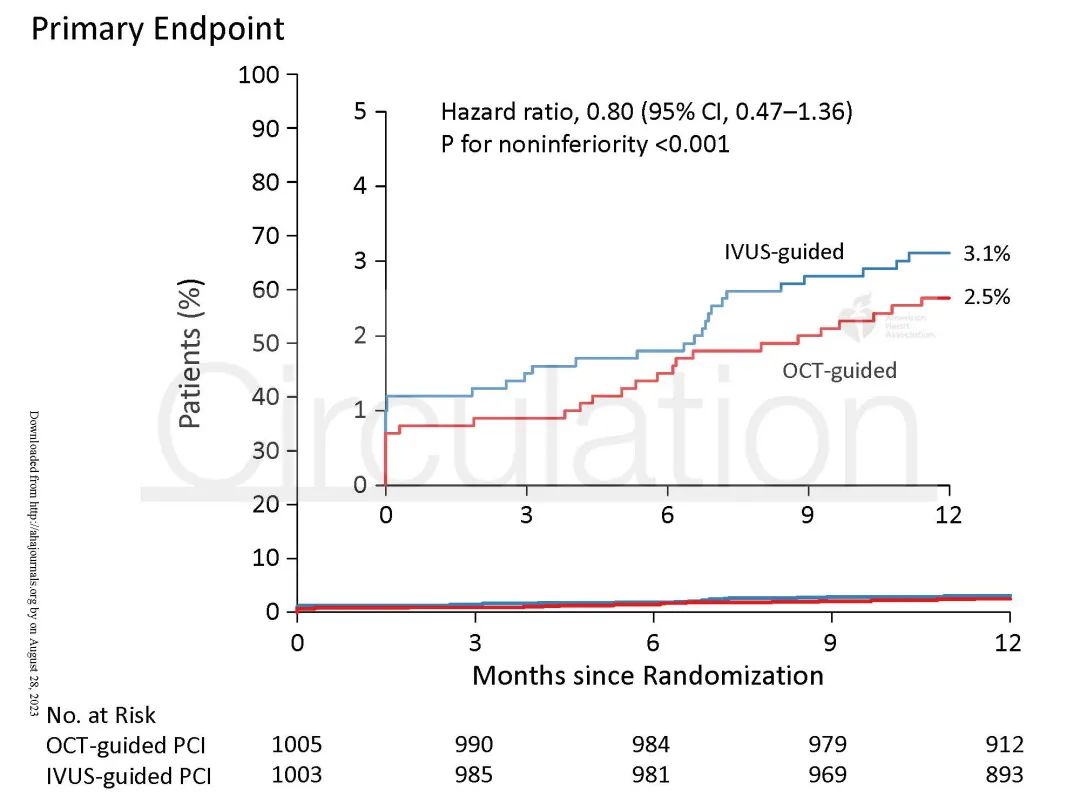
图1
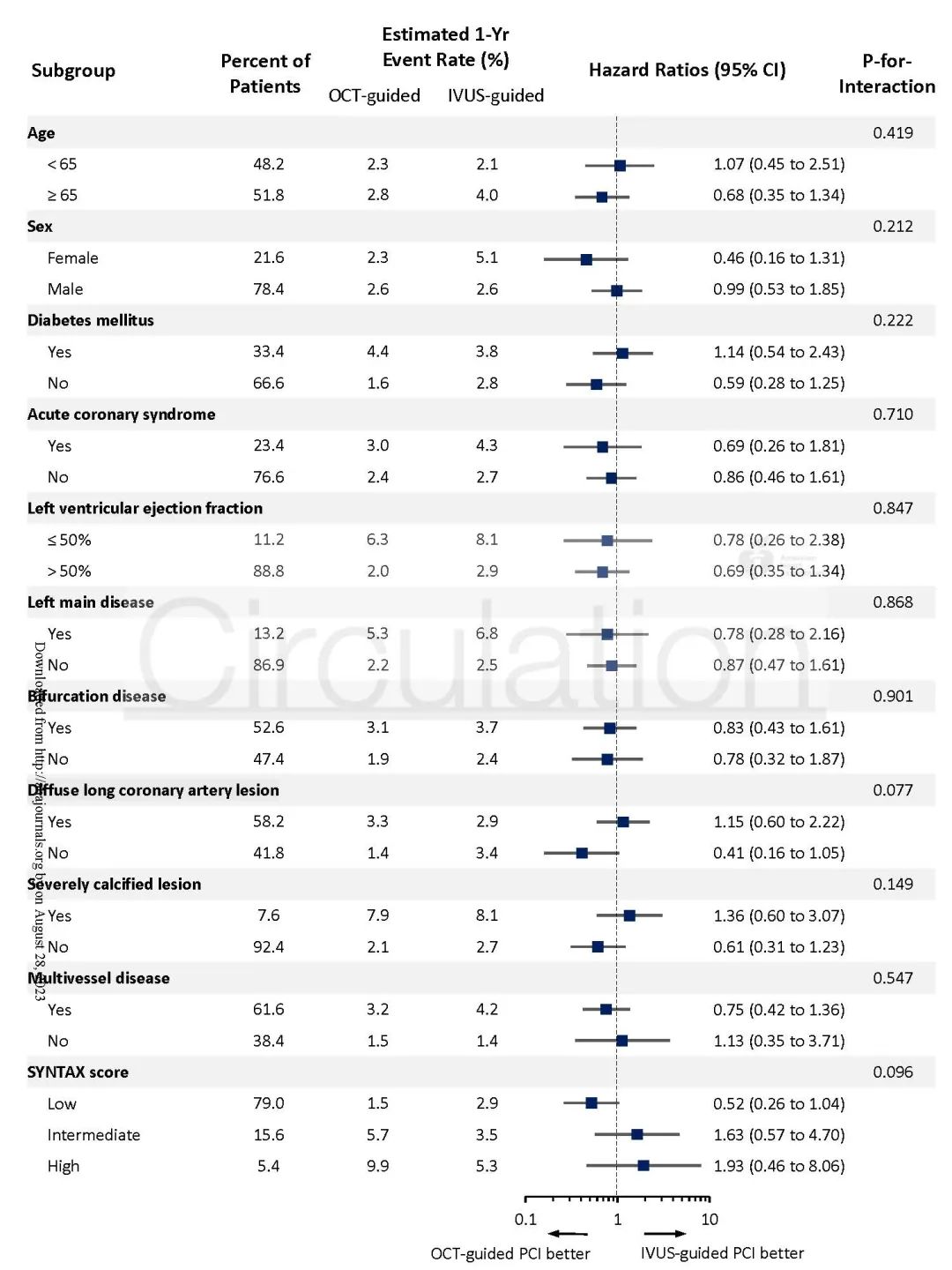
图2
与血管造影指导的PCI相比,血管内成像或功能学指导的PCI更具优势
现有研究显示,与冠脉造影指导的PCI相比,使用腔内影像或功能学指导均能改善患者的预后。但优化预后的最佳策略是腔内影像指导还是功能学指导,以及ACS是否会影响患者临床结局目前尚不清楚。该文作者对32项随机对照研究进行了荟萃分析,供纳入22684例患者,随访时间6个月至5年。结果显示腔内影像指导PCI (RR 0.72; 95% CI: 0.62-0.82)和功能学指导PCI (RR 0.81; 95% CI: 0.69-0.96)与单独血管造影指导的PCI相比,MACE事件均降低,腔内影像和功能学指导PCI的MACE事件无显著差异(RR 0.88; 95% CI: 0.72-1.07)。三种策略的全因死亡无显著差异。与血管造影指导下的PCI相比,腔内影像指导的PCI与心血管死亡率降低(RR 0.56; 95% CI: 0.42-0.75)、支架内血栓形成减少 (RR 0.48; 95% CI: 0.31-0.73)及TLR减少(RR 0.75; 95% CI: 0.57-0.99)相关。腔内影像指导、功能学指导下的PCI均与心肌梗死降低相关(RR 0.81; 95% CI: 0.66-0.99, RR 0.78; 95% CI 0.63-0.96)。腔内影像指导与功能学指导PCI在心血管死亡、心肌梗死、支架血栓、TLR方面无显著差异(图1)。在三种策略中,腔内影像指导的PCI在降低MACE、心血管死亡、支架血栓形成和TLR方面均最具优势。此外,无论是在ACS还是在非ACS人群中,腔内影像指导的PCI是减少MACE、心血管死亡、支架血栓形成和TLR的最佳选择。

图1
与冠脉造影指导相比,腔内影像指导的左主干PCI有更多的临床获益
RENOVATE-COMPLEX-PCI研究已证实,对于所有复杂病变,腔内影像指导的介入治疗与冠脉造影相比更有临床优势。但对左主干病变的结局尚不清楚。RENOVATE-COMPLEX-PCI研究预设的左主干亚组,将左主干病变按2:1随机分配至腔内影像指导组和冠脉造影指导组(研究流程如图1所示),主要终点为靶血管失败(包括心源性死亡、靶血管相关心梗和临床驱动的靶血管血运重建);次要终点为主要终点的各个组分,无操作相关心肌梗死的靶血管失败,以及心源性死亡或靶血管心肌梗死、明确支架内血栓在内的复合终点,总操作时间,造影剂用量,造影剂肾病等。本研究共对192例左主干病变患者进行亚组分析,其中138例为腔内影像指导,54例为冠脉造影指导。腔内影像组中92.8%(128例)使用血管内超声,其他则选用光学相干断层成像。两组的基线信息无显著差异,两组间的冠脉造影特征与病变复杂程度也大致相当。实际干预操作中,两组间的干预术式选择均无差异,腔内影像组选择的非顺应性球囊直径更大(4.0±0.7mm vs 3.8±0.6mm,P=0.046),操作时间更长[77.0min(51.0-100.0) vs 60.0min(46.5-75.0),P=0.003],但总体造影剂用量无显著差异。中位随访时间2.1年,腔内影像组9例(6.8%)发生主要终点,冠脉造影组为11例(25.1%)[HR=0.31, 95% CI=0.13-0.76,P=0.01],主要终点的改善主要受心原性死亡、靶血管相关心肌梗死风险减低驱动(如图2)。其他次要终点的发生率在两组间相当。此外,研究者还对包含本研究在内的18个观察性研究及随机对照研究进行了meta分析,共计10904例患者为腔内影像指导,10797为冠脉造影指导。汇总分析表明,腔内影像指导可显著减低全因死亡(HR=0.53, 95%CI=0.49-0.59, P<0.001)和心原性死亡风险(HR=0.37, 95%CI=0.26~0.53, P<0.001)(如图3)。
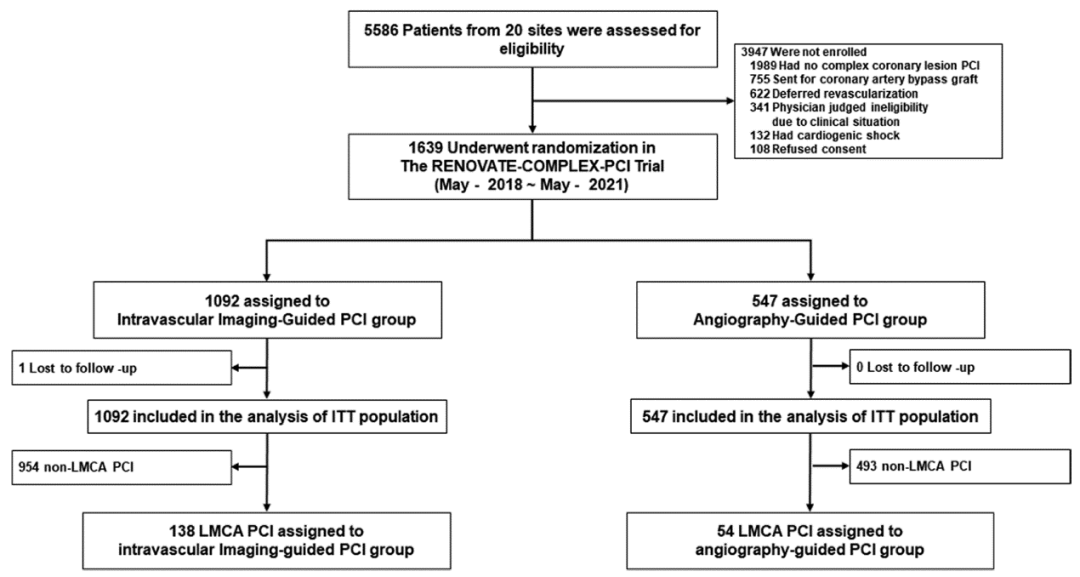
图1
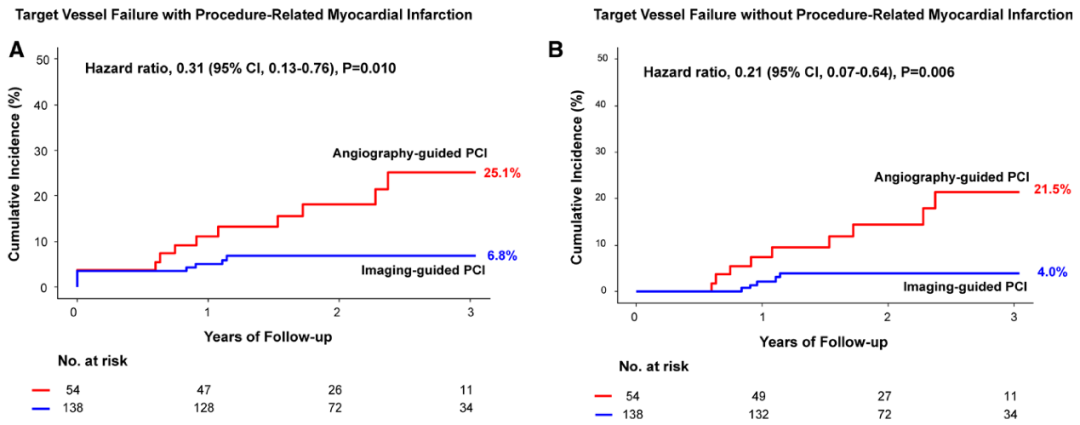
图2

图3
对于多支病变的急性心梗患者,FFR指导的PCI优于造影指导的PCI
既往研究显示,对于急性心肌梗死的患者,相较于仅对罪犯血管行PCI,同期对非罪犯血管行PCI从而实现完全血运重建可以改善患者的临床结局。然而既往的血运重建多基于冠脉造影指导。FFR指导完全血运重建是否优于冠脉造影指导尚不明确。FRAME-AMI研究是一项随机、开放标签、在韩国14个中心进行的多中心试验。562名急性心肌梗死合并多支病变的患者在成功进行梗死相关动脉PCI后,被随机分配到FFR指导的PCI组(FFR≤0.80)或血管造影指导的PCI组(直径狭窄>50%),干预非梗死相关动脉。主要终点为死亡、心肌梗死或再次血运重建的复合终点。研究结果显示562名患者中,60.0%的患者立即接受了非梗死相关动脉的PCI治疗,40.0%的患者在同一住院期间接受了分期手术治疗。FFR指导PCI组中64.1%的患者接受了非梗死相关血管的PCI治疗,而在冠脉造影指导PCI组中,97.1%的患者接受了此类治疗。中位随访时间为3.5年,FFR指导PCI组284名患者中有18名(7.4%)发生了主要终点事件,冠脉造影指导PCI组278名患者中有40名(19.7%)发生了主要终点事件(RR 0.43;95%CI 0.25-0.75;P = 0.003)。FFR指导PCI组中有5名患者死亡(2.1%),7名患者发生心肌梗死(2.5%),10名(4.3%)患者进行了非计划血运重建;相对地,冠脉造影指导PCI组中有16名患者(8.5%)死亡,21名患者(8.9%)发生心肌梗死,16名患者(9.0%)进行了非计划血管重建(图1)。该研究结果显示,对于急性心肌梗死合并多支病变患者非梗死相关动脉的处理,FFR指导的选择性PCI,在死亡风险、心肌梗死风险、再次血运重建风险等方面,均优于基于血管造影的常规PCI治疗。
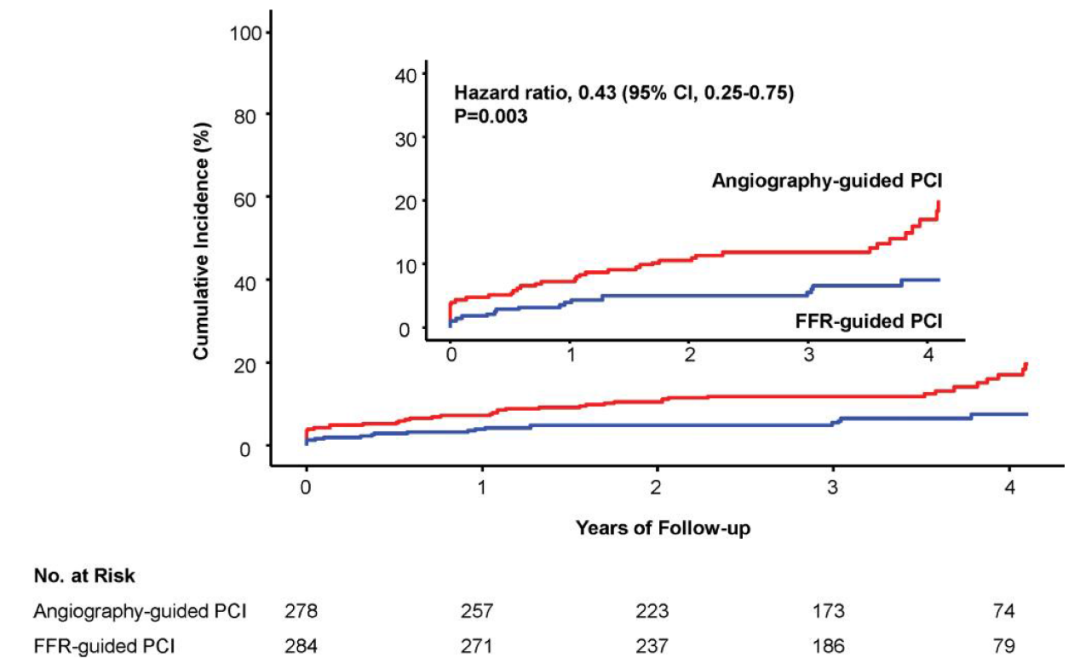
图1
第三代镁合金可吸收支架Freesolve获CE批准上市
可吸收支架的发展之路颇为坎坷。2007年,聚乳酸可吸收支架带头大哥雅培退出市场后群龙无首,留给了国内生物可吸收支架厂家发展的机会。以XINSORB BRS为代表的聚乳酸可吸收支架不仅在国内介入市场开始站稳脚跟,还开始向海外输出产品和成功经验。镁合金支架走出了另外一条道路。Biotronik作为一家可吸收冠脉支架领域坚守者,其在2016年推出第二代可吸收镁合金支架Magmaris(DREAMS 2G),成为第一款上市的可吸收金属支架,去年Magmaris也开启在国内临床应用(在博鳌)。尽管上市近8年,但是Magmaris在市场推广上并不成功(也没有获得FDA批准),也跟其临床效果没有达到预期有关。因此Biotronik在Magmaris基础上进行优化,Freesolve(DREAMS 3G)就此诞生。Freesolve相比于Magmaris,在技术层面取得了更多的突破,包括采用镁基合金材料和西罗莫司药物涂层,使用了BIOmag镁合金技术和BIOlute药物涂层技术(一种可吸收聚左旋丙交酯 (PLLA) 涂层,载有利莫司药物)。BIOmag镁合金技术实现支架均匀吸收,使Freesolve在降解过程中拥有更好力学性能。并且降解过程是可预测。并且比Magmaris更薄,显影效果更佳。在保持12个月降解时间的同时,也兼顾了径向支撑性能更为耐久。BIOMAG-I研究显示:Freesolve植入后12个月,即可完成99.3%的吸收,无论病变特征如何,性能一致,血管运动恢复。为了进一步证实Freesolve优异临床性能,Biotronic将在今年第二季度开启BIOMAG-II临床研究,本项研究纳入1800名患者,是一项超大型随机对照试验。期待BIOMAG-II取得好的结果。
FFR≥0.8的TCFA对MACE的影响
随着腔内影像,尤其是OCT及由此衍生的OCT-NIRS的发展,未来TCFA将是冠心病临床研究的重点。TCFA是急性冠脉事件的始动因素。OCT对TCFA的评估能力,将对MACE有重要影响。COMBINE研究显示,即使是FFR阴性的病变中,TCFA也是未来MACE的驱动因素。COMBINE研究联合了OCT的形态学和FFR的血流动力学,对随访期间TCFA合并糖尿病的患者进行了详细的OCT定性和定量评估(根据是否发生MACE分为两组)。MACE被定义为心原性死亡、靶血管心肌梗死、临床驱动的靶病变血运重建和因不稳定型心绞痛住院的复合终点。研究结果显示,在MACE组中,既往接受PCI更为常见(69.2 vs. 36.5%,P=0.02)。TCFA的定量和定性血管内成像分析发现,MACE组的TCFA体积小于非MACE组(分别为:0.19(0.07-0.33)mm² vs 0.37(0.18–0.76)mm²,P=0.03),并且在两组中,TCFA主要位于最小管腔面积(MLA)病变处的近端(图1)。OCT分析结果发现,两组间的病变长度相似,但MACE组的MLA和最小管腔直径值均显著减小(分别为:1.80(1.30–2.30)mm² vs 2.40(1.80–3.20)mm²,P=0.02;1.20(1.05–1.55)mm vs 1.50(1.23-1.70)mm,P=0.04)(图2)。此外MACE组中,TCFA附近的愈合斑块分布比例具有统计学意义(53.85% vs. 21.18%,P=0.01),而钙化结节、巨噬细胞、新生微血管等在两组间分布相似。本研究显示,合并TCFA的患者中,较小的MLA、较低的FFR值和TCFA附近的愈合斑块与未来发生MACE相关。未来会发生MACE的TCFA病变基线水平的MLA和FFR值较低。
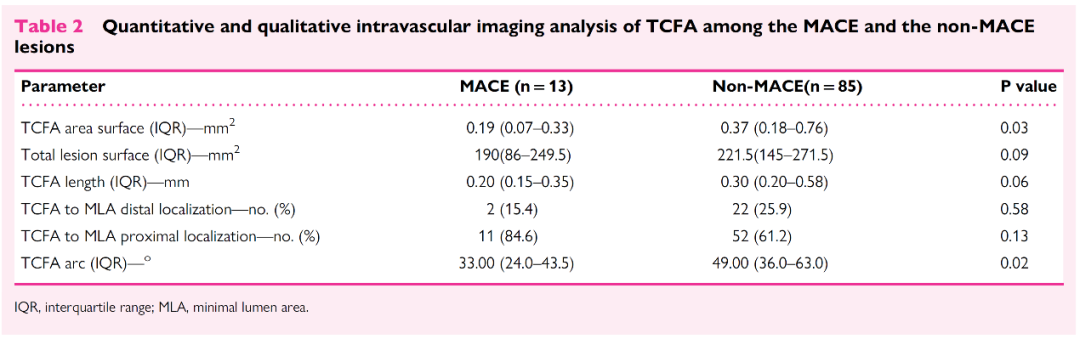
图1
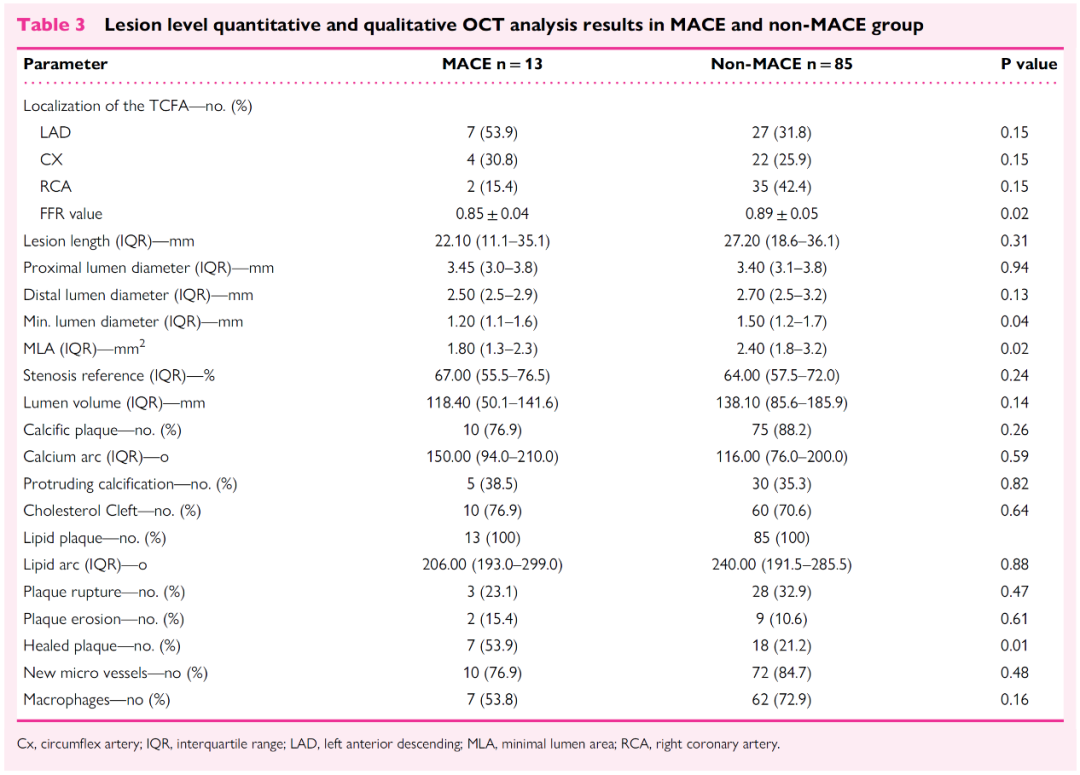
图2
FFRCT在稳定型冠状动脉疾病患者中的作用
稳定型冠心病(CAD)患者存在心肌缺血与不良心血管结局风险增加有关。目前的专业协会指南推荐使用无创策略来评估稳定型CAD的缺血情况。冠状动脉计算机断层血管造影(CCTA)是一种具有高阴性预测值的CAD评估方法。基于CCTA的血流储备分数(FFRCT)是一种新兴的分析工具,其在识别冠脉显著狭窄方面优于传统的CCTA,并与侵入性FFR密切相关,但其预后价值尚未完全建立。研究者纳入了10项研究(共11275例症状稳定型CAD患者)进行分析。平均年龄为65岁;64.8%的受试者为男性,平均随访时间为17个月。主要终点为全因死亡率。次要终点包括主要不良心血管事件(MACE)、随访期间发生急性心肌梗死 (AMI),以及在血管造影时或随访期间进行的所有冠状动脉血运重建。MACE被定义为心源性死亡、任何冠状动脉血运重建需求的复合终点。梗阻性CAD的定义为FFRCT≤0.80(阳性病变),非梗阻性CAD的定义为FFRCT>0.80(阴性病变)。研究结果显示,基于FFRCT 判断的梗阻性CAD和非梗阻性CAD在全因死亡风险方面无差异(OR 1.53, 95%CI 0.62-3.79,p = 0.35),但梗阻性CAD的MACE(OR 2.37, 95%CI 1.48-3.80,p <0.01)、AMI(OR 4.60, 95%CI 1.58-13.41,p <0.01)和冠状动脉血运重建(OR 14.18, 95 %CI 5.13-39.24,p <0.01)风险增加(图1)。FFRCT 有助于对稳定型CAD患者进一步风险分层。
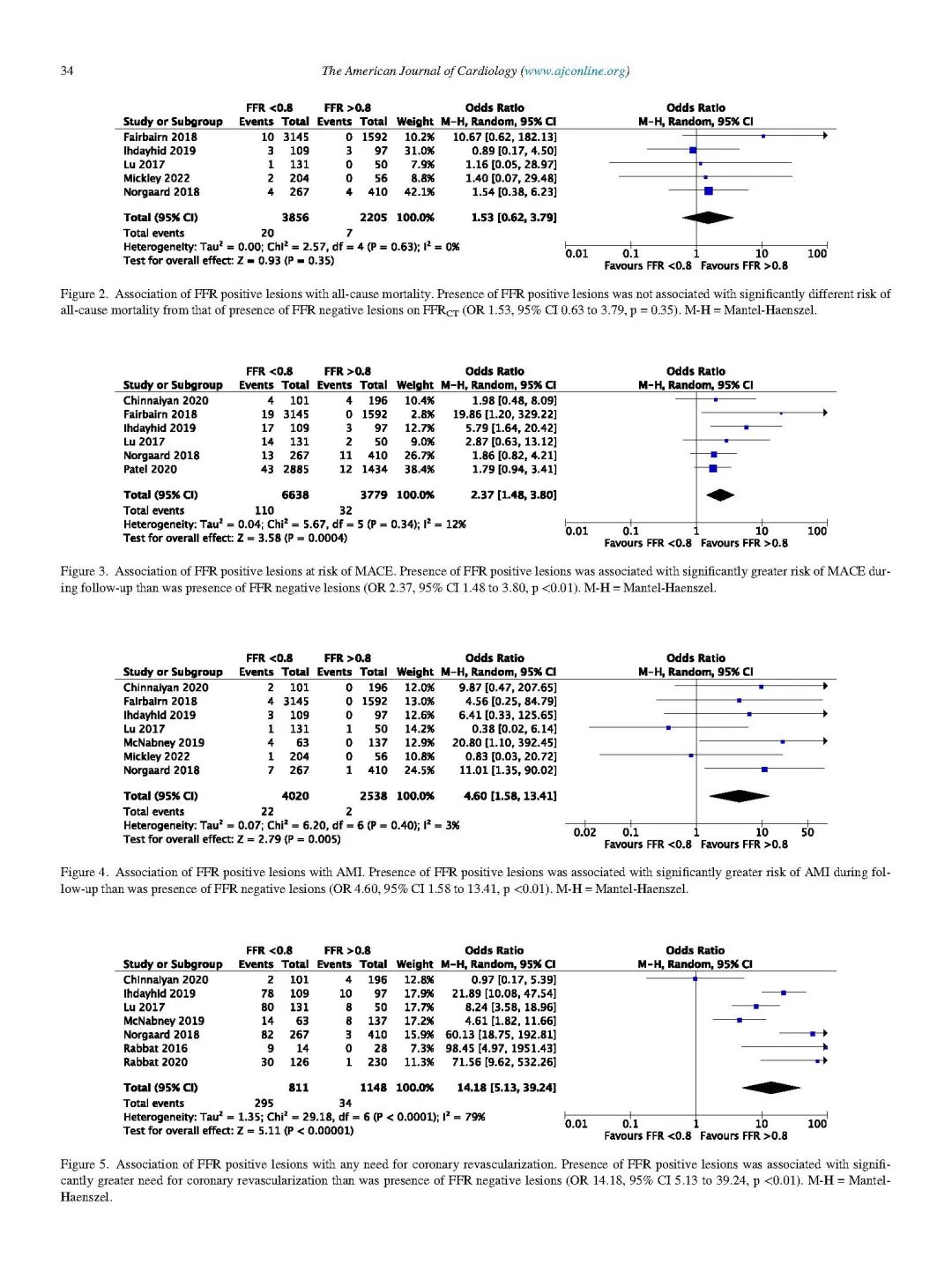
图1
抑制血管炎症将成为继降脂治疗后冠心病的又一重要治疗靶点
自冠心病发病的炎症机制被发现以来,科学家一直在尝试寻找相关药物通过阻断炎症延缓冠心病的进程。LODOCO2、COLCOT等研究显示,与安慰剂相比,秋水仙碱(0.5mg qd)在作为高剂量他汀类药物和其他心脏病预防药物的附加疗法时,能够显著降低心血管死亡、自发性心肌梗死、缺血性中风或缺血驱动的冠状动脉血运重建的总风险达31%,可以使心血管疾病导致的死亡、复苏性心脏骤停、心肌梗死、卒中或因心绞痛紧急住院导致冠状动脉血运重建的风险降低约23%。2023年,《柳叶刀》杂志一项纳入PROMINENT、REDUCE-IT和STRENGTH三项研究的分析显示,在使用他汀类药物治疗的患者中,血管炎症也许比高胆固醇更能强烈预测未来的心血管事件(图1)。文章建议,联合使用积极的降脂和炎症抑制疗法来进一步降低动脉粥样硬化风险。秋水仙碱并非新药,它是一种从秋水仙科植物中提取出来的药物,能抑制微管的组装,并具有多种抗炎机制。从疗效上看,过去的多个试验已经证明了其有效性和安全性。经过优先审评,美国食品药品监督管理局(FDA)批准了秋水仙碱(0.5mg/日)用于治疗ASCVD。国际指南纳入秋水仙碱后,预计国内指南很快也会更新,随后秋水仙碱就可以应用于临床。
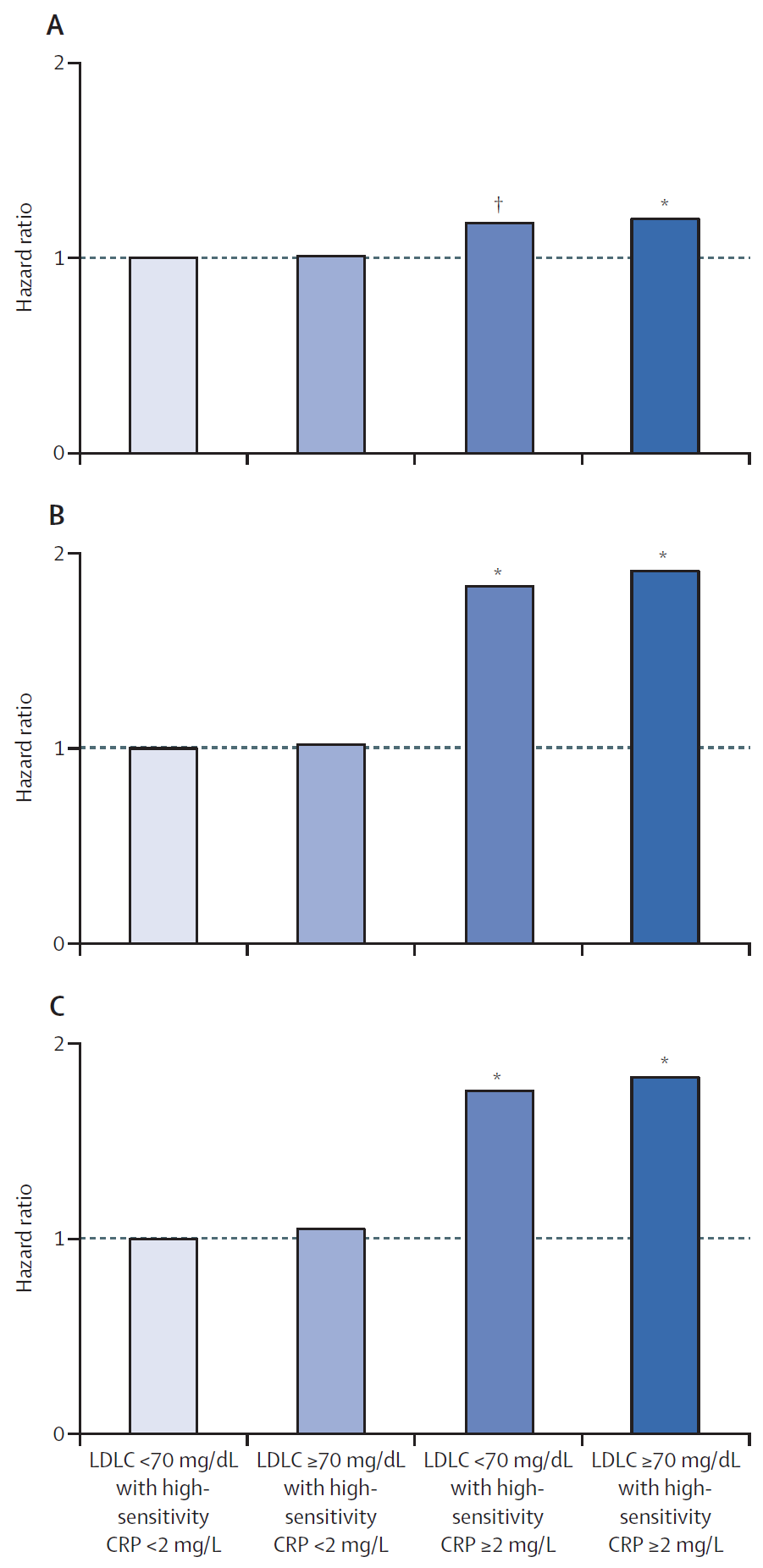
图1
SGLT2抑制剂对多支非阻塞性冠状动脉狭窄合并诱发性心肌缺血的糖尿病患者冠状动脉纤维帽厚度和心血管事件的影响
本研究旨在评估SGLT2i对T2DM合并多支非阻塞性冠状动脉狭窄(Mv-NOCS)患者纤维帽厚度、全身和冠状动脉斑块炎症、MACE的影响。本研究是一项前瞻性、多中心的对照试验,纳入369例合并有Mv-NOCS的T2DM患者,在接受OCT检查后按2:1随机分为SGLT2i治疗组(258例,69.9%)和非SGLT2i治疗组(111例,30.1%)。研究者在1年时随访评估SGLT2i对纤维帽厚度(FCT)变化的影响并作为主要终点;在基线水平和随访12个月时评估炎症反应、斑块负荷、MACE发生率,并通过多变量分析评估MACE的预测因素并作为次要终点。基线时,两组在临床特征、炎症标志物、药物治疗和OCT数据方面没有显著差异。两组患者在病变分布和病变参数(平均管腔面积、平均参考直径、直径狭窄百分比)方面均可比。此外,基线时两组病变的FFR相似(0.82±0.65 vs 0.83±0.58%; p 0.364)。在随访6个月时,SGLT2i治疗组与非SGLT2i治疗组相比,体重指数(BMI)、血糖、Hb1Ac、BNP、炎症细胞和炎性分子(CRP、IL-6、TNFα、硝基酪氨酸)的值均较低(p < 0.05)。在随访12个月时,这些指标在SGLT2i治疗组下降更显著,而最小FCT值更高,脂质弧度和巨噬细胞分级值更低。在随访结束时,SGLT2i治疗组的MACEs发生率更低(10.8% vs 22.1%; p < 0.05)(图1)。Cox回归分析显示,Hb1Ac、巨噬细胞分级和SGLT2i治疗是1年随访时MACE的独立预测因子。本研究显示,SGLT2i在合并多支冠脉病变的糖尿病患者中具有逆转斑块(抗炎、减少脂质负荷、增加纤维帽厚度)、降低MACE发生风险的效果。
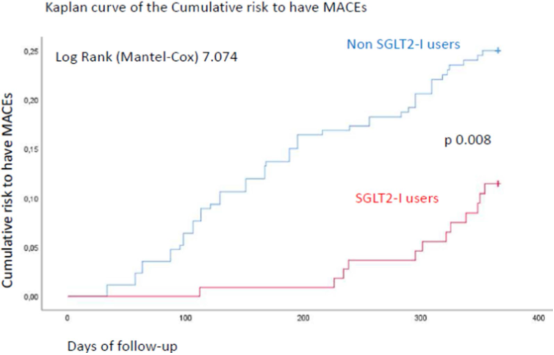
图1
DES植入术后吲哚布芬+氯吡格雷双抗疗效不劣于阿司匹林+氯吡格雷,安全性更好
以阿司匹林为基础的DAPT时目前DES植入后的标准抗血小板方案。然而临床有部分病人阿司匹林不耐受,或服用阿司匹林可出现出血症状。与阿司匹林相比,吲哚布芬具有较好的抗血小板作用,同时出血风险较低。OPTION研究是一项在中国人群中开展的临床研究,评估了稳定型冠心病患者植入DES后,吲哚布芬+氯吡格雷双抗和阿司匹林+氯吡格雷双抗的临床净获益、安全性和有效性。该研究是随机、开放标签、非劣效设计临床研究,肌钙蛋白阴性的冠心病患者植入DES后,按1:1随机纳入吲哚布芬DAPT组和阿司匹林DAPT组。主要终点是术后1年复合终点,包括心血管死亡、非致死性心梗、缺血性卒中、确定/极有可能的支架内血栓和BARC 2-5型出血。本研究共入选4451例患者,吲哚布芬DAPT组2258例,阿司匹林DAPT组2293例。随访1年时,主要终点在吲哚布芬DAPT组发生率为4.47%,在阿司匹林DAPT组为6.11%(差值为-1.63%,非劣效P<0.001,HR 0.73,95% CI 0.56-0.94)(图1)。心血管死亡、非致死性心梗、缺血性卒中、支架内血栓在吲哚布芬DAPT组分别为0.13%、0.40%、0.80%、0.22%;在阿司匹林DAPT组分别为0.17%、0.44%、0.83%、0.17%(P>0.05)。出血事件在吲哚布芬DAPT组为2.97%,阿司匹林DAPT组为4.71%(HR 0.63,95% CI 0.46-0.85,P=0.005),阿司匹林DAPT组主要以BARC 2型出血增多为主。研究结果显示,对于肌钙蛋白阴性接受DES植入的中国冠心病人群来说,与阿司匹林+氯吡格雷的DAPT方案相比,吲哚布芬+氯吡格雷DAPT能显著降低术后1年的净临床结局风险,该获益主要来自出血风险的降低,且并不增加缺血事件。
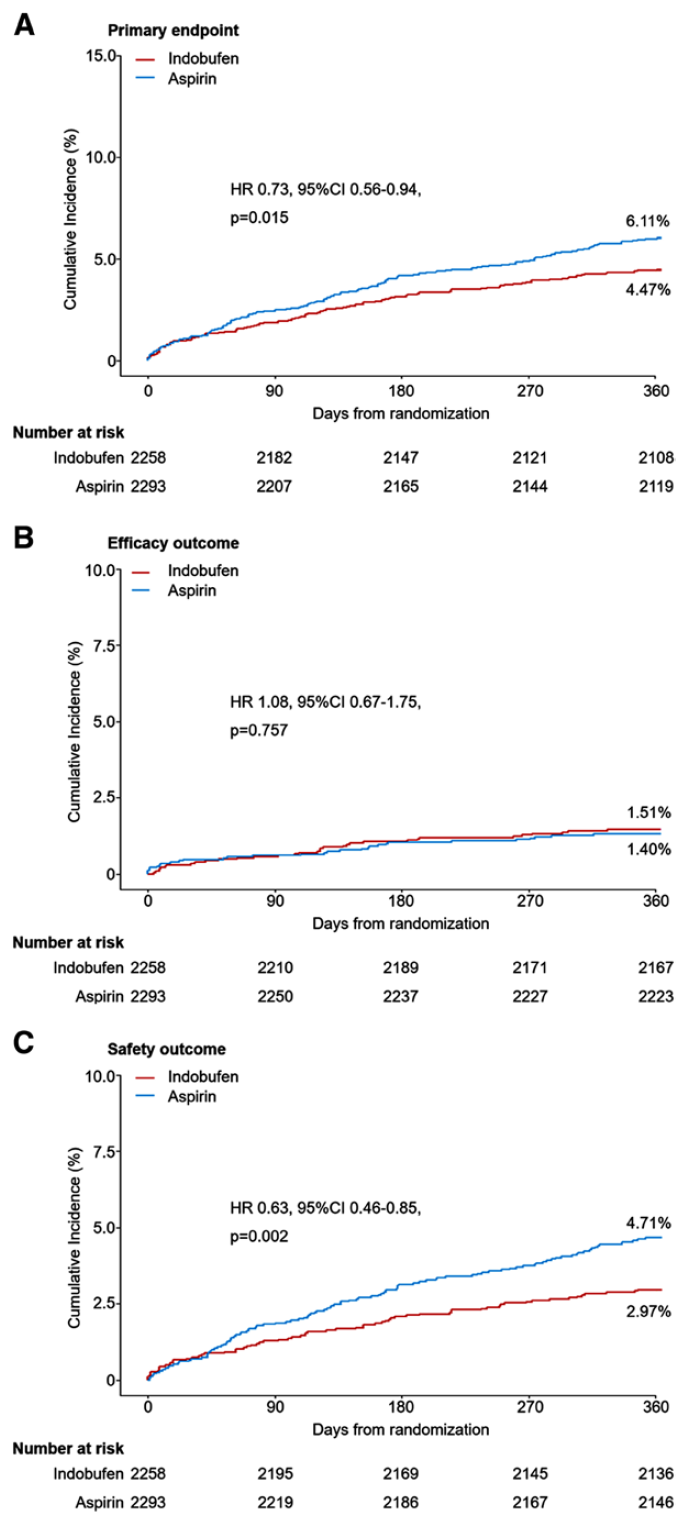
图1
参考文献