2023年,世界瓣膜手术整整一百年。百年来,心脏瓣膜手术经历了数次革新,完成了几大突破,让无数瓣膜病人得以重生。临床诊疗技术日新月异,青年医师作为驱动新技术发展的重要力量,也从未停下精进技能的脚步。
2023年12月2日,“2023亚洲心脏瓣膜中国论坛”隆重举办。论坛上,首都医科大学附属北京安贞医院李岳环医师带来了一例左心室流出道梗阻高风险患者行经心尖ViV-TMVR的病例分享。

neo-LVOT仅为129.5mm²,左心室流出道梗阻风险高,如何选择入路途径和器械避免梗阻的发生?
• 选择球扩瓣是否可行?
• 如何选择合适的入路途径?
• 如何有效避免梗阻?

同轴性差、左心室小、难以选择心尖穿刺点,同时二尖瓣切线投影角度大,重重挑战如何应对?
• 术中注意点都有哪些?
• 术中回撤输送系统有困难怎么解决?
病史简介
患者为79岁女性,2011年行二尖瓣生物瓣置换及三尖瓣成形术,2023年4月因三度房室传导阻滞行永久起搏器植入术。
心脏超声
人工二尖瓣生物瓣重度反流,三尖瓣极重度关闭不全,LVEDd34mm,LAd 59*70*74,LVEF 70%,TAPSE 18mm,下腔静脉呼吸塌陷率<50%。
其他检查
冠脉CTA提示各支冠脉无明显有意义狭窄;腹部超声提示下腔静脉增宽(2.5cm);既往手术记录提示二尖瓣生物瓣型号为Hancock™ II 27mm生物瓣;STS评分计算再次开胸行二尖瓣置换术死亡风险为7.48%。
CTA评估
CTA测量显示二尖瓣生物瓣最大内径为25mm,平均内径24.4mm,最大外径29.6mm,平均外径29mm,瓣架高度为15.8mm。
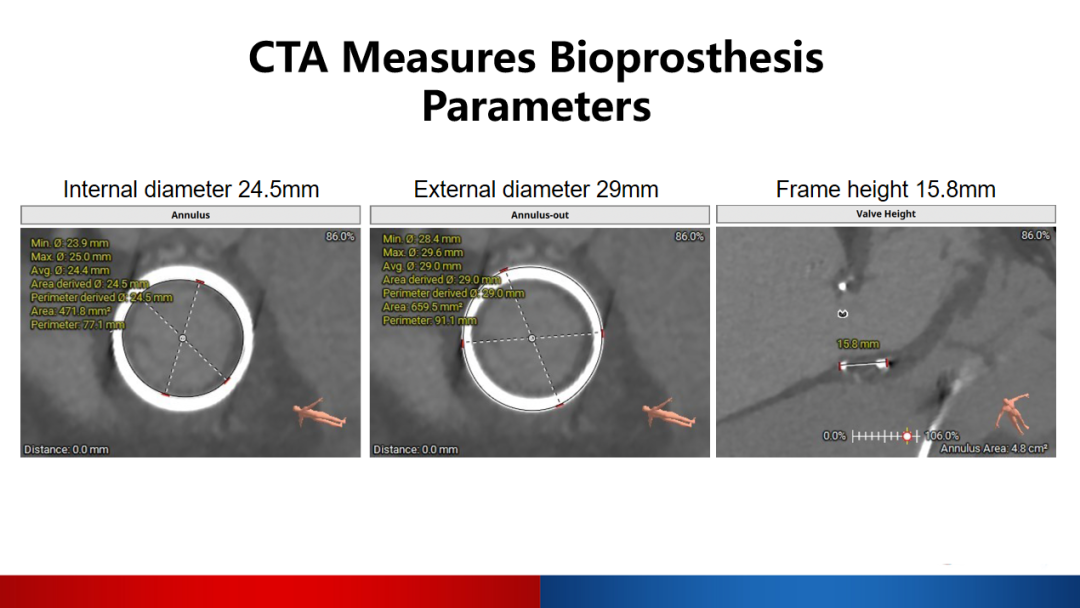
手术难点
左心室流出道面积为256.4mm²,模拟25mm瓣膜植入后,neo-LVOT仅为129.5mm²,提示左心室流出道梗阻高风险。
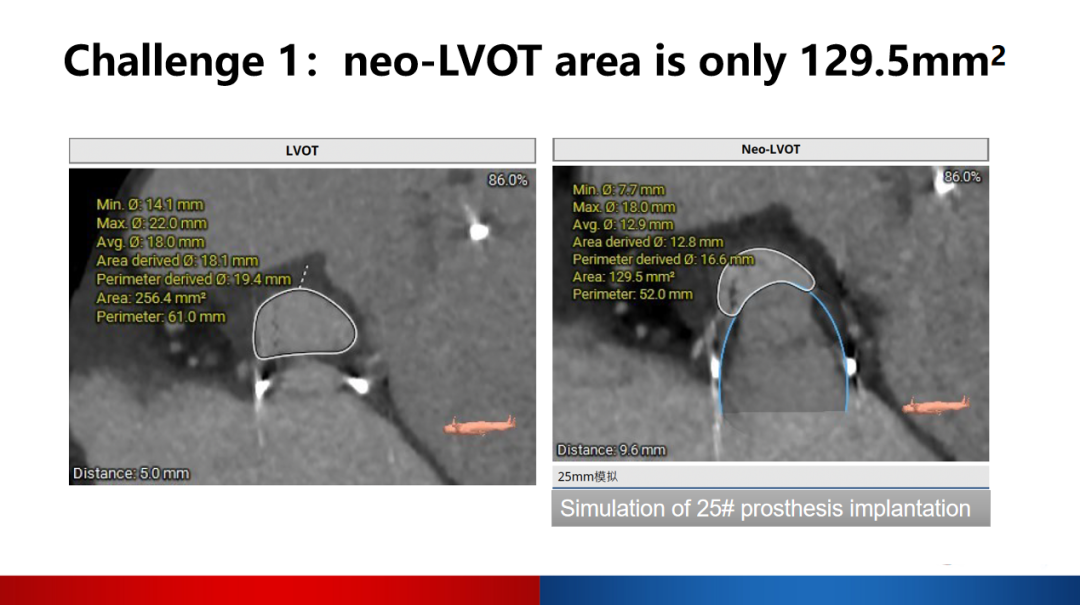
二尖瓣瓣环与左心室成角137°,提示同轴性差;左心室测量舒张末径为39.4mm*78.7mm,提示小左室;右心室测量横径为69.0mm,提示右室扩大,难以选择心尖穿刺点。
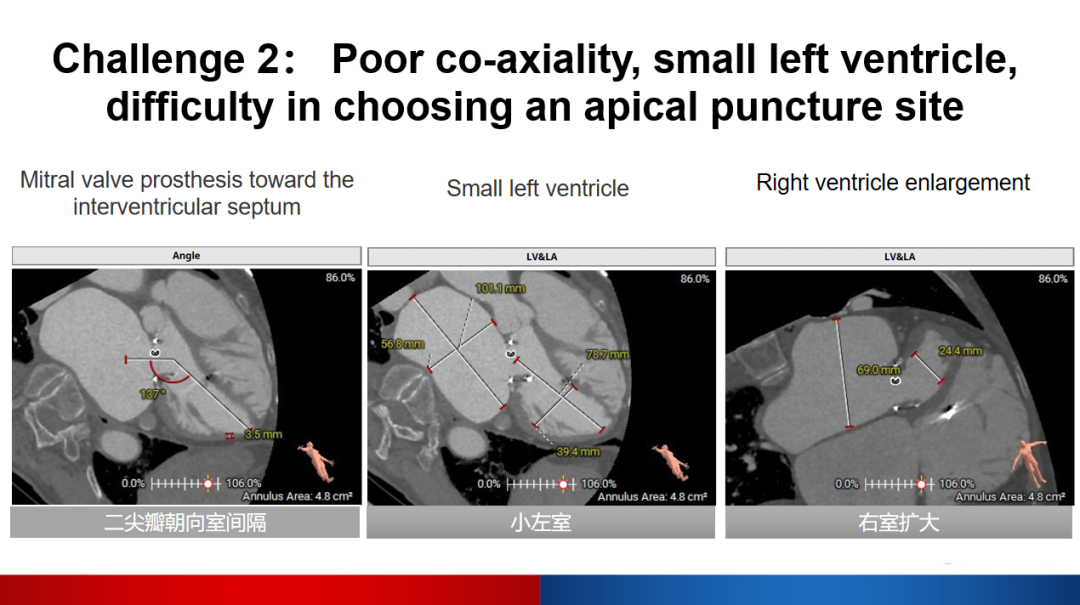
模拟术中投照角度提示二尖瓣切线位投照角度过大,分别为RAO 40°、Cranial 5°及RAO 22°、Cranial 43°,手术难度大大增加。
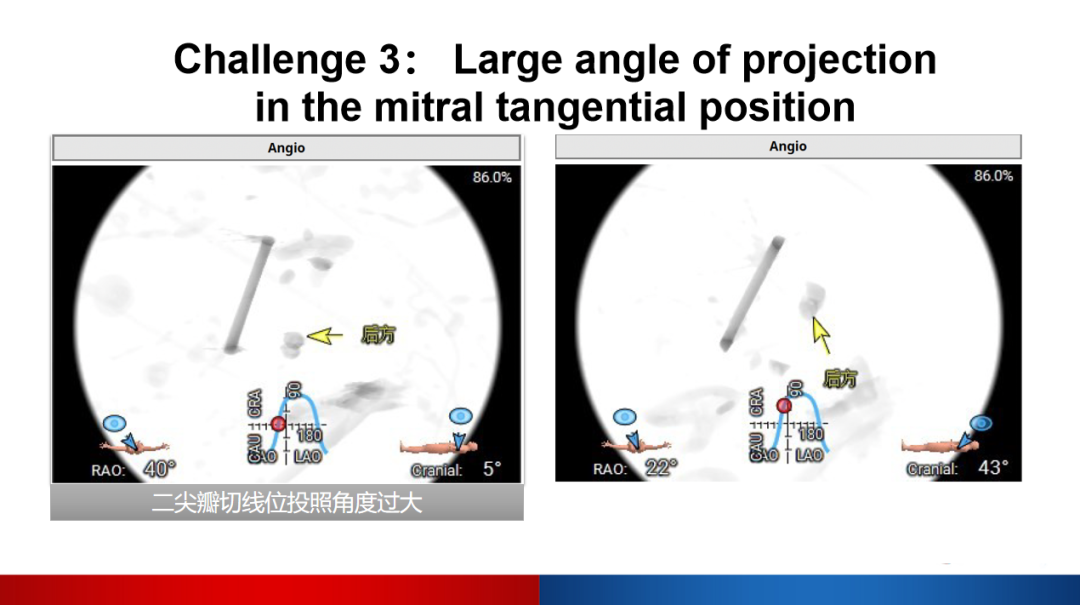
手术策略
• 全身麻醉;
• 体外循环转机;
• 植入临时起搏器;
• 左侧第6肋间切开,经心尖入路植入瓣膜;
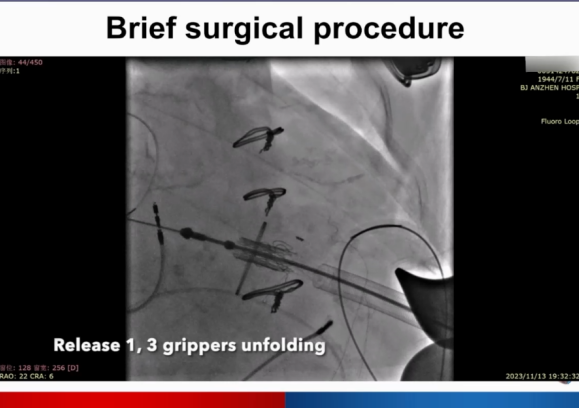
手术过程
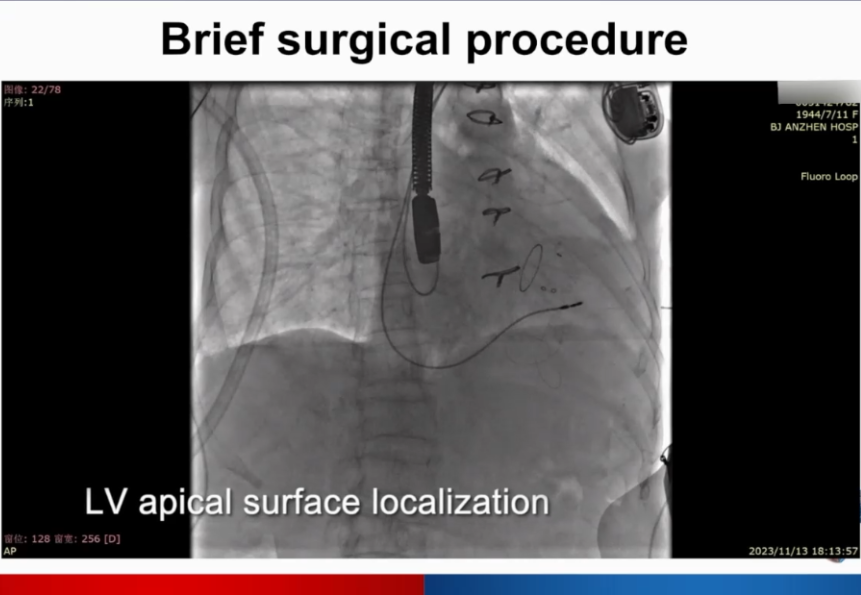
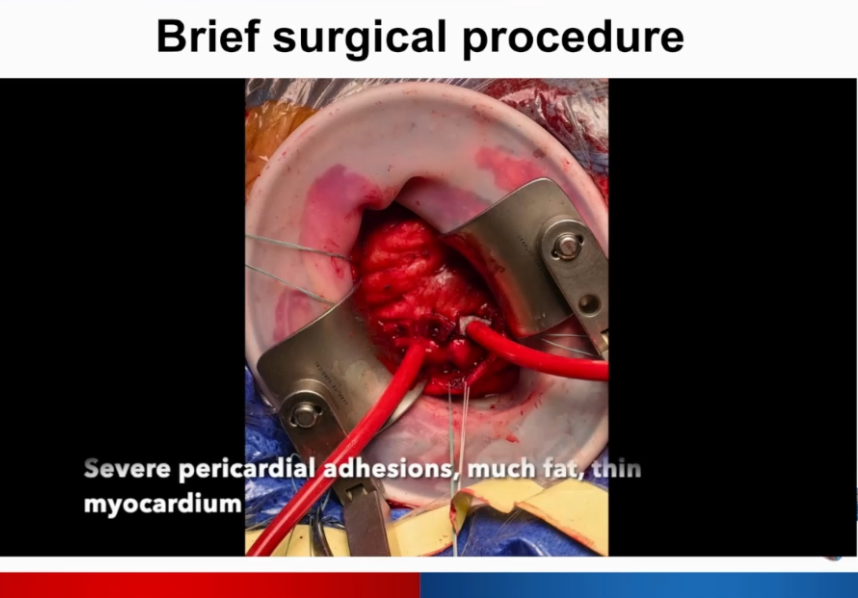
切开定位部位,穿刺心尖,植入临时起搏器。
上下滑动查看更图片
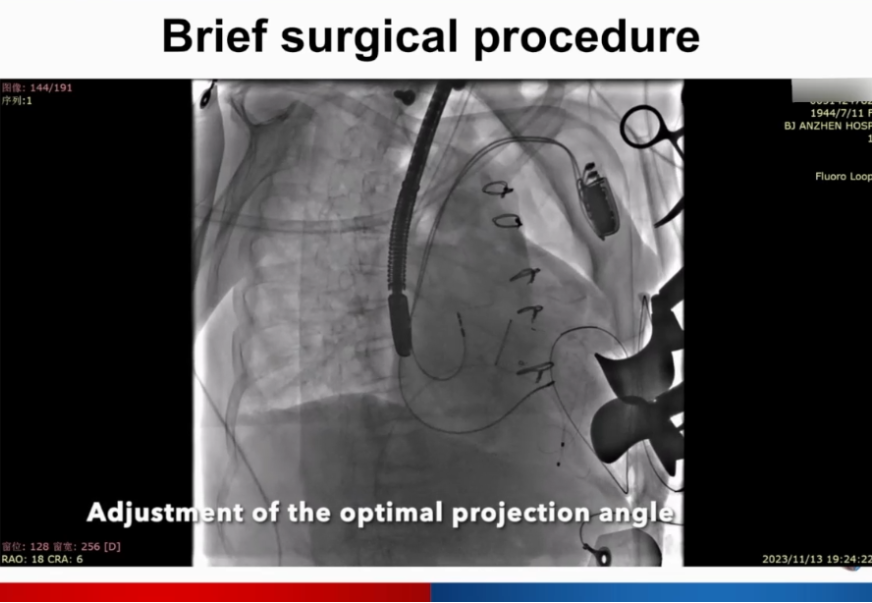
调整最佳投照角度,超硬导丝建立轨道,大鞘扩张穿刺点。
上下滑动查看更图片
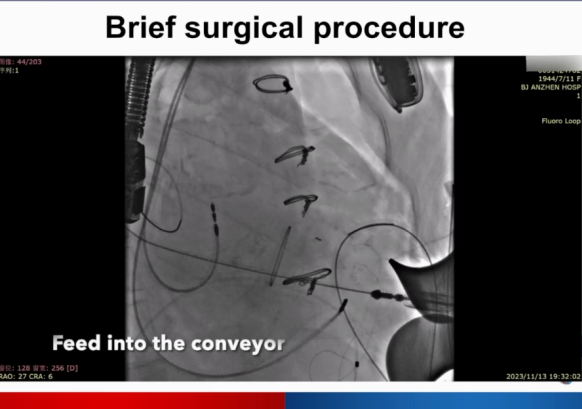
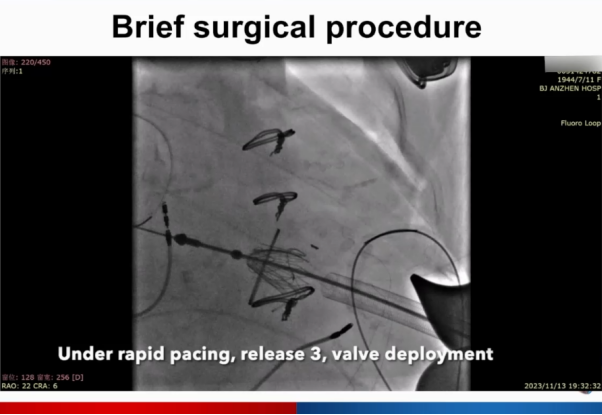
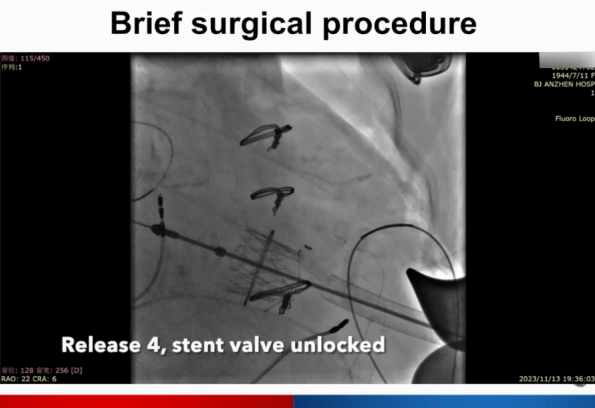
输送系统进入及瓣膜释放。
上下滑动查看更图片
球囊后扩张。
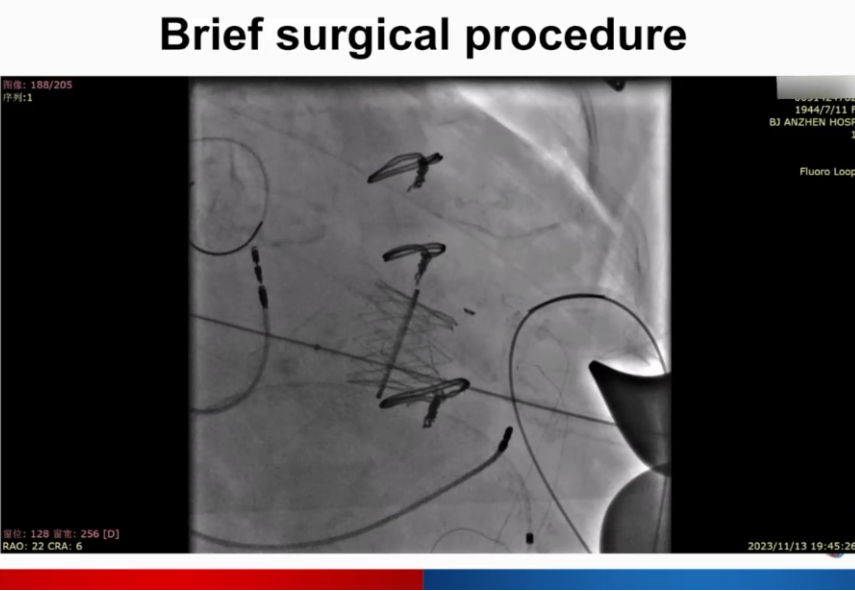
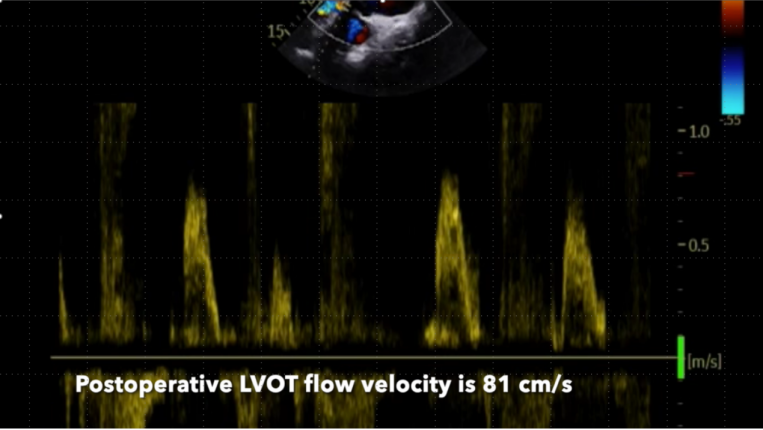
超声提示,术前LVOT流速为59cm/s,术后为81cm/s。
上下滑动查看更图片
病例复盘
neo-LVOT仅为129.5mm²,左心室流出道梗阻风险高,如何选择入路方式和器械避免梗阻的发生?
1.选择球扩瓣是否可行?

——既往研究显示,neo-LVOT面积≤1.7cm²用于预测ViV-TMVR术后左心室流出道梗阻风险的敏感性和特异性分别达96.2% 和92.3%。该病例neo-LVOT面积仅为129.5mm²,若选择球扩瓣会导致梗阻风险过高。
2.如何选择合适的入路途径?
——经房间隔入路目前只能选择球扩瓣,出于避免流出道梗阻风险的考虑,选择经心尖入路。
3.如何有效避免梗阻?
——术中所选器械的3个定位件可实现交界对齐,支架呈非圆柱状,U型缺口可最大程度降低梗阻风险。
同轴性差、左心室小、难以选择心尖穿刺点,同时二尖瓣切线投影角度大,重重挑战如何应对?
1.术中注意点都有哪些?
——对于该患者瓣膜应避免植入深度过低,因为同轴性太差,位置太低,可能导致支架瓣膜脱落至左心室或瓣膜栓塞。该病例术后造影和超声结果显示几乎无瓣周漏,说明术中所选器械在植入深度上的容错性较大,因为3个定位件的锚定作用,发生远期瓣膜迁移至左房的风险较低。
2.术中回撤输送系统有困难怎么解决?
——因为同轴性差,二尖瓣假体朝向室间隔方向,输送器与瓣膜有接触,导致输送器撤回困难;而输送器前端顺应性更好,此时复位2号键,成功撤出输送器。
以“例”论道

李永在教授
具体采取了哪些措施来降低左心室流出道梗阻风险?
该患者术前分析左心室流出道面积较小,neo-LVOT仅为129cm²,球扩瓣为整体圆柱状,左心室流出道梗阻的风险较大;而不选择球扩瓣,便仅能选择经心尖植入瓣膜,根据我中心经验,既往接受治疗的患者,不论是术前还是术后的评估,均未出现左室流出道梗阻。
术中所选器械支架呈非圆柱状,U型缺口可最大程度减少流出道梗阻风险,其定位件可实现交界对齐功能,同时夹持瓣叶,进一步降低风险。
此外,该器械在植入深度上的容错性比较大,左房和左室侧的比例可选择2:8甚至4:6植入;同时,因其3个定位件的锚定作用,远期瓣膜迁移至左房的风险较低。

李岳环医师

李永在教授
Hancock™瓣膜瓣架为22mm,但真实内径接近20mm左右,3-mensio测量时采用圆柱体来模拟,没有考虑到所选器械的皇冠式设计,从而放大了左室流出道梗阻风险,但尽管如此这患者的LVOT梗阻仍然高危。我们中心通常会使用lampoon技术切开植入瓣膜裙边,扩大neo-LVOT面积,减少左室流出道梗阻风险。

刘苏教授
就该病例,假如在术前已经知道各项潜在风险,那么是否还会选择现在的手术策略?
就该患者而言,出于左室流出道梗阻风险的考虑,无法使用球扩瓣,我们认为,经心尖入路植入瓣膜是合适选择。
在术中,患者心脏转位,心室较小,且心尖存在粘连,所以穿刺点较难选择,通过指压实验,在食道超声下,反复尝试定位,我们确定了较理想的穿刺点。
同时,由于患者心腔较小,器械撤出较为困难,也为经心尖手术增加了难度,但由于患者再次开胸手术风险过高,且选择介入治疗意愿较强,所以我们决定进行经心尖介入治疗。

李岳环医师

CHEE Tek-Siong教授
该患者术后血红蛋白较术前下降,是否考虑与瓣周漏造成的溶血相关?
患者手术效果理想,术后造影及食道超声均未见明显瓣周漏,因此,不考虑与瓣周漏造成的溶血相关。

李岳环医师

郭惠明教授
患者极重度三尖瓣反流是否有改善?是否考虑同期处理三尖瓣反流的问题?
该患者术后超声提示三尖瓣反流仍是重度,我们认为同期处理三尖瓣风险较高,且患者有起搏器植入史,同期处理有难度,后期可评估经导管三尖瓣置换或修复的可能。

李岳环医师
妙问巧答
问
术中使用的器械冠脉保护机制的原理有哪些?
答
该器械冠脉保护机制中最突出的是定位件,可夹持瓣叶,避免瓣叶过度推移;其为短瓣架瓣膜,未来进行冠脉再介入较容易,阻挡冠脉开口的风险低;瓣膜径向支撑力较小,无需过度oversize。此外,其在“定位件”和“U型”缺口的作用下实现交界对齐,进一步降低冠脉梗阻风险。
问
瓣膜释放完成,介入器退出来以后,瓣膜的位置、功能状态分别用什么评估?
答
通常我们会通过根部造影确认瓣膜植入深度,以及是否存在瓣周漏。另外,我们也会通过食道超声评价瓣周漏的具体位置,反流量大小,以及决定是否需要进一步后扩。例如狭窄病变,瓣周漏较多,就可以选择后扩减少瓣周漏。当然,超声还可以评估二尖瓣反流是否减少,左室流出道情况等。
郭惠明教授点评
问题一:术中使用的器械冠脉保护机制的原理有哪些?
该器械三个定位件起到了很好的冠脉保护机制,包括U型缺口的交界对齐,可夹持瓣叶,避免瓣叶移位过大等。此外,对于主动脉瓣狭窄患者,可选择适当downsize的策略,也可降低冠脉梗阻风险。
瓣膜释放完成,介入器退出后,通常会通过造影及超声来明确瓣膜判断瓣膜位置和功能,造影可能比超声更明确。