11月7日,Recor Medical Inc. (以下简称“Recor Medical”)和其母公司Otsuka Medical Devices大冢医疗器械联合发布公告,其Paradise™超声消融(uRDN)去肾神经系统获FDA批准上市, 成为RDN领域中第一个获得美国FDA批准的器械,用于治疗血压未控制的高血压患者。其适应症的具体定义尚未揭晓。
Recor的uRDN系统获FDA批准,是RDN行业发展的里程碑事件,标志着这一疗法真正进入临床实际运用。作为中国首个前瞻性、随机、盲法、假手术对照的RDN研究——SMART试验,达成了预设的主要安全性和有效性终点。其使用的肾神经标测/选择性消融系统SyMapCath®/SymPioneer®是全球首创,也是国内首个获得创新医疗器械特别审批程序的RDN产品,正在NMPA审批之中。
此次RDN作为治疗高血压的颠覆性疗法,获得美国FDA的批准,必将对高血压治疗领域带来革命性的影响,为打破当前高血压防治不佳困境提供另一个强有力的武器,成为各国指南认可的高血压治疗“第三大支柱”之一,期待RDN疗法能为广大高血压患者带来福音!
Recor的肾动脉超声消融系统的技术特征是在肾动脉主干以360°的能量投射方式,对肾动脉周围神经进行环形消融。消融系统采用球囊导管,并采用在球囊内循环冷却水保护的方式,从而能够进行环形消融不至于损伤血管内皮和血管壁平滑肌。Recor公司声明消融时间只持续数秒,即可达到消融目的,这一描述在业内造成了超声消融可以更高效的去除肾神经的印象。但根据Recor所披露的手术流程,这一系统在实际使用操作中并不是可以在短时间内即完成手术全过程。这是因为手术操作对血管内径和导管直径之间的匹配,有着明确严格的要求,即当球囊扩张时,必须完全的阻断肾动脉血流。标准是在肾动脉近端注射造影剂时远端不得有任何造影剂的泄漏,即不可在球囊远端有肉眼可见的造影剂通过。
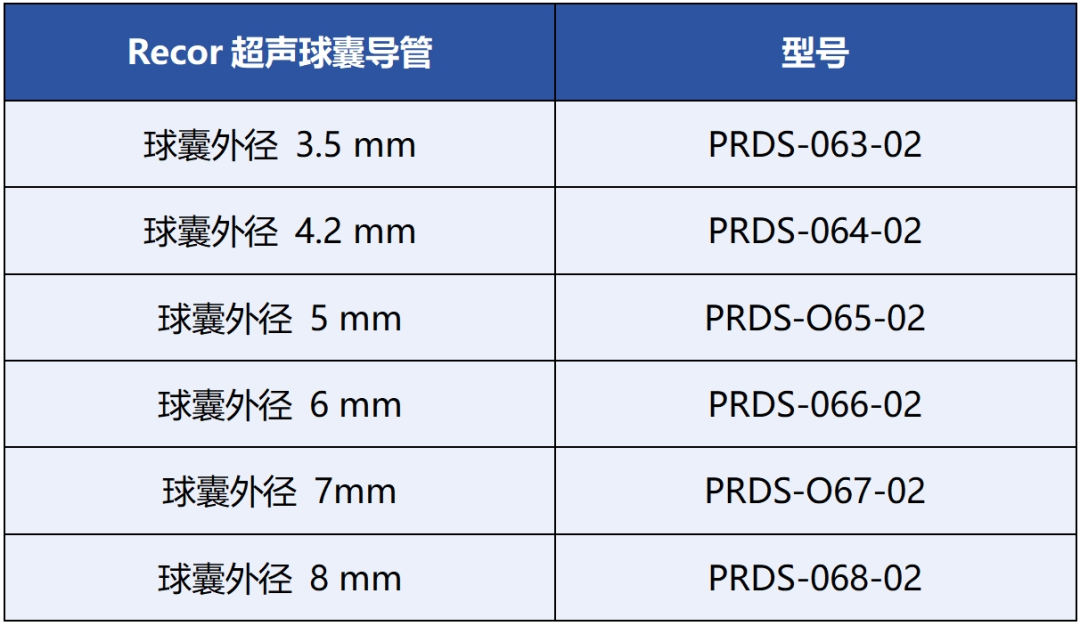
Recor超声球囊导管有6个不同的直径规格(见下表)每个直径规格差别介于0.7-1mm。如果肾动脉主干近端和远端之间的直径差距>1mm(这种差距几乎存在于每一肾动脉主干),就必须更换导管,以获得血管内径和导管球囊的完全贴壁,因此会在手术中花费相当多时间用于更换导管。一般而言,一侧肾动脉平均更换2根导管方能完成手术,这也是为何Recor向FDA递交材料中,所报告的手术时间是72-83分钟。