2023年8月3日,诺华公司和Ionis公司签订合作协议,此次合作,诺华公司将向Ionis公司再提供6000万美元的预付款,以供开发和商业化Lp(a)新型治疗药物(Pelacarsen)。

图1 LPA基因的遗传学、与纤溶酶原、氧化磷脂和临床表型的关系
诺华与Ionis二次签约加强合作
2023年8月3日,诺华公司和Ionis公司签订合作协议,此次合作,诺华公司将向Ionis公司再提供6000万美元的预付款,以供开发和商业化Lp(a)新型治疗药物(Pelacarsen)。Pelacarsen最初由Ionis设计研发,并于2019年获得诺华制药公司的独家全球开发、制造和商业化许可。Pelacarsen是一种反义寡核苷酸药物,通过与LPA的mRNA结合,减少肝脏中载脂蛋白(a)的产生,进而降低Lp(a)(图2)。2期临床研究已公布(图3)。目前一项正在进行的3期临床研究Lp(a)HORIZON(NCT04023552)将对其进一步评估,预计数据将在2025年公布。Ionis首席执行官Brett P. Monia博士表示:“我们很高兴扩大与诺华公司的合作,旨在为心血管事件高危的Lp(a)升高患者提供变革性的治疗手段,此次合作旨在利用Ionis先进的RNA靶向平台技术,提供一种新型Lp(a)靶向疗法,我们预计该疗法将提供业界领先的疗效和给药频率” 。据了解,Pelacarsen是首个进入降低Lp(a)的3期临床研究药物。
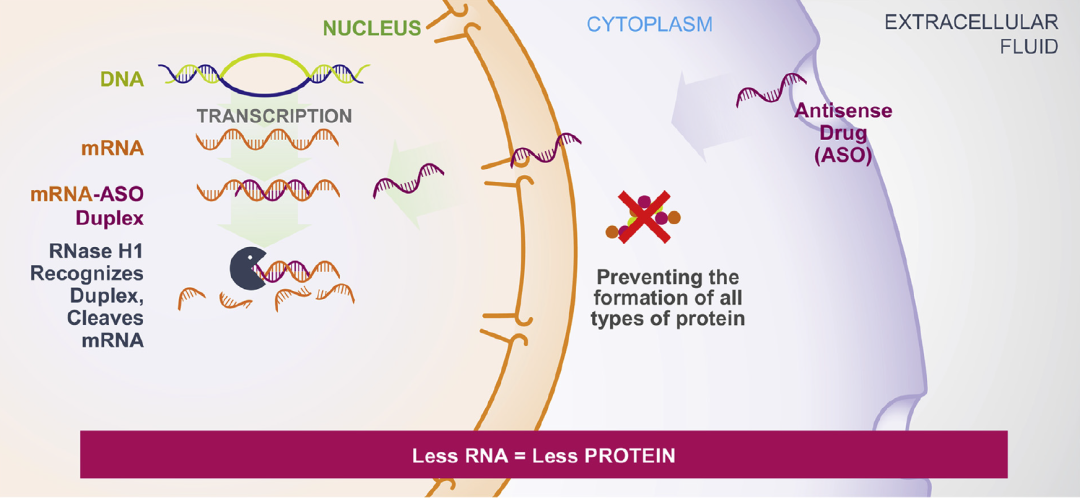
图2 反义寡核苷酸药物的作用机制
反义寡核苷酸(ASO)通过不同的内吞途径进入细胞质,并进入细胞核与其同源mRNA结合,形成mRNA-ASO双链体。核糖核酸酶H1(RNase H1)识别切割降解mRNA,mRNA减少后导致蛋白质翻译减少。

图3 Pelacarsen治疗前后Lp(a)和经校正的LDL-C变化
其他降低Lp(a)的靶向药物
相似的,除了Pelacarsen外,也有几款针对Lp(a)的药物正在研发中。Olpasiran(AMG 890;安进)是一种针对LPA设计的小干扰RNA(siRNA)。OCEAN(a)-DOSE(NCT04270760)2期临床研究针对281例Lp(a)浓度高于60mg/ dL的动脉粥样硬化性心血管疾病(ASCVD)患者初步结果表明,在48周时,Olpasiran治疗能够显著降低这些患者的Lp(a)浓度(图4)。
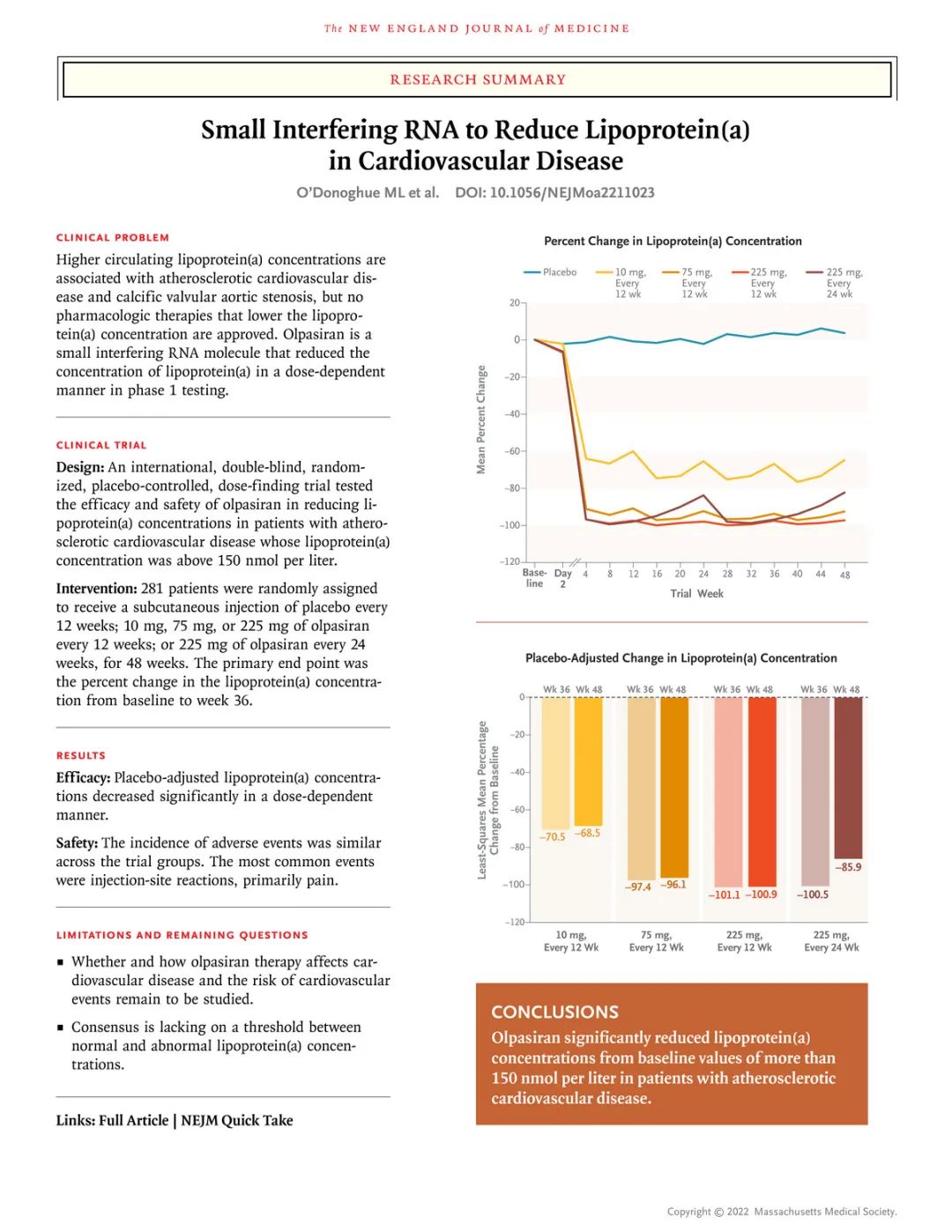
图4 Olpasiran治疗降低ASCVD患者的Lp(a)浓度
此外, LY3819469(礼来)也是一种针对LPA mRNA的siRNA,其正在进行2期临床研究(NCT04914546),评价降低诊断为动脉粥样硬化性心血管疾病患者的Lp(a)水平能力。SLN360(Silence Therapeutics,一种靶向LPA mRNA的siRNA)的APOLLO 1期研究结果于ACC 2022公布。针对32例无心血管疾病的健康人研究结果表明,增加SLN360剂量能够Lp(a)水平呈剂量依赖性降低,并且该药物耐受性良好。SLN360的2期临床研究正在进行中(NCT04606602)。
Lp(a)疗法临床研究设计中面临的挑战
挑战1:应采用什么样的纳入标准?
挑战2:应采用什么样的临床终点?如何确保其临床疗效?
挑战3:能利用替代终点来证明降低LP(a)的临床疗效吗?
目前的临床研究主要侧重于二级预防。然而,重要的是要扩大二级预防的纳入标准。确定Lp(a)基线阈值需要了解其影响大小。而更高的阈值可能会增加招募不同患者的难度。尽管炎症标志物或一些影像学的替代终点已被证明可以反应改变Lp(a)与主要不良心血管事件和ASCVD风险的相关性,但至少应等到亚组分析结果可用后,才能进一步调整Lp(a)治疗方案,并根据这些替代终点设计临床研究。
关键信息
尽管目前还没有降低Lp(a)的药物获批上市,但从这些研发Lp(a)治疗药物的企业中可以看出, Lp(a)已成为人们越来越感兴趣的残余心血管风险因素,这促使了针对Lp(a)基因表达修饰疗法即将问世。考虑到Lp(a)在心血管疾病预防中可能被低估的作用,这些努力对Lp(a)水平升高的患者来说可能是值得的。