
李勇 高稳
复旦大学华山医院心脏科
北京时间2023年8月25日17:15-17:55,在荷兰阿姆斯特丹举办的ESC 2023大会首场HOT LINE将公布STEP-HFpEF临床研究的最新结果,并于当日同步于新英格兰医学杂志在线全文发表。这个评价司美格鲁肽治疗射血分数保留的心衰(HFpEF)合并肥胖患者影响的随机对照试验结果,对今后HFpEF的研究和临床实践可能具有重大价值。

1
STEP-HFpEF研究设计
STEP-HFpEF研究旨在评估司美格鲁肽2.4 mg或安慰剂连续给药52周对体重和Kansas城心脏疾病问卷-临床总结评分(KCCQ-CSS)的影响。
STEP-HFpEF项目包括2项随机、全球多中心、双盲、安慰剂对照试验,研究对象为肥胖型HFpEF患者:STEP-HFpEF (司美格鲁肽治疗肥胖和HFpEF患者的效果(不包含糖尿病人群)和STEP-HFpEF DM (司美格鲁肽治疗肥胖合并HFpEF合并2型糖尿病的疗效观察。在这两项试验中,符合条件的受试者按照1:1随机分配,接受每周一次2.4mg的司美格鲁肽或安慰剂皮下注射,作为标准治疗的补充。根据BMI是否超过35 kg/m2进行分层。随机化后,有一个16周的剂量递增期,旨在减少胃肠道不良事件(ae),每四周增加一次剂量,直到达到最大耐受剂量。此后,每8周进行一次研究访问,直到治疗结束(第52周),治疗结束后随访5周。
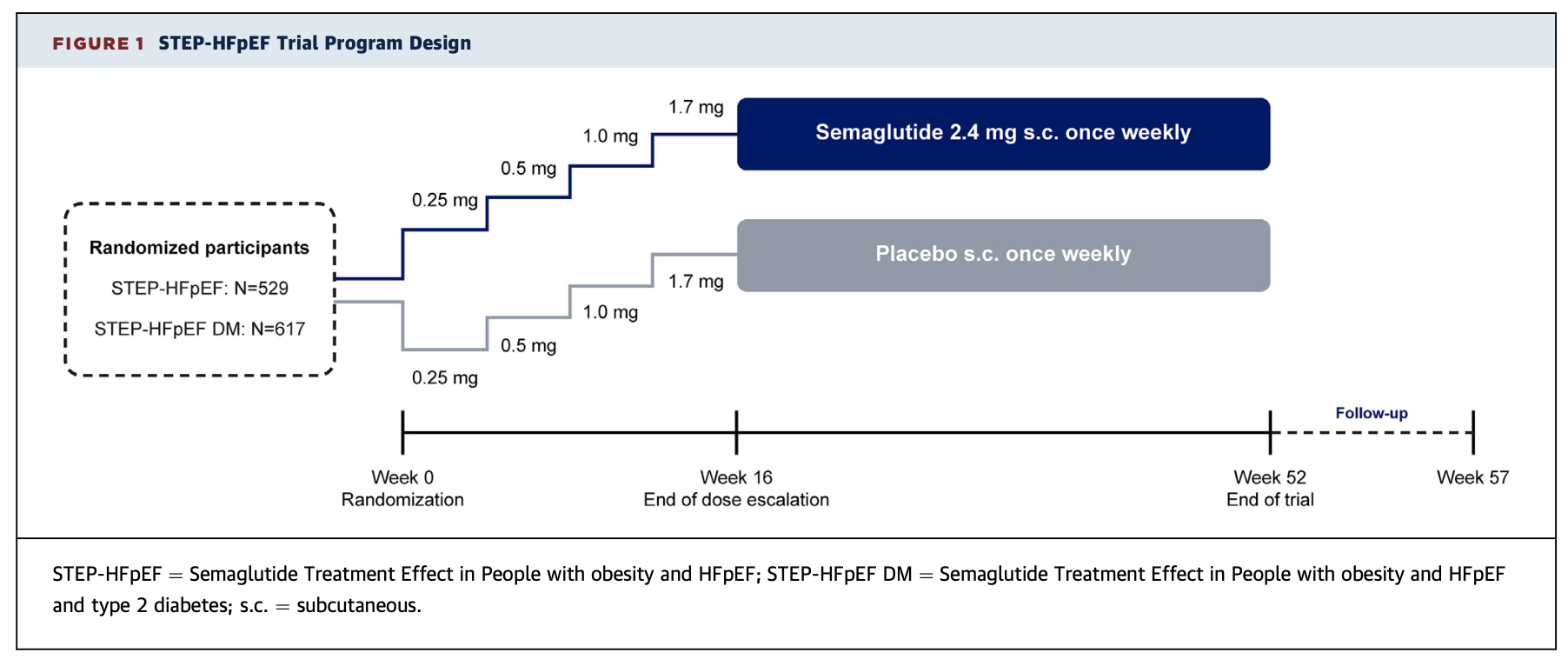
STEP-HFpEF项目的研究设计
STEP-HFpEF研究中,受试者的主要入组标准包含:左心室射血分数(LVEF)在45%以上;NYHA功能等级II至IV;KCCQ-CSS<90分;以及以下标准中的一条: 1)充盈压力升高(基于右心导管或远程肺动脉压力传感器技术);2)利钠肽(NP)水平升高(阈值按基线BMI分层)加上超声心动图异常;或3)过去12个月有心衰住院史,且需要持续使用利尿剂和/或超声心动图异常。主要排除标准为既往或有计划的减肥手术;自我报告在随机分组前90天内体重变化11磅(5公斤);最近(过去30天内)心血管不良事件或心衰住院,或筛查时收缩压>160 mmHg。如果HbA1c≥6.5%,则将患者排除在STEP-HFpEF研究之外;如果HbA1c >10%,则将患者排除在STEP-HFpEF DM之外。
2
STEP-HFpEF研究主要结果
试验纳入了529名患者。中位年龄为69岁,56.1%为女性。基线时的中位体重和BMI分别为105.1 kg和37.0 kg/m2。基线时,患者有相当程度的心力衰竭相关症状、体力活动受限和运动耐受性差的临床状态:66.2%为NYHA II级,33.8%为NYHA III-IV级;KCCQ-CSS中位数为58.9分;6MWD的中位数为320米。

STEP-HFpEF试验达成了研究设计预先设定的主要终点和所有验证性次要终点。从基线到第52周,司美格鲁肽组的KCCQ-CSS平均变化为16.6分,安慰剂组为8.7分(估测治疗差异[ETD]:7.8分,95%CI:4.8-10.9,p<0.001)。从基线到第52周,司美格鲁肽组体重的平均变化为-13.3%,安慰剂组为- 2.6% (ETD: -10.7%, 95% CI:-11.9%至-9.4%,p<0.001)。研究的二个主要终点KCCQ-CSS评分及体重的变化在司美格鲁肽治疗组与安慰剂组之间的差别均达到统计学显著差异,显示出在接受司美格鲁肽2.4mg/周连续治疗一年后,超重/肥胖合并HFpEF的患者在体重显著减轻的同时心功能临床状况显著改善。
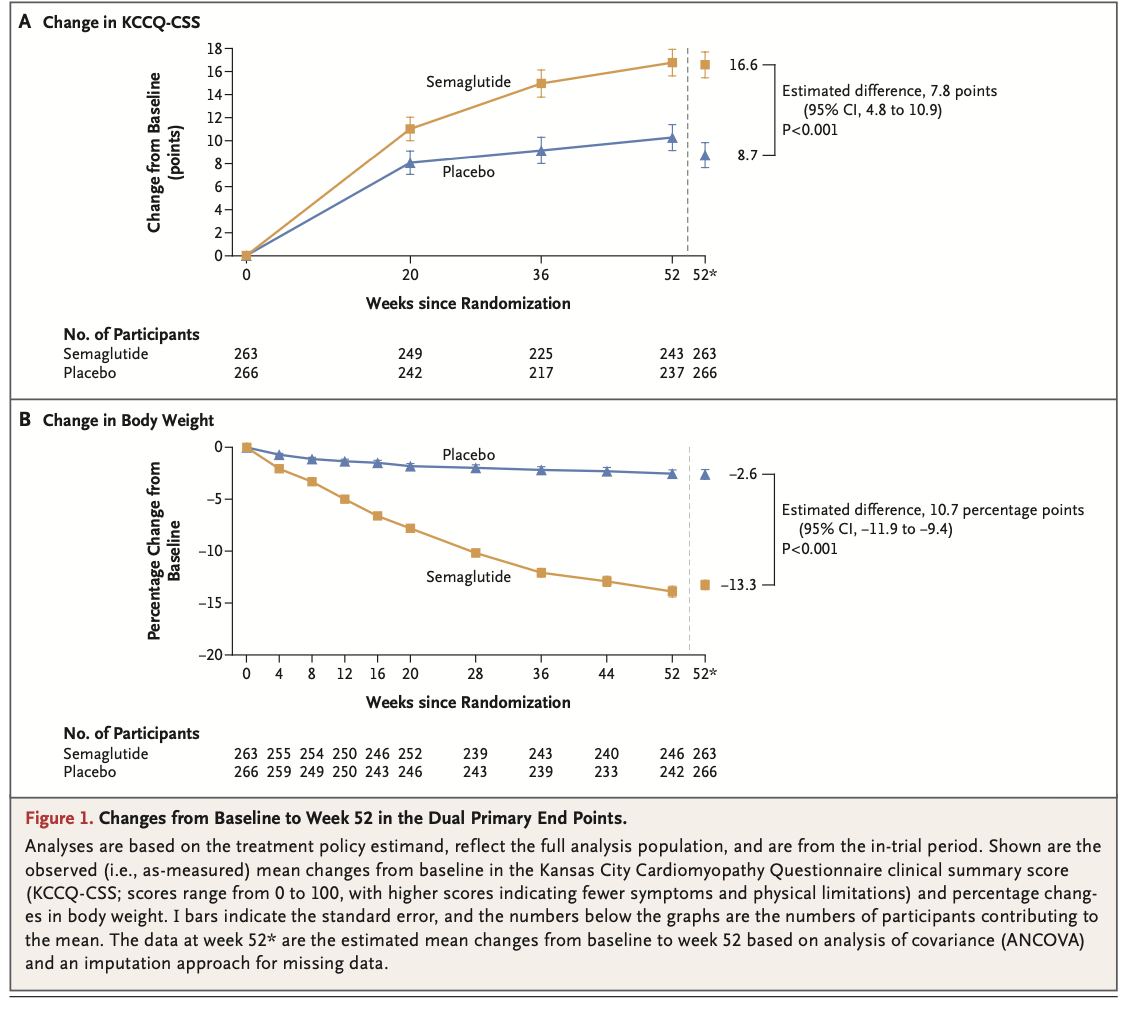
图1. 从基线到52周时的双重主要终点变化
在验证性次要终点上,治疗随访至52周后,司美格鲁肽组6MWD的平均变化为21.5米,安慰剂组为1.2米(ETD: 20.3米,95% CI:8.6 - 32.1;p<0.001)。
在NT-proBNP和hs-CRP水平变化幅度方面,研究随访52周时,司美格鲁肽组和安慰剂组分别为-20.9%和-5.3% (预估治疗比0.84,95% CI:0.71-0.98,p<0.001)。hs-CRP降低幅度分别为43.5%和7.3%(估计治疗比39%,95%CI 0.51-0.72%,p<0.001)。
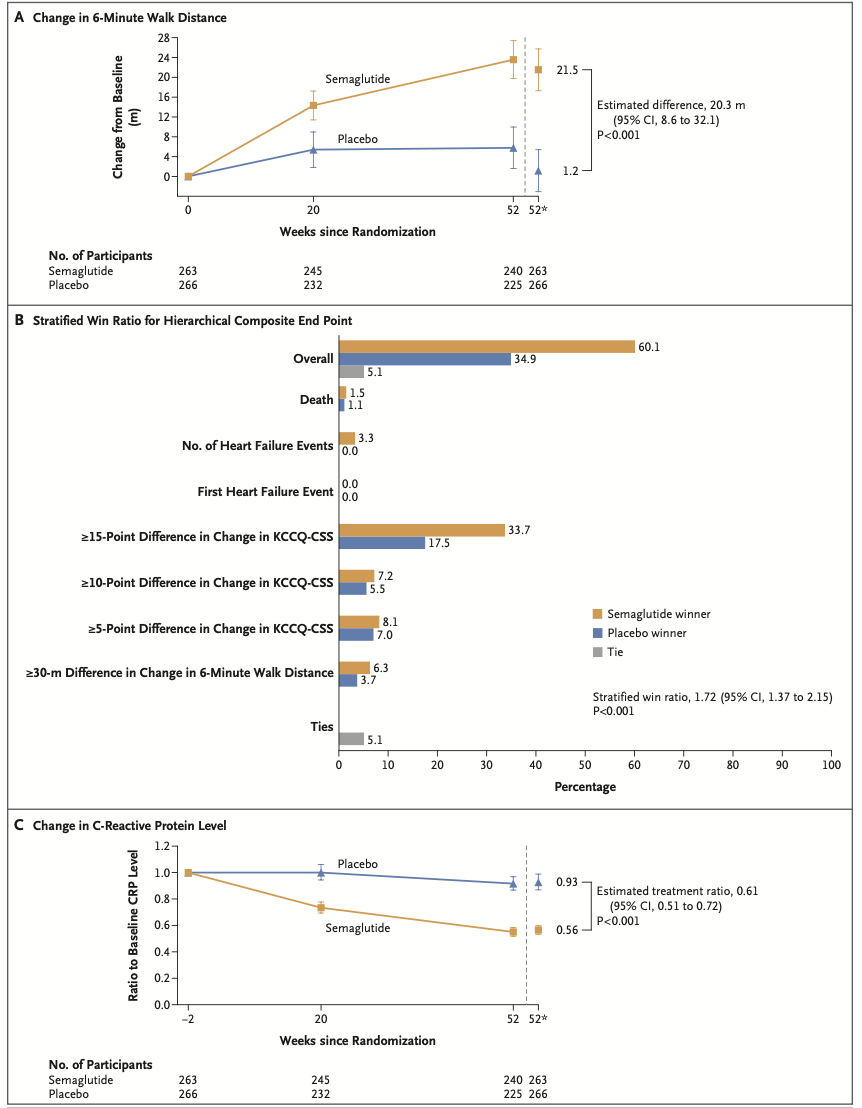
图2. 从基线到52周时验证性次要终点变化
在探索性终点(心力衰竭住院或急诊就诊)上,司美格鲁肽组有1例患者,安慰剂组有12例患者发生心力衰竭住院或紧急就诊风险降低达92%(RR 0.08,95% CI 0.00-0.42)。

图3. 探索性终点首次心力衰竭事件的累积发生率
在安全性方面,司美格鲁肽组和安慰剂组分别有35名(13.3%)和71名(26.7%)受试者报告了严重不良事件(SAE) (p<0.001)。司美格鲁肽的安全性得到再一次印证。整个研究随访中,司美格鲁肽组的不良事件(AE)以消化道症状为主。
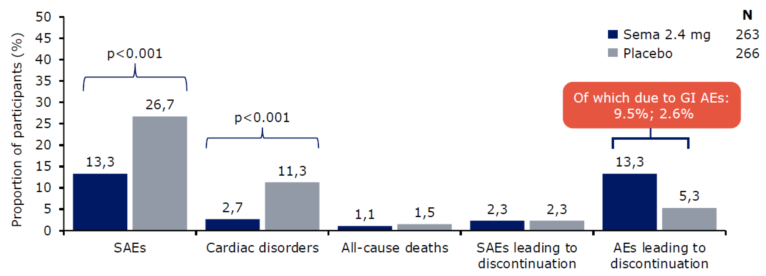
图4. 研究随访过程中的不良反应与严重不良反应发生率
3
STEP-HFpEF研究:对HFpEF认知的一个跨跃
STEP-HFpEF研究是第一个专门针对肥胖作为HFpEF治疗策略的药物试验。其结果表明在HFpEF合并肥胖患者中,与安慰剂相比,每周一次使用2.4mg的司美格鲁肽治疗一年可以显著减轻体重并改善心力衰竭症状、体力活动受限和运动功能,显著降低NTproBNP水平和hs-CRP,同时首次心力衰竭事件显著降低。
左心室内压明显升高导致肺淤血,进而显著降低血流/通气比值,导致机体缺氧的一系列临床表现。而NTproBNP是反映左心室内压升高的一个非常敏感的指标。在临床实践中,测定NTproBNP水平及随访其变化在诊断心力衰竭和判断心力衰竭患者对治疗措施的反应具有着举足轻重的意义。
另一方面,多个大样本的临床研究结果表明,体重与NTproBNP成反比。体重较大或肥胖的心力衰竭患者,NTproBNP水平较低,甚至可能处于正常范围内。因此,当STEP-HFpEF研究中,司美格鲁肽治疗组的受试患者在体重显著减轻的同时,NTproBNP水平显著降低,提示司美格鲁肽对左心室内压力的降低具有确凿的有利影响。因为目前还不能确认心肌细胞上是否存在GLP-1受体,因此,司美格鲁肽的这种下调左心室内压的作用,可能不是来源于对心肌细胞的直接作用,而是通过代谢调控和下调炎症反应活性的综合结果。
已知SGLT2抑制剂治疗HFpEF患者,能够减轻心力衰竭症状、缓解体力活动受限和改善运动功能,同时显著降低NTproBNP水平,提示SGLT2抑制剂同样能显著降低左心室内压。因为SGLT2抑制剂具有明确的排钠利尿作用,目前公认SGLT2抑制剂降低左心室内压和NTproBNP水平的机制可能主要来源于血流动力学中容量的改善。
因此, GLP-1RA司美格鲁肽在STEP-HFpEF研究中显示出来的对HFpEF患者的有利作用,机制上可能与SGLT2抑制剂并不完全相同。GLP-1RA对血流动力学的容量影响甚微。司美格鲁肽可能在心力衰竭的病理生理进程的上游,针对性地减少心包膜脂肪量,并显著调控代谢谱和炎症活性状态,继而纠治或逆转了心肌细胞及其细胞间基质结构和功能,从而显著降低了患者的左心室内压。
从这个角度来看,STEP-HFpEF研究提示,HFpEF可能是一种代谢性疾病。
4
STEP-HFpEF之后
在EMPEROR-Preserved研究和DELIVER研究发表之后,恩格列净和达格列净已经被证实能够显著改善HFpEF患者的临床结局。在STEP-HFpEF研究的结果表明,在GLP-1RA司美格鲁肽治疗超重/肥胖合并HFpEF患者获得明显缓解临床症状,提升运动能力,且与NTproBNP水平降低一致的结果后,下一步必然要启动GLP-1RA司美格鲁肽治疗HFpEF的临床结局终点研究(CVOT)。同时,直接比较SGLT2抑制剂和GLP-1RA对HFpEF代谢谱和病理生理学影响的异同,也值得进一步深入研究和解析。
尽管STEP-HFpEF研究观察到的HFpEF临床表现改善幅度是所有代谢干预药物中最大的,但仍然需要硬终点临床试验来证实司美格鲁肽治疗HFpEF的临床获益。一旦证实GLP-1RA治疗能够显著改善HFpEF患者的临床预后,那将对HFpEF的临床实践产生重大影响,并且将改变超重/肥胖与HFpEF的认知,超重/肥胖不仅与HFpEF呈共病状态,或许超重/肥胖也是HFpEF的病因和需要治疗干预的目标。
5
对临床实践的意义
自1989年以来,美国的肥胖患病率几乎增加了两倍,从15%增加到2018年的约42%。由于过早死亡风险增加、经济负担及对健康相关生活质量的负面影响,肥胖已成为一个重大的公共卫生问题。
中国有世界上最多的肥胖人群,《中国居民营养与慢性病状况报告(2020年)》最新数据显示,我国超过1/2的成年人超重或肥胖,超重和肥胖率分别为34.3%和16.4%。新近发表在国际学术期刊《糖尿病,肥胖和代谢》杂志上的“中国肥胖患病率及相关并发症:1580万出难题的横断面真实世界研究”报告,我国总体超重人群占比达34.8%,肥胖人群占比达14.1%。超过90%的超重和肥胖者合并存在一种或多种代谢异常,其中脂肪肝患病率为65.4%,糖尿病前期患病率 33.8%,血脂异常患病率 36.9%,高血压患病率 28.8%,糖尿病患病率13.8%,颈动脉斑块患病率16.2%,慢性肾脏病合并5.2%。根据全球疾病负担(Global Burden of Disease Study,GBD)研究,2019年中国归因于高体质指数(BMI)的CVD死亡人数为54.95万,11.98%的CVD死亡归因于高BMI。
减重是肥胖管理的基础。已有研究证实,当体重持续减轻5%至15%时,肥胖相关并发症将获得显著临床改善。指南认为体重减轻大于5%是治疗肥胖及相关合并症的推荐最低目标。体重减轻5%以上时,高血压、高血糖和高甘油三酯血症均能获得有益的变化。肥胖可通过多种干预措施进行管理,包括饮食、生活方式、强化行为治疗(Intensive Behavior Treatment,IBT)、药物和/或手术干预。在减重药物中,胰高血糖素样肽-1(GLP-1)受体激动剂通过抑制胰高血糖素的分泌,以葡萄糖依赖的方式增强胰岛β细胞的胰岛素分泌,从而调节餐后血糖。同时通过产生饱腹感,减少食欲和食物消耗,减缓胃排空。
GLP-1受体激动剂已被证明对糖尿病和非糖尿病患者的体重管理有效,并已证明可改善心脏代谢危险因素。2021年,FDA批准司美格鲁肽作为饮食和运动的补充,用于治疗肥胖症。司美格鲁肽对肥胖患者的治疗作用(Semaglutide Treatment Effect in People with obesity ,STEP)项目系列研究考察了司美格鲁肽 2.4 mg用于减重的有效性和安全性,以及对心脏代谢参数和相关肥胖合并症的影响。在整个STEP试验汇总,与安慰剂相比,每周一次司美格鲁肽2.4 mg给药治疗显示出对心脏代谢危险因素和肥胖相关合并症的有益影响:体重平均降低10-15%。此外,腰围平均减少5-10cm,HbA1c平均降低0.5-1.5%,血压平均降低3.0-5.0/1.0-3.0 mmHg,LDL-C平均降低5%,VLDL-C平均降低15-18%,而hs-CRP平均降低达50%。
2023年8月9日SELECT临床三期试验的结果公布,显示每周一次2.4mg司美格鲁肽皮下注射可使ASCVD合并超重或肥胖的患者发生MACE(包括心血管死亡、非致死性卒中和非致死性心肌梗死)风险下降约20%。
SELECT研究共纳入了17,604名45岁以上的超重或肥胖患者,均存在已知的心血管疾病,并排除了HbA1c≥6.5%或已经确诊糖尿病的患者。受试患者的平均年龄为61.6±8.9岁,男性72.3%,白种人84.0%,BMI 33.3±5.0 kg/m2。ASCVD病史中,心肌梗死史76.3%,脑卒中史23.6%,症状性外周血管疾病8.6%,≥2种ASCVD者8.0%。所有受试者中24.3%有过心力衰竭诊断(其中53.1%为射血分数保留心力衰竭)。基线所有受试患者均接受了优化抗ASCVD药物治疗,包括服用降LDL-C药物者占89.8%,抗血小板药物者占85.9%和抗凝药物者12.6%,β-阻滞剂者70.0%,ACEi/ARB/ARNI者76.3%,钙拮抗剂者26.7%,利尿剂者33.3%。SELECT研究的主要终点是第一次出现的MACE(非致死性心肌梗死、非致死性脑卒中及心血管死亡)的复合终点。
经过长达5年的随访,累积主要终点达到1270个MACE后,SELECT研究达成了研究目的。与安慰剂组相比,司美格鲁肽2.4mg组主要转归终点的MACE事件风险降低20%,达到具有统计学意义的显著降低,其中心肌梗死、脑卒中和心血管死亡等主要终点的三个组分事件发生率均有降低。总体上,司美格鲁肽2.4mg/周治疗ASCVD患者的安全性和耐受性良好。
迄今为止,STEP-HFpEF是第一个专门针对肥胖作为治疗目标的临床试验项目,表明长效GLP-1RA司美格鲁肽不仅仅能有效降低体重,改善心血管代谢谱,下调炎症反应活性,而且能够将体重作为肥胖合并HFpEF的治疗靶点,有效缓解心力衰竭的临床症状,减少心力衰竭事件。
由此可见,从STEP系列研究,到SELECT研究,再到今天的STEP-HFpEF研究,展示了GLP-1RA司美格鲁肽在心血管事件链从危险因素,到ASCVD,到心力衰竭的全程保护作用。
6
小结
在肥胖患者常常同时合并多重心血管危险因素,相关的心血管疾病风险显著升高。在这些心血管不良事件中,心力衰竭,尤其是HFpEF占据庞大位置。与非肥胖人群相比,肥胖患者表现为更高的血容量和高负荷状态,更高的高血压和左心室重构患病率(这本身就是HFpEF发生和发展的重要因素),更厚的心外膜脂肪厚度,导致更严重的功能受损和生活质量下降。而观察性研究表明,临床有意义的体重降低可以改善患者的临床症状、体力活动受限和生活质量评分。
就在本次ESC’23大会的同一天发表的《2023 ESC糖尿病患者心血管疾病处理指南》明确建议,对超重/肥胖的患者,在生活方式改变的基础上,应及早启动GLP-1RA的治疗。
多项严谨的随机对照研究表明,对超重/肥胖者而言,使用司美格鲁肽治疗,将体重减轻10%或更多,能够带来超越体重减轻的全面心血管代谢谱改善和炎症活性水平下调。STEP系列试验已经证明,GLP-1RA司美格鲁肽对超重和肥胖患者能有效减重。SUSTAIN 6和SELECT研究表明,对合并或不合并糖尿病的ASCVD患者,司美格鲁肽治疗均能够显著降低主要不良心血管事件风险。今天发表的STEP-HFpEF研究将司美格鲁肽引入心力衰竭的治疗,必将对未来心血管疾病的研究和临床实践带来新的思考和发展。