



VitaFlow®瓣膜5年随访数据公布,为TAVR中长期数据“添砖加瓦”
主动脉瓣狭窄是一种常见的瓣膜性心脏病,其发病率随着年龄的增长而逐渐升高。西方国家流行病学调查结果显示,主动脉瓣疾病的患病率高,常伴随心室重构及升主动脉增宽,临床预后较差。根据NHLBI数据库信息,美国主动脉瓣狭窄患病率在≥75岁的人群中达到2.5%[1]。中国老年心脏瓣膜病队列研究(China-DVD)研究表明,60岁以上中度及以上瓣膜性心脏病的患者主动脉瓣狭窄约占11.5%[1],超过半数的老年主动脉瓣狭窄是由于瓣膜退行性变引起[2]。
作为一种微创介入导管技术,经导管主动脉瓣置换术(TAVR)自诞生以来在国际上得到广泛应用,其安全性和有效性已被多项大型随机对照研究证实。因其无需开胸、心脏停跳和体外循环等优点,TAVR成为无法实施外科手术或手术高危的重度主动脉瓣狭窄患者的有效选择。
2010年,复旦大学附属中山医院葛均波院士率先完成我国第一例TAVR手术,开启了我国经导管瓣膜介入治疗的新时代。历经十余年,TAVR技术在我国飞速发展,技术也越来越成熟。根据“2022结构心脏病年度报告”,2022年度我国商业化TAVR植入8689例,较2021年7319例增长18.7%[3]。
TAVR技术飞速发展的同时,器械也不断优化迭代,国产瓣膜的研发也进入快车道,Venus-A、J-Valve、VitaFlow®瓣膜先后上市,为患者提供了更多选择。但目前关于TAVR中长期数据的证据较缺乏,随着TAVR患者群的不断扩展,了解中长期数据至关重要。


VitaFlow®瓣膜5年随访:心血管相关死亡率仅8.2%
近日,复旦大学附属中山医院葛均波院士团队在《中华心脏与心律电子杂志》发表了关于VitaFlow®经导管瓣膜系统的5年数据[4]。数据分析显示,VitaFlow®经导管瓣膜系统治疗外科手术禁忌或高危的重度主动脉瓣狭窄患者长期预后良好。
该研究为前瞻性、多中心、单臂上市前临床研究,纳入我国11个临床中心应用VitaFlow®经导管瓣膜系统行TAVR的107例不适合外科手术的重度主动脉瓣狭窄患者,主要终点为术后全因死亡和致残性卒中,次要终点为新的永久起搏器植入、心肌梗死、脑卒中、主要血管并发症、急性肾损伤等。

所有中心均将经股动脉入路作为首选,经颈动脉入路为次选。术中采用球囊预扩张狭窄的主动脉瓣膜,快速起搏的同时对主动脉根部进行造影,指导VitaFlow®经导管瓣膜系统瓣膜释放。主要根据MSCTA对瓣膜尺寸进行选择,同时结合术中球囊扩张时球囊测量大小。
患者基线情况如表1所示。
表1. 107例行TAVR患者的基线资料
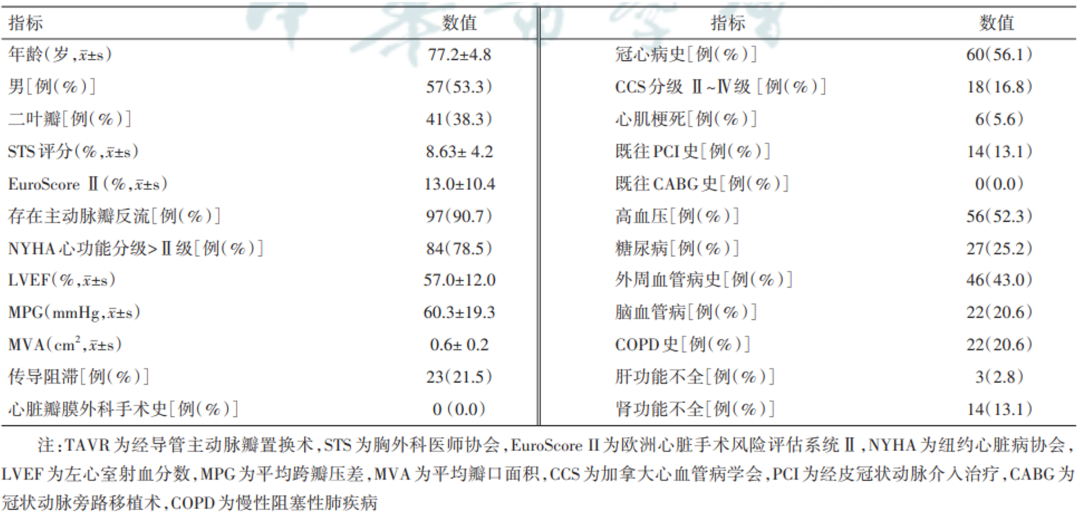
此前公布的1年随访结果显示,患者主动脉瓣口跨瓣压差由术前60.4 mmHg, 改善至1年后9.8 mmHg,瓣口面积由术前0.6 cm2改善至1年后1.8 cm2,中重度瓣周漏发生率为0。
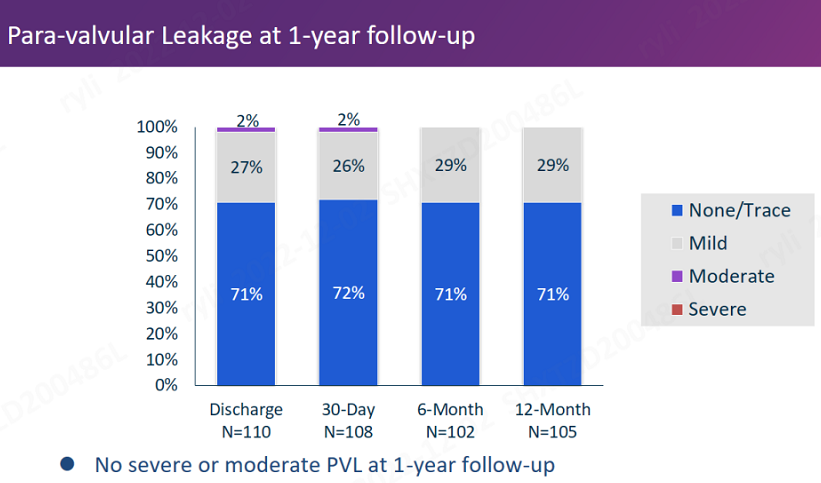
图1. 随访1年瓣周漏发生情况
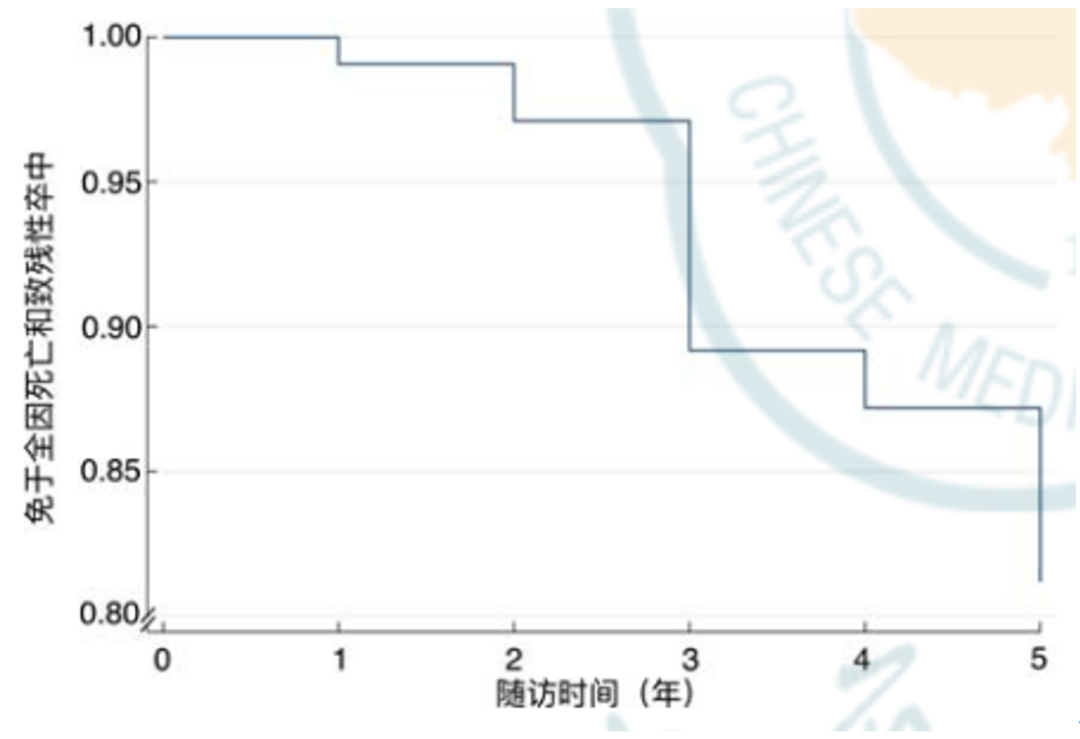
图2. 107例TAVR患者的Kaplan-Meier 生存曲线
表2. 107例患者TAVR后5年临床随访情况

单因素分析结果显示,高血压、糖尿病慢性阻塞性肺疾病史与TAVR术后全因死亡和致残性卒中的发生相关。其中,高血压为保护因素,这与目前的认知不符,故不纳入多因素Cox回归分析。多因素 Cox 回归分析显示,糖尿病(HR=2.63,95%CI 1.04-6.69,P=0.042)是术后全因死亡和致残性卒中发生的独立预测因素。


二叶瓣与三叶瓣亚组分析:5年随访结果无显著差异
所有入组患者中,二叶式主动脉瓣患者占38.3%,5年随访结果显示,二叶式和三叶式主动脉瓣患者在全因死亡率、致残性卒中、新发永久起搏器植入、脑卒中、心梗等方面均无显著差异(P>0.05)。
因此,无论是在二叶瓣患者或三叶瓣患者,VitaFlow®均具有良好的安全性与有效性。而且优异的5年的临床数据,无疑为全球术者在VitaFlow®治疗严重主动脉瓣狭窄患者方面,提供了安全性和有效性的坚实循证医学依据。


为TAVR中长期数据“添砖加瓦”
此次研究公布的是VitaFlow®长达5年的随访数据,为国产TAVR的中长期数据再添浓墨重彩的一笔。研究显示了VitaFlow®瓣膜植入后5年较低的全因死亡率和致残性卒中率,多因素分析显示,糖尿病是术后全因死亡和致残性卒中发生的独立预测因素。
在并发症方面,虽然本研究发现术后PPMI率稍高(术后30天和3年新发起搏器植入率分别为16.4%、20.0%),但在既往报道范围之内(3.4%-25.9%)[5]。研究者对TAVR术后PPMI的危险因素进行了分析,发现基线存在传导阻滞和术中心律失常是TAVR术后PPMI的预测因素。这一点也与既往报道相符。2021年发表在《心脏电生理》杂志的一项荟萃分析[6],纳入37项观察性研究、超过7万例患者,TAVR术后PPMI发生率为22%,男性风险更大,且随着年龄的增长而增加。患有糖尿病、存在右束支传导阻滞、基线房室传导阻滞和左前分支传导阻滞的患者风险更高。

结语

VitaFlow®瓣膜


参考文献
[1]宋光远:经导管主动脉瓣介入治疗年度报告2021. 中国结构性心脏病学组年度总结会暨2021年度行业报告, 2022-01-15.
[2]Distribution, Characteristics, Management of Older Patients With Valvular Heart Disease in China: From China-DVD Study. JACC: Asia. Apr 12, 2022.
[3]潘文志:结构性心脏病年度报告2022. 2022结构心脏病年度报告, 2023-01-27.
[4]翁梓珑, 林大卫, 潘文志, 等. 国产经导管瓣膜系统治疗重度主动脉瓣狭窄长期预后及其预测因素分析. 中华心脏与心律电子杂志[J]. 2023;11(2):114-119.
[5]吕童莲, 邱久纯, 刘彤. 经导管主动脉瓣置换术后心律失常和心电图改变[J].实用心电学杂志, 2023, 32(2):130 - 135.
[6]Mahajan S, Gupta R, Malik AH, Mahajan P, Aedma SK, Aronow WS, Mehta SS, Lakkireddy DR. Predictors of permanent pacemaker insertion after TAVR: A systematic review and updated meta-analysis. J Cardiovasc Electrophysiol. 2021 May;32(5):1411-1420. doi: 10.1111/jce.14986. Epub 2021 Mar 17. PMID: 33682218.

转载自公众号:CFI瓣膜学苑
