在EuroPCR 2023中,Nico Pijls教授汇报了选择性冠脉内低温在急性前壁心肌梗死中研究-EURO-ICE(Selective Intracoronary Hypothermia in STEMI to Reduce Infarct Size)。课题组一直从事亚低温心肌保护的器械研发,现在就这个研究的结果和思考分享如下。
研究背景
急诊再灌注治疗改善了急性心肌梗死患者的预后,然而在再灌注治疗时会发生再灌注损伤,目前无针对再灌注损伤的有效方式。
既往基础研究显示亚低温可以很好的减少心肌缺血再灌注损伤。
目前应用亚低温治疗的器械为全身系统低温,由于低温效率和全身副反应,在临床中无显示可以减少心肌梗死面积。
目前亚低温有多种实现方式,包括全身低温:冷盐水灌注、血管内冷却、腹膜灌洗,局部低温:表面冷却、血液体外冷却再灌注、冠脉内冷盐水灌注等。
研究假设
对梗死区域进行选择性冠状动脉内低温治疗,并通过远端冠状动脉温度测量进行监测,克服了先前全身低温作用的局限性,减少心肌梗死面积。
研究设计
为RCT研究,共在8个中心共纳入200例前壁心肌梗死且TIMI血流0-1级的患者,按1:1随机分配到SIH+PPCI组(实验组)或单独PPCI组(对照组)。排除标准年龄:小于18岁或大于80岁,PPCI术前TIMI血流2-3级,心源性休克/血流动力学不稳定,已知严重左心室功能障碍或严重瓣膜病,已知既往前壁心肌梗死病史,既往CABG,CMR成像禁忌。
试验方案
使用器械:为改良的OTW球囊导管(图1)。

图1 改良的OTW球囊导管
SIH实施:将压力/温度导丝通过闭塞病变,置入前降支远端,用以监测梗死区温度变化;置入工作导丝,沿工作导丝送入OTW球囊,在再灌注前,将OTW球囊送至闭塞处并低压扩张球囊以阻断血流同时对梗死区域灌注22℃的生理盐水(阻塞期,20 ml/min,维持10分钟),随后抽瘪球囊,再以4℃的生理盐水灌注(再灌注期,15-30 ml/min,维持10分钟)。研究主要终点:3个月MRI评价梗死面积。
研究结果
选择性冠脉内治疗可以安全实施,无发生全身不良反应。
温度降低:通过头端带有压力/温度传感器的导丝监测梗死区域的温度变化,当灌注15秒后即可以使梗死区域的心肌达到有效低温(29-33℃)(图2),停止灌注30秒后即恢复正常温度。

图2 低温实时作用效果示例

图3 患者平均温度降低情况
临床结果:基线:两组在总ST抬高幅度幅度、病变在LAD近端和中断比例、术前TIMI血流均无明显差异,选择性冠状动脉内低温治疗延长再灌注时间。安全性:发生室颤比例两组间无差异。结局:两天MRI评价心肌缺血危险区域(AAR)、3个月的心肌梗死面积、射血分数在两组间无差异。选择性冠状动脉内低温治疗组有2例死亡,对照组有1例死亡。在亚组分析中,进行最优治疗的患者,选择性冠状动脉内低温组梗死面积显著减少,射血分数无差异。

图4 临床研究结果
研究结论
EURO-ICE研究中的选择性冠状动脉内低温:适用于目前STEMI患者PPCI的常规流程,无全身低温需要的院前急救和麻醉多学科的参与,使用的器械为临床PCI常用标准器械;在梗死相关区域在20秒内诱导低温(-6°C至-10°C);整体操作安全,没有任何显著的副作用,延长缺血时间15分钟;MRI评价3个月梗死面积没有任何差异,LVEF无差异。
思考
这个研究结果无疑给我们带来了很多思考。亚低温的心肌保护有坚实的理论依据,动物研究充分证明了其良好的保护作用,然而COOL-MI、ICE-IT、PAPID MI-ICE、CHILL-MI、VELOCITY、SHOCK-COOL等临床研究均没有显示亚低温治疗器械的临床有效性。
分析研究使用方法,主要包括全身低温和局部低温两大类(图5),其中全身低温模式包括:冷盐水灌注、腹膜灌洗、血管内冷却;局部低温模式包括:表面冷却、血液体外冷却再灌注、冠脉内冷盐水灌注等。

图5 常见低温装置
注:A:腹膜灌洗亚低温;B:血管内全身低温装置;C:OTW球囊冠脉内盐水灌注
目前低温治疗优缺点(表1):冷盐水灌注法通过在静脉快速输注大量冷盐水(4℃),会导致容量超负荷,影响心脏做功和心功能。血管内冷却法代表是血管内温度管理系统,单独使用难以快速达到目标温最终导致缺血到再灌注时间延长,需与冷盐水灌注等方法联合使用。腹膜灌洗法是进行冷盐水腹膜灌洗,腹膜提供了较大的热交换面积,可以快速达到降温目的,但是会引起腹压增高,进一步影响呼吸和循环功能,同时心肌梗死时进行其他侵入性操作增加了治疗的复杂性,同时腹腔感染、出血风险增加。同时全身低温会出现颤抖,需要镇静等治疗,增加治疗的复杂性。常规的表面冷却方法在实际操作中难以应用于心肌梗死患者。血液体外冷却再灌注是患者自身的血液在体外进行冷却,然后灌注到冠状动脉或者冠状静脉窦,会增加操作的复杂性和血流动力学的改变。
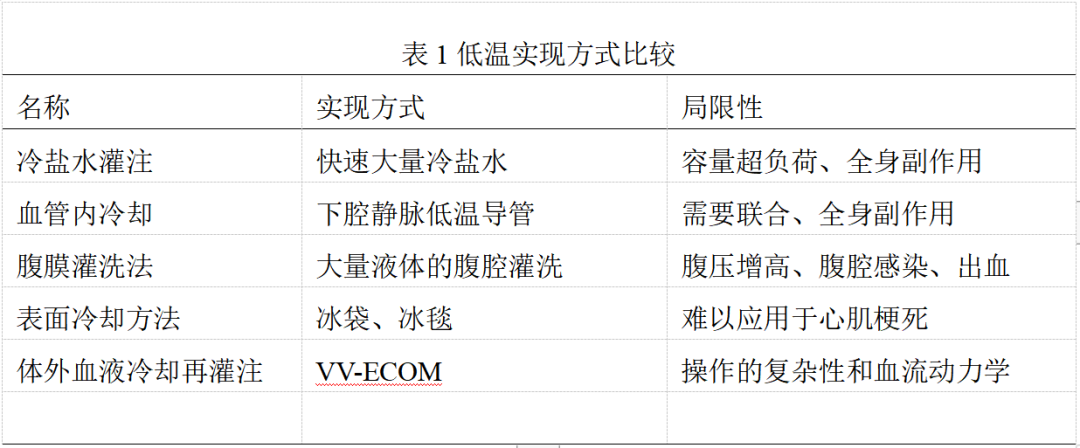
表1 低温实现方式比较
注:VV-ECOM:静脉-静脉体外人工膜肺Extracorporeal artificial membrane lung
基于以上器械的局限性,选择性冠状动脉内低温治疗近年来得到关注和研究,EURO-ICE研究就是基于这样的背景。从研究结果来说,有其良好的可行性和安全性结果,使用装置为冠脉PCI常用器械,可以快速实现目标温度,且无全身副作用。然而在有效性方面没有达到主要终点。分析原因有器械本身应用的局限性:1、本研究在急诊PCI时使用压力温度导丝作用常规使用工具,可以很好的检测温度,调控盐水灌注的速度,然而压力导丝在未开通的罪犯血管使用,有其操作的困难和潜在风险;2、冠脉内20min内注入200-400ml生理盐水,会增加心脏负荷,对再灌注损伤和心脏功能有潜在不利影响,与目前impelia装置减轻心脏负荷改善再灌注损伤的治疗观念不一致;3、延长再灌注时间,争分多秒进行再灌注治疗是急性心肌梗死救治的基石,为获得更多的心肌保护,而延长了缺血时间,这就需要更多的心脏保护要大于缺血时间延长导致的损伤,实际上无相关公式可以借鉴;4、在冠脉闭塞时进行远端冷盐水灌注,我们不好确定远端病变情况和血流;5、本方法使用低温盐水灌注,为不增加过多的心脏负荷,作用时间会受到限制;6、从研究数据来看,亚组分析中,低温治疗有减少梗死面积的作用,提示进一步在合适的病人里面的有效性;7、核磁利用梗死后的水肿评价AAR是常用的有效方法,选择的常用时间为术后5-7天,既往有研究显示有效的心肌保护可能会减少水肿。
综合目前研究,未来思考如下,亚低温治疗有坚实的理论基础,冠脉内低温治疗提供了有益的方向,显示了可行性和安全性,之后关于冠脉内低温治疗的器械应该在以下方向进一步优化:1、更高的作用效率和更新的作用模式,在保障再灌注的基础上尽量少的减少再灌注损伤;2、为冠脉介入治疗常用器械,简单操作;3、不增加心脏负荷和容量;4、可以调整的作用时长;5、观察有效作用人群的特点。期待在这方面的有效探索,为心肌缺血再灌注损伤这个基础与临床转化最大的痛点,提供可能得策略和器械。
主要参考文献: