
陈茂
四川大学华西医院

本文特邀作者 四川大学华西医院 白琳 冯沅 陈茂
导语:
岁序更迭,华章更新。转眼间,2023年翩然将至。
二尖瓣返流(Mitral Regurgitation, MR)是最常见的心脏瓣膜病,在一般人群中发病率约为1.7%,75岁以上人群中约为9.3%[1]。既往MR的治疗以外科开胸二尖瓣修复或置换手术为主,但随着近年来经导管介入技术以及器械的进步,经导管二尖瓣介入治疗也逐渐展现其优势,并让患者受益。
经导管二尖瓣介入治疗技术目前主要分为经导管二尖瓣修复术(Transcatheter mitral-valve repair,TMVr)和经导管二尖瓣置换术(Transcatheter mitral-valve replacement,TMVR)两大类。
本文旨在回顾本年度经导管二尖瓣介入治疗的相关进展,并展望经导管二尖瓣介入治疗的未来。
TMVr主要是基于既往外科二尖瓣修复术相关原理,利用介入手段进行治疗,主要包括了经导管二尖瓣缘对缘修复术(Transcatheter Edge-to-Edge Repair, TEER)、经导管二尖瓣瓣环成型术以及人工腱索介入修复术。
1. 经导管二尖瓣缘对缘修复术
TEER起源于外科二尖瓣缘对缘修复术,是目前循证医学证据最充足、应用最广泛、最受认可、最成熟的经导管二尖瓣治疗技术,对于原发性MR和继发性MR均有一定的治疗效果,其安全性、有效性和耐久性也得到了证实。
其中MitraClip也是唯一一个同时获得中国国家食品药品监督管理局、美国食品药品监督管理局(FDA)、欧洲CE认证的经导管二尖瓣修复产品。今年在TEER治疗领域,公布了众多的研究成果不仅拓展了MitraClip在不同患者中应用的证据,一些如PASCAL等新型二尖瓣修复系统也取得了良好的表现。
1.1 MitraClip受益人群得到拓展
MitraClip作为目前植入量最大的二尖瓣介入治疗器械,在2022年中公布了多项研究的成果,拓展了TEER在不同特征人群中获益的证据。
在符合COAPT标准的MR患者的真实世界研究方面,2022年欧洲心脏病学会(ESC 2022)上,美国Vanderbilt大学的Kashish Goel教授公布了COAPT PAS研究的结果,评估了真实世界中继发性MR患者使用MitraClip的安全性和有效性。该研究连续性纳入美国406个中心5000例使用MitraClip的继发性MR患者,为目前该领域最大的回顾性观察性真实世界研究。同MitraClip RCT研究相比,真实世界研究中患者基线时的年龄更大、女性更多、心功能和生活质量更差、二尖瓣反流程度更严重、使用指南推荐药物治疗更少,风险更高,研究纳入的人群更加复杂。
COAPT PAS研究结果显示,真实世界中MitraClip植入率(98% vs. 98%)、MR反流程度改善的程度(MR程度降至≤2级 91% vs. 95%)、1年时未发生全因死亡或心衰再住院的比例(66.3% vs. 66.5%)均与COAPT RCT研究相似,但手术时长(142±64 min vs. 163±118 min)与器械植入时长(63±46 min vs. 83±81 min)更短,基于堪萨斯城心肌病调查问卷(Kansas City Cardiomyopathy questionnaire,KCQQ)评分显示的生活质量改善状况更加明显(Δ=﹢28 vs. Δ=﹢17),纽约心功能分级(New York Heart Association,NYHA)较基线水平改善程度更大(Δ=﹢63% vs. Δ=﹢35%),卒中(2.4% vs. 2.9%)、心肌梗死(1.3% vs. 3.2%)、器械血栓(0.1% vs. 0.3%)等不良事件的发生率也更低。在单瓣叶夹持(1.4% vs. 0.7%)、再次植入瓣膜(3.5% vs. 2.9%)的发生上略高于COAPT RCT研究[2]。
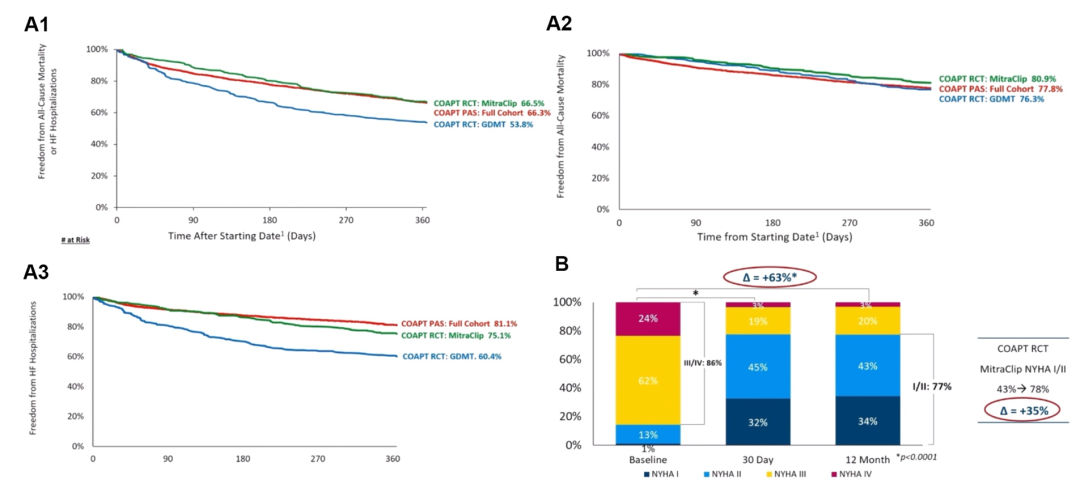
图1 COAPT PAS 部分研究结果[2]
注:A. COAPT PAS研究与COAPT RCT研究中TEER治疗组和药物治疗组在全因死亡率及心衰再入院间的差异。B. COAPT PAS研究与COAPT RCT研究中TEER治疗组在NYHA分级间的差异。
结果发现,在1年随访时,NCL-MMR组、NCL-AHF组与CL组在全因死亡率(19.6% vs. 22.8% vs. 22.6%)、心衰再入院率(25.0% vs. 24.5% vs. 32.6%)上没有统计学差异,而与NCL-AHF组相比,CL组和NCL-MMR组中维持MR≤1+的患者百分比更高(81.3% vs. 86.5% vs. 97.2%)。三个队列的NYHA分级均较基线时有明显改善(NYHA I-II CL: 81% vs. 20%, P<0.001, NCL-MMR: 83% vs. 16%, P<0.001, NCL-AHF: 81% vs. 20%, P<0.001);KCQQ评估的生活质量显示CL组(70.6 vs. 46.9, P<0.001)和NCL-MMR组(68.3 vs. 45.7, P<0.001)有显著改善,而NCL-AHF组趋向于提高(65.4 vs. 54.4, p=0.07),但无统计学意义[3]。
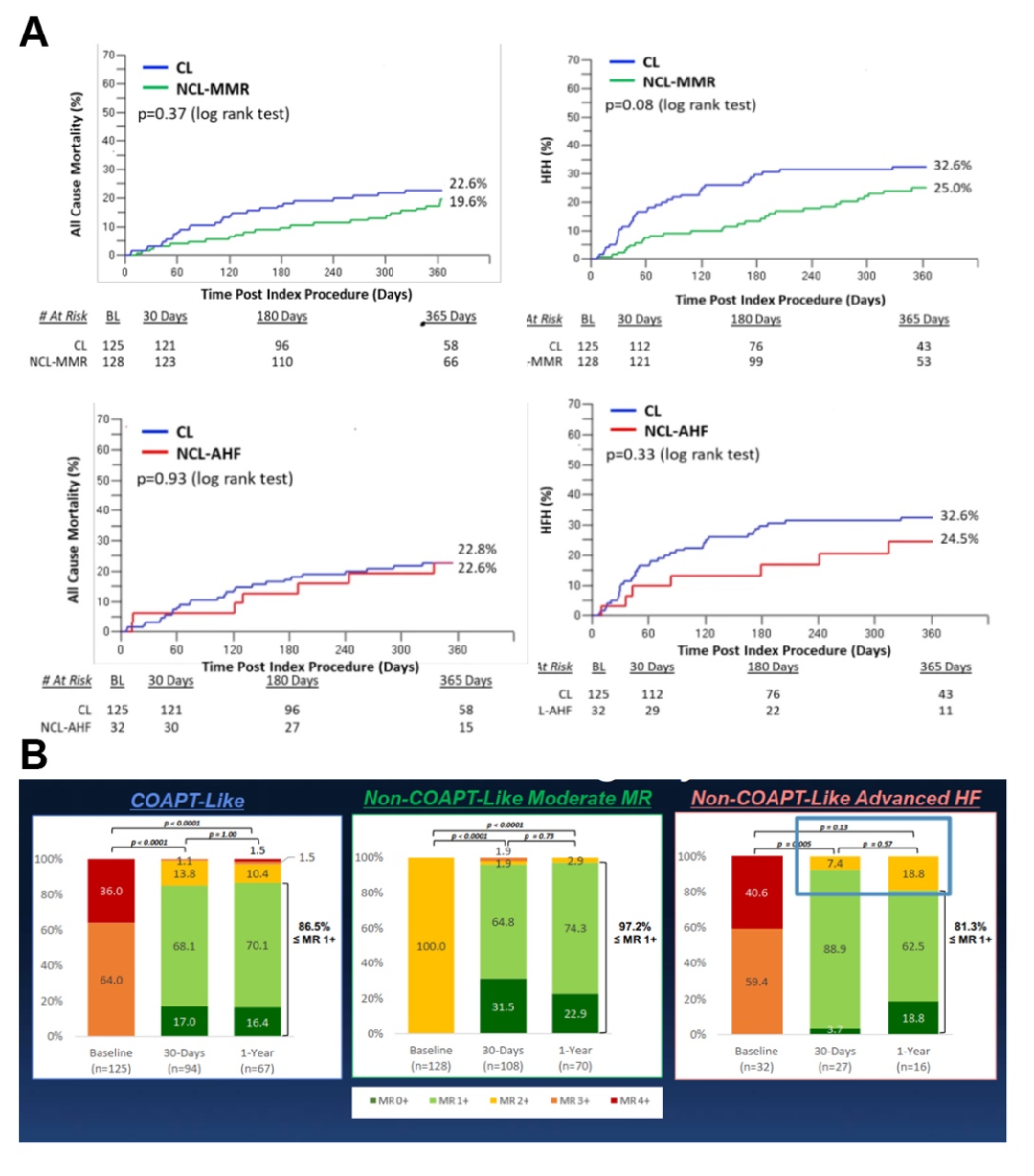
图2 EXPAND研究部分结果[3]
注:A. CL组与NCL-MMR组、NCL-AHF组随访1年内全因死亡率及心衰再入院。B. 三组术后30天及1年是二尖瓣返流情况。
2022年美国经导管心血管治疗学术会议(TCT 2022)会议上,Ralph Stephan Von Bardeleben教授公布的EXPAND G4研究结果确认了MitralClip新一代器械MitraClip G4系统治疗MR的安全性和有效性。EXPAND G4研究与此前EXPAND研究相比,G4研究原发性MR患者占比(41.6% vs. 50.5%)、三尖瓣返流3+/4+患者占比(8.1% vs. 21.5%)、左室舒张末期容积(140.4±62.1 mL vs. 148.1±71.3 mL)更低。MitraClip G4系统的器械植入率为98.0%(1141/1164, 95%CI 97.1%-98.7%),即刻手术成功率为96.2%(1099/1143, 95%CI 94.9%-97.2%)。同时,装置植入时间(35.0 min vs. 46.0 min)和手术时间(77.0 min vs. 80.0 min)均显著低于此前EXPAND报道的研究结果[4]。术后30天随访时,患者全因死亡率为1.3%;瓣膜不良事件(单瓣叶夹持)为1.0%;另外,心肌梗死、卒中和器械相关并发症所致非选择性心血管手术的发生率分别为0.2%、0.0%和0.9%。91%患者返流程度≤1+,98%患者返流程度≤2+,相较基线时MR程度显著减轻(P < 0.0001);对于基线时严重MR患者(MR ≥ 3+),与此前EXPAND研究结果相比,术后30天MR≤1+(89% vs. 83%, P=0.02)与无/轻微MR(29% vs. 19%, P < 0.0001)患者占比显著更高;83%的患者NYHA达到 I/II级,NYHA分级及KCCQ评分均得到显著改善(P < 0.0001)。
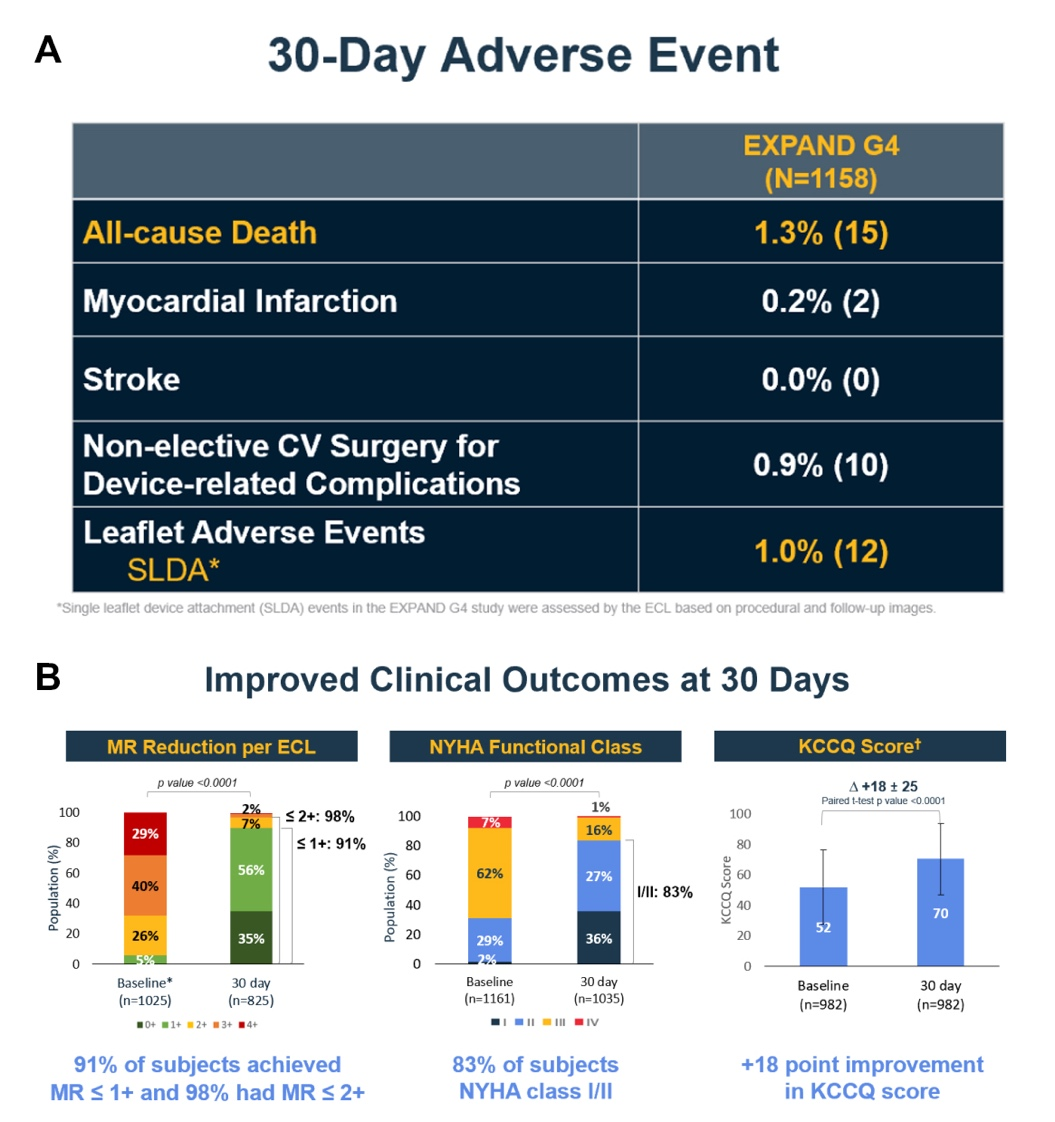
图3 EXPAND G4研究结果[4]
注:A. 术后30天时不良事件发生率。B. 基线与术后30天时临床结局的对比
2022年欧洲心血管介入治疗大会(EuroPCR 2022)上更新的Mitra Bridge 注册研究2年结果,评估了在晚期心衰合并中重度或重度MR患者中,应用MitraClip治疗桥接心脏移植治疗的安全性及有效性,表明MitraClip治疗可帮助患者顺利度过心脏移植的等待期,并改善患者移植前的整体状态。目前该研究已纳入20个中心,153例患者。研究的主要终点2年内未发生不良事件(全因死亡、紧急移植或左室辅助设备植入、心衰首次再入院)比率为47% (CI:37.5-56.5%),次要终点2年免除因心衰首次再住院比率为55% (CI:44.5-64.5%)。2年内共有48例患者出现81人次因心衰再住院。全组患者中位随访19(6-37)个月。全因死亡患者13例(9%),其中心源性死亡患者9例(6%)。共有30 (19.5%)例患者完成心脏移植,19 (12.5%)例患者仍在等待移植名单中,有32 (21%)例患者不再需要心脏移植[5]。
在一些高龄或合并肾功能不全、心原性休克的MR患者中,MitraClip也被证实有助于改善患者预后。ChrisSong等评估年龄对COAPT试验中接受TEER患者结局的影响,其结果表明MitraClip组2年内死亡或心衰再入院的发生率在<74岁(37.3% vs. 64.5%; 校正风险比[Hazard Ratio,HR]: 0.41; 95% 可信区间[Confidence Interval,CI]: 0.29-0.59)和≥74岁(51.7% vs. 69.6%;校正HR:0.58; 95% CI:0.42-0.81)的患者中均较GDMT组低,且无论在年轻和老年患者中,使用MitraClip治疗后死亡率也持续降低(Pint = 0.42)。然而,老年患者接受MitraClip治疗与单独GDMT治疗的心衰再入院率的降幅较年轻患者更小(Pint = 0.03)。年轻和老年患者接受MitraClip治疗后,生活质量的改善与GDMT单独治疗后相似[6]。Nirat Beohar等则在COAPT试验确定了伴有严重MR的心衰患者肾功能不全的影响,以及TEER对新发新发终末期肾病和肾脏替代治疗需求的影响。结果发现无论是否发生肾功能不全, MitraClip与GDMT相比均改善了患者结局(Pint = 0.62),并且减少了新发的终末期肾病(2.9 vs. 8.1%, HR 0.34, 95% CI 0.15-0.76, P = 0.008)和新发的肾脏替代治疗的需求(2.5 vs. 7.4%,HR 0.33, 95% CI 0.14-0.78, P = 0.011)[7]。Trevor Simard等探讨了接受TEER治疗的重度MR合并心原性休克患者的特征和预后,结果显示85.6%的患者器械植入成功,最终MR分级 ≤ 2+(88.2%)和MR下降 ≥1级(91.4%),在TEER后1年时,器械植入成功降低了全因死亡率(34.6% vs. 55.5%; 校正HR: 0.49; 95% CI: 0.41-0.59; P < 0.001)以及由死亡或心衰再入院院构成的复合终点事件(29.6% vs. 45.2%;校正HR:0.51;95% CI:0.42-0.62;P < 0.001)[8]。
房性继发性MR是由于房颤等原因导致左心房重构、二尖瓣瓣环扩张、房源性瓣叶牵拉等造成MR。同室性继发性MR相比,房性继发性MR具有的独特的病理生理机制,TEER用于房性继发性MR患者中的效果上不明确,今年的一些研究结果为TEER在房性继发性MR患者中的应用提供了依据。
在EuroPCR 2022会议上,意大利Antonio Popolo Rubbio教授代表The MITRA-TUNE研究组公布了一项关于MitraClip用于治疗房性二尖瓣返流患者的早期疗效分析研究,为该类患者的治疗方式提供重要依据。这是一项多中心注册研究,由意大利7家中心连续入选从2009~2021年接受TEER治疗患者1135例,其中房性继发性MR患者87例,占比7.6%。研究结果表明MVARC定义的操作成功率为97%;院内累计死亡率为2%(2例),院内急性肾损伤发生率为8%,大出血发生率为4.5%;器械成功率为83%,手术成功率为80%,30天全因死亡率为5%,心原性死亡为4%;术后即刻约70%患者MR等级降至1+级,约90%患者MR等级降至2+级及以下;随访期间,约90%患者心功能恢复至NYHA II级及以下,超声发现左房及瓣环直径出现明显重塑改变;2年随访发现患者免于全因死亡的存活率为60%,免于心原性死亡的存活率为77%,77%的患者未出现心衰再住院,55%的患者未出现全因死亡或心力衰竭再住院[9]。
Philipp Doldi等分析了房性继发性MR患者接受TEER治疗的结果。结果发现手术成功率(出院时MR ≤ 2+)为87.2% (P < 0.001)和NYHA心功能分级在随访期间显著改善(NYHA III/IV级:基线时为86.5%,随访时为36.6%;P < 0.001)。房性继发性MR患者的2年生存率为70.4%。房性继发性MR、非房性继发性MR和室性继发性MR之间的2年生存率无显著差异[10]。
Nishtha Sodhi等也评估了TEER治疗房性继发性MR的安全性、超声心动图结果和临床有效性。其纳入EXPAND中房性继发性MR患者53例,室性继发性MR患者360例。在房性继发性MR队列中,TEER显著降低了术后1年时MR的程度(100.0%的MR分级 ≤ 2级),显著提高了1年时KCCQ评分(+26.6 ± 30.5分;P < 0.0001),并且功能分级相对于基线改善,这与室性继发性MR患者的效果相似(1年时MR分级 ≤2级的比例为99.5%,KCCQ评分1年时增加21.23 ± 24.92分)。两组中30天时的主要不良事件和1年时的瓣叶不良事件均罕见[11]。
Tetsu Tanaka等也证实了TEER是房性继发性MR患者安全可行的治疗选择。其结果显示在房性继发性MR患者中TEER成功率为94.1%,94例(79.7%)房性继发性MR患者在TEER后MR降至≤1。住院死亡率为2.5%[12]。此外,在多变量logistic分析中,较大的左心房容积指数和较低的瓣叶瓣环比与房性继发性MR TEER后MR降低至≤1的发生率较低相关,使用新一代的MitraClip系统(NTR/XTR或G4系统)与MR降低至≤1的发生率较高相关[12]。
1.2 其他TEER器械安全性及有效性研究
同时,Konstantinos Spargias也在此次会议上公布了CLASP研究三年的随访结果。在3年的随访中,患者全因死亡率为22.6%,心衰再入院率为24.2%,二尖瓣返流量明显减少,93%的患者MR≤2+,70%的患者MR≤1+,左室舒张末期容积较前减少(140 vs. 181,P < 0.001),改善了左心室重构,心功能和生活质量得到明显改善,89%的患者NHYA I/II级,继发性MR和原发性MR患者也均有阳性结果[16]。
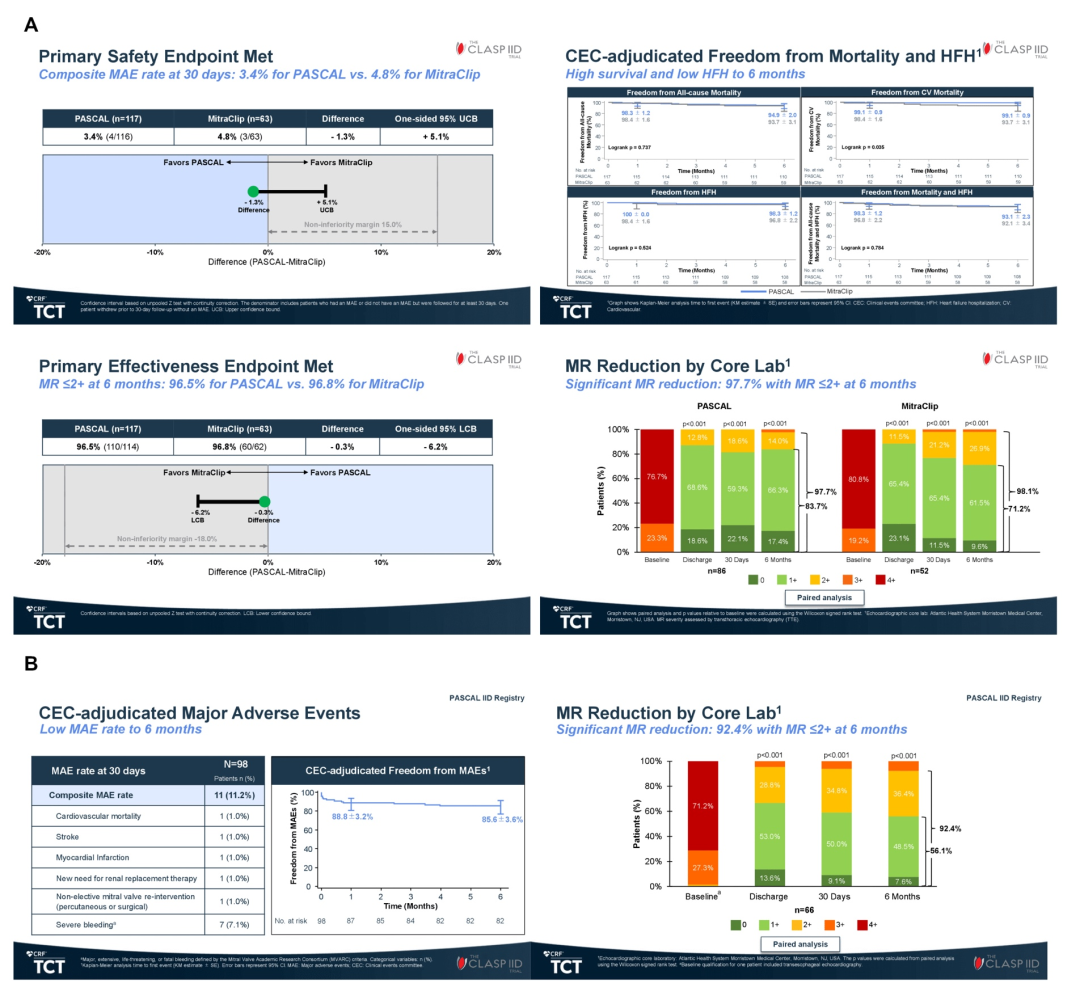
图4 PASCAL经导管二尖瓣修复系统研究相关结果[14, 17]
注:A. CLASP IID研究结果。B. PASCAL IID研究结果
尽管TEER最初是作为手术高危患者的手术替代方案,但随着大规模临床经验的积累,TEER已成为继发性MR的一线介入治疗方案,以及手术风险高的原发性MR的二线治疗方案。然而,TEER干预后仍有相当比例的患者出现临床事件。因此,对这一人群进行更好的特征确定和分层可能有助于区分可能获得临床获益的患者和可能无效的患者。
来自手术患者的预测围手术期死亡率的评分(如EuroSCORE II和STS评分)在TEER人群中分层能力尚不令人满意。为了更高的筛选出可能因为TEER手术获益的患者,Sergio Raposeiras-Roubin等建立并验证一个用户友好的评分(MitraScore),以预测接受TEER患者的死亡风险。MitraScore包含了8个在随访期间死亡的独立预测因素:年龄≥75岁、贫血、肾小球滤过率<60 mL/min/1.73m2,左心室射血分数<40%,外周动脉疾病,慢性阻塞性肺疾病,高利尿剂量,以及未使用肾素-血管紧张素系统抑制剂治疗,每个独立预测因子记1分(c统计量 0.70)。MitraScore评分每增加1分,死亡的相对风险增加55%(HR:1.55;95%CI:1.44-1.67;P < 0.001)。死亡率预测的区分度和校准度均优于EuroSCORE II(c统计量0.61)或STS评分(c统计量0.57)[18]。MitraScore在验证队列中也保持了足够的性能(c统计量 0.66)。该评分还可预测心力衰竭再住院,并与临床改善的概率相关。
2. 经导管二尖瓣环缩术、腱索修复术
外科经皮导管二尖瓣瓣环缩减术可分为直接环缩和间接环缩两大类。
直接环缩常见手段是通过导管在瓣环处放置可调节人工瓣环带使其瓣环直径缩小达到治疗目的,DragonRing是中国首款模拟心脏外科房室瓣瓣环环缩技术,完全自主研发的经股静脉介入瓣环成形系统,可用于因瓣环扩张导致瓣叶对合高度缺失的继发性二、三尖瓣反流患者。2022年10月28日,四川大学华西医院心脏内科陈茂教授带领的多学科心脏团队成功应用经股静脉DragonRing系统完成全球首例人体植入手术。术后即刻二尖瓣反流程度下降到1+,左房肺静脉逆流消失,二尖瓣平均跨瓣压为2mmHg,二尖瓣口面积未见明显狭窄,冠脉血流通畅,术后4天,患者复查经胸超声心动图检查及CT检查,超声测得环缩后二尖瓣反流程度降至1+,对合缘高度由术前1.6mm增加至术后3.8mm,瓣叶瓣环比由术前1.1增加至1.6,提高45%,二尖瓣瓣口面积2.8cm2。CT成像测得二尖瓣瓣环面积下降近22%,瓣环前后径由术前29.3mm下降至24.5mm,减小16%,缩环效果显著。三尖瓣反流由术前2+降低至1+,PASP较术前无明显改变。
然而前三个技术主要依靠既往人工生物瓣的瓣环、成形环或者钙化的自身二尖瓣环作为固定支撑,人群中所占比例较小,不能代表真正意义上MR的患者。自体瓣中瓣作为真正意义上的TMVR技术,近年来克服诸多技术和理念问题,涌现出众多器械并取到了长足的进展(图5)。

图5 经导管二尖瓣置换器械[20]
MITRAL试验是第一项使用球囊扩张主动脉经导管心脏瓣膜对ViMAC、MViR和 MViV进行的前瞻性研究。Mackram F. Eleid等在JACC上发表了其2年随访的结果。共纳入91例患者(ViMAC组31例,MViR组30例,MViV组30例),2年全因死亡率分别为为39.3%、50%和6.7%,NYHA Ⅰ/Ⅱ级患者分别为66.7%、65%和85%,二尖瓣平均跨瓣压差分别为5.6±2.0mmHg、6.5±2.7mmHg和6.9±2.4mmHg,2年时患者二尖瓣关闭不全程度均≤轻度[21]。结果表明,在经过选择的重度MAC、瓣环成形术失败和生物假体MV功能障碍患者中,使用球囊扩张主动脉经导管心脏瓣膜与2年随访时症状、生活质量改善和人工瓣膜稳定相关。MViV患者效果最佳,显著优于ViMAC和MViR组。
CHOICE-MI登记系统包括迄今接受TMVR治疗的患者数量最多的患者,证实了使用包含10个专用器械在内的TMVR手术可在1年时实现可预测的MR减轻和持续的功能改善。其结果表明,在 229例(30.7%)使用10种不同的专用设备进行了TMVR的患者中,1年时95.2%的患者有残余MR≤1+,39.2%接受TMVR治疗的患者发生了全因死亡或心衰再住院。在因左室流出道梗阻、瓣环尺寸、小左室、二尖瓣环钙化等原因不符合TMVR条件的患者(517例,69.3%)中,挽救性TEER(216例,29.0%)、高危手术(62例,8.3%)和药物治疗(240例,32.2%)后残留MR≤1+的比例分别为37.2%、100.0%和2.4%,1年时的主要终点发生率分别为28.8%、42.9%和47.9%[22]。
在TCT 2022大会上,来自俄勒冈健康与科学大学的Firas Zahr教授汇报了经股入路Intrepid EFS研究及经心尖入路Intrepid Pilot研究的中期结果,为TMVR手术的安全性和有效性再次带来了一份有强有力的循证医学证据。
Intrepid EFS研究纳入了30例中重度MR患者,其中原发性MR占比60%,继发性MR占比约40%,中位年龄80岁,67%为男性,中位STS 4.7%,中位手术时间42.5分钟,30例患者中1例患者由于释放后的瓣膜移位中转开胸,29例患者手术成功。根据30名患者30天级15名患者1年随访结果显示,中位随访时间为7.2月,30天和1年时均无患者出现死亡或卒中及短暂性脑缺血发作,主要血管并发症率为27%。心衰的发生率在30天和1年时分别为0%和9%。MR较基线显著改善,1年随访时91%的患者无或者仅有微量MR,9%的患者有轻度MR,全部无或者仅有微量瓣周反流,二尖瓣跨瓣压差呈现下降趋势,中位由30天的5. 0mmHg下降至1年的4.3 mmHg。NYHA分级和生活质量持续改善,1年时全部患者NYHA分级I-II级[23]。
Intrepid Pilot研究也更新了其研究中期超声心动图的结果。在分析的42例患者中,原发性MR占26.2%、继发性MR占66.7%和混合性占7.1%,中位年龄74.5岁,男性占59.5%,中位STS 4.8%。随访1月和3年时,所有患者均未出现中度及以上的瓣口反流,1月时,所有患者均未出现中度及以上的瓣周反流,3年时,仅有1例(2.4%)患者出现了中度瓣周反流,余下患者瓣周反流均在微量及以下。左心室舒张末容积由术前188(140-245)ml显著减少至术后1月的170.5(131-210)ml,3年随访时进一步减少至147.5(117-202)ml,左心室收缩期末容积也可见同样的减少趋势,但无统计学差异(术前 107[72-151];术后30天 97[69-155];随访3年 84[62, 140],P = 0.231)[24]。
同时,国内沛嘉HighLife经导管二尖瓣置换(经房间隔二尖瓣置换,TSMVR)系统的多中心注册临床试验已正式启动,将进一步评估该系统治疗中度至重度或重度二尖瓣返流患者的安全性及有效性。
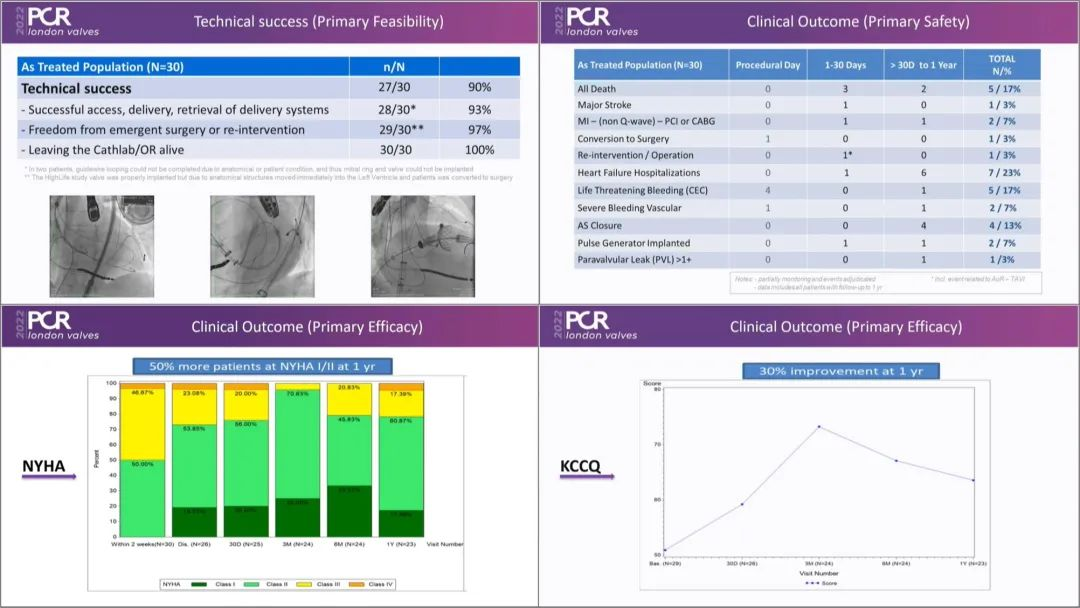
图6 HighLife TSMVR 欧洲/澳洲的可行性试验1年随访结果[25]
Mirjam G. Wild等评估真实世界患者队列中使用Tendyne经心尖二尖瓣系统进行TMVI的手术和30天预后。其回顾性纳入108例手术高危患者。结果显示手术成功率为96%,所有植入成功的患者MR均≤1+,30天全因死亡率为12%。在早期临床随访中,MR降低持续,肺动脉压力显著降低(52 mmHg vs. 42 mmHg, P < 0.001),三尖瓣反流严重程度显著降低(P = 0.013),心力衰竭症状显著改善(NYHA I/II级 73%,P < 0.001)[26]。在PCR London Valves 2022上,Alison Duncan报道了纳入了191例中重度MR患者的Tendyne Expanded临床研究,以评估TMVI术后1年时患者的临床结局。结果发现,1年随访时,患者全因死亡率30.8%,其中器械相关死亡率15.7%,心衰再入院率为53.4%。二尖瓣返流量较术前明显减少,1年随访时无中度或以上的残余返流的情况,症状和生活质量显著改善,NHYA I/II比例(85.9% vs. 29.8%, P < 0.0001)、6分钟步行实验(304.5 vs. 254.8, P < 0.01)、KCCQ评分(70.4 vs. 48.5, P < 0.0001)均较基线时明显改善[27]。
在TMVR适应症方面,华西医院陈茂教授团队成功为一名80岁高龄女性、急性心力衰竭、风湿性心脏病二尖瓣重度狭窄(有效瓣口面积0.5mm2)的患者实施TMVR[28],在国际上首次证明了在二尖瓣瓣叶严重钙化的风湿性二尖瓣狭窄患者中通过球囊扩张式介入瓣膜进行TMVR(Valve-in-MVC)的可行性,为此类患者来了一种新的治疗选择,为TMVR在风湿性二尖瓣狭窄中的应用提供了思路。

国际首例!华西陈茂团队《European Heart Journal》报道经导管二尖瓣植入治疗瓣叶严重钙化的风湿性二尖瓣狭窄
MR是人群中发病率最高的心脏瓣膜病,并且其发病率随着年龄的增加而不断增高,随着介入治疗技术的不断进展,MR介入治疗被认为是继经导管主动脉瓣置换术后心脏介入治疗的一大发展方向,经导管介入治疗的方式也给外科手术高危的患者提供了手术治疗的机会。
近年来,国内二尖瓣介入治疗器械迅猛的发展,Dragonfly、Valveclip-M、JensClip、NovaClasp、Neonova、SQ-Kyrin、ValveClamp、ValveClasp、LifeClip、kokaclip、MemoClip-A等TMVr器械以及Highlife、MitraFix、Mithos等TMVR器械相关的临床试验也在如火如荼的展开。虽然目前仍然缺乏大型的临床研究证实多种治疗策略或器械的长期安全性和有效性,但是相信随着不同中心手术经验的积累,器械的改进,二尖瓣介入治疗领域很快会迎来一个百家争鸣的时代。
然而二尖瓣介入治疗同时也存在诸多挑战。MR是一种高度异质性的疾病,在现实世界的患者中存在不可预见的解剖变异,TEER和TMVR都不能解决所有的解剖变异。与目前的TMVR技术相比,TEER可能适合更多的MR患者,但TEER后双孔化后残留返流、远期MR复发风险较高、后期再次干预的空间有限等问题尚未解决。TMVR虽可以几乎完全减轻MR的程度、提供更大的反向重构、持久消除MR、后期瓣膜衰败可再次植入瓣膜进行干预,但也面临目前的技术仅适用于少数MR患者,现实临床工作中筛败率高、医源性房间隔缺损较大以及瓣膜血栓形成的风险较高等短板。二尖瓣介入治疗器械仍需进一步探索。
此外,由于继发性MR病因复杂,多种因素可能影响MR程度,心脏团队应为患者制定个体化治疗方案,综合考虑药物、心脏再同步化治疗、射频消融、手术治疗等多种治疗方式。其中药物治疗应当得到充分的重视,PROVE-HF研究显示经沙库巴曲缬沙坦治疗后MR程度明显改善,第6个月3+和4+级的患者比例由14.9%降至8.2%(相对降低45%)[29]。因此,在确定对继发性MR患者进行二尖瓣介入治疗前,应确保进行最佳GDMT治疗。遗憾的是,我们目前尚不清楚哪些患者可以通过GDMT治疗使MR程度得到改善,二尖瓣介入治疗前的观察时长尚不明确,这些影响到现实中二尖瓣介入治疗时机的问题仍需得到解决。
作者简介
陈茂
四川大学华西医院
四川大学华西医院心内科主任,教授、博士研究生导师,国家“万人计划”科技创新领军人才、四川省卫生健康首席专家、四川省卫生计生领军人才、四川省卫生厅学术技术带头人、四川省卫生厅“有突出贡献中青年专家”以及首届“国之名医”荣誉称号获得者。FCSC,FACC,FESC,中华医学会心血管病分会常委,中国医师协会心血管内科医师分会常委,中华医学会心血管病分会结构心脏病学组组长,中国医疗保健国际交流促进会心血管健康医学分会副主任委员,四川省国际医学促进会副会长,四川省医学会心血管病专委会前任及候任主任委员,长城国际心脏病学组委员会县域心血管医师联盟副理事长。PCR—CIT China Chengdu Valves会议、中国中西部心血管病会议执行主席,London Valves会议、Tokyo Valves会议联合国际主席,ESC、PCR、TCT、CSI等会议的专家会员。
研究方向:经导管心脏瓣膜病介入治疗相关基础、应用基础及临床研究。
研究成果发表在European Heart Journal、Nature Review of Cardiology、Radiology、JACC: Cardiovascular Interventions等国际高水平学术期刊上,现以第一作者或通讯作者发表SCI论文148篇。主持国家十三五、十二五、国家自然科学基金等国家级、省部级科研项目多项。获四川省科技进步一等奖、中华医学科技二等奖、四川省医学科技一等奖、四川省科学技术进步二等奖等奖项。主刀完成我国西部地区第一例经导管主动脉瓣置换术(TAVR),TAVR完成例数居全国领先水平。在全国率先开展经导管二尖瓣、三尖瓣及肺动脉瓣介入治疗,完成例数居全国前列。
冯沅
四川大学华西医院
主任医师,研究生导师,华西医院先心病亚专业组长,一级专家,中华医学会心血管病分会结构性心脏病学组委员,中国医师协会结构性心脏病学组委员,中华医学会儿科学心血管学组新生儿心脏协作组副组长,中华医学会心血管病分会第10届委员会肺血管病学组委员,四川省心脏瓣膜联盟副主任委员,亚洲心脏瓣膜病学会中国分会心脏瓣膜病介入治疗技术学术委员会常委。临床经验丰富,诊疗技术水平突出,擅长结构性心脏病(先心病、瓣膜病、肺血管病、肺动脉高压)介入诊疗。领先开展多项新技术和挑战、危重症介入手术,高质量完成从新生儿到超高龄患者的各种心脏、肺血管介入手术6000台。发表SCI文章50篇(IF290+),受邀在国内外数十家著名心脏中心指导开展结构性心脏病介入手术。获得2019年四川省科技进步一等奖。
白琳
四川大学华西医院
住院医师,医学硕士,博士研究生在读,主要从事经导管心脏瓣膜病介入治疗临床研究。目前以第一作者身份发表 SCI 论文4篇,其中 1 篇发表于JACC: Cardiovascular Interventions。参与四川省科学技术厅重点研发课题2项、四川省干部保健科研重点研发课题、成都市科技项目重点研发支撑计划、四川大学华西医院临床研究孵化项目各 1 项,参与多项药物、医疗器械临床试验研究。


