袁晓航 高磊
解放军总医院心血管病医学部

研究背景:
目前,临床上对于降脂治疗多采用他汀类药物,且剂量上多采用中等强度他汀剂量(每日剂量降低LDL-C 30%-50%),如果治疗3-4周后血脂仍然不达标,即可加用前蛋白转化酶枯草溶菌素9(PCSK-9)抑制剂。但有研究表明,加用PCSK-9抑制剂会导致低密度脂蛋白-C水平显著降低,缺血性心血管事件逐渐减少。他汀类药物可以阻止冠状动脉粥样硬化的进展,但在他汀类药物治疗的基础上加用PCSK-9抑制剂阿利西尤单抗(alirocumab)对斑块负荷和组成的影响目前不清楚。
研究目的:
在急性心肌梗死患者中,使用多模态冠状动脉内成像来确定PCSK-9抑制剂alirocumab对冠状动脉粥样硬化的影响。
研究设计:
该试验为多中心、随机、双盲的临床试验,在9家欧洲医院招募了300名接受急性心肌梗死经皮冠状动脉介入治疗的患者。在对罪犯病变进行紧急经皮冠状动脉介入治疗后不到24小时起,患者随机接受两周一次的皮下阿利西尤单抗(150 mg;n=148)或安慰剂(n=152)治疗,并且两组患者的治疗均在高强度他汀类药物(瑞舒伐他汀,20 mg)的基础上持续52周。
在基线及52周时,使用NIRS-IVUS联合导管和OCT对至少2个近端在非梗死相关动脉中(non-IRAs)进行冠状动脉成像。对于IVUS,在匹配的感兴趣区(ROI)每隔1 mm分析管腔和外弹力膜。对于NIR,分析与IVUS相同的ROI,并在ROI内确定了具有最大脂质核心负荷指数的4 mm节段。在匹配的ROI内每隔0.4 mm分析OCT记录,并测量纤维帽厚度。
IVUS测量的主要疗效参数是动脉粥样硬化体积百分比(PAV),次要疗效参数是标准的动脉粥样硬化总体积。NIRS的主要疗效参数是具有最大脂质核心负荷指数(LCBI)的4 mm以内最大脂核心负荷指数,次要参数是整个ROI成像内的总LCBI。OCT的主要疗效评价指标为最小纤维帽厚度(FCT),次要疗效评价指标包括平均FCT和巨噬细胞平均角度。
本文主要终点是IVUS的PAV从基线到52周的变化,两个次要终点是在最大脂质核心负荷指数的4 mm内从基线到52周NIRS测量的最大脂核心负荷指数的变化和通过OCT测量的最小FCT的变化。另外,次要非成像相关终点包括已判定的事件(全因死亡率、心源性死亡、心肌梗死、缺血导致的冠状动脉血运重建、中风或短暂性脑缺血发作)和不良事件的发生率以及生物标志物(总胆固醇、低密度脂蛋白胆固醇、高密度脂蛋白胆固醇、甘油三酯、脂蛋白(A)、载脂蛋白A和载脂蛋白B1及高敏C反应蛋白)。
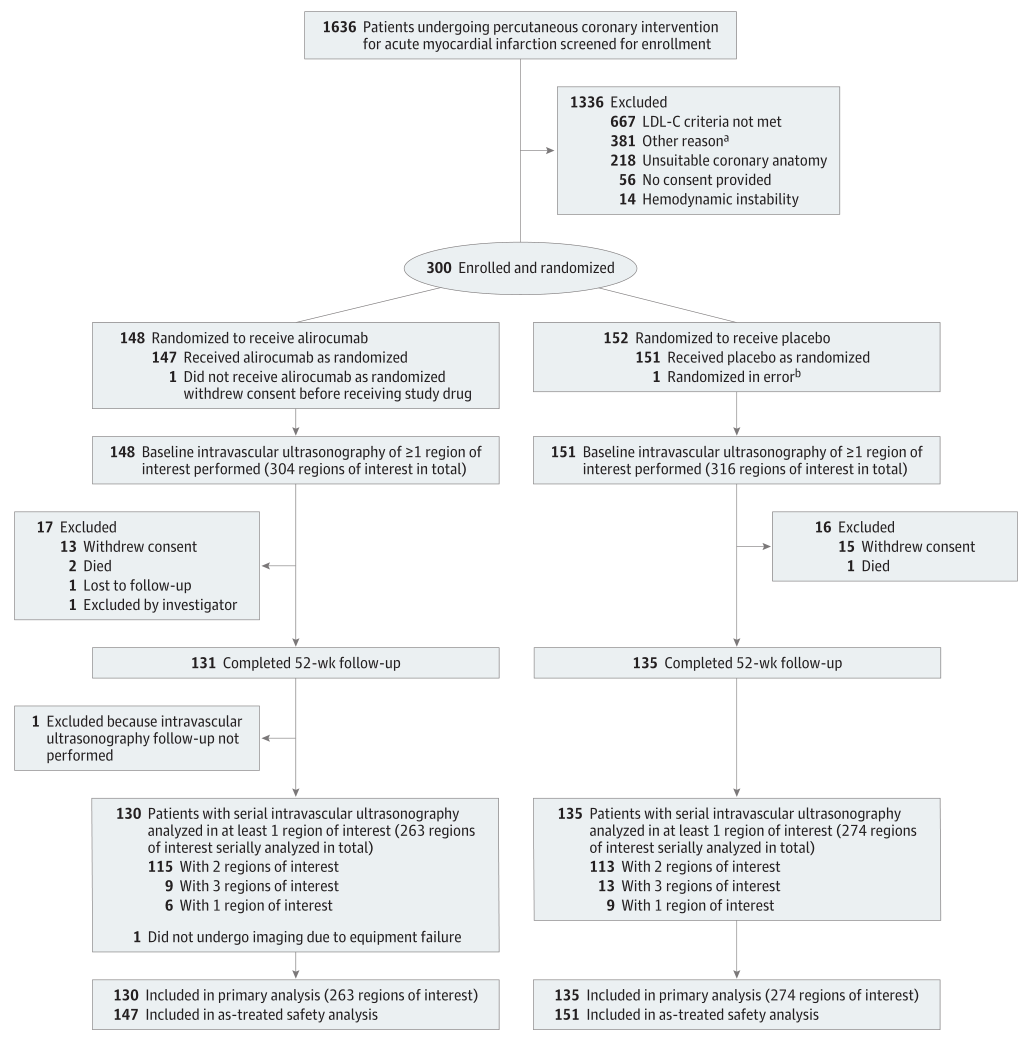
图1 研究流程
主要研究结果:
与安慰剂组相比,PCSK-9抑制剂Alirocumab组的主要疗效终点(平均PAV)的变化显著低[(OR=−2.13, 95%CI:−2.53~ −1.73)vs (OR=−0.92, 95%CI:−1.28~ −0.56);组间差异, (OR=−1.21, 95%CI:−1.78~ −0.65), P<.001]。
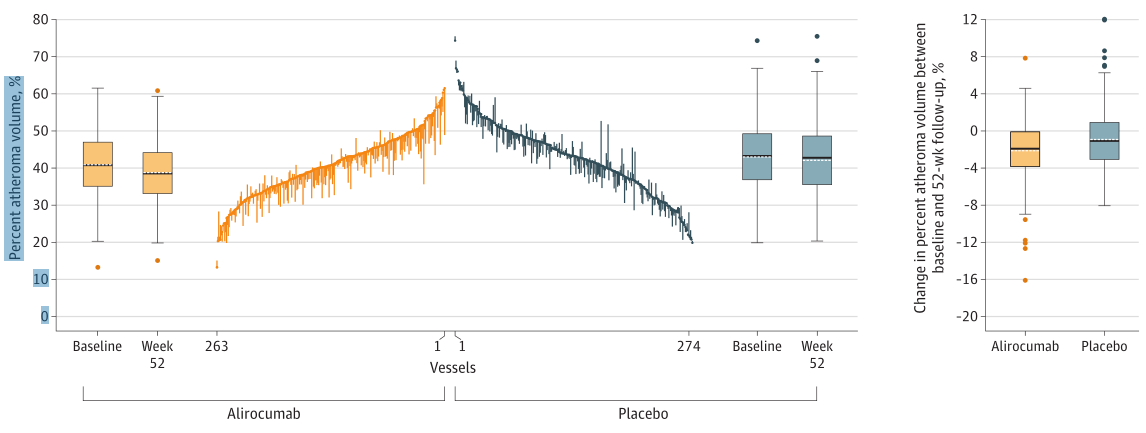
图2 两组患者IVUS检查动脉粥样硬化体积百分比的变化
次要研究结果:
1、IVUS结果:
与安慰剂组相比,PCSK9抑制剂alirocumab组的平均标准动脉粥样硬化总体积的减少明显更大[(OR=−26.12, 95%CI:−30.07~ −22.17)vs (OR=−14.97, 95%CI:−18.14~ −11.80)], P<.001]。
2、NIRS结果:
在确定的4mm阶段内,PCSK9抑制剂alirocumab组与安慰剂组相比,最大脂质核心负荷指数变化显著降低[(−79.42vs−37.60);组间差异, OR=−41.24, 95%CI:−70.71~ −11.77, P=.006]。与安慰剂组相比,服用阿利洛复的患者的平均总LCBI下降幅度明显更大[(−29.30vs−12.38);组间差异, OR=−17.29, 95%CI:−28.98~ −5.60, P=0.004]。
3、OCT结果:
与安慰剂组(OR=33.19, 95%CI:22.22~ 44.16)相比,PCSK9抑制剂alirocumab组OCT终点(平均最小FCT的变化)显著增加(OR=62.67, 95%CI:48.84~ 76.50;组间差异,OR=29.65, 95%CI:11.75~ 47.55, P=0.001)。与安慰剂组相比,PCSK9抑制剂alirocumab组患者的平均FCT显著增加(组间差异,OR=28.22, 95%CI:3.21~ 53.23, P=0.03),巨噬细胞的平均角度显著减少(组间差异,OR=−10.08, 95%CI:−14.72~ −5.43, P<0.001)。
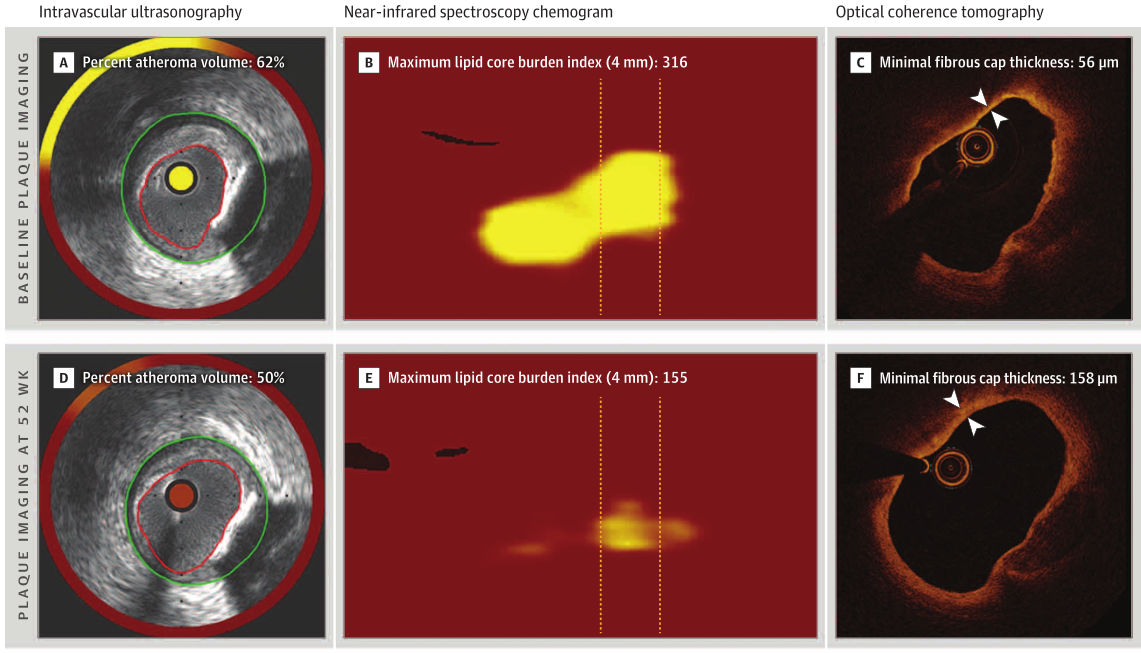
图3 一例典型病例的多模态血管腔内成像(IVUS、NIRS及OCT)
4、临床结局:
PCSK9抑制剂alirocumab组与安慰剂组相比:全因死亡2例(1.4%)vs1例(0.7%),心源性死亡2例(1.4%)vs0例,心肌梗死2例(1.4%)vs3例(2.0%),缺血驱动的冠状动脉血运重建12例(8.2%)vs28例(18.5%)。
研究结论:
在AMI患者中,在高强度他汀类药物治疗的基础上,与安慰剂相比,双周皮下注射PCSK9抑制剂alirocumab可显著促进52周后非梗塞相关动脉的冠状动脉斑块消退。
研究局限性:
第一,安慰剂组的基线PAV在数值上更高。然而,基于先前报道的基线PAV与终点PAV之间的正相关关系,这种不相匹配的情况有可能导致数据对比后,得到的结果低估PCSK-9抑制剂alirocumab对终点PAV的影响。
第二,尽管患者留置率(88%)优于之前已有的IVUS研究,但未完成试验的患者冠状动脉粥样硬化的变化可能与完成试验的患者有所不同,可能使实验结果代表性降低。
第三,与之前的IVUS系列研究相比,本研究中的患者数量不多,但通过研究每个患者的两条动脉,功效增加了,主要和次要终点的功率都达到了统计学意义。
专家点评:
高磊
PACMAN-AMI研究与先前的GLAGOV研究类似,均聚焦于他汀类药物联合PCSK9抑制剂治疗对AMI的影响。2018年在新英格兰杂志发表的ODYSSEY OUTCOMES研究也证明,在AMI并服用高强度他汀类药物治疗的患者中,接受alirocumab治疗的患者复发缺血性心血管事件的风险低于接受安慰剂治疗的患者。与先前研究结果相一致,在本项试验中,AMI患者经高强度他汀类药物治疗中加入PCSK9抑制剂alirocumab治疗后,对冠状动脉粥样硬化产生了良好的效果,并结合新颖的多模态血管内成像系统(3种冠状动脉内成像方式)对目标血管进行血管成像的动态评估,为PCSK9抑制剂的研究提供了在体动态变化的结果参考。结果提示,与单独强化他汀类药物治疗相比,在AMI急性期早期开始抑制PCSK9对冠状动脉斑块的演变、成分和表型产生了越来越大的益处,且目前研究显示,这类药物的安全性和耐受性良好,最常报告的不良反应是局部注射部位反应,通常较轻微。这就提示了PCSK9抑制剂这类药物的巨大临床潜力。PACMAN-AMI研究为今后AMI患者的用药提供指导性新策略,甚至可能会改善AMI患者的远期预后情况。
专家简介
高磊
中国人民解放军总医院
医学博士,副主任医师,副教授,硕士研究生导师,解放军总医院心血管病医学部重症医学科副主任,美国哈佛大学医学院高级访问学者。
专业特长与方向是腔内影像技术指导复杂冠心病介入治疗,尤其是光学相干断层扫描OCT指导急性冠脉综合征、支架内再狭窄病变等介入治疗。
在冠心病介入治疗、心血管危重症急救、高血压、心力衰竭药物治疗等方面积累了丰富的临床经验。个人完成冠心病介入诊疗手术5000余台,成功救治心血管危重患者1000余例。第一完成人承担国家自然科学基金2项,省部级课题1项,医院科技扶持基金2项。获得中国产学研合作创新成果一等奖1项,解放军总医院科技进步一等奖1项,二等奖2项。2014至2015年公派出国赴美国哈佛大学附属麻省总医院从事冠心病临床研究工作。
以第一作者或通讯作者共发表SCI论文15篇,累计影响因子46.6,单篇最高影响因子9.5。主编科普专著《漫谈心肌梗死》1部,副主专著1部,参编专著3部。获得实用新型专利2项。
目前担任中华医学会心血管病分会危重症学组委员,中国医疗保健国际交流促进会胸痛分会委员、《中华老年多器官疾病杂志》编委等职。
声明:
严道医声网致力于传播权威、前沿的学术信息,及时将领域时事、前沿学术内容传递至国内,各项内容资料版权均归ACC.22所有,如有涉及版权等问题,请第一时间与我们联系。


