健心知著
2022.11.25
第220期

球囊无法通过病变的解剖学及形态学特征

刘健、霍黎明、郭萌
北京大学人民医院
健心荐语
近年来,虽然经导管冠脉介入诊疗技术不断发展,但是仍然有一些病变球囊无法顺利通过。既往研究推测严重钙化是导致球囊无法通过的主要原因,但是并非所有无法通过的病变都是严重钙化,非重度钙化为何球囊仍无法顺利通过机制不明。本文旨在运用血管内超声来解释球囊无法通过的病变的解剖学及形态学特征。
文章介绍
本研究是一项单中心、回顾性、观察性研究,将二维造影图像结合血管内超声影像结合以阐明球囊无法通过的病变的特征。本文于2022年4月发表于Catheterization and Cardiovascular Interventions杂志。
研究方法
本研究将冠脉钙化分为中度、重度及钙化突起,将冠脉成角分为中度及重度,将距主动脉开口<3mm病变定义为主动脉开口病变。IVUS下浅表钙化弧度≥270°定义为重度钙化病变。研究者根据球囊是否能顺利通过及IVUS下钙化病变严重程度将病变分为三组:
第1组:球囊无法通过且最大钙化弧度<270°的病变;
第2组:球囊无法通过且最大钙化弧度≥270°的病变;
第3组:球囊可顺利通过且最大钙化弧度≥270°的病变。
本研究对比第1组和第2组,以评估球囊无法通过的病变中存在和不存在重度钙化的病变的差异;比较第2组和第3组,以评估重度钙化病变中球囊可顺利通过的病变有何特征,运用多因素logistic回归模型评价球囊无法顺利通过的病变与形态特征的关系,认为p值< 0.05有统计学意义。
研究结果
本研究共纳入288例患者的290个病变,其中87%(n=252/290)球囊不可通过,16%(n=41/252)没有严重钙化(IVUS最大浅表钙化弧≥270°)。与第3组相比,第2组更常出现血管迂曲(71% vs 21%,p< 0.001)和更长的连续的重度钙化(3.8 mm vs 1.9 mm,p= 0.001)(见表1及表2)。经多因素分析,除了严重钙化(尤其是长段连续钙化)或血管迂曲外,与球囊能否通过相关的解剖因素还有主动脉开口病变和PCI前参考血管直径(见表3)。
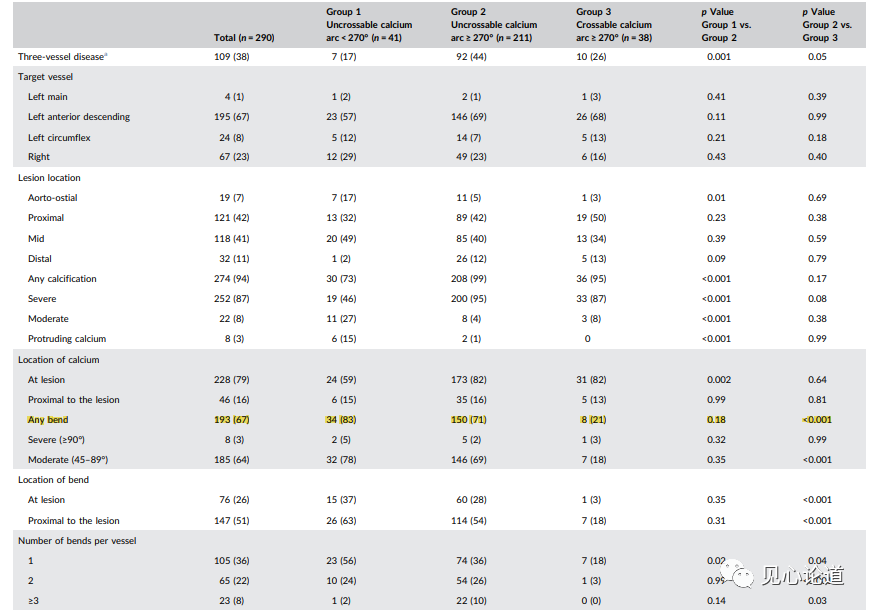
表1:与第2组相比,第1组的重度钙化明显较少。在第3组中,只有21%的可通过钙化病变发现血管迂曲。
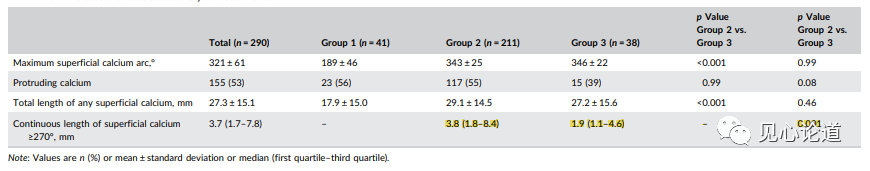
表2:与第1组相比,第2组和第3组的浅表钙化更长。与第3组相比,第2组的连续的重度浅表钙化病变也更长。
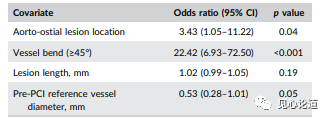
表3:主动脉口病变位置和显著的血管迂曲与不可通过有关,而较大的PCI前参考血管直径与可通过有关。
结 论
球囊无法通过的病变并不总是严重钙化,也与靶血管形态学特征(血管迂曲和主动脉开口病变)有关。相反,严重钙化的病变在血管没有迂曲成角且钙化病变相对局限时球囊也是可以顺利通过的。
点评
虽然该研究存在排除了CTO病变、未使用三维定量血管分析和更高分辨率的IVUS设备等局限性。但是,通过结合冠脉造影及血管内超声影像总结出在严重钙化外,血管迂曲、病变位置及参考直径同样与球囊能否顺利通过有关,有助于介入医生根据病变情况选择相应预处理措施,提高手术成功率。
