2002年法国医生Cribier教授首次报道TAVR以来[1],其安全性、有效性不断得到验证,目前已经成为症状明显的主动脉瓣狭窄患者的标准治疗方案,而常规的外科手术对于一部分患者风险很大或者有明确的禁忌症[2,3]。随着外科技术的不断发展,TAVR的适应症已经延伸到单纯性主动脉瓣重度反流、衰败生物瓣以及主动脉瓣二叶畸形等瓣膜病变[4]。2014年,华西医院郭应强教授等[5]首次报道了1例采用新一代经导管瓣膜器械 J-Valve系统治疗重度主动脉瓣反流患者,术后效果良好。
主动脉角度对TAVR的成败也至关重要。根据之前的研究结果,水平主动脉解剖会给自膨瓣膜的同轴性植入中造成很大困难,如:DSA透视时间延长、瓣膜移位、主动脉损伤、同期二次瓣膜植入、左室穿孔[5]和后扩张,以及术后瓣周漏[7]等。因此,极度横位心患者(主动脉角度大于70°)常被排除在TAVR治疗的适应症之外[8,9],这种复杂解剖下的TAVR数据也仅限于散发病例的报道。
在2021年9月16日中国心脏大会(CHC)手术直播中,在全国结构性心脏病专家的共同见证下,来自四川大学华西医院心外科的郭应强教授团队成功挑战高难度“极度横位心”、单纯主动脉瓣重度关闭不全病例,同时也再次展现了J-Valve出众的性能。
病例介绍
治疗方案:经心尖TAVR
术前CT评估
1.患者主动脉瓣三叶式,瓣叶基本等大,瓣膜增厚,瓣叶未见明显钙化。
2.患者主动脉瓣环周长折算直径约25.6mm。
3.患者双侧冠脉开口高度可LCA:17.2mm,RCA:24.6mm。
4.患者术中造影角度LAO:5°,CAU:3°。
5.主动脉根部增宽。
瓣环直径:25.6mm
窦部瘤样扩张:52.3mm(右窦)
升主动脉直径:42.4mm
窦管交界直径:46.6mm
左冠脉开口高度:17.2mm
右冠脉开口高度:24.6mm
最佳投照角度:LAO:5°,CAU:3°
瓣环、瓣叶无钙化
主动脉根部角度:80°
升主动脉与主动脉窦部夹角:106°
手术过程
经右侧股静脉置入临时起搏器,经右侧股动脉在患者主动脉无冠窦内放置1根6F猪尾导管协助定位。透视下定位后第五肋间小切口进胸,打开心包,选择心尖裸区缝制六边形荷包。心尖穿刺后将泥鳅导丝过主动脉瓣经升主动脉、主动脉弓到达降主动脉膈肌水平(图1),通过TEE确认细导丝没有与二尖瓣腱索缠绕。单弯管交换硬导丝后(图2、图3),用16F扩张鞘预扩心尖穿刺处,后将 J-Valve瓣膜(29mm)装入输送器。将输送器推送至主动脉根部,释放定位件,适当调整定位件角度使其进入三个主动脉窦部,并通过DSA和TEE确定三个定位件准确入窦后完全释放瓣膜,撤出输送器(图4)。通过DSA和TEE观察人工瓣膜膨胀后金属支架的形态、位置良好,无瓣周漏,收缩期左室侧反流消失(图5、图6)。撤出导丝,收紧心尖处荷包线并打结,后鱼精蛋白中和肝素,彻底止血,逐层关胸,封皮,拔出股动脉鞘并在股动脉穿刺处压迫止血。手术过程顺利,患者生命体征平稳。
术中TEE和DSA影像评估
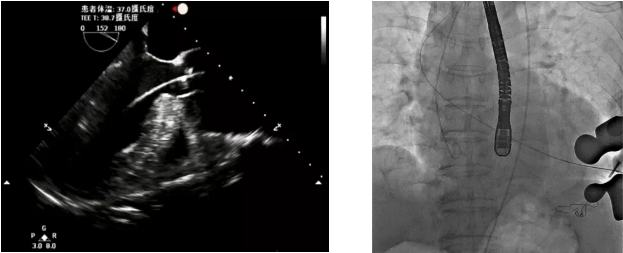
图1 超滑导丝进入左室、升主动脉内
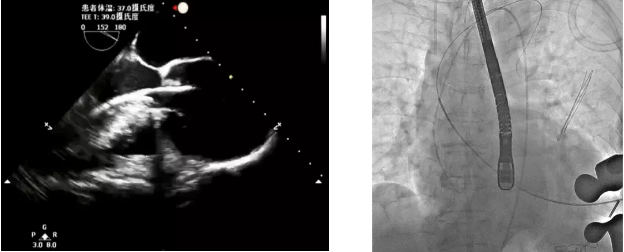
图2 单弯管进入左室、升主动脉内
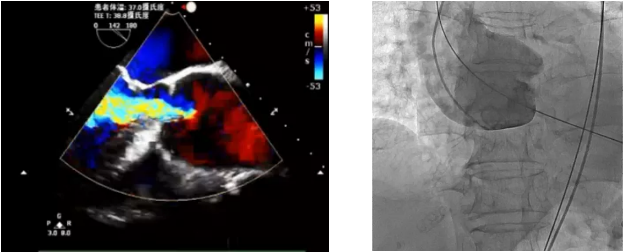
图3 主动脉瓣大量反流;主动脉瓣环平面几乎与脊柱平行
图4 释放定位件-定位件入窦-释放瓣膜-撤出输送器和单弯管
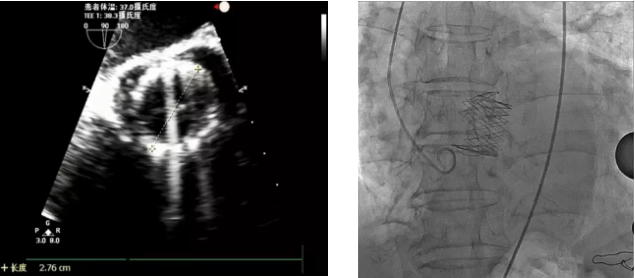
图5人工瓣释放后外径约28mm,形态、位置良好
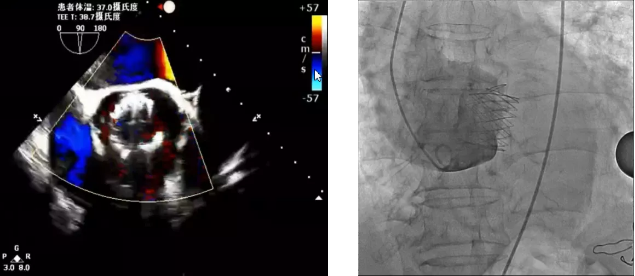
图6 TEE和DSA:人工瓣无瓣周漏
讨论
术后DSA显示,与大弯侧相比,主动脉弓小弯侧人工瓣位置较深,这与极度“横位心”,即主动脉角度过大导致的人工瓣膜同轴性不佳有关,尽管术者已经尽可能在释放瓣膜前将其同轴性调到最佳状态。但术后TEE提示人工瓣短轴形态良好,成 “正圆形”强回声,膨胀后最大外径约28mm,表明瓣环周围组织对人工瓣有足够的径向支撑力,瓣膜稳定,证明术前选择29mm人工瓣是正确的。这要求术者对TEE影像具有极致的解读能力和判断力。
小结
对于高龄、高危的单纯性主动脉瓣反流同时合并极度“横位心”的患者,经心尖TAVR是很好的治疗手段。郭应强教授带领其团队在大会现场手术直播的情况下,从容不迫的完成了这台极具挑战性的手术,体现了郭教授本人及其团队的综合实力,也为今后这类“同轴性不佳、窦部显著扩张”的病例积累了宝贵的经验。
参考文献:
[15] Kaneko U, Hachinohe D, Kobayashi K, et al. Evolut Self-Expanding Transcatheter Aortic Valve Replacement in Patients with Extremely Horizontal Aorta (Aortic Root Angle ≥ 70°). Int Heart J. 2020. 61(5): 1059-1069.
专家简介
心外科主任医师,教授,博士生导师。成人心脏大血管外科及微创手术治疗,尤其在主动脉夹层,微创高危瓣膜病和冠心病外科和微创介入治疗方面,具有丰富经验。
美国胸外科学会(AATS)会员;美国胸外科医师协会(STS)会员;国际微创心胸外科学会(ISMICS)会员;国家心血管病专家委员会微创心血管外科专业委员会副主任委员;四川省学术和技术带头人;四川省卫生健康委学术技术带头人;四川省医学会胸心外科专委会常委;《中国胸心血管外科临床杂志》编委。