
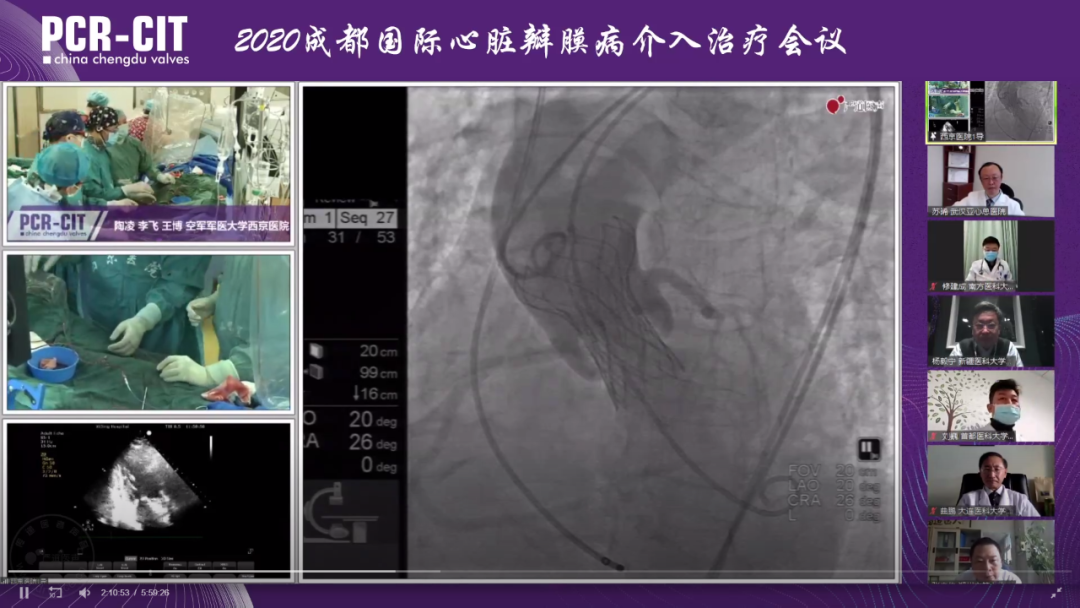
患者是一名67岁的女性,有心功能不全病史3年加重3个月,合并高血压。该名患者有自身免疫性肝炎,处于肝硬化失代偿期,存在低蛋白血症,三系细胞减低,CT提示显示右侧胸腔积液,肝硬化、脾大,胃镜检查显示食道静脉曲张。STS评分7.23%。
超声检查结果显示该名患者为主动脉瓣重度钙化的二叶瓣患者(BAV),平均瓣口面积0.7cm2,峰值流速为5.23m/s,最大跨瓣压差达到109mmHg。同时,超声显示该名患者左房、左室增大,室间隔增厚,伴有轻度对的二、三尖瓣返流,射血分数为55%。
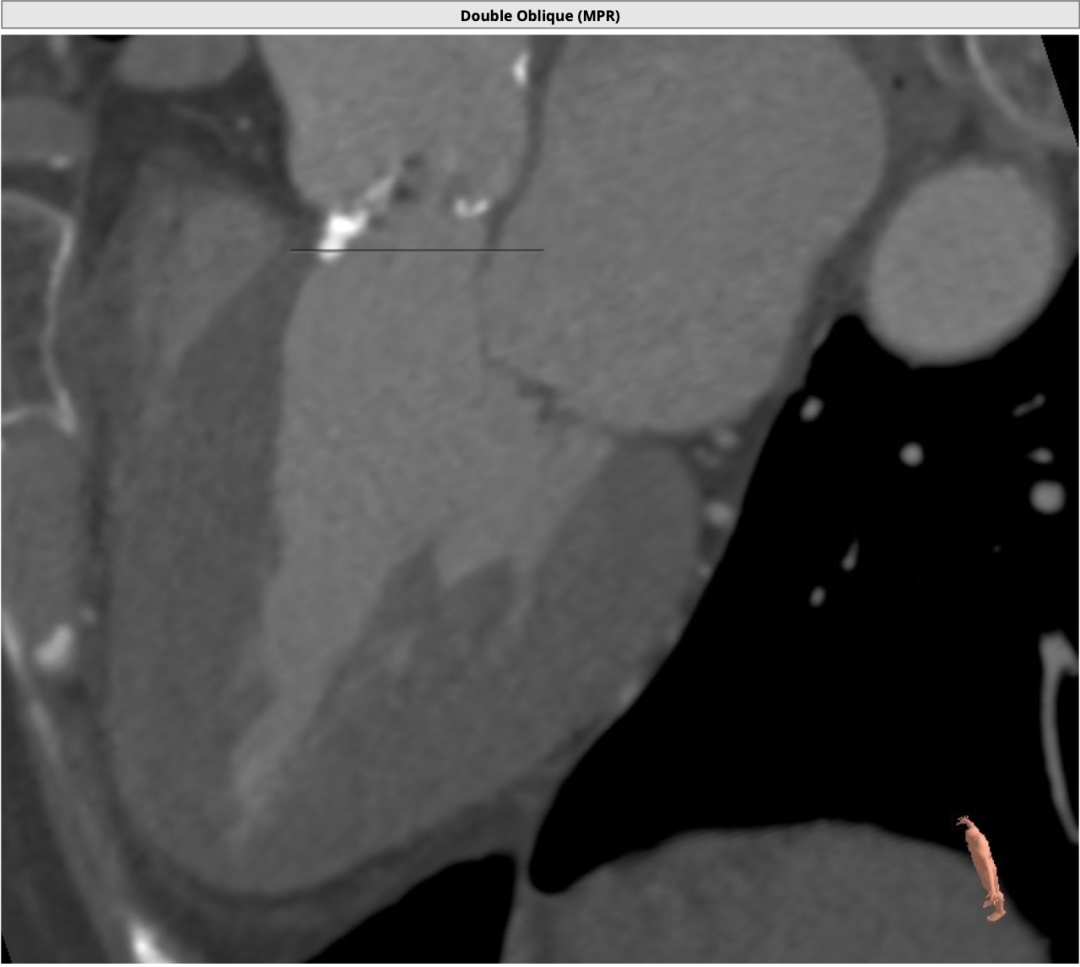
心室非常肥厚,心腔较小
该名患者为Type 0型二叶瓣,钙化分布不对称,瓣叶有轻度增厚。瓣环最短径为19.6mm,最长径为25.2mm,平均瓣环直径为22.4mm。左冠开口高度15.6mm,右冠开口高度15.9mm。
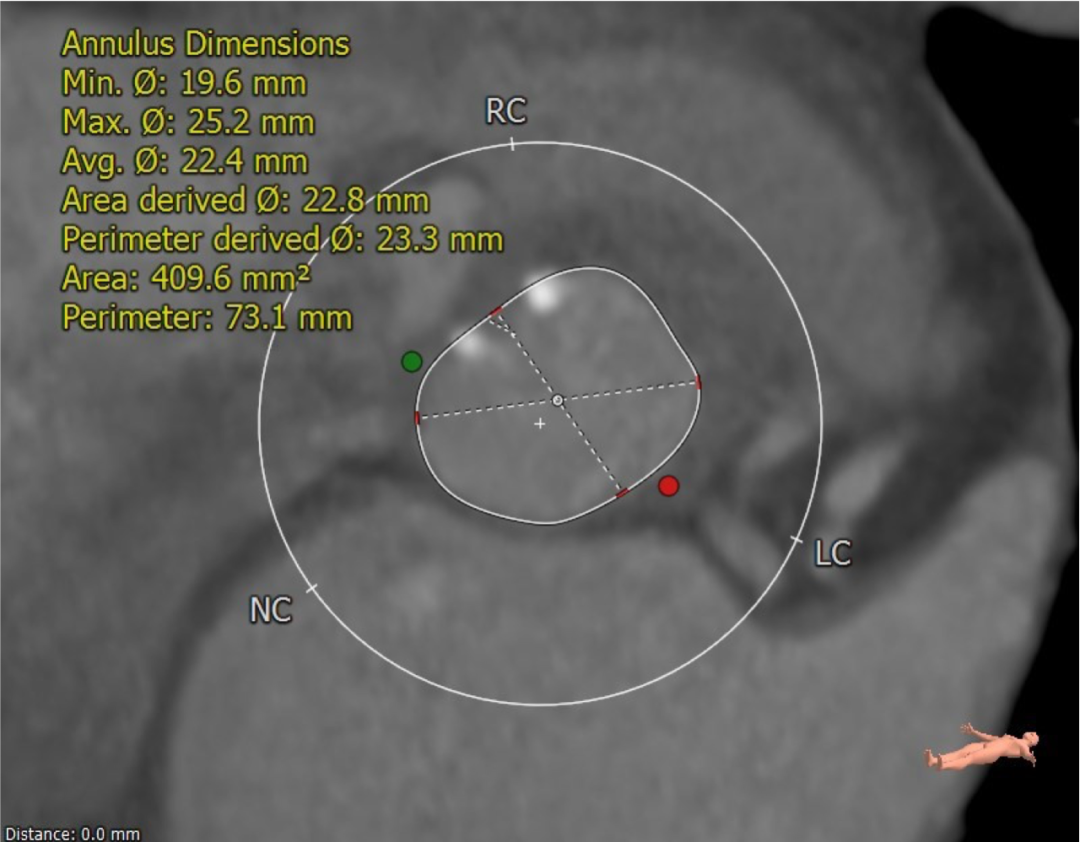
瓣环
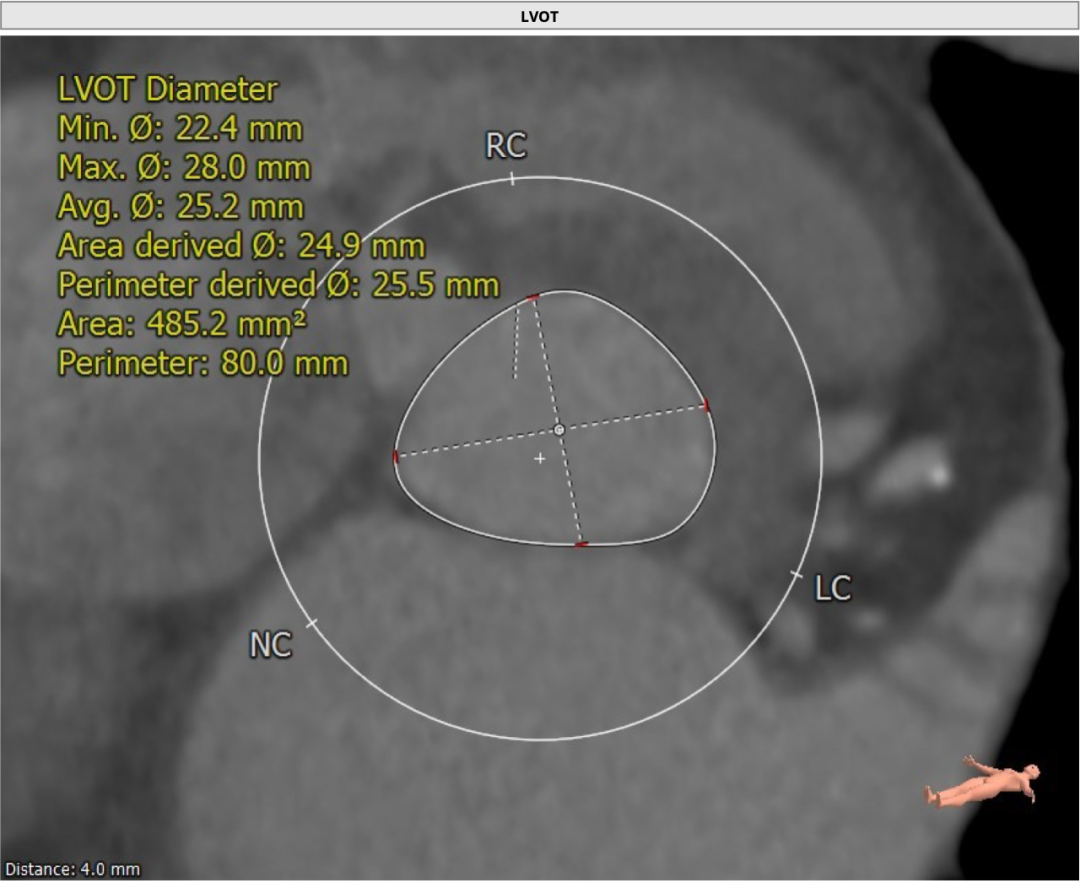
左室流出道
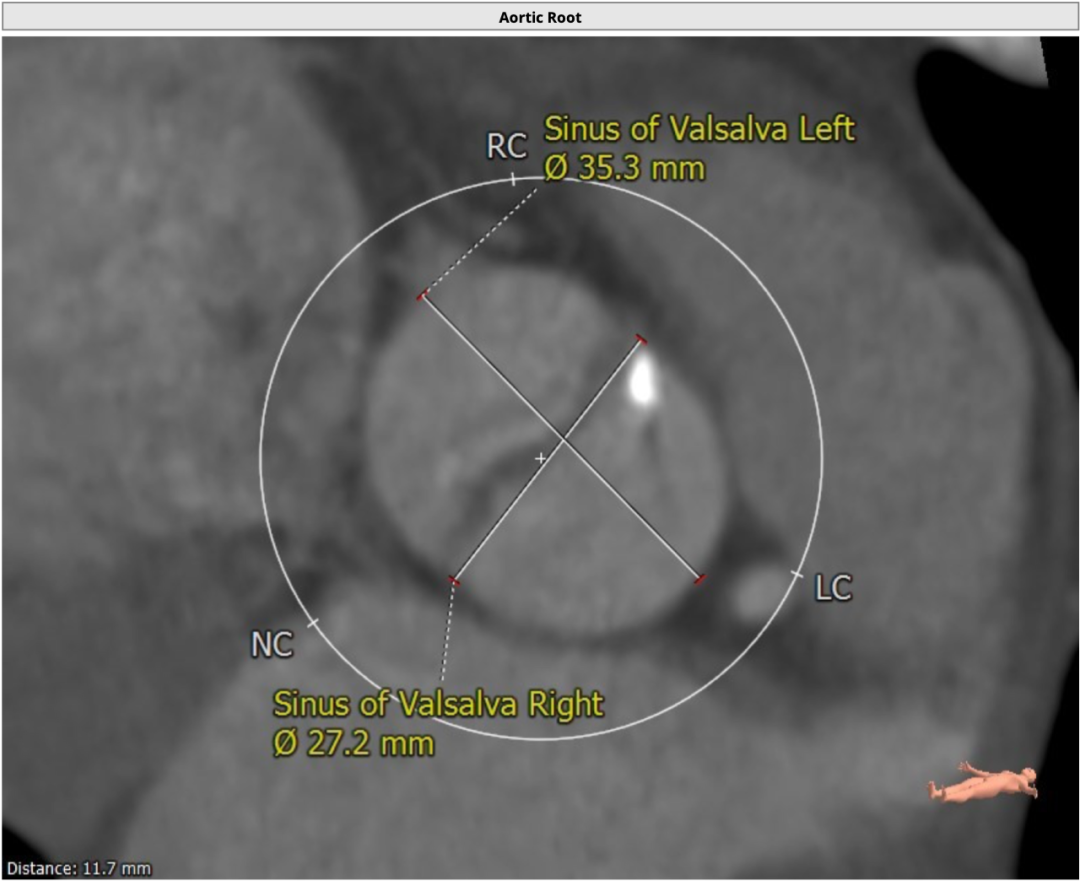
主动脉窦
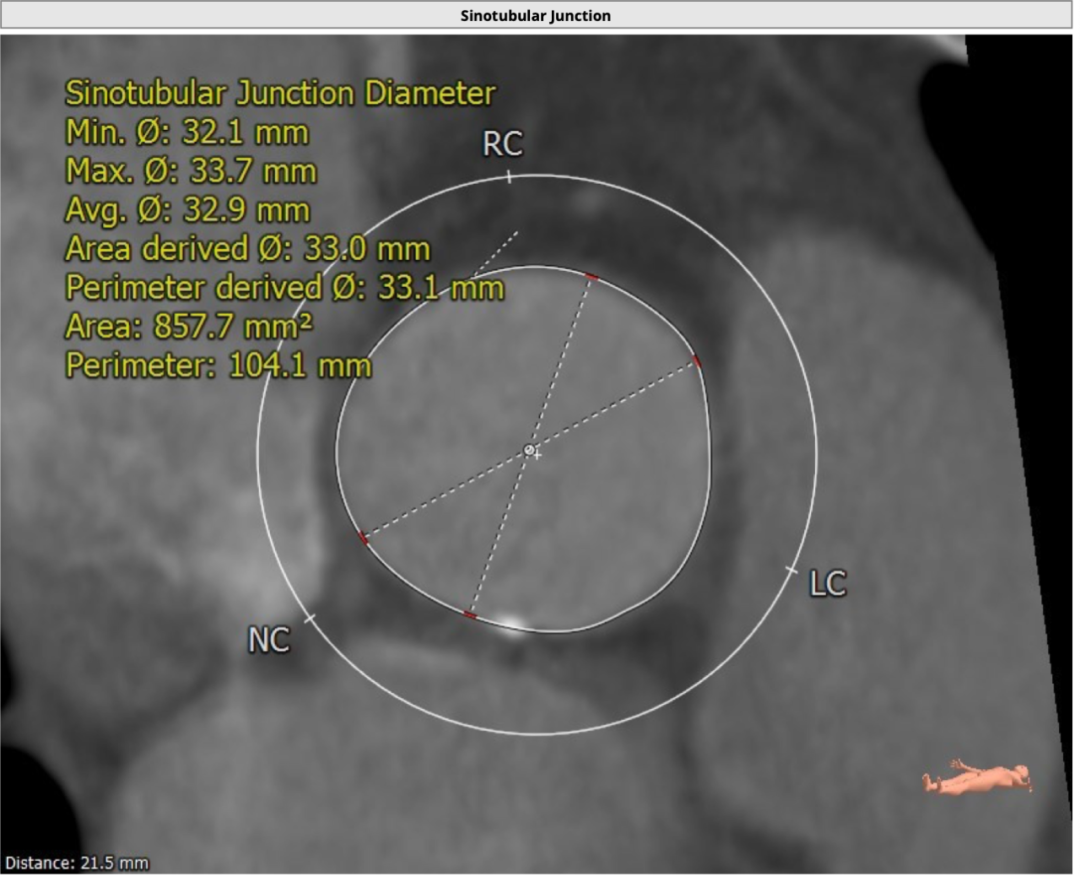
窦管交界处
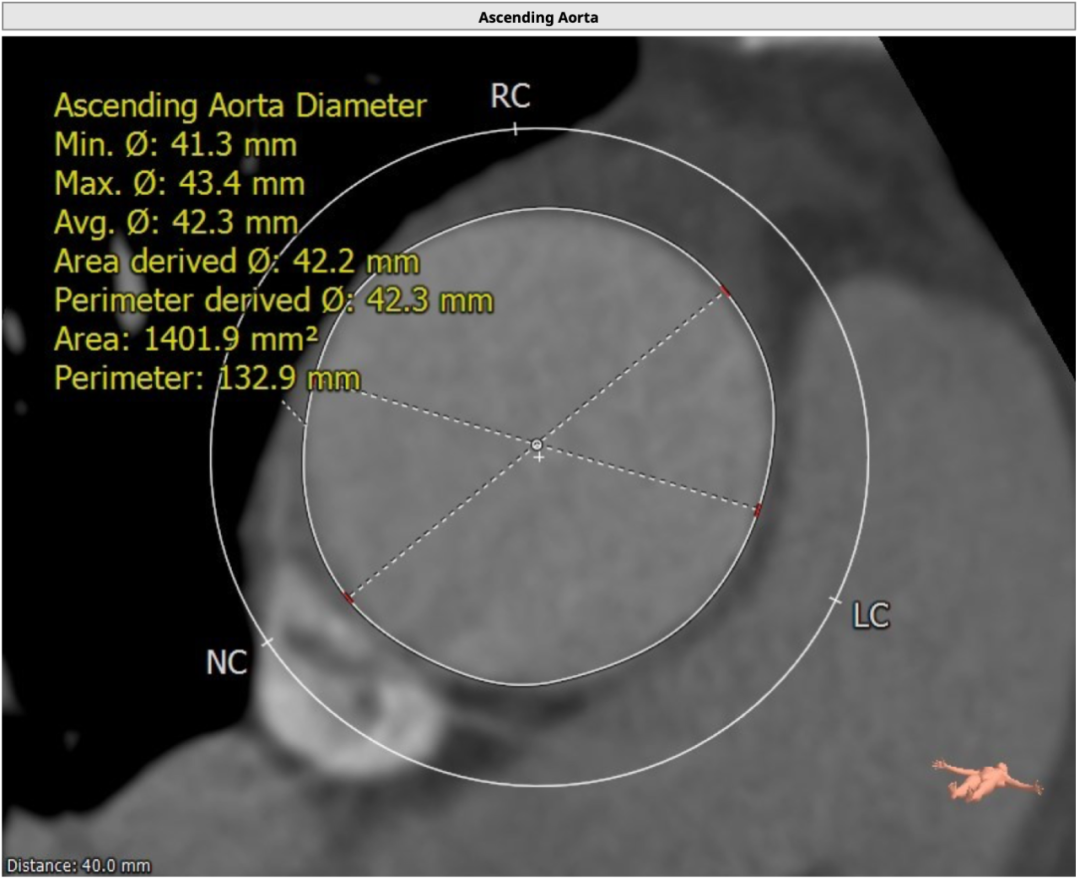
升主动脉
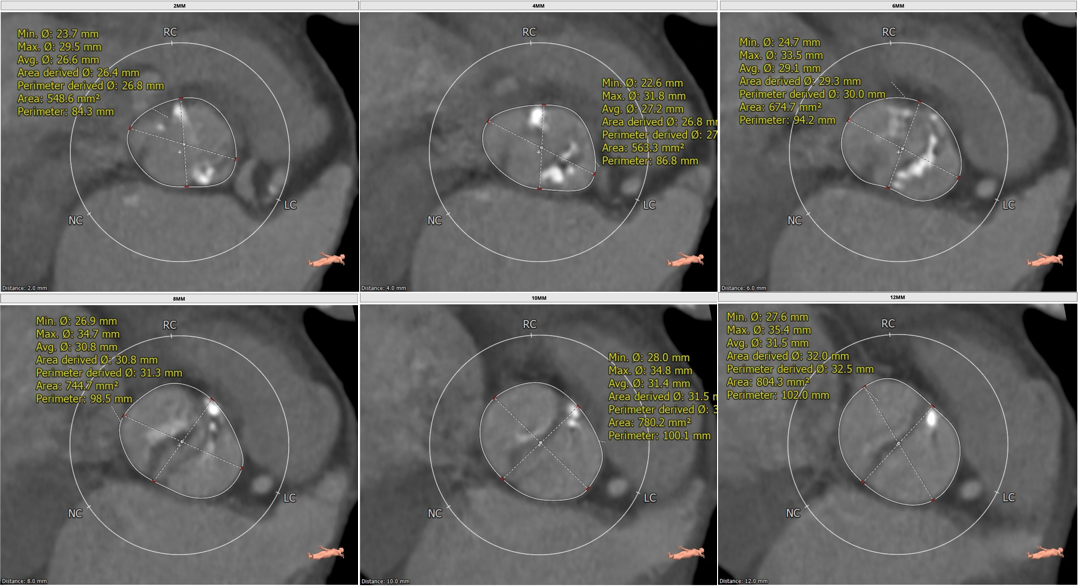
瓣上多平面分析结果
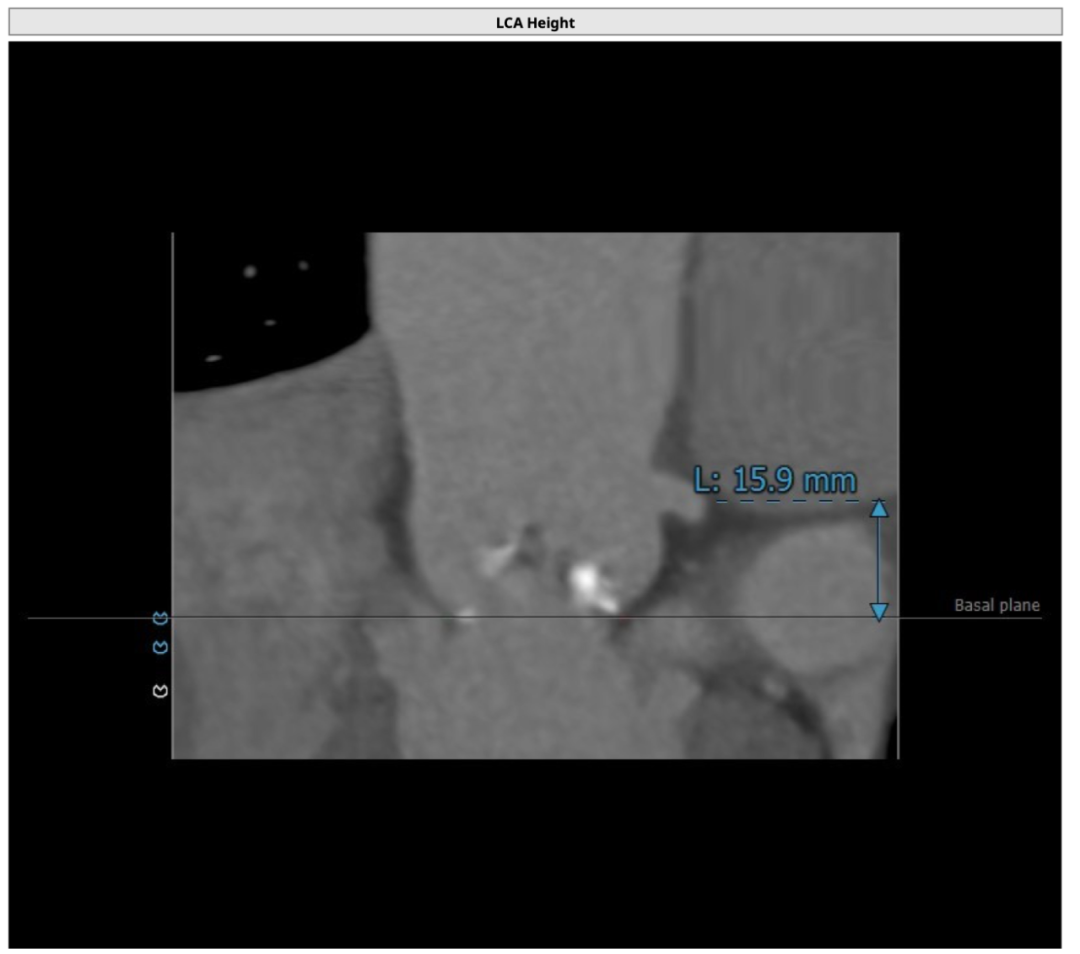
左冠开口
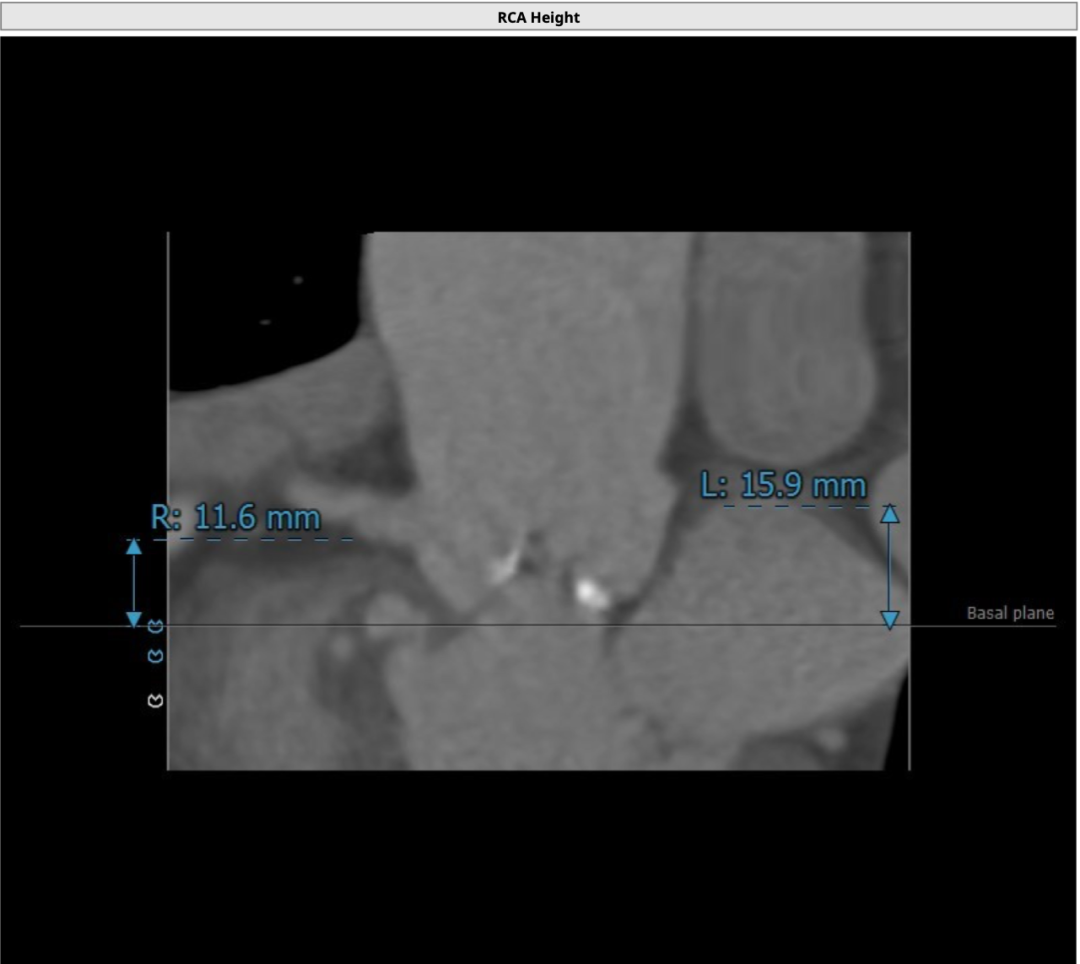
右冠开口
双侧股动脉最小直径均在7mm以上,条件良好。
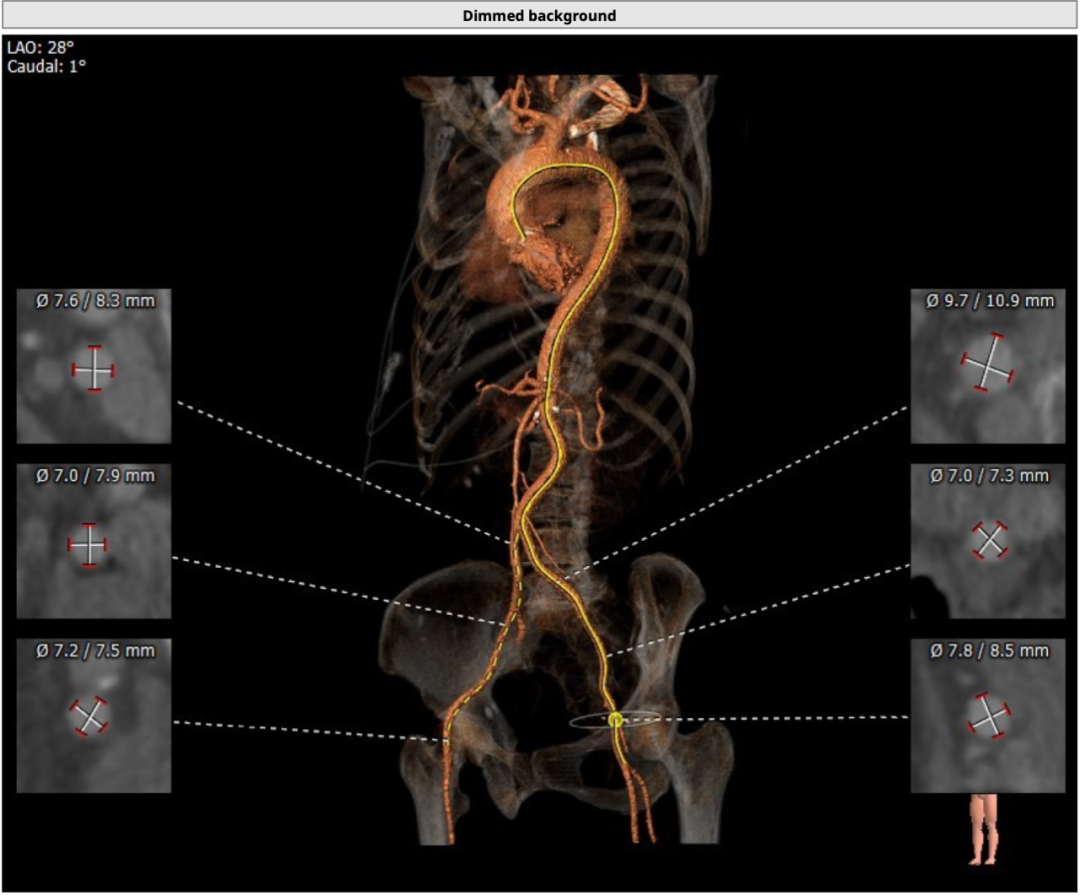
综合考虑患者基本情况,结合超声、CT检查结果,手术团队选择右侧股动脉作为主要入路;由于该名患者患有食道静脉曲张,不宜使用经食道超声进行术中监测,故最后采用经胸超声指导;选择微创心通敖广®22mm球囊进行预扩,VitaFlow 24或27型号瓣膜进行释放。
其中,由于患者凝血功能紊乱,血小板减少,所以针对术后长期的抗血小板策略,陶凌教授团队进行了重点讨论。经过查阅国际最新RCT研究结果,术者团队发现:TAVR术后长期阿司匹林单抗,和TAVR术后三个月阿司匹林+氯吡格雷双抗随后再转为阿司匹林单抗相比,两组的全因死亡率并没有明显的区别,但是出血明显减少。最终,陶凌教授团队决定采用术后阿司匹林单抗作为抗血小板治疗手段。

在无冠窦猪尾的指示下,将装载瓣膜的输送系统送至窦底。考虑到瓣膜是二叶瓣,瓣叶增厚较重,瓣膜在释放过程中可能会有下滑的情况,陶凌主任团队将输送系统调整到较高位置后开始释放。
在前三分之一缓慢释放完成后,VitaFlow瓣膜已经贴壁,没有移位的情况和趋势,术者随即长按电动输送系统释放按钮,一次性完成了释放。释放过程中瓣膜没有出现明显的下滑的现象。
释放完成后基本无压差,但是造影和经胸超声显示少量反流,并且位于左窦,基本可以判断和钙化相关,所以陶凌主任在和线上专家讨论后决定选用22mm的球囊进行后扩。
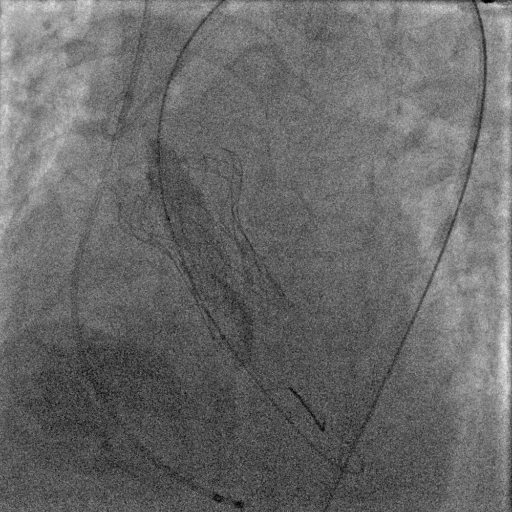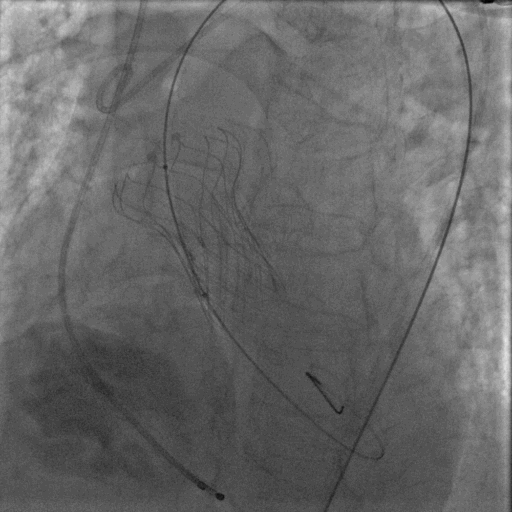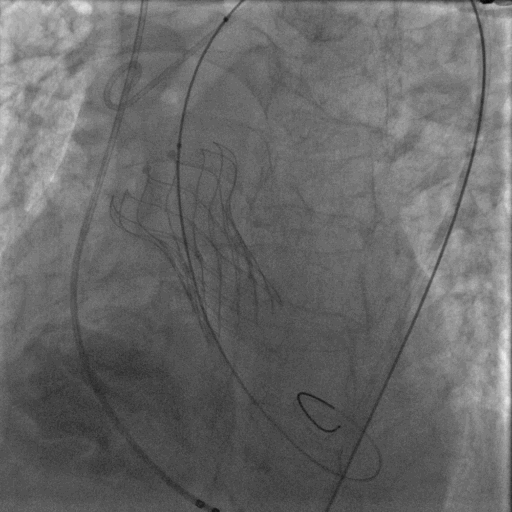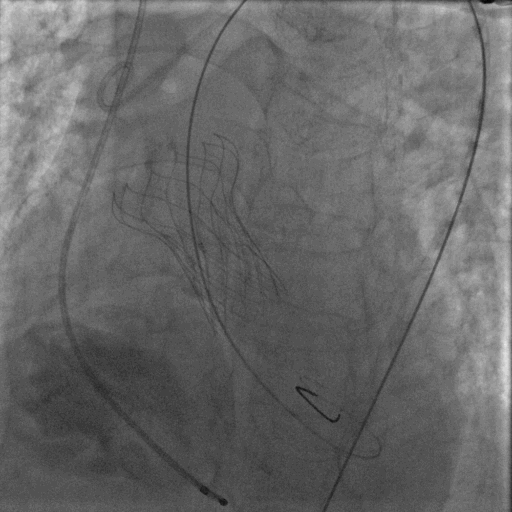
后扩完成后瓣膜形态明显改善,造影显示基本无反流。整台手术圆满完成。
在过程中和术后讨论环节,陶凌主任和线上专家做了如下总结:
1.术前的多平面测量,有利于帮助术者更好地了解窦部形态、瓣叶形态和左室流出道形态,以便更好地判断瓣膜植入的位置和解剖结构的契合程度,判断锚定区域位置和植入深度策略;能够帮助决定预扩的程度,从而判断瓣膜释放后是否容易下滑;同时,能够帮助术者判断一些特殊解剖结构的风险,例如冠脉对侧的团块状钙化会将瓣膜推向冠脉开口,增加迟发性冠脉阻塞的发生率。这些都可以通过术前的多平面测量分析出来。
2.瓣膜释放完成后因为代偿等原因,会出现一过性的血压升高,这时需要采取措施适当降压,降低脑卒中发生的风险。
3.对于Type0二叶瓣,一般需要还是根据压差、瓣膜形态和反流量来决定是否后扩;在这例手术中,释放瓣膜后虽然基本无压差,但是由于还存在着少量的反流,DSA下瓣膜的形态也仍然有改善的空间,同时没有瓣环撕裂、斑块脱落等风险,所以最终仍然选择进行后扩。