欧洲心脏病学杂志年初巨献:由多名心血管领域国际资深专家对急性冠脉综合症、冠脉介入治疗、瓣膜性心脏病、心律失常、心力衰竭、影像、主动脉及外周血管及预防等多个领域2019年公布的数百项研究进行了梳理,令读者获益匪浅。
本期我们全文翻译了由欧洲知名心脏病专家:Andreas Baumbach、Christos V Bourantas、Patric W Serruys及William Wijns针对2019 年在NEJM、Lancet、EHJ、JACC、Circulation、BMJ等权威杂志发表的60篇冠脉介入相关研究及指南和共识进行的梳理和总结,借新春来临之际奉献给国内心血管领域的读者。
本文由河南华中阜外医院心内科孟华医生全文翻译,首都医科大学附属北京安贞医院刘巍教授校正。

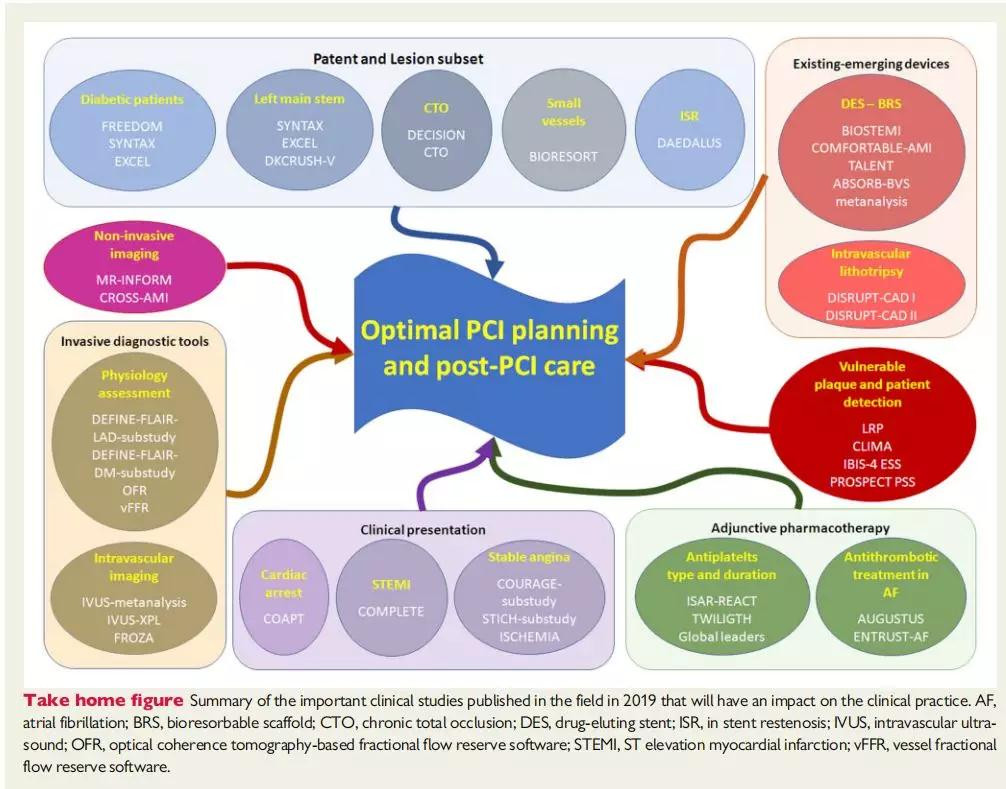
前言
经皮冠状动脉介入治疗(PCI)研究的重点是优化治疗策略,开发能够改善疗效的新型器械和药物疗法,并且建立危险分层,识别能够从针对动脉粥样硬化演变的这些新兴疗法中获益的高危患者。
些重要的临床研究报道了在阻塞性冠状动脉疾病(CAD)患者中应用不同治疗策略及支架的疗效,指南也对这些患者的管理进行了推荐。本文的目的是总结2019年发表的关键性研究,并讨论其对临床实践的影响。
心脏骤停和ACS患者的血运重建
心脏骤停后冠脉造影术(COACT)研究是一个里程碑式研究,这项研究改变了对院外心脏骤停成功复苏的非STEMI患者的入院管理策略1。
在这项前瞻性多中心研究中,纳入了552例最初发现为可电击的心律、且无明显非心源性原因导致的院外心脏骤停的患者,在神经功能恢复后随机分为即刻冠脉造影必要时PCI组和延迟冠脉造影组。急性血栓性闭塞在即刻血管造影组中仅占3.4%,在延迟血管造影组中占7.6%。出院时的生存率(65.2% vs.68.7%)及90天随访时的生存率(64.5% vs.. 67.2%)在即刻血管造影组及延迟造影组间差异无统计学意义。此外,两组复合终点(90天后具有良好的脑功能或轻度或中度损伤)未见显著差异(62.9% vs 64.4%)。
此项研究结果与先前的观察性研究结果相悖,先前观点认为推迟通过侵入性手段来评估冠脉解剖是不当的,而该研究却认为即刻冠脉造影与延迟冠脉造影都是合理的。
相反地,COMPLETE研究肯定了在STEMI合并多支血管病变患者中进行积极血运重建的价值2。
在该研究中,纳入4041名患者,1:1随机分为完全血运重建组和仅干预罪犯血管治疗组,平均随访3年,复合主要终点事件心血管死亡和心肌梗死发生率在完全血运重建组显著低于仅处理罪犯病变组(7.8%vs 10.5%)。
值得注意的是,无论是在住院期间还是出院后45天内再次入院行完全血运重建,两组获益是相似的。然而,这种比较并非随机,再次手术的时间是由术者决定的。
在NSTEMI患者中完全血运重建对预后的影响有待进一步研究。
慢性冠状动脉综合征
血运重建vs药物治疗
尽管强有力的证据支持在STEMI患者中,完全血运重建可以改善患者的预后,但是对于慢性冠脉综合征患者中PCI对预后的价值,相关研究结果不一。
一项回顾性研究分析纳入了16029名患者,对于PECT心肌灌注显像证实缺血负荷>5-10%的患者,早期手术或经皮血运重建可改善预后3。
然而,纳入了1379名进行了负荷灌注成像及定量冠脉造影的稳定性冠心病患者的COURAGE研究临床结果的事后分析并未证实这些发现4。该研究经过7.9年的随访发现,根据血管病变数目定义的CAD严重程度而并非缺血的严重程度是生存的预测因子,与最佳药物治疗相比,PCI联合最佳药物治疗也并不能改善预后。更重要的是,缺血程度或CAD与治疗策略(保守与PCI)之间没有相互作用。
与这些研究不谋而合,ISCHEMIA研究纳入5179例通过非侵入性检查存在中重度心肌缺血的稳定缺血性心脏病患者,随机分为常规介入治疗(在最佳药物治疗基础上)与单纯最佳药物治疗。
随访3.3年发现,两组间主要复合终点事件发生率无显著差异(15.5%vs. 13.8%,P = 0.34)5。在此研究中,PCI与改善生活质量、减少心绞痛症状和降低自发心肌梗死的发生率(HR:0.67 95%CI 0.53-0.83)相关。然而,该研究存在一个重要的局限性是28%的保守治疗组交叉至侵入治疗组,这可能会影响到已报道的结果,处理后的结果(treated analysis)尚未公布。
STICH研究旨在评价有无存活心肌对接受外科手术血运重建的患者预后影响6。该研究纳入601例EF<35%且进行存活心肌评估的患者,随访10.4年,但未能证明心肌存活与否对接受血运重建手术的患者生存获益有影响。
REVIVED试验目前正在研究PCI在改善心力衰竭患者预后方面的安全性和有效性。
患者与病变分型
左主干和三支血管病变
2018年ESC指南对复杂冠心病(左主干病变或三支血管病变)和糖尿病合并复杂血管病变患者进行优化血运重建策略进行了探讨:糖尿病合并三支血管病变患者首选CABG,对于SYNTAX评分<22者PCI为IIb推荐,SYNTAX评分>22分者不推荐PCI7。
这些推荐与FREEDOM研究结果相符,该研究纳入1900例糖尿病合并多支血管病变患者,随机分组外科搭桥组和PCI组,随访8年结果显示PCI死亡率24.3%显著高于CABG组18.3%8。
相反地,SYNTAX扩展生存研究纳入1689例左主干或三支血管病变患者,随访10年,PCI组和CABG组全因死亡率无显著差异(27% vs 24% p=0.092),而亚组分析显示,三支血管病变患者PCI组死亡率高于CABG组(HR 1.41 95%CI 1.1-1.80),而在左主干组两组间死亡率无差异(HR 0.9 95%CI0.68-1.20)。相反的,在糖尿病亚组两种治疗策略全因死亡率差异无统计学意义(P=0.660)9。
两个试验均存在局限性:在PCI组均使用的是第一代DES,与目前实际应用不符,且研究终点为全因死亡而不是以患者为导向的心血管死亡。
EXCEL研究克服了这些局限性,在该研究中纳入1905例左主干病变且SYNTAX评分≤32分患者,随机分为PCI植入第二代DES组或CABG组10。在PCI组77.2%应用IVUS11。随访5年两组复合终点事件全因死亡率、心肌梗死、卒中无统计学差异(PCI:22.0% vs CABG:19.2% P=0.13)。PCI组30天不良事件发生率低于CABG组(4.9%vs 8.0%),30天至1年的时间内,两组事件发生率无差异(4.1%vs 3.8%),但是术后1年至5年的时间段里,PCI组主要终点事件发生率显著高于CABG组(15.1%vs9.7%)。两组患者脑血管事件发生率相似(5.2% vs 3.3%),PCI组有较高的全因死亡率(13% vs 9.9%)和缺血致再次血运重建率(16.9% vs 10.0%)。
与SYNTAX研究结果相同的是,在3年和5年的随访中,糖尿病和非糖尿病患者中两种治疗策略的结局无差异10,12。
分叉病变
2019年,DK-CRUSH V研究3年随访结果发布。
与1年随访结果相似,DK CRUSH组与必要时T支架组相比,具有较低的靶血管再次血运重建率(TLR, 5.0% vs. 10.3%, P=0.029)、靶血管心肌梗死发生率(1.7% vs. 5.8%, P=0.017)和确切的或可能的支架内血栓发生率(0.4% vs. 4.1%, P=0.006)13。但是,DK CURSH技术具有一定的难度,需要较好的PCI技术和经验。考虑到这些因素,因此,DK-CRUSH V研究很难在术者经验较少的中心实施。
欧洲分叉俱乐部最近发布的第14个共识文件主张必要时使用T型支架技术治疗分叉病变,并建议只有在病变解剖结构复杂、难以进入侧支或侧支开口病变>5 mm和或合并钙化时,才采用双支架策略14。在双支架策略的情况下,欧洲分叉俱乐部建议使用Culotte术式或TAP技术,当考虑挤压技术时,建议使用DK CRUSH术。
CTO病变
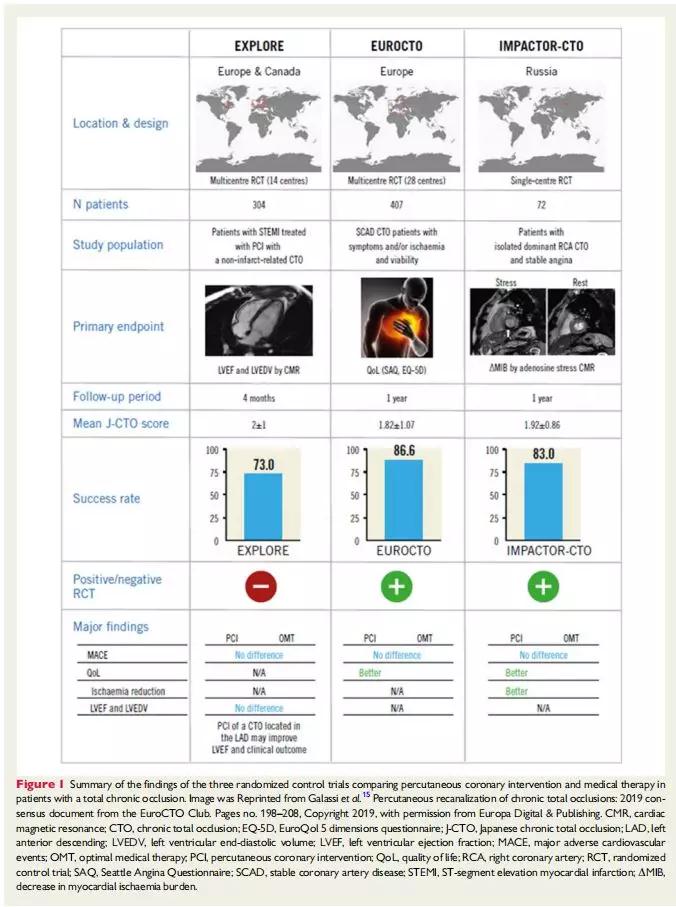
2019年,欧洲CTO俱乐部发布了一份共识文件,总结目前的证据(图1),讨论CTO开通的适应证,展示了CTO器械的进步,并提供关于CTO PCI培训的建议15。
根据ESC心肌血运重建指南,结合随机对照研究的结果,欧洲CTO俱乐部建议:
在最佳药物治疗后仍有症状的情况下应进行CTO再通;
对于无症状患者,建议进行缺血负荷评估,如果有证据表明缺血负荷增加(≥左心室质量的10%),则建议进行CTO血运重建。
这些推荐与近期发表的DECISION-CTO研究结果一致16。
该研究纳入815例CTO患者,随机分为完全血运重建和仅处理非CTO病变组,两组患者中只有25%为单支血管病变。随访4年发现,CTO PCI组和无CTO PCI组在死亡、心梗、卒中或血运重建的复合终点(22.4% vs. 22.3%, P=0.86)及生活质量方面没有差异。
研究表明,在多支血管病变中,在开通CTO病变之前应考虑非CTO病变的血运重建以及重新评估缺血程度和患者症状。该研究局限性仍是本类研究的固有缺陷,存在较高的患者交叉率(19.6%),即由最初的非PCI组转入CTO PCI组,最后由于患者招募太慢而提前终止了研究。
小血管病变和支架内再狭窄
小血管病变进行PCI治疗时,主要不良心血管事件(MACE)和支架内再狭窄引起的TLR发生率较高。
2019年发布BIO-RESORT亚组研究,对比分析了在小血管病变(<2.5mm)中应用超薄钴铬可降解聚合物涂层西罗莫司(支架厚71um)、超薄钴铬可降解聚合物涂层依维莫司支架(支架厚78um)或第二代的较厚的永久聚合物涂层佐他莫司支架(支架厚度102um)的临床结果。
研究显示:较厚的佐他莫司组对比超薄的西罗莫司组有较高的TLR发生率(5.3% vs. 2.1%, P=0.006),而佐他莫司组与依维莫司组支架无统计学差异(4.0% vs. 5.1%, P=0.31)17。这些发现强调了DES时代支架厚度对小血管病变预后的影响,并且与以前报道裸金属支架研究的结果一致18。
支架内再狭窄是支架治疗失败的最常见原因,ISR预后较差且有较高的TLR发生率,因此它的治疗具有一定的挑战性。目前最有效的两种治疗策略是药物涂层球囊血管成形术或DES置入19。
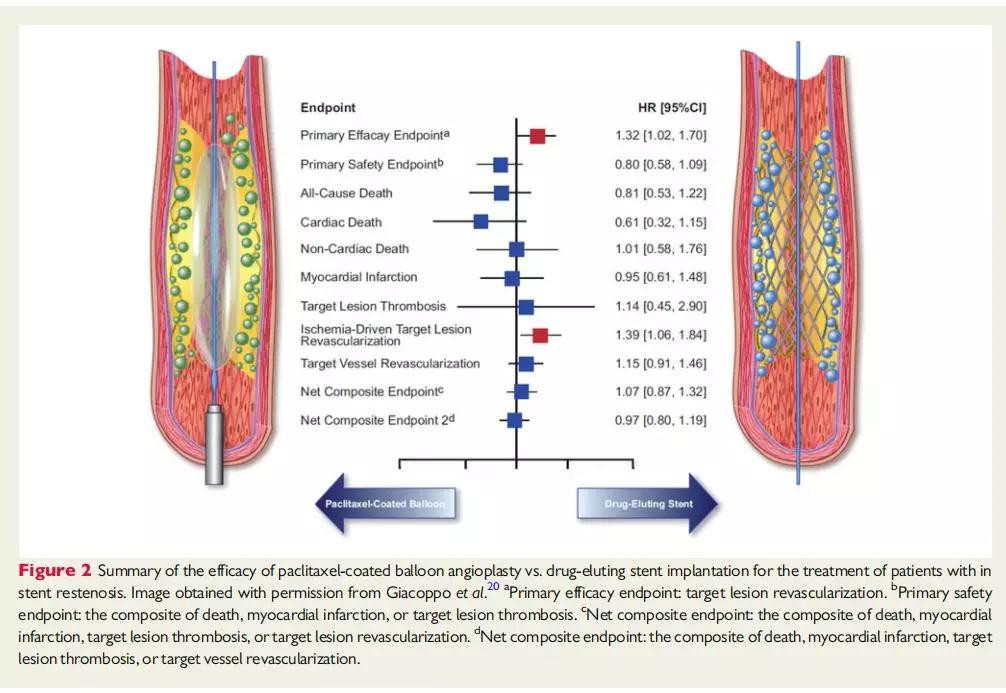
2019年公布的DAEDALUS研究分析了1976名ISR患者中,DES和DCB治疗ISR方面的差异20。3年随访结果显示,与DES置入相比,紫杉醇涂层球囊血管成形术TLR的发生率更高(HR 1.32, 95% CI1.02–1.70; P=0.035)。但是,死亡、心梗或靶病变血栓形成的复合终点在两组之间没有差异(图2)。
现存的和新兴的介入器械
DES 和BVS
《ESC心肌血运重建指南》推荐在临床实践中使用第二代DES7。COMFORTABLE-AMI后期随访研究和血管内影像分析进一步证明了与裸金属支架相比,DES在STEMI患者中的优越性。5年随访结果发现,与金属裸支架组相比,Biolimus支架组具有较低的靶血管心肌梗死(2.2% vs. 5.0, P=0.02)和缺血致使的TLR 发生率(4.4% vs. 10.4%,P<0.001)21。
BIOSTEMI研究比较超薄钴铬合金生物降解聚合物西罗莫司洗脱支架与耐久聚合物依维莫司洗脱支架治疗STEMI的疗效,纳入1300例患者并随机分组,随访12个月结果显示,西罗莫司洗脱支架组靶病变失败的发生率低于依维莫司洗脱支架(4% vs. 6%,RR:0.59,95%CI0.37-0.94)22。
与之相对,TALENT研究在所有PCI患者中对比了超薄西罗莫司支架与耐久聚合物依维莫司洗脱支架的疗效,两组间主要的复合终点事件心源性死亡、靶血管驱动心肌梗死、临床提示的TLR无统计学差异(4.9% vs.5.3%非劣性P< 0.0001)23。
生物可吸收支架的引入克服了DES的局限性,提高了远期疗效。然而,这些器械在短期和中期随访中的事件发生率增加,引起了对其安全性的关注,目前不推荐常规临床使用。
最近一项荟萃分析比较了BVS和依维莫司洗脱支架的随机研究结果,发现在5年的随访中,BVS的TLF发生率更高(14.9% vs. 11.6%,P = 0.030),主要归结于靶血管致心肌梗死和缺血致TLR24。另一阶段性分析表明,在随访的0–3年内,Absorb BVS组的事件发生率更高。但在随访的3-5年期间,在最初3年没有经历过事件的患者中,两组之间的心源性死亡、靶血管心肌梗死、局部缺血性TLR和支架内血栓形成的发生率相似。
这些发现首次为生物可吸收支架不良事件的发生时间提供了依据,并表明完全吸收后的长期事件发生率较低。
介入治疗的辅助器械
钙化病变介入治疗并发症高,预后差。近年来,血管内碎石术(IVL)已成为治疗钙化病变的有效替代方法25。该技术采用半顺应性球囊,球囊导管的中间有排列整齐的小型碎石发射器,通过发射的声波压力波击碎血管内的钙化病变,且周围的纤维组织斑块不受其影响26。
DISRUPT CAD研究是第一个系统评估IVL安全性和有效性的研究。
该研究纳入了60例钙化严重,长度≤32mm的患者。结果显示,该手术在所有病变均成功进行,即刻管腔获得为1.7mm,术后残余狭窄为12.2%。随访6个月时总的MACE事件为8.3%,3例围手术期心梗和2例心源性死亡27。
DISRUPT CAD II研究纳入120例患者,研究结果相似,院内MACE事件5.8%(7例非Q波心梗),30天MACE事件7.6%。48例患者术前应用OCT检查,其中47例术后再次OCT检查,结果显示IVL可使一处钙化出现3.4±2.6个断裂,即刻管腔面积增加4.79±2.45mm2,完美支架膨胀达102.8±30.6%28。
最近,Wilson等报道IVL可导致心室早搏和不同步起搏,但该研究中未发现恶性心律失常事件29。
目前正在进行的DISRUPT CAD III研究有望为IVL治疗钙化病变的安全性和有效性提供进一步的证据(NCT 03595176)。
辅助药物治疗
PCI患者抗血小板治疗的策略和持续时间一直是学者关注的领域。
TWILIGHT试验设计探讨高出血风险患者PCI术后双联抗血小板持续时间30。该研究纳入7119名患者,随机分组为:双抗治疗3个月改替格瑞洛单药治疗组和双抗12个月治疗组。
结果显示,短双抗治疗组与继续DAPT相比,出血风险显著降低(BARC 2,3,5型出血 4.0% vs 7.1% P<0.001),而复合终点死亡、心梗、卒中发生率两组间无差异。
然而,GLOBAL LEADERS研究的最新事后分析结果表明,对于复杂PCI术后患者,与标准抗血小板治疗策略(1年DAPT+1年阿司匹林)相比,长期单用替格瑞洛策略(1个月DAPT后单用替格瑞洛24个月)2年主要终点死亡、心梗的发生率更低(3.51% vs. 5.43%; P=0.002)。值得注意的是,两组间出血风险无差异(BARC 3,5 出血 2.45% vs. 2.54%; P=0.834)。
另外一项纳入8项随机对照的14963名患者的研究也表明,在低出血风险的患者中(PRICISE 评分<25分) 中,延长DAPT治疗时间的缺血事件发生率较低,特别是在接受复杂PCI的患者中。相反,高出血风险的患者长期服用DAPT并不会降低缺血事件风险,反而会增加出血风险31。
PCI治疗合并房颤的患者接受联合抗血小板和抗凝治疗后出血风险增加。近几年,多项大规模随机对照研究对这类患者的最佳治疗方案进行了研究。
备受关注的AUGUSTUS试验结果在今年ACC年会上公布。
该研究为多中心、随机对照、2x2析因设计,纳入4614例PCI后房颤患者,在P2Y12抑制剂治疗基础上,随机分入阿哌沙班或华法林组,再分别给予阿司匹林或安慰剂治疗,随访6个月32。所有入选患者PCI术后随机分组前进行标准的抗栓治疗6天。服用华法林组主要出血或临床相关的非最主要出血事件发生率显著高于阿哌沙班组(14.7% vs. 10.5%, P<0.001),且服用阿司匹林组显著高于安慰剂组(16.1% vs. 9.0%, P<0.001)。阿哌沙班组的死亡或住院比例低于华法林组(23.5% vs. 27.4%, P=0.002),缺血事件相似。相反的,加入阿司匹林与否对这些终点事件无影响。
ENTRUST-AF PCI研究结果与此相似。该研究纳入1506例PCI后合并房颤患者,评估依度沙班+P2Y12抑制剂的双联抗栓治疗和VKA+DAPT安全性和有效性33。入选患者PCI术后45h随机分组,随访12个月,两组患者主要出血事件和临床相关非大出血事件无差异,且复合终点事件(心源性死亡、卒中、栓塞、心肌梗死、确切的支架内血栓)无差异。
今年发表的一项荟萃分析随机对比PCI术后房颤患者双抗vs三联抗血小板治疗的安全性和有效性,再次证实了上述发现,接受双联抗栓治疗的患者出血风险降低(13.4% vs.20.8%;P<0.0001),但支架内血栓的风险增加(1% vs.0.6%;P=0.040)34。
侵入性诊断检查
冠脉生理检查
最近的研究表明,血流储备分数(FFR)和包括瞬时无波速比(iwFR)在内的静息指标不仅可以指导血运重建,在评估PCI术后的最终结果和预测预后方面也具有一定价值35,36。然而,在完全充血的FFR和静息指数之间偶尔存在不一致。
今年的几项研究试图检验FFR和iwFR不一致的病变的生理特征确定何种病变类型和亚组FFR优于iwFR,反之亦然37,38。
DEFINE-FLAIR研究的亚组分析比较了左前降支病变患者在FFR或iwFR评估的基础上延迟血管重建的预后。随访结果表明,iwFR组1年的事件发生率较低(2.22% vs. 4.99%, P=0.03),主要归结于无计划再次血运重建39。与之相反,对糖尿病患者进行的一项研究的事后分析显示,FFR和iwFR组的预后没有差异(7.2% vs. 10.0%; P=0.30);但是,iwFR组非致死性心肌梗死的发生率更高(4.7% vs.1.9%;P=0.05),并且与糖尿病之间存在显著相关性40。
在引入用于评估中间病变功能严重程度的静态指标的同时,研究者们也在努力探索通过计算机方法对冠状动脉造影或侵入性成像数据进行后处理,以获得FFR。
2019年提出了两种新的计算衍生FFR的解决方案:一种是通过三维定量冠状动脉造影来获得血管几何形状并估计病变处的压力降低;另一种是处理OCT成像数据。后者能够结合形态学和生理学评估动脉粥样硬化病变和PCI术后的手术结果41,42。
这些解决方案的初步验证显示出良好的结果;然而,在其广泛应用于临床领域之前,需要进一步在更多患者中评估其疗效。
血管内影像
多项累积证据已经证明血管内超声(IVUS)在指导PCI中的价值。
今年发表的一项纳入4724名患者的荟萃分析强调了IVUS指导的预后获益。与血管造影指导组相比,IVUS指导组的MACE(5.4% vs. 9.0%; P<0.001)、心源性死亡(0.6% vs. 1.2%, P=0.03)、TLR (3.1% vs. 5.2%,P=0.001)和明确/可能的支架血栓形成发生率(0.5% vs. 1.1%,P=0.02)更低43。
与上述发现一致,IVUS-XPL研究纳入1400例病变>28mm患者,随机分为IVUS指导组和造影指导组。随访5年结果显示,IVUS指导组的MACE(5.6% vs. 10.7%, P=0.001)较低,主要归功于TLR发生率(4.8% vs. 8.4%, P=0.007)降低。1-5年阶段性随访研究结果提示IVUS指导PCI与长期的临床获益相关(HR 0.53, 95% CI 0.29–0.95; P=0.031)44。
这些发现强调了IVUS在指导血运重建预后的意义,并支持其常规应用,以优化手术结果和改善PCI术后的短期和长期结局。
FFR目前被推荐用于指导患有中度狭窄病变的慢性冠状动脉综合征患者的血管重建。
FORZA研究评估OCT指导PCI的价值,该研究纳入350例中度狭窄患者随机分为OCT指导和FFR指导组45。OCT指导组血运重建以最小管腔面积的cut off值指导血运重建,而FFR≤0.8则进行血运重建。两组均应用OCT和FFR优化支架植入。随访13个月发现,OCT指导的PCI进行更多的血管重建而且成本较高,但两组之间的全因死亡、心肌梗死、靶血管重建的复合终点没有差异(8.0% vs. 3.4%, P=0.064)。对于研究的主要终点,即MACE和严重的心绞痛在随访13个月时,OCT指导组略优于FFR指导组(14.8% vs. 8.0%, P=0.048)。
FROZA研究是第一个对比腔内影像和生理学指导PCI的研究,显示了两种方法在指导血运重建的局限性(OCT指导PCI增加血管支架植入和成本,FFR指导增加MACE和心绞痛)。联合生理学和影像学指导血运重建可能会克服局限性,优化治疗效果,改善冠心病患者预后。
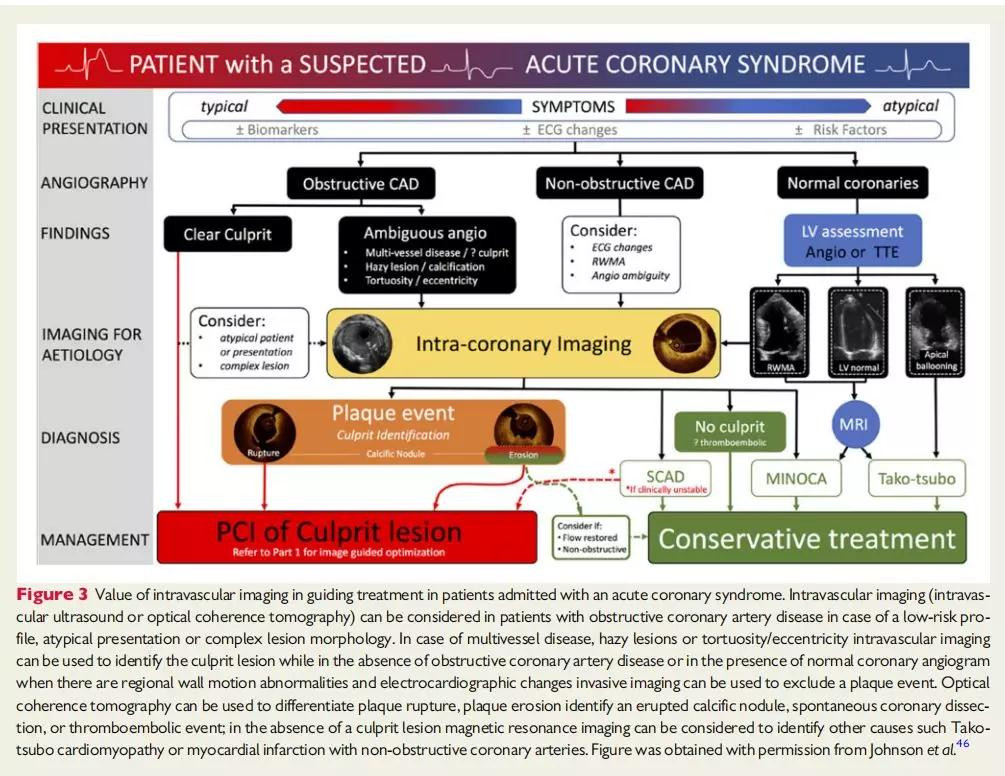
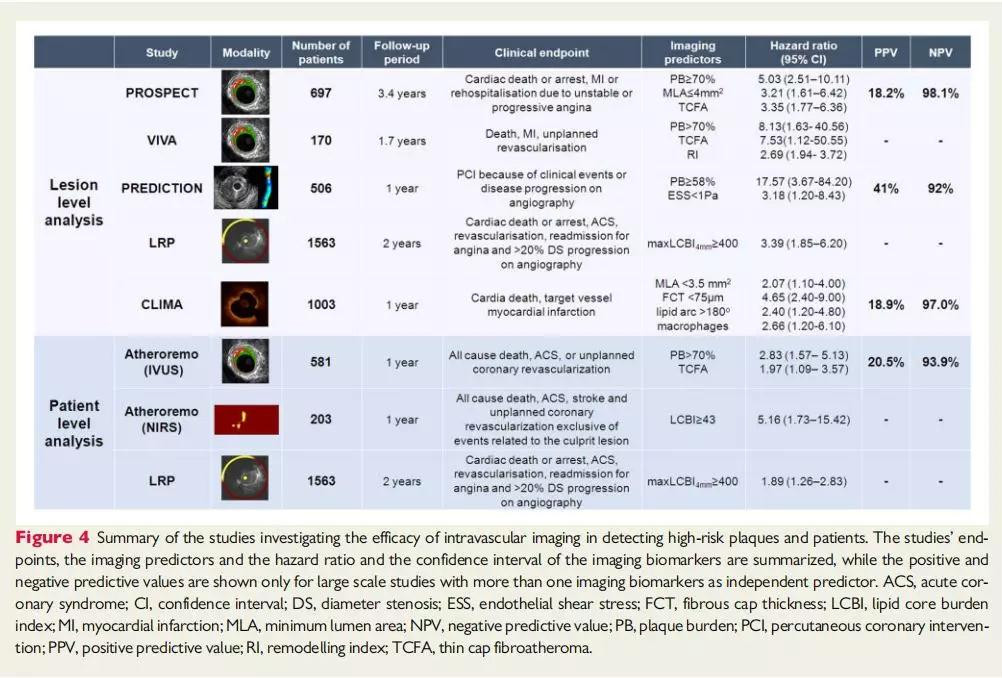
2019年,欧洲经皮心血管介入学会(EAPCI)发布了冠脉腔内影像学检查的临床应用专家共识。本共识强调了血管内成像的价值46。特别是OCT对冠状动脉造影无法检测到的罪犯病变识别和对ACS患者进行个体化治疗时的价值(图3)。同时,共识还强调了血管内影像在评估不明确的冠状动脉造影结果,检测栓塞事件和壁内血肿,评估由其他器官对血管外部压迫引起的病变方面的价值,并总结了其在识别易损斑块和高危患者中作用的证据(图4)
无创成像技术
无创成像技术在有症状的阻塞性CAD患者的诊断中具有重要的作用47。
MR-INFORM研究显示,无创成像技术尤其是心脏磁共振成像(CMR)不仅可用于CAD的诊断也可用于指导血运重建48。该研究纳入918例患者随机分为CMR指导血运重建和FFR指导血运重建,CMR指导组具有较低的冠脉造影和PCI比率 (35.7% vs. 45.0%, P=0.005)。随访1年,两组主要终点事件全因死亡、心梗、靶血管血运重建无显著差异(3.6% vs.3.7%, P=0.91)。
该研究是少有的比较无创影像学和侵入性指导PCI,研究的局限性是事件发生率低于10%评估的事件率,因此,可能不足以检测两组之间的差异。
CROSS-AMI研究取得了相似的结果,该研究比较了冠脉造影与负荷超声心动图指导STEMI患者非罪犯血管狭窄QCA>50%血运重建的差异49。该研究因入选较慢,在入选77%患者后提前终止实验。作者报道冠脉造影指导组有较高的非罪犯血管血运重建率(88% vs. 22%),一年的随访发现,两组之间主要终点事件心源性死亡、心梗、冠状动脉血运重建或因心衰再次入院没有显著差异(14% vs. 14%, P=0.85)。
但CROSS-AMI研究的一个局限性是评估组间差异的能力不足。因此,有必要进一步研究无创成像在指导ACS患者血管重建中的价值。
易损斑块的检测
接受血运重建尤其是ACS患者在短期随访中事件发生率仍很高50。
随着一些能够改善动脉粥样硬化斑块并抑制疾病的进展的新型药物的出现,如何识别高危患者受到关注。由于这些新兴疗法成本较高并且有一定的副作用和局限性,因此,准确的危险分层和高危患者的识别有望为这些患者提供个体化治疗以及积极新药治疗,以改善易损群体的预后51。
大规模前瞻性血管内成像研究强调了IVUS在检测可能进展和引起事件的易损斑块,以及更准确地进行危险分层方面的价值。
2019年公布的Lipid-Rich Plaque(LRP)和CLIMA研究首次评估了近红外光谱(NIRS)-IVUS和OCT在检测易损斑块中的有效性52,53。
LRP研究纳入1563例疑似冠心病并进行了冠脉造影和PCI的患者,在非罪犯血管内均进行NIRS-IVUS检查。2年的随访中,发现脂质负荷增加(max LCBI 4mm>400)患者的非罪犯MACE发生率高于无脂质斑块患者(13% vs. 6%, P<0.0001),max LCBI 4mm>400是2年MACE事件的独立预测因子。该研究为斑块成分对预后影响提供了证据,但由于IVUS不是完整分析,仅限于4 mm段的maxLCBI,因此未能检测NIRS和IVUS在预测事件中的协同价值。
CLIMA研究是一个前瞻性、多中心研究,研究OCT下斑块特征对预后的意义53。研究纳入1003例行冠脉造影患者,采用OCT检查未行PCI的LAD近段病变。该研究发现最小管腔面积<3.5 mm2,脂质弧>180°,纤维帽厚度<75μm,以及巨噬细胞累积是心源性死亡和靶血管段心肌梗死的独立预测因子。具有上述所有斑块特征患者的事件发生率高于其他患者(18.9% vs.3.0%, P<0.001)。
冠脉影像进展
总结这些研究的结果并结合以前的研究发现,斑块特征似乎在病变和患者水平提供了有用的预后信息,但是在预测事件方面的准确性有限。
在过去几年,已经引入几种方法以增强评估斑块特征的有效性,且努力研发混合多模态血管内成像导管,以对斑块形态和生物学进行全面评估。
2019年,首次在人体内应用组合式IVUS-OCT导管54。
此外,2019年首次在人体内应用偏振敏感OCT成像系统,有望更好地描述斑块特征,并对其成分进行更详细的评估55。
近期还有两份报告研究了衰减补偿技术的疗效。衰减补偿技术是一种后处理方法,似乎能够增强OCT成像深度,并能更准确地评估严重病变段的斑块负荷56,57。这些报告强调了这种方法在评估严重病变段原位血管斑块面积方面的潜力,但也因支架段成像伪影,体现这种技术的重大局限性。
越来越多的证据显示局部血流动力学对动脉粥样硬化疾病进展和不稳定的影响。
2019年IBIS-4分析显示,使用计算流体动力学分析估算的切应力分布在预测动脉粥样硬化疾病的进展和斑块形态变化方面具有附加价值,而PROSPECT研究表明,通过处理虚拟组织学IVUS图像估算斑块应力,可以更准确地识别将来会引起事件的病变58,59。认识到局部血流动力学对原位血管和支架段动脉粥样硬化进展的重要性,发布的专家共识中描述了现有方法以及其对研究和未来临床实践的价值60。
结论
2019年发表的研究对不同治疗策略,新兴或现有设备的疗效以及冠脉生理学或血管内成像在PCI中的价值进行了研究,丰富了我们的理解并改进了阻塞性CAD患者的治疗。
STEMI患者应积极治疗,以完全血管重建为目标。相反,对于没有临床证据证明存在急性缺血的院外心脏骤停患者,最初的保守治疗似乎与早期的侵入性治疗同样有效。
有力的证据强调了DES的短期和长期疗效,而冠状动脉生理学的进展和基于图像的FFR计算方法的发展有望扩大其在指导血运重建中的应用。
越来越多的数据强调了血管内成像在指导PCI和评估病变病理方面的预后获益,而血管内成像和计算模型方面的进展有望更好地预测易损病变和有风险的患者,这些患者将受益于针对斑块演变的新疗法。
这些进展有望通过个性化药物治疗和侵入策略改善冠心病患者的手术结局和长期预后。

扫描上方二维码查阅原文
参考文献
1. Lemkes JS, Janssens GN, van der Hoeven NW, Jewbali LSD, Dubois EA, Meuwissen M, Rijpstra TA, Bosker HA, Blans MJ, Bleeker GB, Baak R, Vlachojannis GJ, Eikemans BJW, van der Harst P, van der Horst ICC, Voskuil M, van der Heijden JJ, Beishuizen A, Stoel M, Camaro C, van der Hoeven H, Henriques JP, Vlaar APJ, Vink MA, van den Bogaard B, Heestermans T, de Ruijter W, Delnoij TSR, Crijns H, Jessurun GAJ, Oemrawsingh PV, Gosselink MTM, Plomp K, Magro M, Elbers PWG, van de Ven PM, Oudemans-van Straaten HM, van Royen N. Coronary angiography after cardiac arrest without ST-segment elevation. N Engl J Med 2019;380:1397–1407.
2. Mehta SR, Wood DA, Storey RF, Mehran R, Bainey KR, Nguyen H, Meeks B, Di Pasquale G, Lopez-Sendon J, Faxon DP, Mauri L, Rao SV, Feldman L, Steg PG, Avezum A, Sheth T, Pinilla-Echeverri N, Moreno R, Campo G, Wrigley B, Kedev S, Sutton A, Oliver R, Rodes-Cabau J, Stankovic G, Welsh R, Lavi S, Cantor WJ, Wang J, Nakamya J, Bangdiwala SI, Cairns JA; COMPLETE Trial Steering Committee and Investigators. Complete revascularization with multivessel PCI for myocardial infarction. N Engl J Med 2019;381:1411–1421.
3. Patel KK, Spertus JA, Chan PS, Sperry BW, Thompson RC, Al Badarin F, Kennedy KF, Case JA, Courter S, Saeed IM, McGhie AI, Bateman TM. Extent of myocardial ischemia on positron emission tomography and survival benefit with early revascularization. J Am Coll Cardiol 2019;74:1645–1654.
4. Weintraub WS, Hartigan PM, Mancini GBJ, Teo KK, Maron DJ, Spertus JA, Chaitman BR, Shaw LJ, Berman D, Boden WE. Effect of coronary anatomy and myocardial ischemia on long-term survival in patients with stable ischemic heart disease. Circ Cardiovasc Qual Outcomes 2019;12:e005079.
5. Hochman JS. International Study Of Comparative Health Effectiveness With Medical And Invasive Approaches (ISCHEMIA): primary report of clinical out-comes. American Heart Association Scientific Sessions 2019, Philadelphia 2019: Nov 16–18.
6. Panza JA, Ellis AM, Al-Khalidi HR, Holly TA, Berman DS, Oh JK, Pohost GM, Sopko G, Chrzanowski L, Mark DB, Kukulski T, Favaloro LE, Maurer G, Farsky PS, Tan RS, Asch FM, Velazquez EJ, Rouleau JL, Lee KL, Bonow RO. Myocardial viability and long-term outcomes in ischemic cardiomyopathy. N Engl J Med 2019;381:739–748.
7. Neumann F-J, Sousa-Uva M, Ahlsson A, Alfonso F, Banning AP, Benedetto U, Byrne RA, Collet J-P, Falk V, Head SJ, Ju¨ ni P, Kastrati A, Koller A, Kristensen SD, Niebauer J, Richter DJ, Seferovi´c PM, Sibbing D, Stefanini GG, Windecker S, Yadav R, Zembala MO; ESC Scientific Document Group. 2018 ESC/EACTS Guidelines on myocardial revascularization. Eur Heart J 2019;40:87–165.
8. Farkouh ME, Domanski M, Dangas GD, Godoy LC, Mack MJ, Siami FS, Hamza TH, Shah B, Stefanini GG, Sidhu MS, Tanguay J-F, Ramanathan K, Sharma SK, French J, Hueb W, Cohen DJ, Fuster V, Sharma SK, Zazif TN, Thai H, Shah B, Ramanathan K, Tanguay J-F, Ramanathan K, Burton JR, Schampaert E, Escobedo J, Dubois-Rande J-L, Macaya C, Carrie D, Richardt G, Roguin A, Lotan C, Kornowski R, Presbitero P, Hueb W, Sousa JE, Vela´squez JG, Rodriguez A, Devlin G, French JK, Kaul U; FREEDOM Follow-On Study Investigators. Long-term survival following multivessel revascularization in patients with diabetes: the FREEDOM Follow-On Study. J Am Coll Cardiol 2019;73:629–638.
9. Thuijs DJFM, Kappetein AP, Serruys PW, Mohr F-W, Morice M-C, Mack MJ, Holmes DR, Curzen N, Davierwala P, Noack T, Milojevic M, Dawkins KD, da Costa BR, Ju¨ ni P, Head SJ; SYNTAX Extended Survival Investigators. Percutaneous coronary intervention versus coronary artery bypass grafting in patients with three-vessel or left main coronary artery disease: 10-year follow-up of the multicentre randomised controlled SYNTAX trial. Lancet 2019;394:1325–1334.
10. Stone GW, Kappetein AP, Sabik JF, Pocock SJ, Morice MC, Puskas J, Kandzari DE, Karmpaliotis D, Brown WM 3rd, Lembo NJ, Banning A, Merkely B, Horkay F, Boonstra PW, van Boven AJ, Ungi I, Bogats G, Mansour S, Noiseux N, Sabate M, Pomar J, Hickey M, Gershlick A, Buszman PE, Bochenek A, Schampaert E, Page P, Modolo R, Gregson J, Simonton CA, Mehran R, Kosmidou I, Genereux P, Crowley A, Dressler O, Serruys PW; EXCEL Trial Investigators. Five-year out-comes after PCI or CABG for left main coronary disease. N Engl J Med 2019; 381:1820–1830.
11. Stone GW, Sabik JF, Serruys PW, Simonton CA, Genereux P, Puskas J, Kandzari DE, Morice MC, Lembo N, Brown WM 3rd, Taggart DP, Banning A, Merkely B, Horkay F, Boonstra PW, van Boven AJ, Ungi I, Bogats G, Mansour S, Noiseux N, Sabate M, Pomar J, Hickey M, Gershlick A, Buszman P, Bochenek A, Schampaert E, Page P, Dressler O, Kosmidou I, Mehran R, Pocock SJ, Kappetein AP; EXCEL Trial Investigators. Everolimus-eluting stents or bypass surgery for left main cor- onary artery disease. N Engl J Med 2016;375:2223–2235.
12. Milojevic M, Serruys PW, Sabik JF 3rd, Kandzari DE, Schampaert E, van Boven AJ, Horkay F, Ungi I, Mansour S, Banning AP, Taggart DP, Sabate M, Gershlick AH, Bochenek A, Pomar J, Lembo NJ, Noiseux N, Puskas JD, Crowley A, Kosmidou I, Mehran R, Ben-Yehuda O, Genereux P, Pocock SJ, Simonton CA, Stone GW, Kappetein AP. Bypass surgery or stenting for left main coronary artery disease in patients with diabetes. J Am Coll Cardiol 2019;73:1616–1628.
13. Chen X, Li X, Zhang JJ, Han Y, Kan J, Chen L, Qiu C, Santoso T, Paiboon C, Kwan TW, Sheiban I, Leon MB, Stone GW, Chen SL; DKCRUSH-V Investigators.3-year outcomes of the DKCRUSH-V trial comparing DK crush with provisional stenting for left main bifurcation lesions. JACC Cardiovasc Interv 2019;12:1927–1937.
14. Banning AP, Lassen JF, Burzotta F, Lefevre T, Darremont O, Hildick-Smith D, Louvard Y, Stankovic G. Percutaneous coronary intervention for obstructive bi- furcation lesions: the 14th consensus document from the European Bifurcation Club. EuroIntervention 2019;15:90–98.
15. Galassi AR, Werner GS, Boukhris M, Azzalini L, Mashayekhi K, Carlino M, Avran A, Konstantinidis NV, Grancini L, Bryniarski L, Garbo R, Bozinovic N, Gershlick AH, Rathore S, Di Mario C, Louvard Y, Reifart N, Sianos G. Percutaneous recan- alisation of chronic total occlusions: 2019 consensus document from the EuroCTO Club. EuroIntervention 2019;15:198–208.
16. Lee SW, Lee PH, Ahn JM, Park DW, Yun SC, Han S, Kang H, Kang SJ, Kim YH, Lee CW, Park SW, Hur SH, Rha SW, Her SH, Choi SW, Lee BK, Lee NH, Lee JY, Cheong SS, Kim MH, Ahn YK, Lim SW, Lee SG, Hiremath S, Santoso T, Udayachalerm W, Cheng JJ, Cohen DJ, Muramatsu T, Tsuchikane E, Asakura Y, Park SJ. Randomized trial evaluating percutaneous coronary intervention for the treatment of chronic total occlusion. Circulation 2019;139:1674–1683.
17. Buiten RA, Ploumen EH, Zocca P, Doggen CJM, van der Heijden LC, Kok MM, Danse PW, Schotborgh CE, Scholte M, de Man F, Linssen GCM, von Birgelen C. Outcomes in patients treated with thin-strut, very thin-strut, or ultrathin-strut drug-eluting stents in small coronary vessels: a prespecified analysis of the randomized BIO-RESORT trial. JAMA Cardiol 2019;4:659–669.
18. Kastrati A, Mehilli J, Dirschinger J, Dotzer F, Schu¨ Hlen H, Neumann F-J, Fleckenstein M, Pfafferott C, Seyfarth M, Scho¨ Mig A, Intracoronary stenting and angiographic results: strut thickness effect on restenosis outcome (ISAR- STEREO) trial. Circulation 2001;103:2816–2821.
19. Cassese S, Byrne RA, Schulz S, Hoppman P, Kreutzer J, Feuchtenberger A, Ibrahim T, Ott I, Fusaro M, Schunkert H, Laugwitz KL, Kastrati A. Prognostic role of restenosis in 10 004 patients undergoing routine control angiography after coronary stenting. Eur Heart J 2015;36:94–99.
20. Giacoppo D, Alfonso F, Xu B, Claessen B, Adriaenssens T, Jensen C, Perez- Vizcayno MJ, Kang DY, Degenhardt R, Pleva L, Baan J, Cuesta J, Park DW, Schunkert H, Colleran R, Kukla P, Jimenez-Quevedo P, Unverdorben M, Gao R, Naber CK, Park SJ, Henriques JPS, Kastrati A, Byrne RA. Paclitaxel-coated bal- loon angioplasty vs. drug-eluting stenting for the treatment of coronary in-stent restenosis: a comprehensive, collaborative, individual patient data meta-analysis of 10 randomized clinical trials (DAEDALUS study). Eur Heart J 2019;doi: 10.1093/eurheartj/ehz594.
21. Raber L, Yamaji K, Kelbaek H, Engstrom T, Baumbach A, Roffi M, von Birgelen C, Taniwaki M, Moschovitis A, Zaugg S, Ostojic M, Pedrazzini G, Karagiannis-Voules DA, Luscher TF, Kornowski R, Tuller D, Vukcevic V, Heg D, Windecker S. Five- year clinical outcomes and intracoronary imaging findings of the COMFORTABLE AMI trial: randomized comparison of biodegradable polymer- based biolimus-eluting stents with bare-metal stents in patients with acute ST- segment elevation myocardial infarction. Eur Heart J 2019;40:1909–1919.
22. Iglesias JF, Muller O, Heg D, Roffi M, Kurz DJ, Moarof I, Weilenmann D, Kaiser C, Tapponnier M, Stortecky S, Losdat S, Eeckhout E, Valgimigli M, Odutayo A, Zwahlen M, Juni P, Windecker S, Pilgrim T. Biodegradable polymer sirolimus- eluting stents versus durable polymer everolimus-eluting stents in patients with ST-segment elevation myocardial infarction (BIOSTEMI): a single-blind, prospect- ive, randomised superiority trial. Lancet 2019;394:1243–1253.
23. Zaman A, de Winter RJ, Kogame N, Chang CC, Modolo R, Spitzer E, Tonino P, Hofma S, Zurakowski A, Smits PC, Prokopczuk J, Moreno R, Choudhury A, Petrov I, Cequier A, Kukreja N, Hoye A, Iniguez A, Ungi I, Serra A, Gil RJ, Walsh S, Tonev G, Mathur A, Merkely B, Colombo A, Ijsselmuiden S, Soliman O, Kaul U, Onuma Y, Serruys PW; TALENT trial investigators. Safety and efficacy of a sirolimus-eluting coronary stent with ultra-thin strut for treatment of athero- sclerotic lesions (TALENT): a prospective multicentre randomised controlled trial. Lancet 2019;393:987–997.
24. Stone GW, Kimura T, Gao R, Kereiakes DJ, Ellis SG, Onuma Y, Chevalier B, Simonton C, Dressler O, Crowley A, Ali ZA, Serruys PW. Time-varying out- comes with the absorb bioresorbable vascular scaffold during 5-year follow-up: a systematic meta-analysis and individual patient data pooled study. JAMA Cardiol 2019;doi: 10.1001/jamacardio.2019.4101.
25. Bourantas CV, Zhang YJ, Garg S, Iqbal J, Valgimigli M, Windecker S, Mohr FW, Silber S, Vries T, Onuma Y, Garcia-Garcia HM, Morel MA, Serruys PW. Prognostic implications of coronary calcification in patients with obstructive cor-onary artery disease treated by percutaneous coronary intervention: a patient-level pooled analysis of 7 contemporary stent trials. Heart 2014;100:1158–1164.
26. Dini CS, Tomberli B, Mattesini A, Ristalli F, Valente S, Stolcova M, Meucci F, Baldereschi G, Fanelli F, Shlofmitz RA, Ali ZA, Di Mario C. Intravascular litho-tripsy for calcific coronary and peripheral artery stenoses. EuroIntervention 2019; 15:714–721.
27. Brinton TJ, Ali ZA, Hill JM, Meredith IT, Maehara A, Illindala U, Lansky A, Gotberg M, Van Mieghem NM, Whitbourn R, Fajadet J, Di Mario C. Feasibility of shockwave coronary intravascular lithotripsy for the treatment of calcified cor-onary stenoses. Circulation 2019;139:834–836.
28. Ali ZA, Nef H, Escaned J, Werner N, Banning AP, Hill JM, De Bruyne B, Montorfano M, Lefevre T, Stone GW, Crowley A, Matsumura M, Maehara A, Lansky AJ, Fajadet J, Di Mario C. Safety and effectiveness of coronary intravascu-lar lithotripsy for treatment of severely calcified coronary stenoses: the disrupt CAD II study. Circ Cardiovasc Interv 2019;12:e008434.
29. Wilson SJ, Spratt JC, Hill J, Spence MS, Cosgrove C, Jones J, Strange JW, Halperin H, Walsh SJ, Hanratty CG. Coronary intravascular lithotripsy is associ-ated with a high incidence of “shocktopics” and asynchronous cardiac pacing. EuroIntervention 2019;doi: 10.4244/EIJ-D-19-00484.
30. Mehran R, Baber U, Sharma SK, Cohen DJ, Angiolillo DJ, Briguori C, Cha JY, Collier T, Dangas G, Dudek D, Dzavik V, Escaned J, Gil R, Gurbel P, Hamm CW, Henry T, Huber K, Kastrati A, Kaul U, Kornowski R, Krucoff M, Kunadian V, Marx SO, Mehta SR, Moliterno D, Ohman EM, Oldroyd K, Sardella G, Sartori S, Shlofmitz R, Steg PG, Weisz G, Witzenbichler B, Han YL, Pocock S, Gibson CM.Ticagrelor with or without aspirin in high-risk patients after PCI. N Engl J Med 2019;381:2032–2042.
31. Costa F, Van Klaveren D, Feres F, James S, Raber L, Pilgrim T, Hong MK, Kim HS, Colombo A, Steg PG, Bhatt DL, Stone GW, Windecker S, Steyerberg EW, Valgimigli M; PRECISE-DAPT Study Investigators. Dual antiplatelet therapy dur-ation based on ischemic and bleeding risks after coronary stenting. J Am Coll Cardiol 2019;73:741–754.
32. Lopes et al. Antithrombotic Therapy after Acute Coronary Syndrome or PCI in Atrial Fibrillation. N Engl J Med 2019;380:1509–1524.
33. Vranckx P, Valgimigli M, Eckardt L, Tijssen J, Lewalter T, Gargiulo G, Batushkin V, Campo G, Lysak Z, Vakaliuk I, Milewski K, Laeis P, Reimitz PE, Smolnik R, Zierhut W, Goette A. Edoxaban-based versus vitamin K antagonist-based antith-rombotic regimen after successful coronary stenting in patients with atrial fibrilla-tion (ENTRUST-AF PCI): a randomised, open-label, phase 3b trial. Lancet 2019;394:1335–1343.
34. Gargiulo G, Goette A, Tijssen J, Eckardt L, Lewalter T, Vranckx P, Valgimigli M. Safety and efficacy outcomes of double vs. triple antithrombotic therapy in patients with atrial fibrillation following percutaneous coronary intervention: a systematic review and meta-analysis of non-vitamin K antagonist oral anticoagulant-based randomized clinical trials. Eur Heart J 2019;40:3757–3767.
35. Hakeem A, Ghosh B, Shah K, Agarwal S, Kasula S, Hacioglu Y, Bhatti S, Ahmed Z, Uretsky B. Incremental prognostic value of post-intervention Pd/Pa in patients undergoing ischemia-driven percutaneous coronary intervention. JACC Cardiovasc Interv 2019;12:2002–2014.
36. Jeremias A, Davies JE, Maehara A, Matsumura M, Schneider J, Tang K, Talwar S, Marques K, Shammas NW, Gruberg L, Seto A, Samady H, Sharp A, Ali ZA, Mintz G, Patel M, Stone GW. Blinded physiological assessment of residual ische-mia after successful angiographic percutaneous coronary intervention: the DEFINE PCI study. JACC Cardiovasc Interv 2019;12:1991–2001.
37. Warisawa T, Cook CM, Howard JP, Ahmad Y, Doi S, Nakayama M, Goto S, Yakuta Y, Karube K, Shun-Shin MJ, Petraco R, Sen S, Nijjer S, Al Lamee R,Ishibashi Y, Matsuda H, Escaned J, di Mario C, Francis DP, Akashi YJ, Davies JE. Physiological pattern of disease assessed by pressure-wire pullback has an influ-ence on fractional flow reserve/instantaneous wave-free ratio discordance. Circ Cardiovasc Interv 2019;12:e007494.
38. Lee SH, Choi KH, Lee JM, Hwang D, Rhee TM, Park J, Kim HK, Cho YK, Yoon HJ, Park J, Song YB, Hahn JY, Doh JH, Nam CW, Shin ES, Hur SH, Koo BK. Physiologic characteristics and clinical outcomes of patients with discordance be-tween FFR and iFR. JACC Cardiovasc Interv 2019;12:2018–2031.
39. Sen S, Ahmad Y, Dehbi HM, Howard JP, Iglesias JF, Al-Lamee R, Petraco R, Nijjer S, Bhindi R, Lehman S, Walters D, Sapontis J, Janssens L, Vrints CJ, Khashaba A,Laine M, Van Belle E, Krackhardt F, Bojara W, Going O, Harle T, Indolfi C, Niccoli G, Ribichini F, Tanaka N, Yokoi H, Takashima H, Kikuta Y, Erglis A, Vinhas H, Silva PC, Baptista SB, Alghamdi A, Hellig F, Koo BK, Nam CW, Shin ES, Doh JH, Brugaletta S, Alegria-Barrero E, Meuwissen M, Piek JJ, van Royen N, Sezer M, Di Mario C, Gerber RT, Malik IS, Sharp ASP, Talwar S, Tang K, Samady H, Altman J, Seto AH, Singh J, Jeremias A, Matsuo H, Kharbanda RK, Patel MR,Serruys P, Escaned J, Davies JE. Clinical events after deferral of LAD revasculari- zation following physiological coronary assessment. J Am Coll Cardiol 2019;73: 444–453.
40. DEFINE-FLAIR Trial Investigators, Lee JM, Choi KH, Koo BK, Dehbi HM, Doh JH, Nam CW, Shin ES, Cook CM, Al-Lamee R, Petraco R, Sen S, Malik IS, Nijjer SS, Mejia-Renteria H, Alegria-Barrero E, Alghamdi A, Altman J, Baptista SB, Bhindi R, Bojara W, Brugaletta S, Silva PC, Di Mario C, Erglis A, Gerber RT, Going O, Harle T, Hellig F, Indolfi C, Janssens L, Jeremias A, Kharbanda RK, Khashaba A, Kikuta Y, Krackhardt F, Laine M, Lehman SJ, Matsuo H, Meuwissen M, Niccoli G, Piek JJ, Ribichini F, Samady H, Sapontis J, Seto AH, Sezer M, Sharp ASP, Singh J, Takashima H, Talwar S, Tanaka N, Tang K, Van Belle E, van Royen N, Vinhas H, Vrints CJ, Walters D, Yokoi H, Samuels B, Buller C, Patel MR, Serruys P, Escaned J, Davies JE. Comparison of major adverse cardiac events be- tween instantaneous wave-free ratio and fractional flow reserve-guided strategy in patients with or without type 2 diabetes: a secondary analysis of a randomized clinical trial. JAMA Cardiol 2019;doi: 10.1001/jamacardio.2019.2298.
41. Masdjedi K, van Zandvoort LJC, Balbi MM, Gijsen FJH, Ligthart JMR, Rutten MCM, Lemmert ME, Wilschut J, Diletti R, De Jaegere P, Zijlstra F, Van Mieghem NM, Daemen J. Validation of 3-dimensional quantitative coronary angiography based software to calculate fractional flow reserve: Fast Assessment of STenosis severity (FAST)-study. EuroIntervention 2019;doi: 10.4244/EIJ-D-19-00466.
42. Yu W, Huang J, Jia D, Chen S, Raffel OC, Ding D, Tian F, Kan J, Zhang S, Yan F, Chen Y, Bezerra HG, Wijns W, Tu S. Diagnostic accuracy of intracoronary op- tical coherence tomography-derived fractional flow reserve for assessment of coronary stenosis severity. EuroIntervention 2019;15:189–197.
43. Gao XF, Wang ZM, Wang F, Gu Y, Ge Z, Kong XQ, Zuo GF, Zhang JJ, Chen SL. Intravascular ultrasound guidance reduces cardiac death and coronary revascula- rization in patients undergoing drug-eluting stent implantation: results from a meta-analysis of 9 randomized trials and 4724 patients. Int J Cardiovasc Imaging 2019;35:239–247.
44. Hong MK. IVUS-XPL: 5-year outcomes from a randomized trial of intravascular ultrasound-guided vs. angiography-guided PCI of long coronary lesions. FORZA: A Randomized Trial of Fractional Flow Reserve vs Optical Coherence Tomography to Guide Revascularization of Intermediate Coronary Stenoses. Transcatheter Cardiovascular. Therapeutics; San Francisco, CA; 25–29 Sept 2019.
45. Burzotta F. Transcatheter Cardiovascular Therapeutics; San Francisco, CA; 25– 29 Sept 2019.
46. Johnson TW, Raber L, di Mario C, Bourantas C, Jia H, Mattesini A, Gonzalo N, de la Torre Hernandez JM, Prati F, Koskinas K, Joner M, Radu MD, Erlinge D, Regar E, Kunadian V, Maehara A, Byrne RA, Capodanno D, Akasaka T, Wijns W, Mintz GS, Guagliumi G. Clinical use of intracoronary imaging. Part 2: acute cor- onary syndromes, ambiguous coronary angiography findings, and guiding inter- ventional decision-making: an expert consensus document of the European Association of Percutaneous Cardiovascular Interventions. Eur Heart J 2019;40: 2566–2584.
47. Knuuti J, Wijns W, Saraste A, Capodanno D, Barbato E, Funck-Brentano C, Prescott E, Storey RF, Deaton C, Cuisset T, Agewall S, Dickstein K, Edvardsen T, Escaned J, Gersh BJ, Svitil P, Gilard M, Hasdai D, Hatala R, Mahfoud F, Masip J, Muneretto C, Valgimigli M, Achenbach S, Bax JJ; ESC Scientific Document Group. 2019 ESC Guidelines for the diagnosis and management of chronic coronary syn- dromes. Eur Heart J 2019;doi:10.1093/eurheartj/ehz425.
48. Nagel E, Greenwood JP, McCann GP, Bettencourt N, Shah AM, Hussain ST, Perera D, Plein S, Bucciarelli-Ducci C, Paul M, Westwood MA, Marber M, Richter WS, Puntmann VO, Schwenke C, Schulz-Menger J, Das R, Wong J, Hausenloy DJ, Steen H, Berry C; MR-INFORM Investigators.Magnetic resonance perfusion or fractional flow reserve in coronary disease. N Engl J Med 2019;380: 2418–2428.
49. Calvino-Santos R, Estevez-Loureiro R, Peteiro-Vazquez J, Salgado-Fernandez J, Rodriguez-Vilela A, Franco-Gutierrez R, Bouzas-Mosquera A, Rodriguez-Fernandez JA, Mesias-Prego A, Gonzalez-Juanatey C, Aldama-Lopez G, Pinon-Esteban P, Flores-Rios X, Soler-Martin R, Seoane-Pillado T, Vazquez-Gonzalez N, Muniz J, Vazquez-Rodriguez JM. Angiographically guided complete revascularization versus selective stress echocardiography-guided revascularization in patients with ST-segment-elevation myocardial infarction and multivessel disease: the CROSS-AMI randomized clinical trial. Circ Cardiovasc Interv 2019;12:e007924.
50. Stone GW, Maehara A, Lansky AJ, de Bruyne B, Cristea E, Mintz GS, Mehran R, McPherson J, Farhat N, Marso SP, Parise H, Templin B, White R, Zhang Z, Serruys PW, Investigators P. A prospective natural-history study of coronary ath-erosclerosis. N Engl J Med 2011;364:226–235.
51. Bourantas CV, Garcia-Garcia HM, Torii R, Zhang YJ, Westwood M, Crake T, Serruys PW. Vulnerable plaque detection: an unrealistic quest or a feasible ob-jective with a clinical value?. Heart 2016;102:581–589.
52. Waksman R, Di Mario C, Torguson R, Ali ZA, Singh V, Skinner WH, Artis AK, Cate TT, Powers E, Kim C, Regar E, Wong SC, Lewis S, Wykrzykowska J, Dube S, Kazziha S, van der Ent M, Shah P, Craig PE, Zou Q, Kolm P, Brewer HB, Garcia-Garcia HM, Samady H, Tobis J, Zainea M, Leimbach W, Lee D, Lalonde T, Skinner W, Villa A, Liberman H, Younis G, de Silva R, Diaz M, Tami L, Hodgson J, Raveendran G, Goswami N, Arias J, Lovitz L, Carida Ii R, Potluri S, Prati F, Erglis A, Pop A, McEntegart M, Hudec M, Rangasetty U, Newby D. Identification of patients and plaques vulnerable to future coronary events with near-infrared spectroscopy intravascular ultrasound imaging: a prospective, cohort study. Lancet 2019;394:1629–1637.
53. Prati F, Romagnoli E, Gatto L, La Manna A, Burzotta F, Ozaki Y, Marco V, Boi A, Fineschi M, Fabbiocchi F, Taglieri N, Niccoli G, Trani C, Versaci F, Calligaris G, Ruscica G, Di Giorgio A, Vergallo R, Albertucci M, Biondi-Zoccai G, Tamburino C, Crea F, Alfonso F, Arbustini E, Investigators C. Relationship between coronary plaque morphology of the left anterior descending artery and 12 months clinical outcome: the CLIMA study. Eur Heart J 2019;doi:10.1093/eurheartj/ehz425.
54. Sheth TN, Pinilla-Echeverri N, Mehta SR, Courtney BK. First-in-human images of coronary atherosclerosis and coronary stents using a novel hybrid intravascular ultrasound and optical coherence tomographic catheter. JACC Cardiovasc Interv 2018;11:2427–2430.
55. Otsuka K, Villiger M, Karanasos A, van Zandvoort LJC, Doradla P, Ren J, Lippok N, Daemen J, Diletti R, van Geuns RJ, Zijlstra F, van Soest G, Dijkstra J, Nadkarni SK, Regar E, Bouma BE. Intravascular polarimetry in patients with coronary ar-tery disease. JACC Cardiovasc Imaging 2019;doi: 10.1016/j.jcmg.2019.06.015.
56. Gerbaud E, Weisz G, Tanaka A, Luu R, Osman H, Baldwin G, Coste P, Cognet L, Waxman S, Zheng H, Moses JW, Mintz GS, Akasaka T, Maehara A, Tearney GJ. Plaque burden can be assessed using intravascular optical coherence tomography and a dedicated automated processing algorithm: a comparison study with intra-vascular ultrasound. Eur Heart J Cardiovasc Imaging 2019;doi: 10.1093/ehjci/jez185.
57. Ramasamy A, Ng J, White S, Johnson TW, Foin N, Girard MJA, Dijkstra J, Amersey R, Scoltock S, Koganti S, Jones D, Jin C, Raber L, Serruys PW, Torii R, Crake T, Rakhit R, Baumbach A, Mathur A, Bourantas CV. Efficacy and reprodu-cibility of attenuation-compensated optical coherence tomography for assessing external elastic membrane border and plaque composition in native and stented segments—an in vivo and histology-based study. Circ J 2019;doi:10.1253/circj.CJ-19-0630.
58. Bourantas CV, Raber L, Sakellarios A, Ueki Y, Zanchin T, Koskinas KC, Yamaji K, Taniwaki M, Heg D, Radu MD, Papafaklis MI, Kalatzis F, Naka KK, Fotiadis DI, Mathur A, Serruys PW, Michalis LK, Garcia-Garcia HM, Karagiannis A, Windecker S. Utility of multimodality intravascular imaging and the local hemo-dynamic forces to predict atherosclerotic disease progression. JACC Cardiovasc Imaging 2019;doi: 10.1016/j.jcmg.2019.02.026.
59. Costopoulos C, Maehara A, Huang Y, Brown AJ, Gillard JH, Teng Z, Stone GW, Bennett MR. Heterogeneity of plaque structural stress is increased in plaques leading to MACE: insights from the PROSPECT study. JACC Cardiovasc Imaging 2019;doi: 10.1016/j.jcmg.2019.05.024.
60. Gijsen F, Katagiri Y, Barlis P, Bourantas C, Collet C, Coskun U, Daemen J, Dijkstra J, Edelman E, Evans P, van der Heiden K, Hose R, Koo BK, Krams R, Marsden A, Migliavacca F, Onuma Y, Ooi A, Poon E, Samady H, Stone P, Takahashi K, Tang D, Thondapu V, Tenekecioglu E, Timmins L, Torii R, Wentzel J, Serruys P. Expert recommendations on the assessment of wall shear stress in human coronary arteries: existing methodologies, technical considerations, and clinical applications. Eur Heart J 2019;40:3421–3433.