
目前,经导管主动脉瓣置换术(TAVR)治疗重度主动脉瓣狭窄(AS)在我国的不少中心已经开展,越来越多经验丰富的术者也应运而生。尽管不可能完全避免,TAVR术后的主动脉瓣反流AR是每个术者都不愿见到的并发症。但是似乎每个术者都有这样的经历,在TAVR手术后存在少量的AR时,我们会回顾术前的主动脉造影及超声影像,如果术前也有一定量主动脉瓣反流,我们通常会认为这样的结果应该也能接受。
实际上,我们内心当中已经接受了这样的概念:术前即合并有主动脉瓣反流的AS患者比起初没有AR的AS患者应该更能耐受TAVR术后发生的残余瓣周漏。当然,从生理上讲,它确实能讲的通。术前单纯AS患者往往左心室僵硬,小而肥厚。对任何容积负荷没有适应,即使较轻的AR也可以使左心室舒张末期压力不成比例地增加,导致其不能耐受,以至于术后症状改善不明显;相反,如果患者术前存在AR,对术后瓣周漏的耐受也许会更好。但事实真的如此吗?
最新一期美国知名杂志 JACC cardiovascular intervention就发表了这样一篇研究:Outcomes of Transcatheter Aortic Valve Replacement in Mixed Aortic Valve Disease (混合性主动脉瓣疾病TAVR治疗的预后),回答了术前AR存在与否对TAVR预后的影响。
首先让我们来简要的了解一下这个研究 。

背景介绍:
经导管主动脉瓣置换术(TAVR)的问世,彻底改变了主动脉瓣疾病的传统治疗方法。目前,TAVR不但成为具有高手术风险的症状性严重主动脉瓣狭窄(AS)患者的主要治疗手段,其适应证已扩展到包括具有中等手术风险,甚至更为低危的患者。对于那些患有严重AS并伴有主动脉关闭不全AR的患者(即混合性AV病[MAVD]),TAVR也已成为一种治疗选择。然而,关于MAVD患者TAVR的总体安全性和有效性,尚缺乏可靠的数据,也难以提出循证医学的建议。有证据表明,MAVD比单纯的AS病程发展更为迅速,也需要更为积极有效的治疗策略。本研究的目的比较接受TAVR的MVAD患者和单纯AS患者的术后结局,并着重分析既往AR对预后的影响。
试验设计:
这是一项在美国克利夫兰诊所进行的单中心,回顾性观察性研究。纳入2014年1月至2017年12月期间接受股动脉路径的TAVR的AS患者。有外科手术或AV置换史的患者被排除在外。根据TAVR前AR的存在与否将患者进一步分为两组,纯AS(无或微量AR)和MVAD(伴有轻,中或重度AR的AS)。所有患者在TAVR之前均接受了超声心动图检查,绝大多数患者在手术后接受了重复超声心动图检查。主要终点是全因死亡率。次要临床终点根据Valve Academic Research Consortium-2标准确定的出血和血管并发症、中风、肾脏损伤、瓣膜功能障碍以及早期的安全性(TAVR 30天内)和临床的有效性(30天后)。超声心动图变量包括:AR严重程度、左心室射血分数、AV平均梯度、AV峰值梯度、左心室流出道[LVOT]平均流速、AV平均流速、AV速度-时间积分、面积、AV指数、LVOT直径、LVOT每搏量和LVOT搏动量指标。
试验采用倾向得分匹配用于排除可能的混杂因素,使用了多元逻辑回归分析来评估患者特征(包括TAVR术前AR)与死亡率之间的关联。
研究共1,133例患者入选。随访时间平均为27个月(18 -38个月)。其中,有688例(61%)患有MAVD。平均年龄83岁(76- 87岁),该队列中有43%是女性。MAVD组的卒中或短暂性脑缺血病史者更高。
TAVR后AR发生的比率
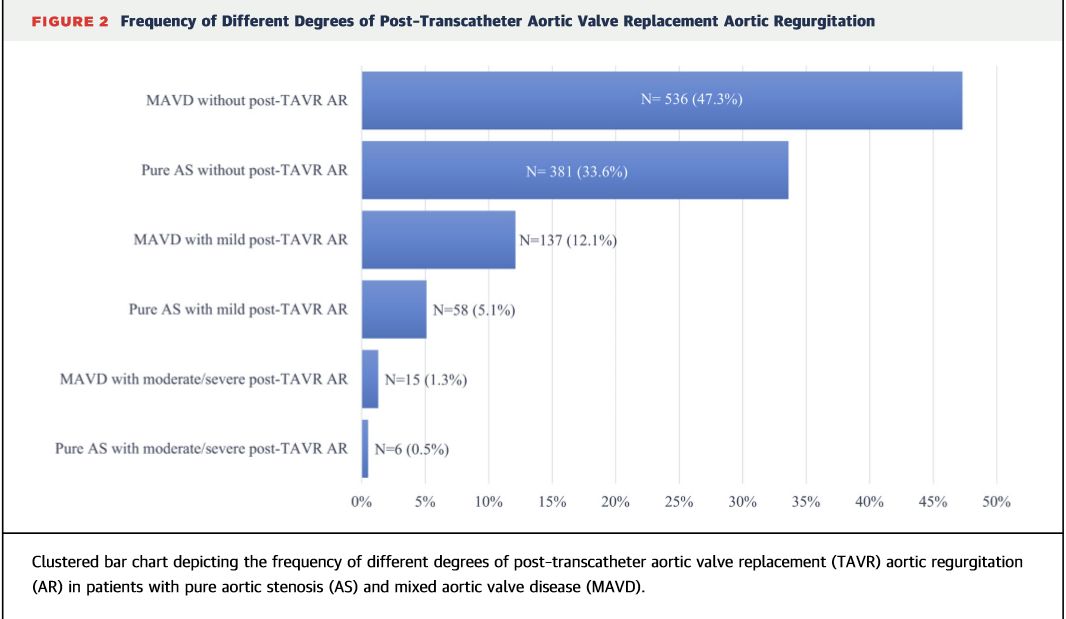
TAVR后大多数(81%)患者没有AR,17%轻度,2%中度,<1%的患者的TAVR后发生严重AR。MAVD组的TAVR后AR患病率较单纯AS高(22.1%比14.4%;P= 0.001)。
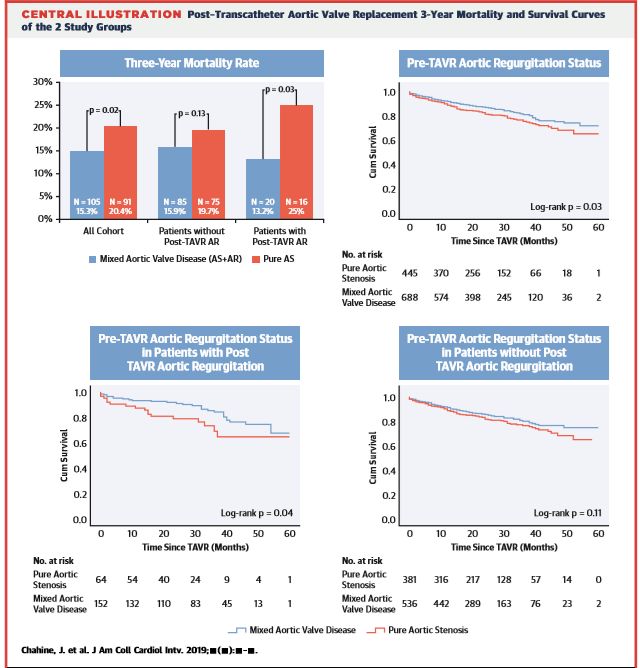
主要终点事件:生存率的比较
Kaplan-Meier曲线显示:MAVD组的患者的总生存期比纯AS组的患者更好(p = 0.03), 在TAVR并发AR的患者中,MAVD组的患者存活率更高(p= 0.04)。相反,在TAVR后无AR的患者中,TAVR前并发AR不能改善生存率(p = 0.11)。此外,还发现MAVD患者的3年总死亡率降低,在发生TAVR后AR的患者中死亡率下降(p = 0.03) 。
两组之间的次要结局差异无统计学意义。术后30天,纯AS组再充血性心力衰竭或瓣膜相关症状再入院率稍高,但未达到显着性差异水平(10.3% vs.14.2%;p = 0.051)。有严重威胁生命的出血发生率在两组之间无显着统计学差异(MAVD组为17.4%,纯AS组为18.7%;p = 0.6)。复合终点(TAVR后30天内的早期安全终点和TAVR后30天内的临床疗效终点)无差异(分别为p = 0.12和p = 0.21)。
文中的结论:
1)与纯AS组相比,MAVD组的患者长期累积生存率更高。
2)在发生TAVR后AR的患者中,MAVD组的患者存活率更高。相反,在没有发生TAVR后AR的患者中,两组之间的死亡率没有差异。
3)次要结果两组之间(TAVR后30天内和30天内)无统计学可比差异。
TAVR相关不良结局的主要原因之一是TAVR后瓣周关闭不全(PVR)的发展, TAVR 术后 瓣周漏(PVR)的存在已被证明是短期和长期死亡率增加的独立预测因子。单纯AS的TAVR后中重度PVR的发生率范围为6%至21%,具体取决于所用瓣膜系统的类型(球囊扩张型与自膨胀式),所用评估方式(经胸超声心动图,经食道超声心动图,DSA),评估时间(植入后立即,出院前30天)等。在此研究中,纯AS中TAVR后PVR的发生率约为6%(轻度AR为5%,中度或重度AR为0.5%),与先前的报道一致。
MAVD患者的主动脉瓣和左心室的解剖结构与单纯AS患者不同。后者由于压力负荷过重,引起左心室肥大及随后的舒张功能障碍,但预先存在的AR会导致容量超负荷,从而导致左心室扩张和离心性肥大。
在本研究中,尽管MAVD组TAVR后AR的总体发生率较高(22.1%vs. 14%; p = 0.001),但预后反而不差,而纯AS术后PVR预后较差。 可能的解释为: 在患有AR的MAVD患者中,左心室已经适应了容量超负荷而进行了重塑,从而使这些患者更容易耐受TAVR后AR。相反,纯AS患者左心室肥厚,顺应性下降,使其不太可能耐受TAVR后AR。 所以本研究中在TAVR后发生AR 的患者中MAVD组观察到的更好结果,而在未发生TAVR后AR患者中,MAVD患者中未观察到此中差异。
来自于英国布莱顿皇家萨塞克斯郡医院的David Hildick-Smith 教授发表述评指出:

将TAVR后发生的轻度AR与术前AR相关联在临床上有一定的重要性。根据本文的建议,如果患者术前已经存在AR,TAVR术后发生AR可以有更宽的自由度。
举个例子来讲,在尝试是否给予进一步扩张时,要考虑其相关的额外风险。其实球囊后扩张也并非万无一失,后扩张可能带来瓣环撕裂,栓塞,中风或冠状动脉闭塞的风险。尽管这些风险可能很小,但如果发生,大多数术者都会对此铭记在心,从而后悔当时对后扩张的选择。
我们都知道,TAVR术后避免AR发生非常重要,残留AR的患者症状缓解有限,寿命也会受到影响。但是我们有时无法使患者提供最完美的结果,是否要进行后扩,有诸多的考虑因素,目前的考虑因素之一是预先存在的AR的程度。
█ 参考文献:
1. Chahine J, Kadri AN, Gajulapalli RD, et al. Out- comes of transcatheter aortic valve replacement in mixed aortic valve disease. J Am Coll Cardiol Intv 2019:XX:xxx–xx.
1. Otto CM, Kumbhani DJ, Alexander KP, et al. 2017 ACC expert consensus decision pathway for transcatheter aortic valve replacement in the management of adults with aortic stenosis: a report of the American College of Cardiology Task Force>
2. Grover FL, Vemulapalli S, Carroll JD, et al. 2016 annual report of the Society of Thoracic Surgeons/ American College of Cardiology Transcatheter Valve Therapy Registry. J Am Coll Cardiol 2017; 69:1215–30.
3. Reardon MJ, Van Mieghem NM, Popma JJ, et al. Surgical or transcatheter aortic-valve replacement in intermediate-risk patients. N Engl J Med 2017; 376:1321–31.
4. Leon MB, Smith CR, Mack MJ, et al. Trans- catheter or surgical aortic-valve replacement in ntermediate-risk patients. N Engl J Med 2016; 374:1609–20.
5. Sawaya FJ, Deutsch M-A, Seiffert M, et al. Safety and efficacy of transcatheter aortic valve replacement in the treatment of pure aortic regurgitation in native valves and failing surgical bioprostheses: results from an international reg- istry study. J Am Coll Cardiol Intv 2017;10: 1048–56.
6. Rawasia WF, Khan MS, Usman MS, et al. Safety and efficacy of transcatheter aortic valve replacement for native aortic valve regurgitation: a systematic review and meta-analysis. Catheter Cardiovasc Interv 2019;93:345–53.
7. Haussig S, Linke A. Transcatheter aortic valve replacement indications should be expanded to lower-risk and younger patients. Circulation 2014; 130:2321–31.
8. Baumgartner H, Falk V, Bax JJ, et al. 2017 ESC/ EACTS guidelines for the management of valvular heart disease. Eur Heart J 2017;38:2739–91.
9. Nishimura RA, Otto CM, Bonow RO, et al. 2017 AHA/ACC focused update of the 2014 AHA/ACC guideline for the management of patients with valvular heart disease: a report of the American College of Cardiology/American Heart Association Task Force>10. Egbe AC, Poterucha JT, Warnes CA. Mixed aortic valve disease: midterm outcome and pre- dictors of adverse events. Eur Heart J 2016;37: 2671–8.
11. Zoghbi WA, Adams D, Bonow RO, et al. Rec- ommendations for noninvasive evaluation of native valvular regurgitation: a report from the American Society of Echocardiography developed in collaboration with the Society for Cardiovascu- lar Magnetic Resonance. J Am Soc Echocardiogr 2017;30:303–71.
12. Baumgartner H, Hung J, Bermejo J, et al. Recommendations>13. Kappetein AP, Head SJ, Genereux P, et al. Updated standardized endpoint definitions for transcatheter aortic valve implantation: the Valve Academic Research Consortium-2 consensus document (VARC-2). Eur J Cardio-Thoracic Surg 2012;42:S45–60.
14. Svensson LG, Tuzcu M, Kapadia S, et al. A comprehensive review of the PARTNER trial. J Thorac Cardiovasc Surg 2013;145 3 suppl: S11–6.
15. Iung B, Baron G, Tornos P, Gohlke-Barwolf C, Butchart EG, Vahanian A. Valvular heart disease in the community: a European experience. Curr Probl Cardiol 2007;32:609–61.
16. Egbe AC, Luis SA, Padang R, Warnes CA. Out- comes in moderate mixed aortic valve disease: is it time for a paradigm shift? J Am Coll Cardiol 2016; 67:2321–9.
17. Rashedi N, Popovic ZB, Stewart WJ, Marwick T. Outcomes of asymptomatic adults with combined aortic stenosis and regurgitation. J Am Soc Echo- cardiogr 2014;27:829–37.
18. Stathogiannis K, Toutouzas K, Drakopoulou M, et al. The effect of mixed aortic valve disease in clinical outcomes after transcatheter aortic valve replacement. J Am Coll Cardiol 2017;69:1223.
19. Abdelghani M, Cavalcante R, Miyazaki Y, et al. Transcatheter aortic valve implantation for mixed versus pure stenotic aortic valve disease. Euro- Intervention 2017;13:1157–65.
20. Seeger J, Gonska B, Mörike J, Rottbauer W, Wöhrle J. Outcome of patients with mixed aortic valve disease undergoing transfemoral aortic valve replacement. Struct Hear 2017;1:162–7.
21. Philip JL, Zens T, Lozonschi L, et al. Outcomes of surgical aortic valve replacement for mixed aortic valve disease. J Thorac Dis 2018;10: 4042–51.
22. Catovic S, Popovic ZB, Tasic N, et al. Impact of concomitant aortic regurgitation>23. Parker MW, Aurigemma GP. The simple arithmetic of mixed aortic valve disease: LVH þ volume load ¼ trouble. J Am Coll Cardiol 2016; 67:2330–3.
24. Athappan G, Patvardhan E, Tuzcu EM, et al. Incidence, predictors, and outcomes of aortic regurgitation after transcatheter aortic valve replacement: meta-analysis and systematic re- view of literature. J Am Coll Cardiol 2013;61: 1585–95.
25. Genereux P, Head SJ, Hahn R, et al. Para- valvular leak after transcatheter aortic valve replacement: the new Achilles’ heel? A compre- hensive review of the literature. J Am Coll Cardiol 2013;61:1125–36.
26. Gotzmann M, Korten M, Bojara W, et al. Long- term outcome of patients with moderate and se- vere prosthetic aortic valve regurgitation after transcatheter aortic valve implantation. Am J Cardiol 2012;110:1500–6.