2019年欧洲心脏病学会年会(ESC2019)正在光明之城巴黎火热召开,在ESC和中华医学会心血管病学分会(CSC)的联合专场会议中,来自东方的中国声音吸引了众多与会专家。本场会议由复旦大学附属中山医院葛均波院士、英国谢菲尔德大学Robert Storey教授共同主持,首都医科大学附属北京安贞医院刘巍教授代周玉杰教授结合来自我国的原创研究向大家介绍了亚洲ACS患者的个体化抗栓治疗。
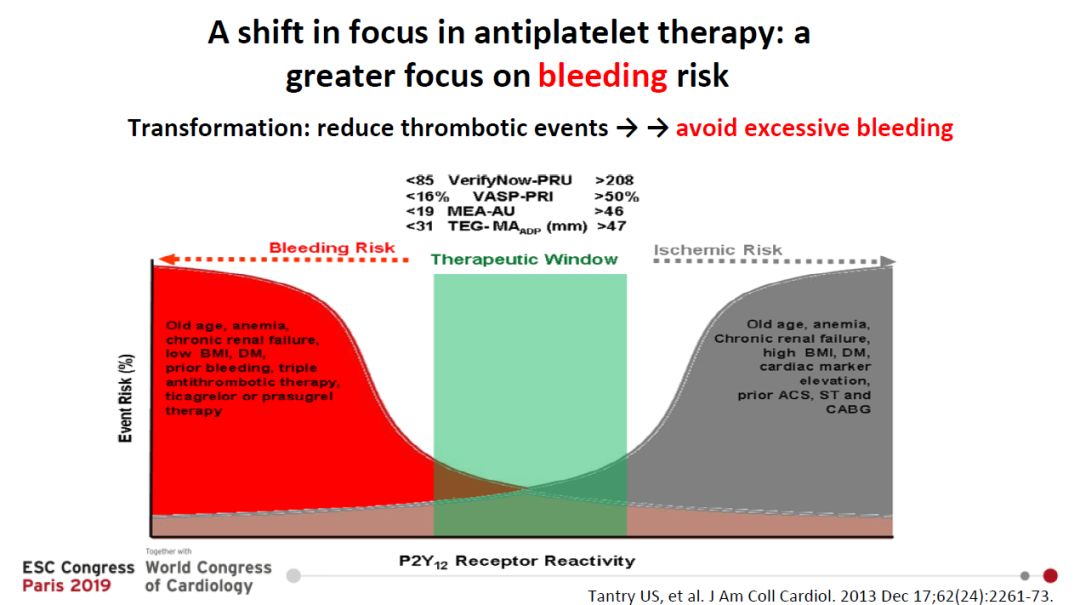
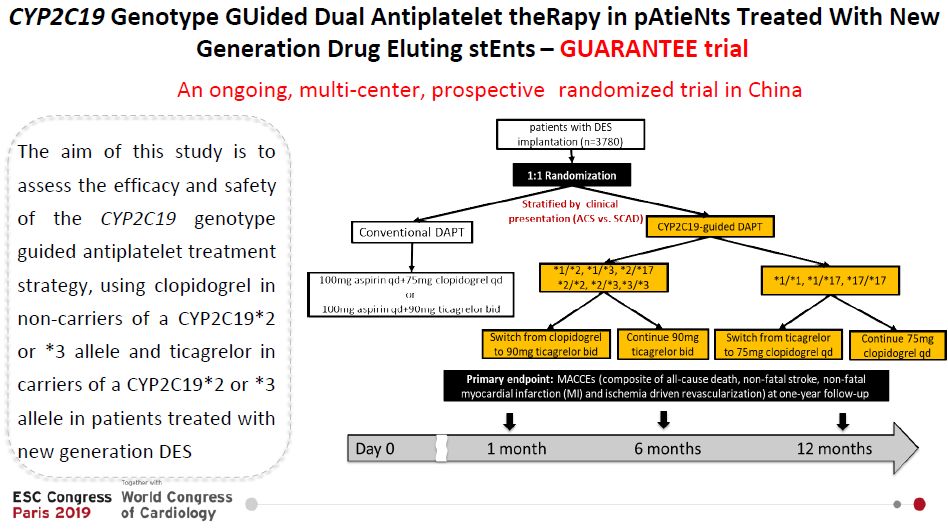
血小板治疗中的东亚悖论 由阿司匹林和P2Y12抑制剂组成的双联抗血小板治疗是急性冠状动脉综合征患者的标准治疗之一。然而抗血小板治疗同时与出血风险增高有关。随着技术的进步和新一代支架的广泛应用,术后缺血事件的风险大大降低。但与此同时,出血的风险引起了越来越多的关注,抗血小板治疗的重点已经在逐步转移到出血风险上。 此前的几项研究表明,相较于白种人,亚洲ACS患者的缺血风险较低,但出血的风险较高。例如,来自纳入了40余万名受试者的CathPCI注册研究数据显示,亚洲人PCI术后死亡或心肌梗死的风险明显低于白人。另一项CHARISMA研究是一项纳入15000余名受试者的前瞻性观察性研究。研究对象包括白人(80.1%)、黑人(3.1%)、亚裔(5.0%)和西班牙裔(10.3%),其结果显示,亚洲人的出血风险明显高于白人。 在血小板反应方面,东亚人群发生MACE事件的血小板反应的最适临界值始终高于西方人。虽然亚洲ACS/PCI患者血小板反应性较高,但缺血风险与白人患者相似甚至更低。 在此基础上,有专家提出了著名的东亚悖论,即东亚ACS患者血小板反应性(HPR)较高,缺血风险较低。其中原因之一可能在于东亚人群的促凝活性较低,《柳叶刀》杂志的一项荟萃分析发现,东亚人群凝血因子V和凝血酶原的单核苷酸多态性(SNPs)频率低于白种人,这可能导致血液促凝活性降低。 PHILO试验是一项多中心、双盲、随机的试验,比较了替格瑞洛与氯吡格雷在801例ACS患者中的安全性和有效性。结果表明,替格瑞洛在东亚ACS患者中具有较高的出血风险,可能是因为东亚人的体重指数较低。此外,东亚和白人个体的抗血小板治疗窗口不同。Levine, G. N.等人的一项研究描述了白人和东亚人群之间血小板反应活性最佳“治疗窗口”的显著差异,发现相同的治疗窗口不能帮助减少缺血事件,但可能导致亚洲出血风险增加。 东亚人群中强效P2Y12抑制剂的应用 具有代表性的里程碑式研究PLATO证实,ACS患者中强效P2Y12抑制剂替格瑞洛相对于传统氯吡格雷的优越性,并改写了指南。但PLATO研究中纳入的均为西方人群。上述PHILO试验纳入了来自日本、台湾和韩国的ACS患者,发现接受替格瑞洛治疗的患者主要终点事件的发生风险更高,其中包括重大出血事件、心肌梗死、中风或心血管源性死亡。值得注意的是替格瑞洛治疗组的大出血事件发生率明显高于氯吡格雷治疗组。 来自韩国的一项全国性前瞻性多中心观察队列研究—KAMIR-NIH注册研究的发现,与氯吡格雷相比,替格瑞洛显著降低了全因死亡的发生率,但增加了出血事件的发生率。此外,普拉格雷增加出血事件(p<0.01),并且对所有死因无显著影响。 因此,强有力的P2Y12抑制剂(替格瑞洛和普拉格雷)虽然有利于降低东亚患者的缺血事件风险,但会显著增加出血事件风险。 减量应用强效P2Y12抑制剂 那么对于东亚人群,有没有一种有效的P2Y12抑制剂选择策略可以在不增加出血风险的情况下降低缺血风险? PEGASUS-TIMI 54试验是一项多中心、随机、安慰剂对照、双盲研究,研究将21162例有心肌梗死病史的受试者随机分为安慰剂组、替格瑞洛60 mg bid组和替格瑞洛90 mg bid组,所有患者随访近3年。主要终点为心血管死亡、心肌梗死或中风。与安慰剂相比,两种剂量的替格瑞洛均显著减少主要终点事件,且没有增加致命性出血和非致命性颅内出血的风险。而这项研究只纳入了11.2%的亚洲人口。 因此,东亚患者使用减低剂量的替格瑞洛的可行性仍然不确定,P2Y12受体抑制剂的减剂量策略可能是东亚ACS患者的一个重要选择。 双联抗血小板治疗疗程的调整 调整双抗血小板治疗的疗程是优化抗血小板治疗的另一种策略。 SMART-DAPT是一项随机、开放、非劣效性的试验,在韩国的31个研究中心进行,旨在研究在亚洲人群中,6个月的DAPT疗程是否不劣于传统的12个月或更长时间的DAPT疗程。将2712例患者随机分为6个月DAPT组和12个月或以上DAPT组。结果显示,6个月DAPT 组的MACE的主要终点发生率不低于12个月或以上DAPT组。然而,6个月组的心肌梗死发生率明显高于12个月或以上DAPT组。因此我们不能得就此判断短期DAPT在 ACS患者中是安全的。 简而言之,目前的临床研究并不支持亚洲ACS患者PCI术后常规缩短DAPT持续时间。延长DAPT可显著增加亚洲人群出血的风险。亚洲ACS患者的DAPT疗程的调整应基于缺血和出血风险的平衡。在接受PCI治疗的ACS亚洲患者中,DAPT常规推荐使用12个月,除非有过高出血的风险。在接受PCI治疗的ACS患者中,缺血性风险高且耐受DAPT且无出血并发症的,可以考虑将DAPT持续12个月以上。 基因指导下制定抗血小板治疗策略 传统的氯吡格雷是目前最常见的P2Y12受体抑制剂。氯吡格雷是一种需要肝脏CYP生物酶将其转化为其活性代谢物的药物前体。CYP2C19基因功能缺失(LOF)的等位基因可降低人体对氯吡格雷的代谢能力。最常见的功能缺失等位基因序列为CYP2C19*2和CYP2C19*3。大约30%的白人和黑人以及60%的亚洲人携带一个或两个无功能的CYP2C19等位基因,被分别归类为CYP2C19中间代谢型(IMs)和慢代谢型(PMs)。 CYP2C19基因的突变频率存在明显的种族差异。携带至少一个CYP2C19 LOF等位基因的携带者约占黑人和白人人口的30%,在亚洲人群中最高可达50-60%。 在我们之前的一项研究中,我们从20项在亚洲进行的研究中获得数据进行荟萃分析显示,在亚洲人群中,至少有一个CYP2C19 LOF等位基因携带者比非携带者面临更高的MACE风险。支架血栓形成(ST)在LOF等位基因携带者中也更为常见(2.22% vs. 0.44%, OR: 4.77, 95% CI: 2.84 ~ 8.01, p < .001)。同时,LOF等位基因携带者的出血风险较低。 我们自己的另一项研究比较了替格瑞洛和氯吡格雷在携带两个CYP2C19功能丧失等位基因的PCI患者中的应用。我们从11988名进行了基因检测的病人中选择了携带了两个功能丧失等位基因的病人,通过倾向评分匹配进行进一步调整之间的偏差,生存分析结果表明,两各功能缺失的等位基因携带者中,替格瑞洛主要终点事件风险明显低于氯吡格雷组。大出血事件在开给替格瑞洛和氯吡格雷组中无差异,而用替格瑞洛的患者发生小出血事件的风险更高。 因此,CYP2C19基因型指导下的抗血小板治疗可能是一种合理的抗血小板治疗策略,国内已有三项关于基因型指导下抗血小板治疗的研究。在中国香港进行的一项单中心、前瞻性、随机、开放标签的研究表明,基因型引导组的高血小板反应发生率(PRU>208)明显低于标准组。一项纳入628例患者的单中心前瞻性随机试验表明,基因型引导组在1个月、6个月和12个月的ace发生率远低于常规组。两组间出血率无显著性差异。另一个单中心前瞻性随机试验纳入600例患者,发现ACS患者PCI术后根据CYP2C19基因型进行个性化抗血小板治疗可降低主要不良事件发生率。 我们正在进行中的GUARANTEE试验是在中国进行的一项多中心前瞻性随机试验。我们研究的目的是评估CYP2C19基因指导抗血小板治疗策略的有效性和安全性。 我们的研究将为个体化基因型指导抗血小板治疗提供更多的信息,并为精准医疗的发展提供更多依据和动力。